2. 100048 北京, 解放军总医院第一附属医院普外科
2. Department of General Surgery, First Affiliated Hospital of Chinese PLA General Hospital, Beijing, 100048, China
随着生物医学模式向生物-心理-社会医学模式的转变, 心理因素对疾病的影响引起了广泛的关注。临床和流行病学研究已证实慢性应激等社会心理因素促进了癌症的进展[1-2]。恶性肿瘤诊治过程中, 长期的负面情绪、抑郁、绝望等心理应激与肿瘤患者的预后明显相关, 证实长期的慢性应激能够促进恶性肿瘤的进展[3-5]。肝癌是预后较差的恶性肿瘤之一, 肝癌患者慢性应激状态是否与肝癌的预后相关, 在肝癌的诊治过程中如何评价患者的慢性应激水平, 目前尚不清楚。
早在1955年就有研究者发现心理因素能影响人心率的变异程度即心率变异性(heart rate variability, HRV)[6]。HRV是指连续心动周期的微小差异, 是心率连续的瞬时波动, 心率的波动受心理、神经内分泌的调控。HRV是评估一个人情绪和压力状态的无创性指标[7]。在以往的研究中, 已证实慢性应激能够影响乳腺癌[8]、卵巢癌[9]等恶性肿瘤的进展。HRV检测用来评估患者的应激水平, 并用于研究应激水平对乳腺癌远处转移的影响[10]。本研究利用心率变异检测仪检测肝癌患者应激指数和HRV时间域和频率域多项指标, 分析应激指数与HRV指标的相关性, 并根据这些应激相关参数来评估肝癌患者慢性应激水平, 初步探讨肝癌患者慢性应激水平与患者无疾病生存期和总生存期的相关性。
1 材料与方法 1.1 研究对象收集筛选符合入组条件的肝癌病例78例, 所有患者于2012-2016年在西南医院肝胆外科进行了肝癌根治性切除术, 且经病理诊断为肝细胞性肝癌。所有入组患者符合以下标准:①18~70岁之间; ②原发肿瘤已完成根治性治疗(手术、射频)。排除标准:①入组时有转移或活动性肿瘤; ②心血管疾病病史; ③心理疾病病史; ④长期或正在服用能改变交感神经系统活性的食物、药物等; ⑤未能准时随访和参加检测的患者。符合纳入条件的患者对自己所患疾病已明确知晓, 并签署知情同意书, 研究通过陆军军医大学第一附属医院伦理委员会评审(2012), 遵照赫尔辛基宣言执行。患者入组后完成调查问卷, 了解患者社会教育水平、婚姻状况、家庭经济情况等是否有重大变故, 以排除实验过程中其他因素对评估心理应激状态的干扰。
所有78例患者进行检测和随访, 随访截止日期为2017年3月, 最长随访时间为64个月, 排除失访或未完成3次HRV检测的患者37例, 符合入组且具有完整数据的病例41例。收集汇总41例患者的临床数据, 包括年龄、性别、肿瘤直径、血管癌栓、肿瘤分化、TNM分期、肿瘤术后复发等(表 1)。
| 病理特征 | 例数 | 所占比例(%) |
| 性别 | ||
| 女 | 5 | 12.2 |
| 男 | 36 | 87.8 |
| 年龄(岁) | ||
| < 50 | 22 | 53.7 |
| ≥50 | 19 | 46.3 |
| 肿瘤直径(cm) | ||
| < 5 | 11 | 26.8 |
| ≥5 | 30 | 73.2 |
| 甲胎蛋白(ng/mL) | ||
| < 400 | 21 | 51.2 |
| ≥400 | 20 | 48.8 |
| 血管癌栓 | ||
| 无 | 30 | 73.2 |
| 有 | 11 | 26.8 |
| 肝内转移 | ||
| 无 | 26 | 63.4 |
| 有 | 15 | 36.6 |
| 分化程度 | ||
| 低分化 | 4 | 9.7 |
| 中分化 | 35 | 85.4 |
| 高分化 | 2 | 4.9 |
| TNM分期a | ||
| Ⅰ | 9 | 21.9 |
| Ⅱ | 10 | 24.4 |
| Ⅲ, Ⅳ | 22 | 53.7 |
| 术后复发 | ||
| 是 | 29 | 70.7 |
| 否 | 12 | 29.3 |
| a:根据UICC-TNM分期 | ||
1.2 仪器与方法
利用Body-Checker检测仪(韩国迈迪克公司)检测患者应激指数和HRV时间域和频率域的多项指标, 统计分析临床患者的HRV水平和应激指数, 应激指数是根据患者心率、HRV等多项指标综合分析所得结果, 是用于评价患者应激水平的综合性指标。基于这些指标, 我们进一步分析肝癌患者的慢性应激状态。
分别于患者术后5 d, 3、6个月检测患者HRV水平, 患者先静待10 min, 仪器中录入ID、性别、年龄、检测次数等, 待患者静待10 min后于患者左或右手食指或中指接上Body-Checker检测导联, 检测5~10 min, 记录数据。统计应激指数和HRV时间域指标R-R间期标准差(standard deviations of normal-to-normal R-R intervals, SDNN)、相邻R-R间期差值的均方根(root mean square standard deviations of R-R intervals, RMSSD)及频率域指标低频功率(low frequency, LF)、高频功率(high frequency, HF), 得到3次检测的均值, 分析应激指数和HRV指标的分布情况。利用X-tile软件分别分析应激指数和HRV参数对患者总生存时间的影响, 确定各指标的最优cut-off值[11]。根据cut-off值分别比较分析应激指数和HRV各指标对患者无疾病生存期和总生存期的影响, 并分别探讨应激指数和SDNN与肝癌患者临床病例特征的相关性。
1.3 统计学方法采用SPSS 22.0和Graphpad Prism 6统计软件, 计量资料以x±s表示, 计数资料以百分率表示。X-tile软件用于确定各指标的最佳cut-off值。采用Spearman进行相关性分析, 采用Kaplan-Meier进行生存分析。检验水准:α=0.05。
2 结果 2.1 利用心率变异检测仪检测分析肝癌患者应激指数和HRV水平我们收集了符合入组条件的41例肝癌患者, 其中有29例患者在随访期间出现肝癌复发(表 1)。利用心率变异检测仪分析了41例肝癌患者术后应激指数和HRV多个指标的水平, 根据患者心率、HRV等多项指标综合分析得到应激指数这一综合性指标, 应激指数和HRV各指标的分布情况见表 2。
| 参数 | 应激指数 | HRV时间域指标 | HRV频率域指标 | |||
| SDNN (ms) | RMSSD (ms) | LF (ms2) | HF (ms2) | |||
| 均值 | 47.93 | 27.96 | 42.39 | 178.11 | 154.35 | |
| 标准差 | 14.68 | 8.57 | 24.29 | 210.31 | 139.14 | |
| 中位数 | 45 | 26.62 | 39.09 | 109.33 | 108.10 | |
| 最小值 | 23 | 15.56 | 10.62 | 14.19 | 7.24 | |
| 最大值 | 82 | 57.70 | 115.95 | 1 042.78 | 645.20 | |
| 四分位数 | ||||||
| 25% | 36 | 22.37 | 23.95 | 43.67 | 48.81 | |
| 50% | 45 | 26.62 | 39.09 | 109.33 | 108.10 | |
| 75% | 61 | 30.80 | 59.91 | 187.82 | 220.15 | |
2.2 比较分析肝癌患者应激指数和HRV水平的相关性
HRV的检测能够评价恶性肿瘤患者的应激水平, SDNN与患者预后具有明显的相关性[12]。本研究提出了应激指数这一综合性指标, 并将应激指数和SDNN等多种HRV指标进行相关性分析, 发现应激指数与HRV时间域指标SDNN、RMSSD呈显著负相关(r=-0.703, P < 0.01;r=-0.674, P < 0.01);进一步分析应激指数与频率域指标LF和HF的相关性, 结果显示, 应激指数与LF和HF也分别呈负相关关系(r=-0.508, P < 0.01;r=-0.707, P < 0.01)。
2.3 慢性应激状态与肝癌患者无疾病生存期和总生存期的相关性探讨应激指数和HRV指标与肝癌患者预后的相关性, 我们首先利用X-tile软件分析得到应激指数和4个HRV指标评估患者总生存时间的cut-off值, 应激指数对于评估患者预后最佳cut-off值为52;时间域指标SDNN和RMSSD的最佳cut-off值分别为23.79 ms和31.71 ms, 频率域指标LF和HF的最佳cut-off值分别为44.15 ms2和127.91 ms2(表 3)。
| 变量 | x±s | P值 |
| 应激指数 | ||
| < 52(n=23) | 36.65±6.52 | < 0.001 |
| ≥52(n=18) | 62.33±7.75 | |
| SDNN(ms) | ||
| < 23.79(n=17) | 21.04±2.29 | < 0.001 |
| ≥23.79(n=24) | 32.87±7.96 | |
| RMSSD(ms) | ||
| < 31.71(n=15) | 19.49±6.21 | < 0.001 |
| ≥31.71(n=26) | 55.61±20.65 | |
| LF(ms2) | ||
| < 44.15(n=11) | 32.86±9.01 | 0.006 |
| ≥44.15(n=30) | 231.36±223.71 | |
| HF(ms2) | ||
| < 127.91(n=20) | 49.96±25.61 | < 0.001 |
| ≥127.91(n=21) | 253.78±129.69 | |
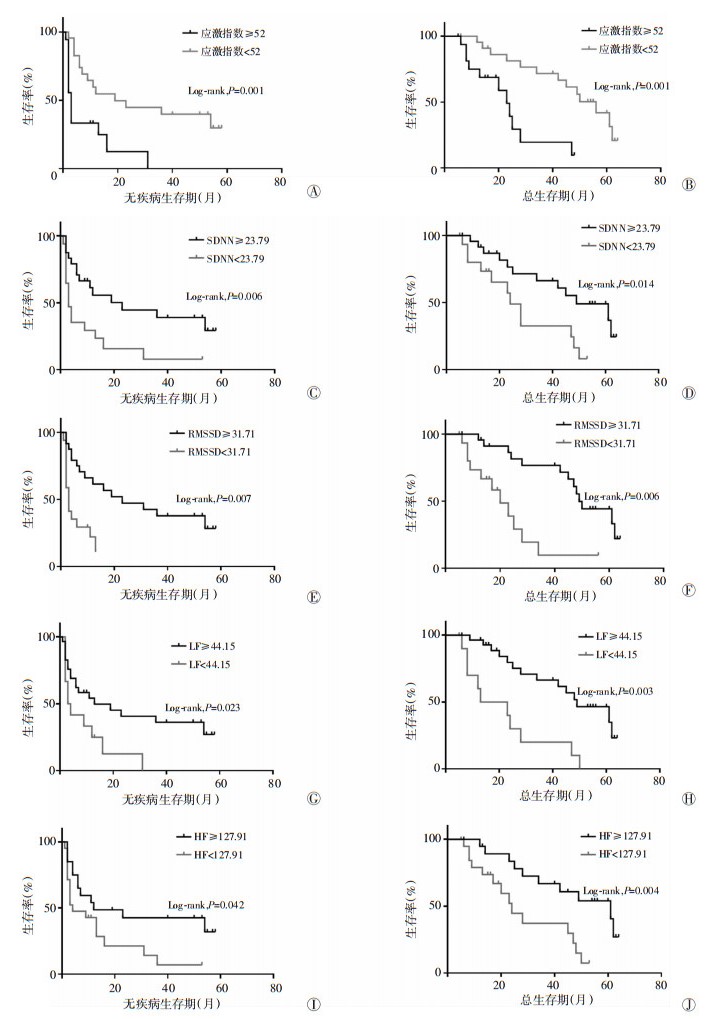
以上述cut-off值分别对应激指数和HRV指标进行分组, 比较分析各种应激指标对肝癌患者无疾病生存期和总生存期的影响。Kaplan-Meier生存分析结果发现:应激指数大于52的肝癌患者无疾病生存期较短(P=0.001), 并且该组患者总生存期也比应激指数低于52的患者明显较短, 中位生存期分别为23个月和56个月(P=0.001, 图 1A、B), 提示应激水平较高的肝癌患者预后较差。进一步分析HRV时间域指标SDNN和RMSSD与患者预后的关系, 发现SDNN和RMSSD低水平的患者无疾病生存期(SDNN:P=0.006;RMSSD:P=0.007)较高水平组明显缩短, 低水平组总生存期也明显短于高水平组(中位生存期分别为SDNN:24个月 vs 49个月, P=0.014;RMSSD:20个月 vs 49个月, P=0.006, 图 1C~F)。分析HRV频率域指标LF和HF与患者预后的关系, 发现LF低水平的患者无疾病生存期较高水平组明显缩短(P=0.023), 低水平组总生存期也明显短于高水平组(中位生存期分别为18个月 vs 49个月, P=0.003, 图 1G、H)。HF低水平的患者无疾病生存期较高水平组短(P=0.042), 总生存期也明显短于HF高水平组(中位生存期分别为24个月 vs 56个月, P=0.004, 图 1I、J)。
|
| A、B:应激指数高水平组与低水平组的无疾病生存曲线和总生存曲线; C、D:SDNN高水平组与低水平组的无疾病生存曲线和总生存曲线; E、F:RMSSD高水平组与低水平组的无疾病生存曲线和总生存曲线; G、H:LF高水平组与低水平组的无疾病生存曲线和总生存曲线; I、J:HF高水平组与低水平组的无疾病生存曲线和总生存曲线 图 1 应激指数和HRV指标与肝癌患者无疾病生存期和总生存期的相关性 |
2.4 慢性应激指数和SDNN与肝癌患者临床特征的相关性分析
SDNN是HRV指标中被用于评价恶性肿瘤患者预后的重要参数。为了进一步验证应激指数的有效性, 我们分析了SDNN和应激指数与患者临床特征的相关性。结果显示, 低水平的SDNN与患者的复发明显相关(P=0.021);而应激指数高水平也与肝癌术后复发明显相关(P=0.024)。比较分析应激指数和SDNN与肝内转移、TNM分期等临床指标的相关性发现, 应激指数和SDNN与患者肝内转移、TNM分期、性别、甲胎蛋白等指标无明显相关性(表 4), 证实患者的应激指数水平和SDNN均能够用于研究患者术后复发情况。
| 临床参数 | 应激指数 | P值 | SDNN | P值 | ||
| < 52 (n=23) |
≥52 (n=18) |
< 23.79 (n=17) |
≥23.79 (n=24) |
|||
| 年龄(岁) | 0.410 | 0.488 | ||||
| < 50 | 11 | 11 | 8 | 14 | ||
| ≥50 | 12 | 7 | 9 | 10 | ||
| 性别 | 0.452 | 0.382 | ||||
| 男性 | 21 | 15 | 14 | 22 | ||
| 女性 | 2 | 3 | 3 | 2 | ||
| 肿瘤直径(cm) | 0.567 | 0.761 | ||||
| < 5 | 7 | 4 | 5 | 6 | ||
| ≥5 | 16 | 14 | 12 | 18 | ||
| 甲胎蛋白(ng/mL) | 0.656 | 0.153 | ||||
| < 400 | 13 | 8 | 11 | 10 | ||
| ≥400 | 10 | 10 | 6 | 14 | ||
| 血管癌栓 | 0.567 | 0.697 | ||||
| 无 | 16 | 14 | 13 | 17 | ||
| 有 | 7 | 4 | 4 | 7 | ||
| 肝内转移 | 0.368 | 0.252 | ||||
| 无 | 16 | 10 | 9 | 17 | ||
| 有 | 7 | 8 | 8 | 7 | ||
| 分化程度 | 0.083 | 0.073 | ||||
| 低分化 | 1 | 3 | 3 | 1 | ||
| 中分化 | 20 | 15 | 14 | 21 | ||
| 高分化 | 2 | 0 | 0 | 2 | ||
| TNM分期 | 0.232 | 0.891 | ||||
| Ⅰ | 6 | 3 | 4 | 5 | ||
| Ⅱ | 7 | 3 | 2 | 8 | ||
| Ⅲ、Ⅳ | 10 | 12 | 11 | 11 | ||
| 术后复发 | 0.024 | 0.021 | ||||
| 是 | 13 | 16 | 12 | 17 | ||
| 否 | 10 | 2 | 5 | 7 | ||
3 讨论
原发性肝癌是临床上最常见的恶性肿瘤之一, 目前随着诊疗技术的不断发展, 外科手术、射频消融、化学栓塞等治疗方式被用于治疗原发的肝癌取得了不错的效果, 但大部分的肝癌患者最终却死于肿瘤的复发和转移[13]。因此, 探索肝癌复发转移的机制对于延长患者的生存时间具有重要的意义。恶性肿瘤的确诊及长期的病痛能带给患者持续的心理应激刺激, 肿瘤患者大多存在焦虑、恐惧和绝望等负面情绪, 这些应激源的长期存在使癌症患者处于慢性应激的状态。慢性应激已被证实能够通过激活交感神经系统加速卵巢癌[9]、乳腺癌[14]、胰腺癌等[15]恶性肿瘤的进展。肝癌作为临床常见的恶性肿瘤之一, 患者在长期诊治过程中是否处于慢性应激状态, 如何评价患者的应激水平, 慢性应激是否影响肝癌患者预后尚不清楚。因此, 本研究利用HRV检测仪检测肝癌患者HRV水平和应激指数, 证实HRV指标与应激指数呈显著负相关, HRV和应激指数能够用于评估肝癌患者术后慢性应激水平, 长期处于慢性应激状态的肝癌患者预后较差。
慢性应激是指由应激源引起的长期的慢性应激状态。长期的慢性应激可以导致精神、心血管系统和消化系统疾病, 还能调控癌症的发生和发展[16]。慢性应激对于恶性肿瘤的影响已有报道, 但以往研究慢性应激对恶性肿瘤进展的影响多基于动物模型或者体外实验研究, 而对于临床肿瘤患者慢性应激状态的评估目前仍没有系统的方法。在本研究中, 我们利用应激指数和HRV指标检测联合评估肝癌患者的慢性应激状态, 探索慢性应激的评价方法。已有的研究发现肿瘤患者HRV水平能够用于评估患者应激水平, 且SDNN等HRV指标对评估肿瘤患者预后有重要意义[12, 17-18]。本研究提出了应激指数这一综合性指标, 并证实应激指数和SDNN均与肝癌患者术后复发显著相关, 应激指数高水平的患者无疾病生存期和总生存期较短。应激指数用于评价患者的慢性应激水平能使研究慢性应激与恶性肿瘤进展的关系更为简便。为了验证这一指标的科学性和有效性, 我们将SDNN、RMSSD、LF、HF等多项HRV指标与应激指数进行相关性分析, 发现4个HRV指标均与应激指数呈显著负相关, 而HRV低水平的恶性肿瘤患者处于应激状态并且预后较差[19], 证实应激指数和HRV指标一样能够用于评估慢性应激状态。进一步研究发现应激指数与肝癌患者的无疾病生存期和总生存期呈负相关, 表明应激指数与HRV能够作为快速评估患者慢性应激水平的客观指标用来研究慢性应激与预后关系。
慢性应激可通过激活交感神经系统从多个方面调控恶性肿瘤进展。在之前的研究中, 应激已经被证实能够激活交感神经系统增加蛋白水解酶或MMPs的表达, 促进肿瘤细胞的侵袭和转移[20-21], 还能通过交感神经系统作用于肿瘤微环境, 促进肿瘤相关巨噬细胞活化和血管生长[9, 22]。癌症患者从疾病诊断到治疗大多一直处于压力应激状态, 慢性应激能够促进肿瘤的进展。更深入的研究慢性应激促进肿瘤转移的心理-神经生物学机制, 将为减轻患者心理应激对癌症进展的影响奠定理论基础。对于临床癌症患者, 已有研究表明如果在临床治疗肿瘤过程中, 减少应激刺激, 调节患者情绪状态将有助于癌症患者获得更好的预后[23-24]; 对癌症患者进行心理干预也能够抑制癌症进展, 提高临床预后[25]。建立科学的慢性应激评价体系对癌症患者心理干预的评估, 应激通路靶向药物的研发有重要的作用。本研究证实应激指数和HRV能通过检测患者生理反应评估患者的应激状态, 但更科学系统地评估患者慢性应激水平还需要更多的研究, 从患者心理反应的角度探讨患者主观心理改变的重要意义。
综上所述, 本研究通过利用HRV检测仪检测肝癌患者应激指数和HRV指标水平来评估肝癌患者慢性应激状态, 并发现应激指数与HRV多项指标显著负相关, 利用应激指数和HRV检测能够评估肝癌患者慢性应激水平。本研究证实了慢性应激水平较高的肝癌患者无疾病生存期和总生存期较短, 改善肝癌患者心理应激水平, 给予良好的社会家庭支持对于肝癌的治疗可能有巨大的帮助。
| [1] | SPIEGEL D, GIESE-DAVIS J. Depression and cancer:mechanisms and disease progression[J]. Biol Psychiatry, 2003, 54(3): 269–282. DOI:10.1016/s0006-3223(03)00566-3 |
| [2] | CHIDA Y, HAMER M, WARDLE J, et al. Do stress-related psychosocial factors contribute to cancer incidence and survival[J]. Nat Clin Pract Oncol, 2008, 5(8): 466–475. DOI:10.1038/ncponc1134 |
| [3] | WATSON M, HAVILAND J S, GREER S, et al. Influence of psychological response on survival in breast cancer:a population-based cohort study[J]. Lancet, 1999, 354(9187): 1331–1336. DOI:10.1016/s0140-6736(98)11392-2 |
| [4] | BUCCHERI G. Depressive reactions to lung cancer are common and often followed by a poor outcome[J]. Eur Respir J, 1998, 11(1): 173–178. DOI:10.1183/09031936.98.11010173 |
| [5] | COHEN S, WILLS T A. Stress, social support, and the buffering hypothesis[J]. Psychol Bull, 1985, 98(2): 310–357. DOI:10.1037//0033-2909.98.2.310 |
| [6] | FISKE D W, RICE L. Intra-individual response variability[J]. Psychol Bull, 1955, 52(3): 217–250. DOI:10.1037/h0045276 |
| [7] | KREIBIG S D. Autonomic nervous system activity in emotion:a review[J]. Biol Psychol, 2010, 84(3): 394–421. DOI:10.1016/j.biopsycho.2010.03.010 |
| [8] | DUIJTS S F A, ZEEGERS M P A, BORNE B V. The association between stressful life events and breast cancer risk:A meta-analysis[J]. Int J Cancer, 2003, 107(6): 1023–1029. DOI:10.1002/ijc.11504 |
| [9] | THAKER P H, HAN L Y, KAMAT A A, et al. Chronic stress promotes tumor growth and angiogenesis in a mouse model of ovarian carcinoma[J]. Nat Med, 2006, 12(8): 939–944. DOI:10.1038/nm1447 |
| [10] | CARO-MORÁN E, FERNÁNDEZ-LAO C, GALIANO-CASTILLO N, et al. Heart rate variability in breast cancer survivors after the first year of treatments:A case-controlled study[J]. Biol Res Nurs, 2016, 18(1): 43–49. DOI:10.1177/1099800414568100 |
| [11] | CAMP R L, DOLLED-FILHART M, RIMM D L. X-tile:a new bio-informatics tool for biomarker assessment and outcome-based cut-point optimization[J]. Clin Cancer Res, 2004, 10(21): 7252–7259. DOI:10.1158/1078-0432.CCR-04-0713 |
| [12] | GUO Y, KOSHY S, HUI D, et al. Prognostic value of heart rate variability in patients with cancer[J]. J Clin Neurophysiol, 2015, 32(6): 516–520. DOI:10.1097/WNP.0000000000000210 |
| [13] | FORNER A, LLOVET J M, BRUIX J. Hepatocellular carcinoma[J]. Lancet, 2012, 379(9822): 1245–1255. DOI:10.1016/S0140-6736(11)61347-0 |
| [14] | LE C P, NOWELL C J, KIM-FUCHS C, et al. Chronic stress in mice remodels lymph vasculature to promote tumour cell dissemination[J]. Nat Commun, 2016, 7: 10634. DOI:10.1038/ncomms10634 |
| [15] | KIM-FUCHS C, LE C P, PIMENTEL M A, et al. Chronic stress accelerates pancreatic cancer growth and invasion:a critical role for beta-adrenergic signaling in the pancreatic microenvironment[J]. Brain Behav Immun, 2014, 40: 40–47. DOI:10.1016/j.bbi.2014.02.019 |
| [16] | REICHE E M, NUNES S O, MORIMOTO H K. Stress, depression, the immune system, and cancer[J]. Lancet Oncol, 2004, 5(10): 617–625. DOI:10.1016/S1470-2045(04)01597-9 |
| [17] | WANG Y M, WU H T, HUANG E Y, et al. Heart rate variability is associated with survival in patients with brain metastasis:a preliminary report[J]. Biomed Res Int, 2013, 2013: 503421. DOI:10.1155/2013/503421 |
| [18] | KIM D H, KIM J A, CHOI Y S, et al. Heart rate variability and length of survival in hospice cancer patients[J]. J Korean Med Sci, 2010, 25(8): 1140–1145. DOI:10.3346/jkms.2010.25.8.1140 |
| [19] | GIESE-DAVIS J, WILHELM F H, CONRAD A, et al. Depression and stress reactivity in metastatic breast cancer[J]. Psychosom Med, 2006, 68(5): 675–683. DOI:10.1097/01.psy.0000238216.88515.e5 |
| [20] | WU W, YAMAURA T, MURAKAMI K, et al. Involvement of TNF-alpha in enhancement of invasion and metastasis of colon 26-L5 carcinoma cells in mice by social isolation stress[J]. Oncol Res, 1999, 11(10): 461–469. |
| [21] | YANG E V, BANE C M, MACCALLUM R C, et al. Stress-related modulation of matrix metalloproteinase expression[J]. J Neuroimmunol, 2002, 133(1/2): 144–150. DOI:10.1016/s0165-5728(02)00270-9 |
| [22] | SLOAN E K, PRICEMAN S J, COX B F, et al. The sympathetic nervous system induces a metastatic switch in primary breast cancer[J]. Cancer Res, 2010, 70(18): 7042–7052. DOI:10.1158/0008-5472.CAN-10-0522 |
| [23] | SCHULLER H M, AL-WADEI H A N, ULLAH M F, et al. Regulation of pancreatic cancer by neuropsychological stress responses:a novel target for intervention[J]. Carcinogenesis, 2011, 33(1): 191–196. DOI:10.1093/carcin/bgr251 |
| [24] | ANDERSEN B L, KIECOLT-GLASER J K, GLASER R. A biobehavioral model of cancer stress and disease course[J]. Am Psychol, 1994, 49(5): 389–404. DOI:10.1037//0003-066x.49.5.389 |
| [25] | SPIEGEL D. Mind matters in cancer survival[J]. Psychooncology, 2012, 21(6): 588–593. DOI:10.1002/pon.3067 |



