癫痫是一种常见的中枢神经系统疾病,以神经元过度放电所致的突然、反复和短暂的中枢神经系统功能紊乱为特征,并可导致相应的神经生物学、认知、心理学以及社会学等方面的后果[1]。目前,全球有7 000多万癫痫患者,其中90%以上分布于发展中国家。我国目前约有900万余例癫痫患者,每年新发病例约45万例[2-3]。由于癫痫的发病原因繁杂且发病机制迄今尚未完全阐明,目前临床的治疗仍主要局限于临床症状的控制[4]。
近年来的研究表明:神经元异常同步放电是导致癫痫发作的关键,其中神经元的异常突触传递是造成其异常放电的重要原因。因此,本研究主要讨论癫痫的发生与突触传递间的联系[5]。神经突触递质的释放常发生在突触前膜活性区,活性区存在特定的囊泡相关蛋白来调节突触囊泡的融合及神经递质的释放,其中神经突触前膜胞内蛋白13-1(mammalian uncoordinated 13-1,Munc13-1)是一种在突触前膜活性区特异性表达的多结构域蛋白,它广泛分布于中枢神经系统并在突触囊泡循环过程中发挥作用[6]。Munc13-1是突触囊泡的启动装置的重要组成部分,其N端可能通过与突触融合蛋白的结合来介导突触传递的启动,并且Munc13-1能干扰突触融合蛋白复合体的形成,以致缺失Munc13-1蛋白的突触囊泡尽管形态正常,但是不具有突触传递的功能[7]。再者,突触囊泡的异常释放还可以导致异常的突触重塑,而突触重塑的异常已证实与神经元异常放电有密切关系[8]。然而,Munc13-1在癫痫患者中的表达情况及其是否参与癫痫的发生,目前尚不清楚。
同时,在突触前膜活性区存在另一种蛋白——突触膜胞外分泌蛋白1(rab-interacting molecules 1,RIM1),其N端锌指结构与同源蛋白Rab3A的结合可以将囊泡挤向突触前膜活性区[9]。有研究已将RIM1与癫痫持续状态联系起来,认为RIM1在突触前引起异常的电活动,参与癫痫的发生[10],并且在胰高血糖素样肽-1(glucagon-like peptide-1, GLP-1)介导的胞吐中Munc13-1可与RIM1结合并产生功能性的相互作用[11]。
鉴于RIM1与癫痫有着密切的联系,且Munc13-1与RIM1可能存在相互作用,而Munc13-1在癫痫病灶中的表达情况及其是否参与癫痫发生均不清楚。本研究试图通过测定颞叶癫痫患者、脑外伤患者颞叶皮质中及癫痫大鼠、正常大鼠皮质和海马中Munc13-1及RIM1的表达,验证Munc13-1与RIM1的结合,探究在癫痫发生过程中Munc13-1以及其与RIM1相互作用的意义。
1 材料与方法 1.1 人脑标本的收集患者颞叶皮质标本取自重庆医科大学附属第一医院神经病学重点实验室脑库。癫痫患者的纳入标准:患者的诊断和发作类型符合2001年国际抗癫痫联盟的癫痫分类;24 h动态脑电图、视频脑电图、术中电生理等证实脑组织异常放电;正规抗癫痫药物治疗无效;影像学证实无占位性病变;已排除继发性癫痫。选取18例难治性颞叶癫痫患者[收集重庆医科大学附属第一医院、陆军军医大学(第三军医大学)第二、第三附属医院2013-2016年手术切除的标本]作为癫痫组[女性8例,男性10例,年龄为(33.22±11.86)岁]。15例脑外伤(收集重庆医科大学附属第一医院2014-2016年手术切除的标本)患者作为对照组[男性7例,女性8例,年龄为(35.47±11.69)岁],其纳入标准:无癫痫发作病史;未服用抗癫痫药物;排除脑外伤以外有其他神经系统疾病。癫痫组与对照组之间年龄、性别差异无统计学意义(P>0.05)。本研究获重庆医科大学的伦理委员会批准(2016年),所有程序的执行符合《赫尔辛基宣言》。
1.2 戊四氮动物模型的制备[12]饲养40只SPF级雄性大鼠(购于重庆医科大学动物实验中心,雄性,6~8周龄)至体质量达200~250 g, 抽签分为2组。其中1组大鼠经注射戊四氮(pentylenetetrazole,PTZ)建立颞叶癫痫(temporal lobe epilepsy,TLE)模型,即以PTZ亚惊厥剂量(35 mg/kg,Sigma-Aldrich公司,美国)进行腹腔注射,1次/d,连续注射21 d,每日PTZ注射后观察30~60 min,并记录癫痫发作的等级。惊厥评定采用Racine评分标准,出现连续3 d Ⅳ级及以上癫痫发作的大鼠即达到点燃模型标准。本实验中大鼠癫痫发作的平均潜伏期(第1次出现Ⅳ级及以上)为5~7 d,21 d后,出现连续3 d Ⅳ级及以上癫痫发作的大鼠有15只,纳入癫痫组;另一组20只大鼠注射生理盐水,剂量与方法同PTZ。实验21 d后,处死大鼠,分离得到海马和皮质。
1.3 标本的制备癫痫患者皮层脑组织和大鼠脑组织均分为3个部分。一部分立即置于液氮保存,用于Western blot检测。第二部分以4%多聚甲醛室温下固定48 h,按程序梯度脱水后用石蜡包埋,连续冠状切片,厚度为5 μm, 置于室温保存,用于免疫组化检测。第三部分则以4%多聚甲醛固定48 h,依次放置在20%、30%梯度蔗糖溶液24 h,用冰冻切片机(Leica公司,德国)切成10 μm切片,-20 ℃存储,用于免疫荧光检测。
1.4 免疫荧光双标对Munc13-1进行定位将-20 ℃保存的冰冻组织切片取出,放入丙酮浸泡30 min,PBS冲洗5 min×3次,滴加驴血清封闭液37 ℃封闭3 h,弃掉血清,滴加羊来源Munc13-1(1 :100),小鼠来源的神经元标记物(microtubule-associated protein 2,MAP2)(1 :100, Proteintech公司, 美国)、兔来源的星形胶质细胞标记物(glial fibrillary acidic protein,GFAP)(1 :50,中国博士德公司)的一抗,置于湿盒4 ℃过夜;第2天,37 ℃复温1 h,弃掉表面液体后PBS冲洗5 min × 3次,避光条件下滴加驴抗羊Dylight633(1 :50,Immuno Reagents公司,美国)、驴抗小鼠Dylight488(1 :50,Abbkine公司,美国)、驴抗兔Alexa Fluor555(1 :50,中国碧云天公司)37 ℃孵育1 h,PBS冲洗5 min ×3次,滴加细胞核标记物(4’, 6-diamidino-2-phenylindole,DAPI)抗核抗体(1 :20)室温孵育10 min,PBS冲洗5 min × 4次,甘油封片,运用激光共聚焦显微镜(Nikon公司,日本)采集图像。
1.5 免疫组化检测Munc13-1的表达采用免疫组化SABC染色法,取石蜡切片进行3% H2O2室温孵育10 min阻断,加入0.01 mol/L柠檬酸抗原修复缓冲液(pH=6.0)后置于微波炉中,高火3 min后低火15 min进行抗原修复,山羊血清封闭30 min,弃封闭液后滴加兔抗Munc13-1(1 :100, 中国博奥森公司), 4 ℃过夜, 弃一抗PBS冲洗5 min×3次,滴加山羊抗兔二抗,SABC孵育30 min后加显色剂(中国中杉金桥公司)显色,苏木精复染后脱水干燥,中性树胶封片。运用Olympus PM20全自动显微镜(Olympus公司,日本)在400倍视野下观察,运用Image-Pro Plus 6.0软件进行光密度值分析。
1.6 Western blot检测Munc13-1及RIM1的表达提取每例样本的总蛋白,检测其浓度并配平。蛋白样品上样于聚丙烯酰胺凝胶电泳系统,采用10%SDS-PAGE凝胶(中国碧云天公司)进行电泳,至标记相应条带跑出停止电泳、开始转膜,成功转至PVDF膜上后用脱脂奶粉封闭2 h,滴加稀释后的兔抗Munc13-1(1 :500, 中国博奥森公司)、兔抗RIM1(1 :900)、兔抗β-actin(1 :3 000, Proteintech公司, 美国)抗体,4 ℃置于摇床过夜,次日,弃一抗,TBST洗膜5 min×4次,用辣根过氧化物酶标记的羊抗兔二抗(1 :3 000,Proteintech公司, 美国)孵育2 h,弃二抗,TBST洗膜5 min×4次。运用ECL法在Fusion仪器显色,分析光密度值,计算Munc13-1/β-actin及RIM1/β-actin的值。
1.7 免疫共沉淀检测Munc13-1与RIM1的相互作用按Protein A/G Agarose beads(中国碧云天公司)说明书处理大鼠海马,用含PMSF的RIPA裂解液(中国碧云天公司)裂解组织,充分研磨后于4 ℃静置1 h,4 ℃、12 000 ×g离心10 min后弃沉淀取上清,加入一定量的兔抗IgG,并将ProteinA/G beads与上清液以1 :10体积比混合,4 ℃缓慢摇动30 min去除非特异性结合,4 ℃、12 000 ×g离心10 min后取上清分为4份,将一份上清与5× SDS上样缓冲液以1 :4体积比混合,沸水变性5 min后存于-80 ℃备用,即为阳性对照组(input)。其余3份上清中分别加入兔抗Munc13-1、兔抗RIM1和兔抗IgG 4 ℃过夜;每份中加入70 μL的ProteinA/G beads 4 ℃缓慢摇动3 h;4 ℃、1 000 × G离心5 min后弃上清,加入500 μL PBS洗涤沉淀后离心弃上清,重复3次。每份中加入50 μL 1× SDS上样缓冲液,煮沸5 min。得到的蛋白存于-80 ℃备用。采用Western blot实验进一步验证Munc13-1与RIM1的相关性。
1.8 统计学分析采用SPSS 19.0统计软件,计量资料以x±s表示,对癫痫组及对照组的光密度值分别进行正态性和方差齐性检验,若符合正态分布且方差齐,两组间比较采用t检验。检验水准:α=0.05。
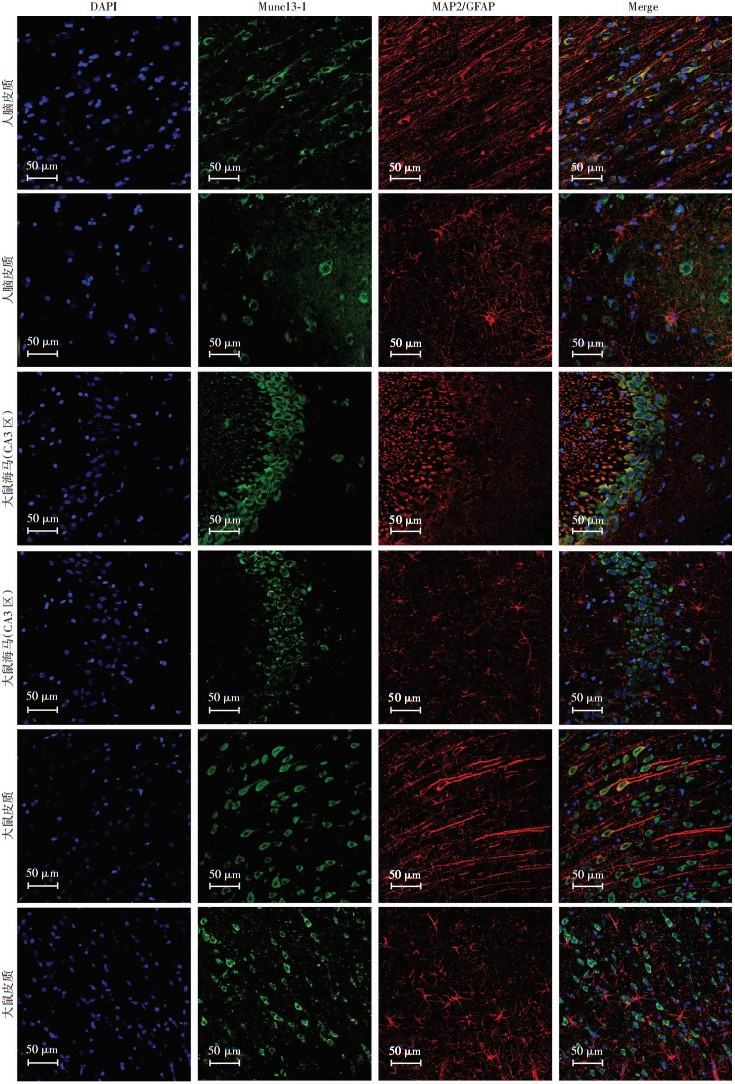
2 结果 2.1 Munc13-1在脑组织中的定位MAP2为神经元特异性标志物,GFAP为星形胶质细胞标志物,DAPI为细胞核标志物。通过免疫荧光双标染色检测Munc13-1在脑组织中的定位。结果显示:在癫痫患者皮质和模型大鼠海马、皮质中,Munc13-1(绿色)均与MAP2(红色)重合而与GFAP(红色)不重合,说明Munc13-1主要表达于神经元,而不表达于星形胶质细胞(图 1)。
|
| 图 1 免疫荧光双标染色检测Munc13-1在癫痫患者皮质及模型大鼠皮质、海马中的定位 (激光共聚焦显微镜) |
2.2 Munc13-1及RIM1的表达
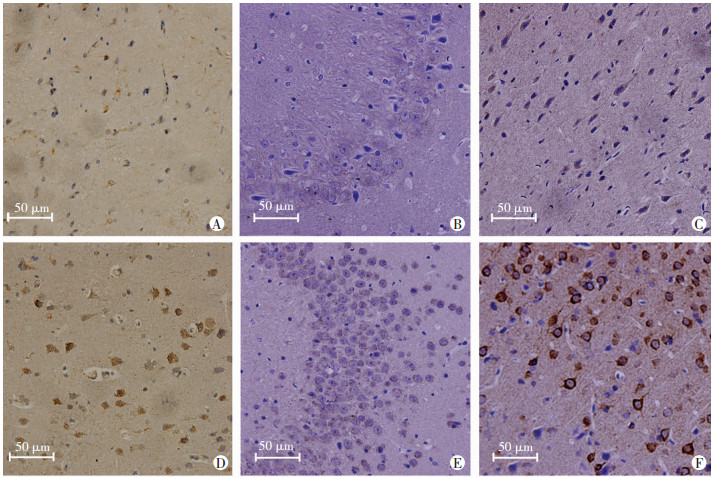
免疫组化检测结果显示:Munc13-1在癫痫患者及对照组皮质中均呈现阳性染色,且主要集中于神经元细胞,其中Munc13-1在癫痫组中的平均光密度值明显高于对照组(P<0.01),即癫痫患者皮质中Munc13-1的表达较正常人升高;同样,Munc13-1在动物癫痫组与对照组海马CA3区及皮层中也呈阳性染色,且其在癫痫组中的平均光密度值明显高于对照组(P<0.01,图 2,表 1)。运用Western blot进一步检测Munc13-1及RIM1在癫痫组和对照组中的表达,结果显示,Munc13-1、RIM1在癫痫患者皮质、模型大鼠的海马和皮质中表达水平较对照组明显升高(P<0.01,图 3,表 2)。
|
| A:对照组人皮质;B:癫痫组人皮质;C:对照组大鼠海马CA3区;D:癫痫组大鼠海马CA3区;E:对照组大鼠皮质;F:癫痫组大鼠皮质 图 2 免疫组化检测癫痫患者皮质和大鼠模型大脑皮质、海马中Munc13-1的表达 (SABC) |
| 组别 | 患者皮质 | 大鼠皮质 | 大鼠海马 |
| 对照组 | 0.81±0.05(n=15) | 0.81±0.05(n=20) | 0.82±0.03(n=20) |
| 癫痫组 | 1.16±0.07a(n=18) | 1.52±0.06a(n=15) | 1.26±0.07a(n=15) |
| a: P<0.01, 与对照组比较 | |||

|
| 1、2:对照组患者皮质;3、4:癫痫组患者皮质;5、6:对照组大鼠海马;7、8:癫痫组大鼠海马;9、10:对照组大鼠皮质;11、12:癫痫组大鼠皮质 图 3 Western blot检测Munc13-1及RIM1在癫痫患者皮质和模型大鼠皮质、海马中的表达 |
| 组别 | Munc13-1 | RIM1 | |||||
| 患者皮质 | 大鼠皮质 | 大鼠海马 | 患者皮质 | 大鼠皮质 | 大鼠海马 | ||
| 对照组 | 0.40±0.13(n=15) | 0.55±0.19(n=20) | 0.56±0.09(n=20) | 0.38±0.10(n=15) | 0.54±0.14(n=20) | 0.46±0.04(n=20) | |
| 癫痫组 | 0.79±0.23a(n=18) | 1.13±0.26a(n=15) | 1.41±0.28a(n=15) | 1.50±0.11a(n=18) | 0.92±0.09a(n=15) | 1.09±0.14a(n=15) | |
| a: P<0.01, 与对照组比较 | |||||||
2.3 Munc13-1与RIM1的相互作用
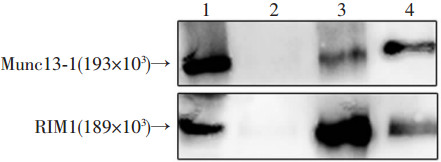
分别用Munc13-1抗体和RIM1抗体免疫沉淀后的蛋白,再用Munc13-1及RIM1抗体孵育条带,Western blot检测结果显示:Munc13-1与RIM1可通过直接或间接的方式相互结合(图 4)。
|
| 1:阳性对照组;2:阴性对照组;3:anti-RIM1组;4:anti-Munc13-1组 图 4 Western blot检测Munc13-1与RIM1的相互作用 |
3 讨论
癫痫的发病机制非常复杂,影响因素较多,其中突触重塑异常是其发病机制的重要理论之一。突触重塑是生物个体发育过程中应对环境变化而普遍存在的生物学现象,通过突触相关因子和神经递质释放的数量改变而启动[13-14]。其中神经递质释放的改变受多种囊泡相关蛋白的调节,而本研究中的Munc13-1即是其中一种[15]。
Munc13-1主要分布于中枢神经系统突触前膜[16],它通过参与突触融合蛋白复合体的形成而促进囊泡的启动[17]。有研究提示Munc13-1基因的突变可以刺激突触后电位振幅增强引起严重的神经功能障碍[18],且Munc13-1基因缺陷的小鼠在神经递质传递中存在递质释放的异常[19]。最近,ENGEL等[20]的研究还表明Munc13-1功能的缺失预示着Syntaxin1B失活、突触囊泡启动和释放的异常及患者皮质的过度兴奋。本研究首先以颞叶癫痫患者作为研究对象,检测Munc13-1在其脑组织中的定位及表达情况。免疫荧光双标结果显示:Munc13-1主要表达于神经元而非星形胶质细胞,并且荧光在神经元轴突处更为集中,提示Munc13-1发挥生理功能的部位在突触连接处。免疫组化及Western blot检测结果显示癫痫患者脑组织中Munc13-1的表达均明显上调。鉴于戊四氮致痫大鼠模型能很好地模拟颞叶癫痫的发病机制[21],本研究选用该模型进一步施行动物实验。结果发现:戊四氮诱导大鼠模型中Munc13-1表达也升高,与在癫痫患者中的研究结果一致,提示Munc13-1的异常表达与癫痫的发生密切相关。
目前已经研究的与Munc13-1相互作用的囊泡释放相关蛋白有RIM1、Munc-18[22]、syntaxin[23]、Doc2[24]等。RIM1作为Rab3蛋白的效应因子,参与调节囊泡的融合速度,且影响突触囊泡释放及突触的异常重塑而备受重视[25]。SCHOCH等[26]还证明了Munc13-1在突触前膜活性区的量与RIM1有关,他们发现在RIM1基因敲除后Munc13-1的浓度随之降低,且Munc13-1在突触前膜活性区的定位及功能也受到影响。这些研究预示了RIM1与Munc13-1的结合及相互调节。因此,本研究接着检测了RIM1的表达变化,并采用免疫共沉淀法验证RIM1与Munc13-1之间的结合。结果显示:RIM1在癫痫患者及戊四氮大鼠模型脑组织中表达均明显升高,这与FU等[27]的研究结果相一致,且进一步的免疫共沉淀实验证实在中枢神经系统中Munc13-1与RIM1确实有结合。
我们推测:Munc13-1以直接或间接结合的方式与RIM1相互作用,影响突触囊泡的释放;突触囊泡释放的改变进一步影响神经突触的重塑,从而引起神经元的兴奋性异常导致癫痫的发生。Munc13-1作为一个新发现的参与癫痫发生的因子,其具体的作用途径尚不清楚,与RIM1之间的调控规律及分子机制亦未明确。然而,Munc13-1所含结构域复杂,其与RIM1的结合位点仍存在争议,即以往相关分子结构研究认为Munc13-1与RIM1的结合发生在C端,但BETZ等[28]的研究观察到RIM1与Munc13-1的结合发生在N端,同时还证明RIM1与Munc13-1的结合不需C2结构域的存在。由此看来,明确Munc13-1与RIM1之间相互作用的具体机制还需要进行大量深入的研究。
| [1] | DULAC O, MILH M, HOLMES G L. Brain maturation and epilepsy[J]. Handb Clin Neurol, 2013, 111: 441–446. DOI:10.1016/B978-0-444-52891-9.00047-6 |
| [2] | SCOTT J A, BAUNI E, MOISI J C, et al. Profile: the kilifi health and demographic surveillance system (KHDSS)[J]. Int J Epidemiol, 2012, 41(3): 650–657. DOI:10.1093/ije/dys062 |
| [3] |
常琳, 王小姗.中国癫痫流行病学调查研究进展[J].国际神经病学神经外科学杂志, 2012, 39(2): 161-164.
CHANG L. Progress in epidemiological investigation of epilepsy in China[J]. J Int Neuro Neurosurg, 2012, 39(2): 161-164. |
| [4] | PICKRELL W O, SMITH P E. Treatment of resistant epilepsy[J]. Clin Med (Lond), 2014, 14(Suppl 6): s1–s6. DOI:10.7861/clinmedicine.14-6-s1 |
| [5] | ROGAWSKI M A, L SCHER W, RHO J M. Mechanisms of action of antiseizure drugs and the ketogenic diet[J]. Cold Spring Harb Perspect Med, 2016, 6(5): a022780. DOI:10.1101/cshperspect.a022780 |
| [6] | LIU X, SEVEN A B, CAMACHO M, et al. Functional synergy between the Munc13 C-terminal C1 and C2 domains[J]. ELife, 2016, 5.Pii: e13696. DOI:10.7554/elife.13696 |
| [7] | ASHERY U, VAROQUEAUX F, VOETS T, et al. Munc13-1 acts as a priming factor for large dense-core vesicles in bovine chromaffin cells[J]. EMBO J, 2000, 19(14): 3586–3596. DOI:10.1093/emboj/19.14.3586 |
| [8] | HOLDERITH N, LORINCZ A, KATONA G, et al. Release probability of hippocampal glutamatergic terminals scales with the size of the active zone[J]. Nat Neurosci, 2012, 15(7): 988–997. DOI:10.1038/nn.3137 |
| [9] | SHEN Y, GE W P, LI Y, et al. Protein mutated in paroxysmal dyskinesia interacts with the active zone protein RIM and suppresses synaptic vesicle exocytosis[J]. Proc Natl Acad Sci USA, 2015, 112(10): 2935–2941. DOI:10.1073/pnas.1501364112 |
| [10] | PITSCH J, OPITZ T, BORM V, et al. The presynaptic active zone protein RIM1α controls epileptogenesis following status epilepticus[J]. J Neurosci, 2012, 32(36): 12384–12395. DOI:10.1523/JNEUROSCI.0223-12.2012 |
| [11] | KWAN E P, XIE L, SHEU L, et al. Interaction between Munc13-1 and RIM is critical for glucagon-like peptide-1 mediated rescue of exocytotic defects in Munc13-1 deficient pancreatic beta-cells[J]. Diabetes, 2007, 56(10): 2579–2588. DOI:10.2337/db06-1207 |
| [12] | DIEHL R G, SMIALOWSKI A, GOTWO T. Development and persistence of kindled seizures after repeated injections of pentylenetetrazol in rats and guinea pigs[J]. Epilepsia, 1984, 25(4): 506–510. DOI:10.1111/j.1528-1157.1984.tb03452.x |
| [13] | CAVAZOS J E, GOLARAI G, SUTULA T P. Mossy fiber synaptic reorganization induced by kindling: time course of development, progression, and permanence[J]. J Neurosci, 1991, 11(9): 2795–2803. |
| [14] | CAVAZOS J E, CROSS D J. The role of synaptic reorganization in mesial temporal lobe epilepsy[J]. Epilepsy Behav, 2006, 8(3): 483–493. DOI:10.1016/j.yebeh.2006.01.011 |
| [15] | DOBIE F, CRAIG A M. A fight for neurotransmission: SCRAPPER trashes RIM[J]. Cell, 2007, 130(5): 775–777. DOI:10.1016/j.cell.2007.08.020 |
| [16] | AUGUSTIN I, BETZ A, HERRMANN C, et al. Differential expression of two novel Munc13 proteins in rat brain[J]. Biochem J, 1999, 337(Pt 3): 363–371. DOI:10.1042/0264-6021:3370363 |
| [17] | ROSENMUND C, SIGLER A, AUGUSTIN I, et al. Differential control of vesicle priming and short-term plasticity by Munc13 isoforms[J]. Neuron, 2002, 33(3): 411–424. DOI:10.1016/s0896-6273(02)00568-8 |
| [18] | VAROQUEAUX F, SIGLER A, RHEE J S, et al. Total arrest of spontaneous and evoked synaptic transmission but normal synaptogenesis in the absence of Munc13-mediated vesicle priming[J]. Proc Natl Acad Sci USA, 2002, 99(13): 9037–9042. DOI:10.1073/pnas.122623799 |
| [19] | LIPSTEIN N, VERHOEVEN-DUIF N M, MICHELASSI F E, et al. Synaptic UNC13A protein variant causes increased neurotransmission and dyskinetic movement disorder[J]. J Clin Invest, 2017, 127(3): 1005–1018. DOI:10.1172/JCI90259 |
| [20] | ENGEL A G, SELCEN D, SHEN X M, et al. Loss of MUNC13-1 function causes microcephaly, cortical hyperexcitability, and fatal myasthenia[J]. Neurol Genet, 2016, 2(5): e105. DOI:10.1212/nxg.0000000000000105 |
| [21] | KALYNCHUK L E. Long-term amygdala kindling in rats as a model for the study of interictal emotionality in temporal lobe epilepsy[J]. Neurosci Biobehav Rev, 2000, 24(7): 691–704. DOI:10.1016/s0149-7634(00)00031-2 |
| [22] | GARCIA E P, GATTI E, BUTLER M, et al. A rat brain Sec1 homologue related to Rop and UNC18 interacts with syntaxin[J]. Proc Natl Acad Sci USA, 1994, 91(6): 2003–2007. DOI:10.1073/pnas.91.6.2003 |
| [23] | KASULA R, CHAI Y J, BADEMOSI A T, et al. The Munc18-1 domain 3a hinge-loop controls syntaxin-1A nanodomain assembly and engagement with the SNARE complex during secretory vesicle priming[J]. J Cell Biol, 2016, 214(7): 847–858. DOI:10.1083/jcb.201508118 |
| [24] | DE JONG A P, MEIJER M, SAARLOOS I, et al. Phosphorylation of synaptotagmin-1 controls a post-priming step in PKC-dependent presynaptic plasticity[J]. Proc Natl Acad Sci USA, 2016, 113(18): 5095–5100. DOI:10.1073/pnas.1522927113 |
| [25] | GIRACH F, CRAIG T J, ROCCA D L, et al. RIM1α SUMOylation is required for fast synaptic vesicle exocytosis[J]. Cell Rep, 2013, 5(5): 1294–1301. DOI:10.1016/j.celrep.2013.10.039 |
| [26] | SCHOCH S, CASTILLO P E, JO T, et al. RIM1alpha forms a protein scaffold for regulating neurotransmitter release at the active zone[J]. Nature, 2002, 415(6869): 321–326. DOI:10.1038/415321a |
| [27] | FU P, WEN Y, XIONG Y, et al. Abnormal expression of FBXL20 in refractory epilepsy patients and a pilocarpine-induced rat model[J]. Neurochem Res, 2016, 41(11): 3020–3031. DOI:10.1007/s11064-016-2021-y |
| [28] | BETZ A, THAKUR P, JUNGE H J, et al. Functional interaction of the active zone proteins Munc13-1 and RIM1 in synaptic vesicle priming[J]. Neuron, 2001, 30(1): 183–196. DOI:10.1016/s0896-6273(01)00272-0 |



