膀胱癌是泌尿外科中最常见的恶性肿瘤之一,全球发病率居恶性肿瘤第9位。我国发病率远低于西方国家,但仍呈逐年增加趋势[1-2]。近年来肿瘤基因治疗越发受到重视,其中自杀基因疗法是热门方案之一[3]。酿酒酵母菌胞嘧啶脱氨酶/5-氟胞嘧啶(yeast cytosine deaminase /5-fluorocytosine,YCD/5-FC)是目前比较成熟的自杀基因,它使无毒性5-FC脱氨后生成细胞毒性产物5-FU,诱导肿瘤细胞死亡[4]。但目前自杀基因在治疗肿瘤疾病方面依然存在基因无靶向性、杀灭效率低、缺乏安全高效的基因载体和转染方法等缺点。其杀灭肿瘤主要依赖自杀效应和旁观者效应[5]。但旁观者效应的机制尚不清楚,可能与缝隙连接相关,而缝隙连接的通透性又与缝隙连接蛋白家族表达水平有关[6]。connexin26(Cx26)是缝隙连接蛋白家族中的重要成员, 能直接影响细胞间连接通讯, 在促进细胞分化成熟、调控膀胱上皮细胞的分化凋亡、维持细胞间协调稳定、抑制肿瘤生长等方面起重要作用[7-8]。LI等[9]发现, 正常人膀胱上皮组织中有Cx26基因大量表达, 而在癌组织中Cx26基因表达明显下调或缺失。恢复或上调Cx26表达可能会有效提高自杀基因系统对肿瘤细胞的杀灭作用。所以如何恢复或上调Cx26表达并达到自杀基因的高效转染成为急需解决的关键问题。超声微泡结合超声靶向微泡破坏是一项新兴的基因转染技术,具备安全性好和辐照靶向性等优势[10-11]。阳离子纳泡(CMB)其表面带正电荷,具有比普通微泡粒径更小、基因运载力及转染效率更高等优点[12]。超声靶向微泡破坏技术其原理是当微泡通过血液循环到达全身组织, 用超声探头在目标组织区域进行超声辐照, 产生空化及声孔效应,使细胞膜出现可逆性小孔,增加细胞膜通透性,使外源基因进入细胞内[11, 13]。本实验以CMB为基因载体结合超声靶向微泡破坏进行基因转染,探讨恢复或上调表达缝隙连接蛋白Cx26后,是否加强YCD/5-FC的旁观者效应,提高对膀胱癌细胞的杀灭效率, 从而为研究自杀基因机制和提高基因治疗效果提供新的思路。
1 材料与方法 1.1 主要试剂CMB(重庆医科大学超声影像研究所),人膀胱尿路上皮癌T24细胞(重庆医科大学生命科学院),RNA提取试剂TRIzol、逆转录试剂盒、RT-PCR试剂盒(美国Invitrogen公司),RPMI1640培养基、澳洲胎牛血清(美国Gibco公司),羊抗YCD多克隆抗体、兔抗CX26多克隆抗体(德国Thermo Fisher Scientific公司), 驴抗羊、羊抗兔(碧云天公司),YCD-pcDNA3.1-EGFP、CX26-pcDNA-EGFP、pcDNA3.1-EGFP质粒(重庆茂百科技有限公司), 质粒提取纯化试剂盒(Omega公司)等。
1.2 主要仪器倒置荧光显微镜(日本尼康公司),NanoDrop 2000分光光度仪(Thermo Fisher Scientific美国),超声基因转染治疗仪(重庆医科大学超声影像研究所),流式细胞检测仪、凝胶成像系统、PCR仪(美国Bio-Rad公司)。
1.3 细胞培养人膀胱癌T24细胞培养于含10%胎牛血清的RPMI1640培养基,37 ℃、5% CO2、湿度95%的孵箱内,按常规传代培养。
1.4 质粒提取、鉴定取质粒菌液接种在含氨苄青霉素的LB培养基中,37 ℃振摇16 h至饱和。按质粒抽提纯化试剂盒说明书,提取并纯化质粒。限制性内切酶KpnⅠ、NheⅠ酶切质粒后,用1%的琼脂糖凝胶电泳鉴定酶切DNA片段并送质粒测序。
1.5 载基因纳泡(YCD+Cx26-CMB)的制备取阳离子纳泡100 μL,加入5 μg不同质粒混合后置于4 ℃,待其反应15 min使二者充分结合。
1.6 载基因纳泡(CMB)联合超声辐照转染T24细胞取T24细胞接种在24孔板,待细胞汇合度80%~90%时转染。为比较不同方式下转染效率,将实验分4组:无处理对照组、pcDNA3.1-EGFP组、YCD+Cx26+ CMB组、YCD+Cx26+CMB+US组。各组加入预转染液,用无血清RPMI1640培养基定容为500 μL,给予平移性辐照(频率为1 MHz、占空比为20%、功率1.0 W/cm2、辐照时间45 s)。6 h后换成含血清的完全培养基,24 h后荧光显微镜下观察EGFP表达。用PBS重悬细胞并调整到5×105/mL,每个EP管中加入细胞悬液200 μL、5 μL Annexin V-FITC和10 μL PI,在暗室常温下孵育15 min后送流式细胞仪检测。
1.7 qRT-PCR和Western blot检测细胞转染48 h后用TRIzol法提取细胞总RNA。依照qRT-PCR试剂盒说明书合成cDNA,以此cDNA为模板进行扩增。GAPDH为内参,引物序列见表 1。细胞转染48 h后提取总蛋白,上样30 μg。用15% SDS-PAGE电泳,湿转至PVDF膜,TBST封闭1 h, 将膜浸入稀释的一抗溶液中(绵羊抗YCD 1:500;兔抗CX26 1:1 000),4 ℃过夜,TBST再洗膜10 min,HRP标记的相应二抗(驴抗绵羊1:1 000;羊抗兔1:5 000)室温摇床上孵育1 h。ECL试剂盒化学发光,凝胶成像系统显影。
| 引物 | 引物序列 | 片段大小 | |
| YCD | 上游引物: | 5′-TACAGGTGCCATCATCAT-3′ | 126 bp |
| 下游引物: | 5′-CTCTCATCGTCAACAACAA-3′ | ||
| Cx26 | 上游引物: | 5′-GAGAAGAAGAGGAAGTTCATCA-3′ | 119 bp |
| 下游引物: | 5′-ATGCTGCTTGTGTAGGTC-3′ | ||
| GAPDH | 上游引物: | 5′-AGAAGGCTGGGGCTCATTTG-3′ | 258 bp |
| 下游引物: | 5′-AGGGGCCATCCACAGTCTTC-3′ |
1.8 流式细胞仪检测细胞凋亡
为比较不同基因对T24细胞的凋亡影响,将实验分5组:无处理空白对照、载pcDNA3.1-EGFP纳泡组、载Cx26纳泡组、载YCD纳泡组、载YCD+Cx26纳泡组。联合超声辐照转染24 h后加入前药5-FC(300 μmol/L),48 h后用PBS重悬细胞,按Annexin V-PI凋亡检测试剂盒说明书操作,1 h内上机检测。
1.9 统计学分析采用SPSS 24.0统计软件进行数据处理。满足方差齐性及正态分布的计量资料:多组间比较采用单因素方差分析,两组间比较采用t检验;不满足则采用秩和检验。以P < 0.05为差异有统计学意义。
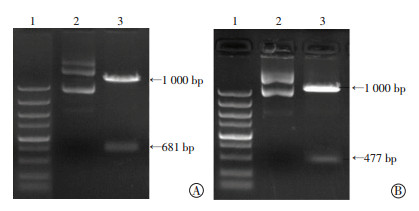
2 结果 2.1 重组质粒的鉴定质粒经双酶切电泳后出现两条高亮条带,说明酶切位点正确;重组质粒中含有载体片段和目的基因片段。未酶切的质粒则可能出现超螺旋、线性、开环三条或以上的条带。基因测序结果与GenBank中登录的序列比对完全正确,无任何碱基突变,己成功扩增YCD和Cx26的DNA序列(图 1)。
|
|
1:标准;2:未酶切;3:双酶切 A: Cx26-pcDNA-EGFP质粒酶切电泳;B:YCD-pcDNA-EGFP质粒酶切电泳 图 1 重组质粒的酶切电泳图 |
2.2 阳离子纳泡的一般特性
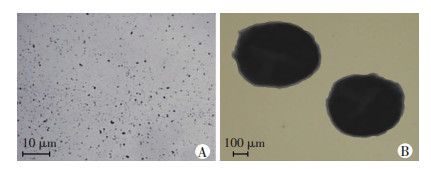
肉眼观测纳泡呈稍浑浊乳白色液体。光镜下见大量纳泡,外形规则呈球形,表面光滑,大小均一,分散度好, 无明显堆集粘连。透射电镜下见内部深色的C3F8气体和浅色的外层脂质包膜。纳泡表面电位及粒径范围测值集中性好,表面电位+(28.32±2.78)mv,粒径(472.5±48.57)nm,且粒径<700 nm的微泡比例>80%。纳泡在2周内非常稳定,理化性状基本保持一致(图 2)。
|
| A:电子显微镜;B:透射电子显微镜 图 2 纳泡的形态观察 |
2.3 载质粒纳泡的转染情况
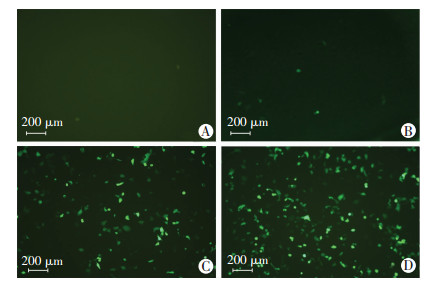
无处理对照组、pcDNA3.1-EGFP组、YCD+Cx26+CMB组、YCD+Cx26+CMB+US组转染效率分别为(0.31±0.17)%、(1.01±0.43)%、(18.06±0.96)%、(30.28±1.13)%。无处理对照组转染效率与pcDNA3.1-EGFP组比较差异无统计学意义(P > 0.05);YCD+Cx26+CMB组、YCD+Cx26+CMB+US组转染效率比无处理对照组高(P < 0.01,图 3),YCD+Cx26+CMB+US组转染效率比YCD+Cx26+CMB组高, 差异均有统计学意义(P < 0.01)。说明超声纳泡联合超声辐照能促进质粒转染入细胞, 提高转染效率。
|
| A:无处理对照组;B:pcDNA3.1-EGFP组;C:YCD+Cx26+CMB组;D:YCD+Cx26+CMB+US组 图 3 荧光显微镜下各组转染细胞的增强绿色荧光蛋白表达情况 |
2.4 转染目的基因后mRNA和蛋白表达
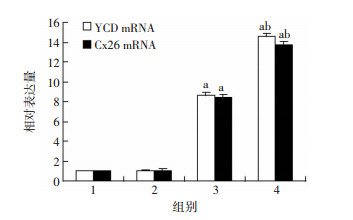
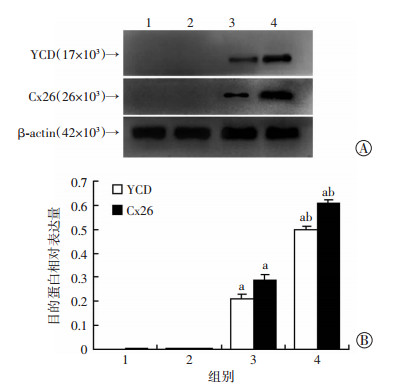
YCD+Cx26+CMB组、YCD+Cx26+CMB+US组与无处理对照组、pcDNA3.1-EGFP组相比,在mRNA及蛋白层面上相对表达量更高,差异有统计学意义(P < 0.01,图 4、5)。
|
|
1:无处理对照组;2:pcDNA3.1-EGFP组;3:YCD+Cx26+CMB组;4:YCD+Cx26+CMB+US组 a:P < 0.01,与无处理对照组及pcDNA3.1-EGFP组比较;b: P < 0.01,与YCD+Cx26+CMB组比较 图 4 qRT-PCR检测各组目的基因mRNA的相对表达量(2-△△Ct法) |
|
|
1:无处理对照组;2:pcDNA3.1-EGFP组;3:YCD+Cx26+CMB组;4:YCD+Cx26+CMB+US组 A: Western blot检测目的蛋白表达;B: YCD/Cx26半定量分析结果 a: P < 0.01,与无处理对照组及pcDNA3.1-EGFP组比较, b: P < 0.01,与YCD+Cx26+CMB组比较 图 5 Western blot检测各组目的蛋白的表达水平 |
2.5 恢复表达Cx26后对T24细胞凋亡的影响
分组处置48 h后,无处理空白对照、载pcDNA3.1 -EGFP纳泡组、载Cx26纳泡组、载YCD纳泡组、载YCD+Cx26纳泡组细胞凋亡率分别为(5.53± 1.21)%、(8.34±1.34)%、(9.53±1.75)%、(46.42± 2.13)%、(60.68±2.61)%。无处理空白对照细胞凋亡率与载pcDNA3.1-EGFP纳泡组、载Cx26纳泡组比较差异无统计学意义(P > 0.05);载YCD纳泡组、载YCD+Cx26纳泡组凋亡率比无处理空白对照高(P < 0.01),载YCD+Cx26纳泡组转染效率比载YCD纳泡组高, 差异均有统计学意义(P < 0.01)。说明恢复表达CX26后能加剧细胞凋亡。
3 讨论基因表达联合化疗可提高药物靶向释放及降低全身性毒副作用,因此自杀基因疗法越来越受到重视[3, 14]。目前基因治疗大多依靠病毒载体,但其有免疫原性、毒性及致瘤性等缺点。超声微泡具有无免疫原性、低毒、无致瘤性、可连接靶向抗体等优势而备受关注[10]。本实验制备的阳离子纳泡其粒径为(472.5± 48.57)nm,具有比普通微泡更小的粒径从而有更强的穿透力。数据表明当粒径小于700 nm时可顺利通过血管内皮细胞间隙进入靶组织[15];此外纳泡具有更高的稳定性,可长时间在血液循环中不被破坏,从而到达各个靶器官。阳离子纳泡相比普通中性或阴离子微泡更容易通过静电吸附及络合作用携载带负电荷的质粒。此制备方式简单便捷,容易普及推广。阳离子纳泡的出现使基因的运载能力大大提升,然而如何获得较高的转染效率成为关键性难题。本实验中运用超声靶向微泡破坏技术,利用低频超声辐照联合阳离子纳泡进行基因转染。流式细胞仪分析转染效率发现YCD+Cx26+CMB+US组明显高于YCD+Cx26+CMB组,说明纳泡联合超声辐照能进一步提高基因转染效率。这就为将来探索多个基因间相互作用提供了一种新的安全、快捷、高效的转染方式。同时超声微泡作为一种造影剂,能通过超声仪显像实时察看载基因或药物的微泡到达靶器官,在相应位置给予超声辐照,起到靶向治疗目的。并利用超声辐照对血管内皮细胞的损伤,进一步加速肿瘤的死亡[16]。超声纳泡结合超声辐照固然有一定被动靶向性,仍缺少特异性识别肿瘤细胞的主动靶向性。在接下来的研究中可利用纳泡偶联膀胱癌特异性抗体BCMαβ1[17],主动靶向识别膀胱癌细胞,达到基因更精确的靶向释放。
自杀基因(YCD/5-FC)治疗的一个显著优势即存在旁观者效应。旁观者效应即导入自杀基因的细胞自身被杀死,同时其邻近未导入自杀基因的细胞也被杀死的现象[18]。而缝隙连接(GJ)机制是旁观者效应的首要机制之一。在肿瘤生成的过程中,会发生GJ功能的减弱或缺失,导致自杀基因疗法的旁观者效应减弱,降低自杀基因治疗的效果,因此改善或恢复细胞缝隙连接通讯(GJIC)将对肿瘤的自杀基因治疗发挥极其重要的作用[19]。GJ由相邻的两个细胞各供应一个缝隙连接蛋白(Connexin,Cx)两两对接而成,构成GJ通道的Cx可以是一种或一种以上,经过其介导的GJIC实现细胞间信息交换和能量传递,调控细胞的增殖、分化、代谢等进程。Cx26是缝隙连接蛋白家族Cx的重要成员, 能直接影响GJIC。因此理论上恢复Cx26的表达,能一定程度改善GJIC, 从而加强自杀基因的旁观者效应。本实验中qRT-PCR和Western blot发现T24细胞中Cx26表达缺如,恢复表达Cx26基因后,载YCD+Cx26纳泡组(60.68±2.61)%明显比单载YCD纳泡组(46.42±2.13)%的细胞凋亡率更高,论证了其在一定程度上改善GJIC,加强了YCD/5-FC的旁观者效应,所以进一步加剧细胞凋亡。另有文献报道[19-21],加强Connexin43表达后,表现出明显的旁观者效应。此外GJ还可通过“旁细胞效应”增强电离辐射和多种抗肿瘤药物对肿瘤细胞的杀灭作用[22]。在接下来的研究中将尝试恢复或上调表达多种缝隙连接蛋白,并联合肿瘤抑制因子及多种自杀基因系统共表达,进一步提高基因治疗的有效性。
| [1] | ANTONI S, FERLAY J, SOERJOMATARAM I, et al. Bladder cancer incidence and mortality: A global overview and recent trends[J]. Eur Urol, 2017, 71(1): 96–108. DOI:10.1016/j.eururo.2016.06.010 |
| [2] | MIYAZAKI J, NISHIYAMA H. Epidemiology of urothelial carcinoma[J]. Int J Urol, 2017, 24(10): 730–734. DOI:10.1111/iju.13376 |
| [3] | NAVARRO S A, CARRILLO E, GRINAN-LISON C, et al. Cancer suicide gene therapy: a patent review[J]. Expert Opin Ther Pat, 2016, 26(9): 1095–1104. DOI:10.1080/13543776.2016.1211640 |
| [4] | MA S L, YANG X P, LIU L, et al. Human sulfatase-1 improves the effectiveness of cytosine deaminase suicide gene therapy with 5-fluorocytosine treatment on hepatocellular carcinoma cell line hepG2 in vitro and in vivo[J]. Chin Med J, 2015, 128(10): 1384. DOI:10.4103/0366-6999.156800 |
| [5] | YATA V K, GOPINATH P, GHOSH S S. Emerging implications of nonmammalian cytosine deaminases on cancer therapeutics[J]. Appl Biochem Biotech, 2012, 167(7): 2103–2116. DOI:10.1007/s12010-012-9746-0 |
| [6] | ZHANG J, KALE V, CHEN M. Gene-directed enzyme prodrug therapy[J]. AAPS J, 2015, 17(1): 102–110. DOI:10.1208/s12248-014-9675-7 |
| [7] | ZHU Y, ZONG L, MEI L, et al. Connexin26 gap junction mediates miRNA intercellular genetic communication in the cochlea and is required for inner ear development[J]. Sci Rep, 2015, 5: 15647. DOI:10.1038/srep15647 |
| [8] | DE TOLEDO S M, BUONANNO M, HARRIS A L, et al. Genomic instability induced in distant progeny of bystander cells depends on the connexins expressed in the irradiated cells[J]. Int J Radiat Biol, 2017, 93(10): 1182–1194. DOI:10.1080/09553002.2017.1334980 |
| [9] | LI X, SU Y, PAN J, et al. Connexin 26 is down-regulated by KDM5B in the progression of bladder cancer[J]. Int J Mol Sci, 2013, 14(4): 7866–7879. DOI:10.3390/ijms14047866 |
| [10] | WANG L, ZHANG M, TAN K, et al. Preparation of nanobubbles carrying androgen receptor siRNA and their inhibitory effects on androgen-independent prostate cancer when combined with ultrasonic irradiation[J]. PLoS ONE, 2014, 9(5): e96586. DOI:10.1371/journal.pone.0096586 |
| [11] | CAO S, ZHOU Q, CHEN J L, et al. Enhanced effect of nuclear localization signal peptide during ultrasound-targetedmicrobubble destruction-mediated gene transfection[J]. Mol Med Rep, 2017, 16(1): 565–572. DOI:10.3892/mmr.2017.6661 |
| [12] | ZHOU Y, GU H, XU Y, et al. Targeted antiangiogenesis gene therapy using targeted cationic microbubbles conjugated with CD105 antibody compared with untargeted cationic and neutral microbubbles[J]. Theranostics, 2015, 5(4): 399–417. DOI:10.7150/thno.10351 |
| [13] | WOOD A K, SEHGAL C M. A review of low-intensity ultrasound for cancer therapy[J]. Ultrasound Med Biol, 2015, 41(4): 905–928. DOI:10.1016/j.ultrasmedbio.2014.11.019 |
| [14] | SMELSER W W, AUSTENFELD M A, HOLZBEIERLEIN J M, et al. Where are we with bladder preservation for muscle-invasive bladder cancer in 2017[J]. Indian J Urol, 2017, 33(2): 111–117. DOI:10.4103/iju.IJU_279_16 |
| [15] |
阳孟君, 王洛夫, 郭燕丽, 等. 携载G250单克隆抗体的纳米微泡靶向于肾细胞癌的体内外实验研究[J].
第三军医大学学报, 2016, 38(2): 112–118.
YANG M J, WANG L F, GUO Y L, et al. In vivo and in vitro study of nanoscale microbubbles with G250 monoclonal antibodies targeting to renal cell carcinoma[J]. J Third Mil Med Univ, 2016, 38(2): 112–118. DOI:10.16016/j.1000-5404.201508106 |
| [16] | ZHANG W, SHOU W D, XU Y J, et al. Low-frequency ultrasound-induced VEGF suppression and synergy with dendritic cell-mediated anti-tumor immunity in murine prostate cancer cells in vitro[J]. Sci Rep, 2017, 7(1): 5778. DOI:10.1038/s41598-017-06242-8 |
| [17] | LI C, YANG Z, DU Y, et al. BCMab1, a monoclonal antibody against aberrantly glycosylated integrin α3β1, has potent antitumor activity of bladder cancer in vivo[J]. Clin Cancer Res, 2014, 20(15): 4001–4013. DOI:10.1158/1078-0432.CCR-13-3397 |
| [18] | WU K, YANG L, HUANG Z, et al. A double suicide gene system driven by vascular endothelial growth factor promoter selectively kills human hepatocellular carcinoma cells[J]. Oncol Lett, 2016, 11(5): 3152–3160. DOI:10.3892/ol.2016.4360 |
| [19] | XIAO J, ZHANG G, QIU P, et al. Tanshinone ⅡA increases the bystander effect of herpes simplex virus thymidine kinase/ganciclovir gene therapy via enhanced gap junctional intercellular communication[J]. PLoS ONE, 2013, 8(7): e67662. DOI:10.1371/journal.pone.0067662 |
| [20] | XIAO J, ZHANG G, LI B, et al. Dioscin augments HSV-tk-mediated suicide gene therapy for melanoma by promoting connexin-based intercellular communication[J]. Onco-target, 2017, 8(1): 798–807. DOI:10.18632/oncotarget.13655 |
| [21] | SUN P, LIU Y, YING H, et al. Action of db-cAMP on the bystander effect and chemosensitivity through connexin 43 and Bcl-2-mediated pathways in medulloblastoma cells[J]. Oncol Rep, 2012, 28(3): 969–976. DOI:10.3892/or.2012.1900 |
| [22] | TAKAHASHI M, VALDES G, HIRAOKA K, et al. Radiosensitization of gliomas by intracellular generation of 5-fluorouracil potentiates prodrug activator gene therapy with a retroviral replicating vector[J]. Cancer Gene Ther, 2014, 21(10): 405–410. DOI:10.1038/cgt.2014.38 |



