2. 400060 重庆, 重庆爱尔麦格眼科医院
2. Chongqing Aier Mega Eye Hospital, Chongqing, 400060, China
角膜散光是影响白内障患者术后视觉质量的重要因素。白内障患者中, 合并1.0D左右角膜散光的数量高达66.9%[1]。临床上, 超过0.75D的散光, 尤其是逆规散光, 即可出现复视、眩光、视物模糊等不适。因此, 白内障术中矫正角膜散光, 有助于改善术后视觉质量[2]。如何通过手术精准矫正白内障术前合并的角膜规则散光, 这是亟待解决的临床难题。
目前的方法主要有以下3种:①传统的手工方法:即在角膜最大屈光力轴方向做透明角膜切口, 或联合对侧透明角膜松解切口。该方法的优点是操作简便, 器械要求低, 花费少。但是, 手工制作切口长度、深度和形态难以精准把控, 受切口位置、术者手术习惯等影响[3]。②散光矫正型人工晶体植入:该方法的优点是矫正规则散光的疗效较好[4]。问题是人工晶体在囊袋内有发生旋转的风险[5], 引起散光矫正的偏差。另外, 散光矫正型人工晶体的度数一般在6~30D之间, 在超高度近视或远视患者的应用上受到限制。③飞秒激光辅助白内障手术(femtosecond laser assisted cataract surgery, FLACS):近年来, 飞秒激光辅助系统应用于白内障手术中, 可矫正术前合并的角膜规则散光[6]。比较于传统的手工方法, 该方法有望更精准矫正散光。目前, 对FLACS矫正角膜规则散光的疗效, 需要进一步临床对照研究。为此, 本文通过对比手工和FLACS两种方法, 观察矫正角膜规则散光的安全性和疗效, 为白内障合并角膜规则散光的手术设计提供理论依据。
1 资料与方法 1.1 临床资料2016年5月至2017年5月, 选择就诊于重庆爱尔麦格眼科医院, 符合纳入标准的白内障合并角膜规则散光(0.75~4.00D)的患者60例, 每例患者选择符合纳入标准的一眼作为研究对象, 对于双眼均符合纳入标准者, 选择其右眼作为研究对象。其中男性23例, 女性37例, 年龄46~85(70.53±7.73)岁。纳入标准:①根据中华医学会2007年版《临床诊疗指南-眼科学分册》符合白内障手术条件(最佳矫正远视力≤0.5)、合并角膜规则散光(0.75~4.00D)的患者; ②理性认知术后效果者。排除标准[7-8]:①角膜明显白斑、斑翳、翼状胬肉、圆锥角膜等; ②眼部外伤及眼部手术史; ③合并晶状体脱位或悬韧带异常患者; ④瞳孔散大<6 mm; ⑤急性眼部感染性疾病; ⑥影响视力的眼底病变; ⑦眼压控制不理想的进展期青光眼患者。按照患者意愿分为手工组和飞秒组, 每组30例(30眼)。本研究通过重庆爱尔麦格眼科医院医学伦理委员会审查[批号:2015伦审第(IRB003)], 所有患者签署知情同意书。
1.2 药物、仪器和设备左氧氟沙星滴眼液(可乐必妥, 日本参天公司); 裂隙灯检查仪(Topcon SL-1E, 日本Topcon); 角膜地形图测量仪器(Pentcam, 日本Topcon); 超声乳化仪器(Alcon Infinity, 美国爱尔康); 飞秒激光辅助系统(Lensx, 美国爱尔康)。
1.3 手术方法依据2009年版《老年性白内障临床路径》, 所有患者术前左氧氟沙星滴眼液(点术眼, 4次/d, 共3 d)。术前1 h, 在裂隙灯下坐位标记轴向, 手工组标记陡峭轴及90°位置, 飞秒组标记0°和180°。术前1 h散瞳, 术前常规麻醉及消毒。手工组:1.5D>散光>0.75D者, 在陡峭轴上做3.0 mm透明角膜切口后施行白内障超声乳化吸出联合单焦点非球面折叠人工晶体植入; 散光≥1.5D者, 除按上述步骤完成白内障超声乳化联合人工晶体植入术以外, 再用3.0 mm宝石刀在主切口对侧做一个周边透明角膜松解切口。对于主切口不能做在陡峭轴上的患者, 在12点做2.2 mm透明角膜主切口, 按常规施行超声乳化吸出联合人工晶体植入术后, 用3.0 mm宝石刀按照前面标准及方法在陡峭轴上一个或一对弧形周边透明角膜松解切口, 两切口之间相距180弧度, 长度、深度参照NICHAMIN[9]列线图计算。飞秒组:表麻后开睑, 建立负压吸引环, 在前节光学断层扫描仪引导下调整角膜缘定位及瞳孔中心。医助在电脑系统输入手术参数(包括连续环形撕囊大小; 主切口、辅助切口位置、长度; 患者角膜曲率矢量值; 术源性散光值), 电脑根据矢量计算器自动计算并确定角膜松解切口的位置、深度、弧度数。启动激光, 激光结束后解除负压。移除负压环, 将患者移至常规超乳手术台, 常规超声乳化完成余下步骤。两组所有患者均由经验丰富的超声乳化手术医师一人施行, 所有手术进行顺利, 无1例发生前囊口撕裂、后囊膜破裂或人工晶体不能植入等严重并发症。
1.4 观察指标根据角膜地形图的测量, 得出术前、术后的角膜曲率。目标矫正散光量(target-induced astigmatism, TIA)是根据术前角膜地形图测量的陡峭轴角膜曲率与平坦轴角膜曲率的差值确定; 散光差异量(difference vector, DV)是根据术后1个月和3个月时的角膜地形图测量的角膜曲率得出残余散光量; 手术矫正散光量(surgically-induced astigmatism, SIA)是指TIA和DV的差值。
观察术后早期并发症, 通过问卷调查法计算术后3个月的远视力脱镜率。脱镜率=[(术前戴镜人数-术后戴镜人数)/术前戴镜人数]×100%。
1.5 散光矢量分析方法采用Alpins矢量分析法[10]计算散光矫正指数(CI), CI=SIA/TIA。
1.6 统计学分析采用SPSS 19.0软件, 计量资料以x±s表示。对于两组术前、术后1和3个月的散光量、裸眼远视力、CI采用单因素方差分析(ANOVA)进行统计学检验。两组术前、术后1和3个月的TIA、SIA、DV、CI对比, 采用独立样本t检验。术后两组患者看远脱镜率、术后并发症的比较, 采用四格表χ2检验。检验水准α=0.05。
2 结果 2.1 两组患者术前一般资料两组患者术前一般资料比较见表 1。飞秒组高度近视患者多于手工组, 两组间人工晶体度数及预留度数差异有统计学意义(P < 0.05)。
| 组别 | n | 术前裸眼视力 | 术前矫正视力 | 术前散光量 | 人工晶体度数 | 术前预留度数 |
| 手工组 | 30 | 0.20±0.14 | 0.27±0.14 | 1.72±0.67D | +19.38±5.28Da | -0.29±0.27Da |
| 飞秒组 | 30 | 0.12±0.13 | 0.22±0.16 | 1.94±0.92D | +12.33±8.76D | -0.67±0.64D |
| a:P < 0.05, 与飞秒组比较 | ||||||
2.2 术后裸眼远视力、最佳矫正远视力变化
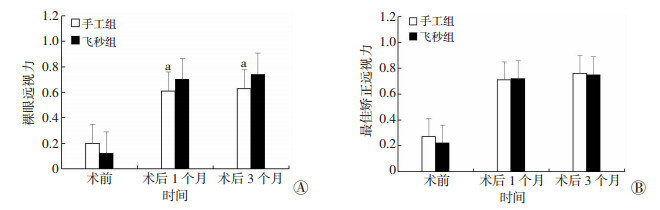
术后1个月, 手工组与飞秒组裸眼远视力差异有统计学意义(P=0.01);最佳矫正远视力的差异无统计学意义(P=0.837)。术后3个月, 手工组与飞秒组裸眼远视力差异有统计学意义(P=0.01);最佳矫正远视力差异无统计学意义(P=0.870)。手工组术后1个月和3个月组内比较, 裸眼远视力差异无统计学意义(P=0.611), 飞秒组术后1个月和3个月组内比较, 裸眼远视力差异无统计学意义(P=0.827), 提示飞秒组术后裸眼远视力较手工组好, 术后1个月时两组屈光状态均已达稳定状态(图 1)。
|
| a:P < 0.05, 与飞秒组比较 图 1 两组患者术前及术后各时间点裸眼远视力(A)及最佳矫正远视力(B)比较 |
2.3 术后残余散光的矢量观察
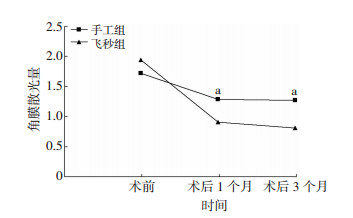
手工组术前TIA及术后1、3个月DV的方差齐性检验F=1.203, P=0.312, 方差齐, 在95%可信区间P分别为0.007和0.018, 提示术前术后散光量有统计学差异, 手工组矫正散光有效。组内术后1个月和3个月DV比较在95%可信区间P为0.443, 差异无统计学意义, 提示在手工组术后1个月时屈光状态达到稳定。飞秒组术前TIA及术后1、3个月的DV的方差齐性检验F=1.292, P=0.280, 方差齐, 在95%可信区间P分别为0.000、0.000, 提示术前术后散光量有统计学差异, 飞秒组矫正散光有效。术后1个月和3个月DV比较在95%可信区间P为0.605, 差异无统计学意义。提示飞秒组在术后1个月时屈光状态达到稳定(图 2)。手工组与飞秒组术后3个月残余散光的方差齐性检验F=0.263, P=0.610, 方差齐, 在95%可信区间P=0.026, 差异有统计学意义, 说明飞秒组术后残余散光明显小于手工组。
|
| a:P < 0.05, 与飞秒组比较 图 2 两组患者术前及术后各时间点散光量比较 |
2.4 两组术后3个月散光矫正指数比较
依据前述TIA和DV的结果, 计算TIA和DV的差值, 得出手工组和飞秒组的SIA, 分别为0.60±0.27D和1.12±0.61D。依据公式CI=SIA/TIA得出手工组和飞秒组的CI, 分别为0.39±0.16和0.60±0.20(<1, 表示欠矫)。两组CI比较, 差异有统计学意义(方差齐性检验F=1.435, P=0.236, 方差齐, t=-4.589, P=0.000), 提示飞秒组散光矫正效果明显好于手工组。
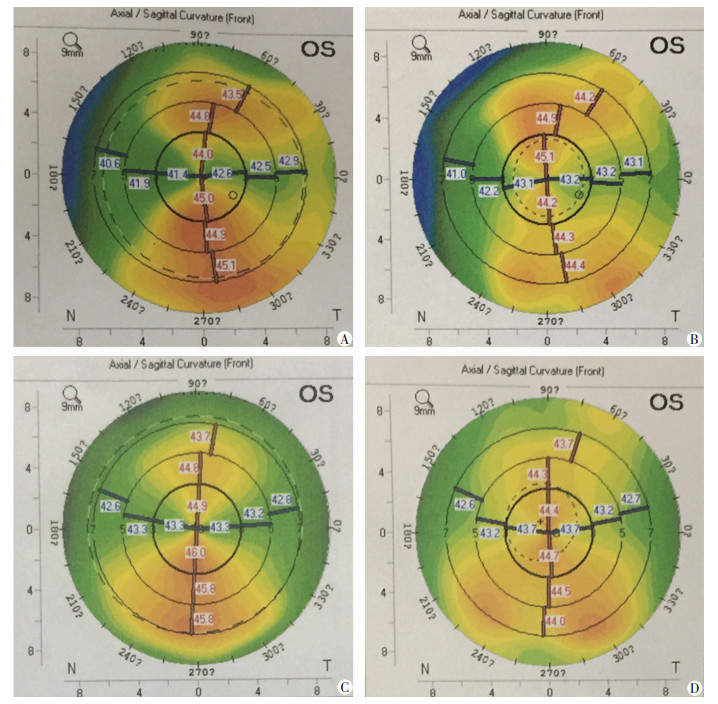
2.5 手工组和飞秒组患者术前、术后裸眼远视力和角膜地形图手工组同一患者术前术后角膜散光量对比显示:术前目标矫正散光量2.4D(图 3A), 术后3个月残留散光量1.5D(图 3B), 手术矫正散光量为0.9D, 散光矫正指数为0.375;飞秒组另一患者术前术后散光量对比显示:术前目标矫正散光量2.0D(图 3C), 术后3个月残留散光量0.9D(图 3D), 手术矫正散光量为1.1D, 散光矫正指数为0.55。由此可证实, 飞秒组患者散光矫正效果好于手工组。
|
| A:手工组术前; B:手工组术后3个月; C:飞秒组术前; D:飞秒组术后3个月 图 3 两组术前、术后角膜地形图对比 |
2.6 两组术后3个月远视力脱镜率的观察
手工组术前需戴镜看远人数12例, 术后需要戴镜人数7例, 不需要戴镜23例, 脱镜率41.67%;飞秒组术前需戴镜看远人数12例, 术后需要戴镜人数3例, 不需要戴镜27例, 脱镜率75.00%;Pearson χ2=2.00, P=0.01(<0.05), 两组间术后3个月远视力脱镜率差异有统计学意义。
2.7 术后并发症的观察手工组术后1 d发生角膜水肿2例(6.7%), 2例均为Ⅳ级核白内障, 主切口不整齐有渗漏1例(3.3%)。术后1周复查时切口愈合较好, 散光矫正切口漏水2例(6.7%), 给予加压包扎后于次日恢复。术后高眼压3例(10%), 其中2例为高度近视眼, 1例为术前诊断高眼压症患者, 经过前房穿刺放液后于术后3 d内恢复正常眼压。飞秒组术后1 d发生角膜水肿1例(3.3%), 为1例Ⅴ级核白内障, 主切口不整齐0例, 散光矫正切口漏水0例, 术后高眼压3例(10%), 其中2例为高度近视眼患者, 另1例术前无特殊, 经过前房穿刺放液后于术后3 d内恢复正常眼压。所有患者术后随访无1例发生眼内感染。手工组术后发生角膜相关并发症共5例(16.7%), 飞秒组共1例(3.33%), 组间差异有统计学意义(P < 0.05)。两组术后发生高眼压均为3例(16.7%)。
3 讨论在白内障手术过程中, 联合角膜切开矫正角膜散光的方法是通过板层或穿透性切开角膜, 改变陡峭轴的角膜曲率, 以期减少或消除陡峭轴与平坦轴之间的曲率差, 从而达到部分或全部矫正角膜规则散光的目的, 其方法包括传统的手工法和新近的飞秒激光法。由于散光矫正的效果与切口的长度、深度、结构、整齐度等有关[11], 本研究观察手工法和飞秒激光法在矫正角膜散光方面的临床价值。手工制作的切口不需要特殊的手术设备, 操作简便, 费用低廉, 但受到陡峭轴子午线方向的影响, 在鼻侧的切口无法制作, 且手工切口长度、深度、整齐度难以把控, 精准性差, 且受操作者熟练程度的影响, 不同操作者之间的手术效果差异较大, 因此矫正效果与预期相差较远。手法角膜松弛切开5°的轴向偏差, 便可使散光矫正效果降低17%[3]。而飞秒激光可在图像指导系统的定位下设置不同的切口长度、深度参数, 从而构建最优形状的角膜切口及散光矫正切口, 使精确性、可预测性和安全性大大提高, 源于术者经验和技巧之间的差异也会相对缩小[12], 可重复性强。对于飞秒激光制作的透明角膜切口, MASKET等[13]证实其整齐度及闭合性更好。曾凡超等[14]发现飞秒激光制作角膜切口没有引起全角膜高阶像差的明显改变, 飞秒激光制作角膜切口与手工制作角膜切口相比, 精准性及术后稳定性更好。在散光矫正效果方面, 飞秒激光依靠其精确切割大大增加了散光矫正切口的可靠性, 从而改善视觉质量, 术后散光矫正效果更好。不同于手工制作切口, 飞秒激光制作的散光矫正切口可在任何方向上, 不受位置的局限。据文献报道, 飞秒激光最高可矫正3.5D的角膜规则散光, 使患者术后视觉效果最大程度接近角膜屈光手术[6]。本研究结果显示手工组角膜切口不整齐及渗漏者共5例(16.7%), 而飞秒组共1例(3.3%), 与MASKET等[13]的研究结果相符, 进一步证实了飞秒激光制作角膜切口比手工制作角膜切口更整齐, 密闭性更好[13-14]。
本研究通过Alpins矢量分析法[10]计算散光度数的矢量平均值来分析术前、术后散光矫正情况[15]。TIA为术前散光量与患者最终想要达到的术后散光量的矢量差。本文中的TIA设置为术前散光量。DV为目标矫正散光量与手术矫正散光量的矢量差, 代表了术后残留散光的大小和方向。理想情况下该值应为0。SIA为手术引起的散光量的变化, 即术前与术后散光量的矢量差。从某种意义上讲, 即为术源性散光。CI=SIA/TIA, 理想情况下=1, >1表示过矫, <1表示欠矫。应用Alpin矢量分析法[10]得知, 本研究中手工组和飞秒组术后3个月CI分别为0.39±0.16、0.60±0.20, 均<1, 表示欠矫; 飞秒组CI>手工组, 两组之间差异有统计学意义(P < 0.05);两组患者术后3个月残留散光差异有统计学意义(P < 0.05);以上结果均显示飞秒组散光矫正效果明显好于手工组。该研究中两组CI值偏低, 是因为TIA设置为术前散光量, 为最大值。两组术后1个月和3个月裸眼远视力与术前相比, 差异均有统计学意义(P < 0.05), 术后3个月飞秒组视远脱镜率更高, 间接证实了飞秒组散光矫正效果优于手工组。
与传统手工方法比较, 我们认为飞秒激光辅助白内障手术矫正低、中度角膜规则散光的疗效优异, 可重复性强, 为白内障合并角膜规则散光患者增添了一种安全、有效的治疗选择[16]。但目前手术费用昂贵是其最大缺点, 使临床应用受到限制。另外更长期的术后效果需要长时间大样本量的观察来验证。
| [1] | ISYAKU M, ALI S A, HASSAN S. Preoperative corneal astigmatism among adult patients with cataract in Northern Nigeria[J]. Indian J Ophthalmol, 2014, 62(11): 1094–1095. DOI:10.4103/0301-4738.146751 |
| [2] | LIU Z, SHA X, LIANG X, et al. Toric introcular lens vs.peripheral corneal relaxing incision to correct astigmatism in eyes undergoing cataract surgery[J]. Eye Sci, 2014, 29(4): 198–203. |
| [3] | MOHAMMAD-RABEI H, MOHAMMAD-RABEI E, ESPANDAR G, et al. Three methods for correction of astigmatism during phacoemulsification[J]. J Ophthalmic Vis Res, 2016, 11(2): 162–167. DOI:10.4103/2008-322X.183924 |
| [4] | KESSEL L, ANDRESEN J, TENDAL B, et al. Toric intraocular lenses in the correction of astigmatism during cataract surgery:a systematic review and meta-analysis[J]. Ophthalmology, 2016, 123(2): 275–286. DOI:10.1016/j.ophtha.2015.10.002 |
| [5] | ZHU X, HE W, ZHANG K, et al. Factors influencing 1-year rotational stability of AcrySof Toric intraocular lenses[J]. Br J Ophthalmol, 2016, 100(2): 263–268. DOI:10.1136/bjophthalmol-2015-306656 |
| [6] |
刘奕志. 应当客观评价飞秒激光在白内障摘除手术中的应用[J].
中华眼科杂志, 2016, 52(2): 81–84.
LIU Y Z. Objective evaluation the application of femtosecond laser in cataract surgery[J]. Chin J Ophthalmol, 2016, 52(2): 81–84. DOI:10.3760/cma.j.issn.0412-4081.2016.02.001 |
| [7] | SUTTON G, BALI S J, HODGE C. Femtosecond cataract surgery:transitioning to laser cataract[J]. Curr Opin Ophthalmol, 2013, 24(1): 3–8. DOI:10.1097/ICU.0b013e32835a936b |
| [8] | MASTROPASQUA L, TOTO L, MASTROPASQUA A, et al. Femtosecond laser versus manual clear corneal incision in cataract surgery[J]. J Refract Surg, 2014, 30(1): 27–33. DOI:10.3928/1081597X-20131217-03 |
| [9] | NICHAMIN L D. Modified astigmatism correction nomogram[J]. J Refract Surg, 2008, 24(6): 562–563. |
| [10] | CHAN T C, CHENG G P, WANG Z, et al. Vector analysis of corneal astigmatism after combined femtosecond-assisted phacoemulsification and arcuate keratotomy[J]. Am J Ophthalmol, 2015, 160(2): 250–255. DOI:10.1016/j.ajo.2015.05.004 |
| [11] |
管怀进. 重视白内障合并角膜散光的精准手术矫正问题[J].
中华实验眼科杂志, 2017, 35(3): 193–196.
GUAN H J. Paying attention to precision correcting surgery for cataract associated with corneal astigmatism[J]. Chin J Exp Ophthalmol, 2017, 35(3): 193–196. DOI:10.3760/cma.j.issn.2095-0160.2017.03.001 |
| [12] |
李朝辉, 叶子. 飞秒激光辅助白内障摘除手术的利与弊[J].
中华眼科杂志, 2016, 52(2): 89–92.
LI C H, YE Z. The pros and cons of femtosecond laser-assisted cataract surgery[J]. Chin J Ophthalmol, 2016, 52(2): 89–92. DOI:10.3760/cma.j.issn.0412-4081.2016.02.003 |
| [13] | MASKET S, SARAYBA M, IGNACIO T, et al. Femtosecond laser-assisted cataract incisions:architectural stability and reproducibility[J]. J Cataract Refract Surg, 2010, 36(6): 1048–1049. DOI:10.1016/j.jcrs.2010.03.027 |
| [14] |
曾凡超, 司马晶, 杨浩江, 等. 飞秒激光白内障手术术源性散光及术后角膜像差的变化研究[J].
临床眼科杂志, 2016, 24(2): 97–100.
ZENG F C, SI M J, YANG H J, et al. Surgically induced astigmatism and changes in corneal aberrations after femtosecond laser-assisted cataract surgery[J]. J Clin Ophthalmol, 2016, 24(2): 97–100. DOI:10.3969/j.issn.1006-8422.2016.02.001 |
| [15] |
王静, 王涵, 马立威, 等. LenSx飞秒激光辅助白内障手术安全性和有效性的临床研究[J].
国际眼科杂志, 2016, 16(10): 1858–1861.
WANG J, WANG H, MA L W, et al. Clinical studies of the safety and effect of Lensx femtosecond laser-assisted cataract surgery[J]. Int Eye Sci, 2016, 16(10): 1858–1861. DOI:10.3980/j.issn.1672-5123.2016.10.17 |
| [16] | YOO A, YUN S, KIM J Y, et al. Femtosecond laser-assisted arcuate keratotomy versus toric IOL implantation for correcting astigmatism[J]. J Refract Surg, 2015, 31(9): 574–578. DOI:10.3928/1081597X-20150820-01 |



