目前,全球每年大约有100万对夫妇需要接受体外受精胚胎移植(in vitro fertilisation-embryo transfer,IVF-ET)治疗[1]。使用控制性超促排卵(controlled ovarian hyperstimulation,COH)能获取多个优质卵子,故其一直被视为体外受精胚胎移植成功的重要因素[2]。在COH中,卵巢的反应性主要指卵巢对外源性促性腺激素(gonadotropin,Gn)刺激做出的反应,卵巢低反应(poor ovarian response,POR)是指卵巢对Gn刺激反应不良,是导致IVF失败的重要因素之一。目前最常用的COH方案为用促性腺激素释放激素激动剂(GnRH-agonist,GnRH-a)进行垂体降调节的长方案和用促性腺激素释放激素拮抗剂(GnRH-antagonist,GnRH-ant)抑制早发的黄体生成素峰的拮抗剂方案。与长方案相比,拮抗剂方案可减少卵巢过度刺激综合征(ovarian hyperstimulation syndrome, OHSS)的发生[3],但在各文献报道中,其临床妊娠率却较低[3-4]。在卵巢低反应患者,常规促排卵方案效果均不佳。最近提出了GnRH-a联合GnRH-ant超短方案(ultrashort flare GnRH-agonist combined with GnRH-antagonist protocol)[5]。有研究报道在许多卵巢低反应、胚胎质量差、反复IVF失败的患者中,GnRH-a联合GnRH-ant超短方案得到了更好的IVF/卵胞浆内单精子注射技术(ICSI)结局[6-8]。但亦有研究表明其较常规促排卵方案无明显改观。本研究收集了国内外使用GnRH-a联合GnRH-ant超短方案促排卵的随机对照、临床对照试验,以Meta分析的方法,从Gn用药总量、Gn用药时间、获卵数、受精率、胚胎移植数、临床妊娠率等方面来探讨GnRH-a联合GnRH-ant超短方案,以期为其临床应用提供参考。
1 资料与方法 1.1 资料来源按Cochrane协作网的要求制定检索策略。检索MEDLINE、EMBASE、the Cochrane Central Register of Controlled Trials (CENTRAL)、中国生物医学数据库和万方数据库公开发表的全部文献。检索词包括:in vitro fertilisation/IVF、intracytoplasmic sperm injection/ ICSI、ultrashort flare GnRH-agonist combined with GnRH-antagonist、ultrashort flare GnRH-agonist、flexible multidose GnRH-antagonist、controlled ovarian hyperstimulation/ COH、poor responder、repeated IVF failures、IVF outcome、体外受精、卵巢低反应、超短方案等;检索时间自各数据库建库开始至2017年7月。并对检索获得文献的参考文献进行人工检索。
1.2 纳入标准与排除标准纳入标准:①无论是否采用盲法,不受发表类型和语种的限制。②研究对象为卵巢低反应、反复IVF失败或胚胎质量差的接受IVF/ICSI助孕的妇女。不受患者年龄、种族的限制。③干预措施为GnRH-a联合GnRH-ant超短方案。上一月经周期服用口服避孕药(oral contraceptive pills,OCP),至少使用2周,停药3 d后开始皮下注射GnRH-a 0.1 mg/d,连用3 d,次日开始使用Gn,用B超监测卵泡发育,并监测E2、P水平。当主导卵泡直径达14 mm,和/或E2水平超过400 pg/mL,加用GnRH-ant 0.25 mg/d直到板机日。④疗效判断指标:Gn用药总量、Gn用药时间(d)、获卵数、受精率、胚胎移植数、临床妊娠率等。排除标准:①会议报告、综述、指南;②数据无法利用的文献。
1.3 纳入研究的偏倚风险评估和资料提取2名研究者根据Cochrane Handbook推荐的方法分别对纳入研究进行偏倚风险评估和资料提取,当意见不一致时,和第3位研究者讨论解决。对每一项研究参照Cochrane library治疗评价标准进行质量评价。对于每一项纳入的研究,提取以下信息:作者、发表年限、研究国家、样本量、IVF促排卵方案、Gn用药总量、Gn用药时间、获卵数、受精率、胚胎移植数、临床妊娠率等。
1.4 统计学分析采用RevMan 5.3软件。连续变量采用加权均数差(WMD)表示,二分类变量采用Peto OR表示,评价均给出95%可信区间(confidence intervals, CI)表示。各纳入研究结果间的异质性采用x2检验和I2值表达,以P=0.1为是否具有统计学意义的分界点,当P < 0.1和I2>50%时,纳入的研究存在较大的异质性。无异质性的数据采用固定效应模型;有异质性者,对无法消除异质性的文献采用随机效应模型合并分析。
2 结果 2.1 检索结果及纳入研究的基本特征初检中英文文献共获得151篇相关文献,经过阅读题目和(或)摘要后剔除明显不符合标准的文献,再查找全文阅读和质量评价后,进一步剔除重复发表和交叉的文献,获得符合纳入标准的文献6篇[6-11],共计评价336个周期,其中对照组182例,GnRH-a联合GnRH-ant超短方案组154例。纳入研究的基本特征见表 1。
| 纳入研究 | ART | 总例数 | 结局比较 | |
| 对照组 | GnRH-a联合GnRH-ant超短方案 | |||
| ORVIETO等[6](2008年) | IVF/ICSI | 21 | 21 | ①②③④⑤ |
| ORVIETO等[7](2009年) | IVF/ICSI | 10 | 10 | ①②③④⑤ |
| BERKER等[9](2010年) | ICSI | 41 | 41 | ①②③④⑤⑥ |
| ORVIETO等[8](2010年) | IVF/ICSI | 19 | 19 | ①②③④⑤⑥ |
| EFTEKHAR等[10](2011年) | IVF/ICSI | 60 | 60 | ①②③④⑤⑥ |
| ORVIETO等[11](2013年) | IVF/ICSI | 31 | 3 | ①②③④⑤⑥ |
| ①~⑥分别是Gn用药总量、Gn用药时间(d)、获卵数、受精率(%)、胚胎移植数、临床妊娠率 | ||||
2.2 纳入研究的质量评价
纳入6篇均为国外文献。其研究方法质量评价见表 2。
2.3 Meta分析结果 2.3.1 Gn用药总量
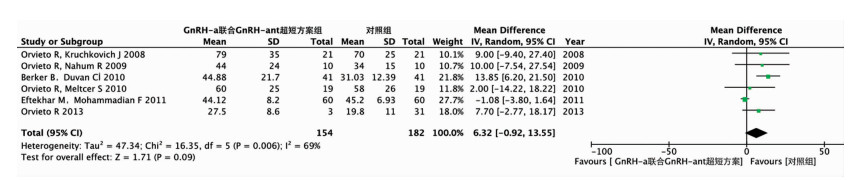
6篇文献Gn用药总量(支)各研究间存在统计学异质性(χ2=16.35, df=5, P=0.006, I2=69%)。采用随机效应模型合并,结果显示:两组Gn用药总量差异无统计学意义(WMD=6.32,P=0.09, 95% CI:-0.92~13.55, 图 1)。
|
| 图 1 GnRH-a联合GnRH-ant超短方案与对照组Gn用药总量的Meta分析 |
2.3.2 Gn用药时间
6项研究间Gn用药时间不存在统计学异质性(χ2=6.06, df=5, P=0.30, I2=18%)。采用固定效应模型,合并结果表明:GnRH-a联合GnRH-ant超短方案组和对照组间Gn用药时间差异无统计学意义(WMD=0.38,P=0.07, 95% CI:-0.04~0.81, 图 2)。

|
| 图 2 GnRH-a联合GnRH-ant超短方案与对照组Gn用药时间的Meta分析 |
2.3.3 获卵数
6项各研究间获卵数不存在统计学异质性(χ2=1.18, df=5, P=0.95, I2=0%)。采用固定效应模型进行Meta分析,结果表明:GnRH-a联合GnRH-ant超短方案组的获卵数较对照组高,但两组间差异无统计学差异(WMD=0.29,P=0.40, 95% CI:-0.38~0.96, 图 3)。

|
| 图 3 GnRH-a联合GnRH-ant超短方案与对照组获卵数的Meta分析 |
2.3.4 受精率
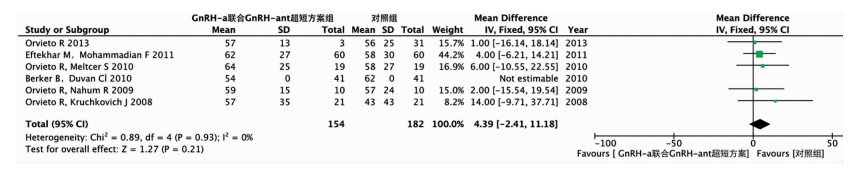
6项研究间受精率(%)不存在统计学异质性(χ2=0.89, df=4, P=0.93, I2=0%)。采用固定效应模型进行Meta分析,结果表明,受精率在GnRH-a联合GnRH-ant超短方案组中较高,但与对照组相比差异无统计学意义(WMD=4.39. P=0.21, 95% CI: -2.41~11.18, 图 4)。
|
| 图 4 GnRH-a联合GnRH-ant超短方案与对照组受精率的Meta分析 |
2.3.5 胚胎移植数
6项研究间胚胎移植数存在统计学异质性(χ2=19.09, df=4, P=0.000 8, I2=79%)。采用随机效应模型进行Meta分析,结果表明:胚胎移植数在GnRH-a联合GnRH-ant超短方案组和对照组间差异无统计学意义(WMD=0.24,P=0.49, 95% CI:-0.44~0.91, 图 5)。

|
| 图 5 GnRH-a联合GnRH-ant超短方案与对照组胚胎移植数的Meta分析 |
2.3.6 临床妊娠率
所纳入6项研究中,其中4项对临床妊娠率进行了统计学分析。各研究间存在统计学异质性(χ2=6.37, df=3, P=0.09, I2=53%)。采用随机效应模型进行Meta分析,结果表明:GnRH-a联合GnRH-ant超短方案组临床妊娠率较对照组明显升高,但差异无统计学意义(OR=1.72,P=0.38, 95%CI: 0.52~5.71,图 6)。

|
| 图 6 GnRH-a联合GnRH-ant超短方案与对照组临床妊娠率的Meta分析 |
3 讨论
目前,对于卵巢反应不良的患者最好的促排卵方案仍存在争议。一个好的促排卵方案特点应包括周期取消率低、获卵数多、胚胎质量好、可获得最大的妊娠率和活产率[12]。现在临床上常用的方案有长方案、短方案、拮抗剂方案、超短方案、微刺激方案、自然周期取卵等。在临床应用中,最常用的COH方案是长方案,它运用GnRH-a降调节来抑制早发的黄体生成素峰,由于GnRH-a的抑制作用可直接作用于卵巢上,卵巢低反应患者常常在长方案降调后出现Gn用量增加、内源性FSH的抑制导致卵巢反应不良[13-14]。而拮抗剂方案的优势体现在Gn用药量减少、用药时间短、患者花费少、周期间隔时间短[15],但其妊娠率尚存争议[15-17]。为了避免这些不良影响,出现了GnRH-a超短方案和微刺激方案[18],其目的是通过增加早卵泡期FSH的释放来提高卵巢反应,并通过卵巢的GnRH受体有效地抑制早发的LH峰[19]。本研究的GnRH-a联合GnRH-ant超短方案,GnRH-a的超短刺激作用促进了早卵泡期内源性FSH的迅速释放,有利于窦卵泡的募集,同时亦不引起雄激素及LH升高[19];与一般超短方案不同的是,此方案当主导卵泡直径达14 mm,和/或E2水平超过400 pg/mL,加用GnRH-ant直到板机日。GnRH-ant能快速抑制LH,尽可能地提高胚胎质量。另外,GnRH-a联合GnRH-ant超短方案常常使用OCP进行预处理,口服避孕药中的高效孕激素成分能够对下丘脑和垂体产生影响,抑制FSH、LH、E2及T等基础内分泌指标的升高,但并不削弱FSH的效应;此外,复方口服避孕药预处理降低了LH,因此阻止了卵巢源性雄激素及相应血清孕酮的升高。一些研究已经证实该方案可提高卵巢反应,但无一能证明其明显的提高妊娠率[20]。
本研究系统地评价了GnRH-a联合GnRH-ant超短方案对Gn用药总量、Gn用药时间、获卵数、受精率、胚胎移植数、临床妊娠率等的影响,发现在获卵数、受精率、临床妊娠率上,GnRH-a联合GnRH-ant超短方案组优于对照组,但差异无统计学意义。尽管本Meta分析的整体设计和实施参考了Cochrane协作网系统评价工作手册,但仍存在一定的局限性:①纳入文献仅6篇,分析的患者数目远远低于排除1个临床重要差异所需的样本量。6篇文献均为国外研究,但仅2篇为随机对照试验,1篇为队列研究,其余3篇均为病例对照研究,可能造成选择性偏倚。因此,尚需要更多大样本的设计良好的RCT来进一步评估GnRH-a联合GnRH-ant超短方案的疗效。②本研究纳入的文献仅有1篇采用双盲。③本研究纳入文献的患者均为卵巢低反应、反复IVF失败或胚胎质量差的接受IVF/ICSI助孕的妇女,并未对患者年龄、BMI、卵巢功能进行具体分组讨论,这些因素亦有可能影响IVF结局。④由于患者临床特征的差异,且病例对照的3篇文献并未对对照组使用的促排卵方案进行具体描述,另3篇分别为GnRH-a联合GnRH-ant超短方案与短方案或拮抗剂方案比较,故在Gn用药量及Gn用药时间上未能体现优势,亦未能进行基于对照组不同的超排卵方案以及不同研究群体的亚组分析,这些在下一步研究累积后或许可以实施。⑤由于本研究纳入文献数目少,未能进行有意义的发表偏倚的评价。虽然研究存在缺陷不足,但现有的资料还是为设计后续研究提供了一个良好的基础,在未来的研究中希望可以纳入更多的患者来进一步明确该方案对卵巢低反应患者的疗效。
综上所述,控制性促排卵方案是IVF治疗关键所在,致力于找出能有最高妊娠率、活产率及最低周期取消率、OHSS风险的方案是当务之急[21]。当前证据表明:GnRH-a联合GnRH-ant超短方案对卵巢低反应患者在获卵数、受精率、临床妊娠率上稍优于其他促排卵方案,且在各文献中可看出,其成功运用于卵巢反应差[6]、胚胎质量差[7]及反复IVF失败的患者[8]。基于GnRH-a联合GnRH-ant超短方案的优点,希望有更多大样本、多中心的高质量前瞻性随机对照试验去阐明其在卵巢低反应患者临床治疗中的作用,并与其他促排卵方案比较其功效。
| [1] | ZEGERS-HOCHSCHILD F, ADAMSON G D, DE MOUZON J, et al. International committee for monitoring assisted reproductive technology (ICMART) and the world health organization (WHO) revised glossary of ART terminology[J]. Fertil Steril, 2009, 92(5): 1520–1524. DOI:10.1016/j.fertnstert.2009.09.009 |
| [2] | PENZIAS A S. Improving results with assisted reproductive technologies: individualized patient-tailored strategies for ovulation induction[J]. Reprod Biomed Online, 2004, 9(1): 43–46. DOI:10.1016/s1472-6483(10)62108-6 |
| [3] | LAMBALK C B, BANGA F R, HUIRNE J A, et al. GnRH antagonist versus long agonist protocols in IVF: a systematic review and meta-analysis accounting for patient type[J]. Hum Reprod Update, 2017, 23(5): 560–579. DOI:10.1093/humupd/dmx017 |
| [4] | ORVIETO R, PATRIZIO P. GnRH agonist versus GnRH antagonist in ovarian stimulation: an ongoingdebate[J]. Reprod Biomed Online, 2013, 26(1): 4–8. DOI:10.1016/j.rbmo.2012.11.001 |
| [5] | ORVIETO R, LAUFER N. Ultrashort flare gonadotropin-releasing hormone (GnRH) agonist/GnRH antagonist protocol: a valuable tool in the armamentarium of ovulation induction for in vitro fertilization[J]. Fertil Steril, 2014, 102(5): 1254–1255. DOI:10.1016/j.fertnstert.2014.09.003 |
| [6] | ORVIETO R, Kruchkovich J, Rabinson J, et al. Ultrashort gonadotropin-releasing hormone agonist combined with flexible multidose gonadotropin-releasing hormone antagonist for poor responders in in vitro fertilization/embryo transfer programs[J]. Fertil Steril, 2008, 90(1): 228–230. DOI:10.1016/j.fertnstert.2007.06.022 |
| [7] | ORVIETO R, NAHUM R, RABINSON J, et al. Ultrashort flare GnRH agonist combined with flexible multidose GnRH antagonist for patients with repeated IVF failures and poor embryo quality[J]. Fertil Steril, 2009, 91(4 Suppl): 1398–1400. DOI:10.1016/j.fertnstert.2008.04.064 |
| [8] | ORVIETO R, MELTCER S, LIBERTY G, et al. A combined approach to patients with repeated IVF failures[J]. Fertil Steril, 2010, 94(6): 2462–2464. DOI:10.1016/j.fertnstert.2010.03.057 |
| [9] | BERKER B, ILTEMIR DUVAN C, KAYA C, et al. Comparison of the ultrashort gonadotropin-releasing hormone agonist-antagonist protocol with microdose flare -up protocol in poor responders: a preliminary study[J]. J Turk Ger Gynecol Assoc, 2010, 11(4): 187–193. DOI:10.5152/jtgga.2010.35 |
| [10] | EFTEKHAR M, MOHAMMADIAN F, YOUSEFNEJAD F, et al. Microdose GnRH agonist flare-up versus ultrashort gnRH agonist combined with fixed GnRH antagonist in poor responders of assisted reproductive techniques cycles[J]. Int J Fertil Steril, 2013, 6(4): 266–271. |
| [11] | ORVIETO R, NAHUM R, ZOHAV E, et al. GnRH-agonist ovulation trigger in patients undergoing controlled ovarian hyperstimulation for IVF with ultrashort flare GnRH-agonist combined with multidose GnRH-antagonist protocol[J]. Gynecol Endocrinol, 2013, 29(1): 51–53. DOI:10.3109/09513590.2012.705376 |
| [12] | GRIESINGER G, DIEDRICH K, TARLATZIS B C, et al. GnRH-antagonists in ovarian stimulation for IVF in patients with poor response to gonadotrophins, polycystic ovary syndrome, and risk of ovarian hyperstimulation: a meta-analysis[J]. Reprod Biomed Online, 2006, 13(5): 628–638. DOI:10.1016/S1472-6483(10)60652-9 |
| [13] | BEN-RAFAEL Z, LIPITZ S, BIDER D, et al. Ovarian hyporesponsiveness in combined gonadotropin-releasing hormone agonist and menotropin therapy is associated with low serum follicle-stimulating hormone levels[J]. Fertil Steril, 1991, 55(2): 272–275. DOI:10.1016/s0015-0282(16)54114-4 |
| [14] | SHEEHAN K L, CASPER R F, YEN S S. Induction of luteolysis by luteinizing hormone-releasing factor (LRF) agonist: sensitivity, reproducibility, and reversibility[J]. Fertil Steril, 1982, 37(2): 209–212. DOI:10.1016/S0015-0282(16)46041-3 |
| [15] | MAHUTTE N G, Arici A. Role of gonadotropin-releasing hormone antagonists in poor responders[J]. Fertil Steril, 2007, 87(2): 241–249. DOI:10.1016/j.fertnstert.2006.07.1457 |
| [16] | FASOULIOTIS S J, LAUFER N, SABBAGH-EHRLICH S, et al. Gonadotropin-releasing hormone (GnRH)-antagonist versus GnRH-agonist in ovarian stimulation of poor responders undergoing IVF[J]. J Assist Reprod Genet, 2003, 20(11): 455–460. DOI:10.1023/b:jarg.0000006707.88826.e7 |
| [17] | MALMUSI S, LA MARCA A, GIULINI S, et al. Comparison of a gonadotropin-releasing hormone (GnRH) antagonist and GnRH agonist flare-up regimen in poor responders undergoing ovarian stimulation[J]. Fertil Steril, 2005, 84(2): 402–406. DOI:10.1016/j.fertnstert.2005.01.139 |
| [18] | SCOTT R T, NAVOT D. Enhancement of ovarian responsiveness with microdoses of gonadotropin-releasing hormone agonist during ovulation induction for in vitro fertilization[J]. Fertil Steril, 1994, 61(5): 880–885. DOI:10.1016/s0015-0282(16)56700-4 |
| [19] | SURREY E S, BOWER J, HILL D M, et al. Clinical and endocrine effects of a microdose GnRH agonist flare regimen administered to poor responders who are undergoing in vitro fertilization[J]. Fertil Steril, 1998, 69(3): 419–424. DOI:10.1016/S0015-0282(97)00575-X |
| [20] | KAHRAMAN K, BERKER B, ATABEKOGLU C S, et al. Microdose gonadotropin-releasing hormone agonist flare-up protocol versus multiple dose gonadotropin-releasing hormone antagonist protocol in poor responders undergoing intracytoplasmic sperm injection-embryo transfer cycle[J]. Fertil Steril, 2009, 91(6): 2437–2444. DOI:10.1016/j.fertnstert.2008.03.057 |
| [21] | SIGHINOLFI G, GRISENDI V, LA MARCA A. How to personalize ovarian stimulation in clinical practice[J]. J Turk Ger Gynecol Assoc, 2017, 18(3): 148–153. DOI:10.4274/jtgga.2017.0058 |



