近年来,肿瘤组织新血管生成与肝癌发生、发展及转移的相关性成为研究热点,血管内皮生长因子(vascular endothelial growth factor, VEGF)、血小板-内皮细胞黏附分子(CD31)[1-2]。已有一部分临床研究对VEGF、CD31在乳腺癌、结直肠癌等恶性肿瘤疾病病理组织中的表达特征进行分析,并观察了化疗药物对两者表达水平的影响[3-4]。但关于VEGF、CD31在肝癌病理组织中表达特征的研究却鲜有报道。苦参素和顺铂均为现阶段我国临床上应用较为广泛的化疗药物。本研究对苦参素与顺铂合用对人肝癌裸鼠皮下移植瘤组织VEGF、CD31表达的影响及临床意义进行探讨,现将研究内容进行以下报告。
1 资料与方法 1.1 一般资料细胞株:人肝癌细胞株HepG2,购自中科院上海细胞库。
实验动物:雄性SPF级雄性裸鼠40只,6周龄,体重18~22 g,由我院动物实验中心提供,饲养室温19~24 ℃,相对湿度30%~70%,每笼5只。
1.2 研究方法 1.2.1 人肝癌裸鼠模型建立将人肝癌细胞株HepG2培养至对数生长期后,加入25%胰酶消化后使用离心机进行离心,使用磷酸缓冲盐溶液制作成细胞悬液,细胞浓度为2.5×107 mL。对裸鼠右腋部进行消毒,使用带6号针头的注射器抽取0.2 mL细胞悬液给予裸鼠皮下注射,注射后定期观察肿瘤生长情况,当所有裸鼠肿瘤直径达到5 mm时,将40只裸鼠随机分为对照组、苦参素组、顺铂组、联合组,每组各10只。
1.2.2 给药方法苦参素组:给予该组裸鼠腹腔注射苦参素(批准文号:国药准字H20058750;生产单位:江西天施康中药股份有限公司; 药品特性:化学药品,2 mL :0.2 g),剂量为100 mg/kg,每周连续给药5 d,用药2周。
顺铂组:给予该组裸鼠腹腔注射顺铂(批准文号:国药准字H20043889;生产单位:云南生物谷灯盏花药业有限公司; 药品特性:化学药品,2 mL :10 mg)剂量为2 mg/kg,每周连续给药5 d,用药2周。
联合组:给予该组裸鼠腹腔注射苦参素组(100 mg/kg)、顺铂(2 mg/kg),每周连续给药5 d,用药2周。
对照组:给予该组裸鼠腹腔注射生理盐水,剂量为10 mg/kg,每周连续给药5 d,用药2周。
1.2.3 VEGF、CD31检测给药结束后第15天将4组裸鼠处死,分离皮下移植瘤组织,放置在液氮中,保存在-80 ℃的冰箱中。将肿瘤组织切成连续5 μm的切片,石蜡包埋,过夜后常规脱蜡,使用0.3%H2O2孵育30 min,将内源性过氧化物酶阻断,使用磷酸缓冲盐溶液冲洗3次,每次5 min,将切片浸入pH值为6.0的柠檬酸盐抗原修复液中经微波加热至95 ℃,保温10 min,在室温中自然冷却,再次使用磷酸缓冲盐溶液冲洗3次,每次5 min,滴加一抗(鼠抗人单克隆抗体),放置在湿盒中,4 ℃孵育过夜。阴性对照,使用磷酸缓冲盐溶液代替一抗。过夜后使用磷酸缓冲盐溶液冲洗3次,每次5 min,滴加经生物素标记的二抗,室温中孵育30 min,再次冲洗。DAB显色,充分水洗,苏木液复染,充分水洗,酒精脱水,使用中性树脂封片,选择10个高倍镜视野进行计数,观察VEGF、CD31表达情况。
VEGF阳性判定标准:VEGF细胞质出现棕黄颗粒为阳性表达,阳性细胞所占比例≥10即判定为阳性表达。
CD31阳性判定标准:CD31细胞膜出现棕黄色为阳性表达,阳性细胞所占比例≥5即判定为阳性表达。
1.3 观察指标本研究对比4组裸鼠皮下移植瘤体积以及肿瘤组织中VEGF、CD31的表达情况。
皮下移植瘤体积计算公式为:V=1/2×a×b2,其中a、b分别为肿瘤长径和肿瘤短径。
1.4 统计学分析基于SPSS 22.0版本统计学软件建立数据统计分析模型,计数型资料采用例数和率(%)的形式描述,采用卡方(χ2)检验资料间差异,计量资料采用x±s的形式描述,采用配对t检验,P值小于0.05表示两者之间存在的差异具有统计学意义。
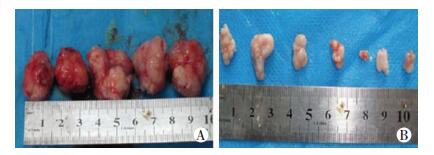
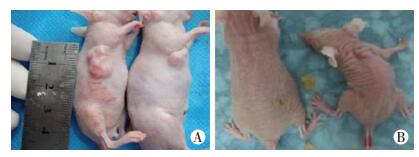
2 结果 2.1 4组裸鼠皮下移植瘤体积比较联合组裸鼠皮下移植瘤体积较其他3组裸鼠小(P < 0.05),见图 1~3。
|
| A:对照组,B:联合组 图 1 对照组与联合组裸鼠离体肿瘤体积比较 |
|
| A:苦参素组(左)与联合组(右); B:联合组与(左)与顺铂组(右) 图 2 各组裸鼠给药后15 d在体肿瘤比较 |

|
| a:t=11.926,P=0.000,与苦参素组比较; b:t=10.450,P=0.000,与顺铂组比较; c: t=17.583,P=0.000,与对照组比较 图 3 四组裸鼠皮下移植瘤体积比较 |
2.2 4组裸鼠皮下移植瘤组织中VEGF的表达情况
联合组裸鼠的VEGF阳性表达率明显低于其他3组裸鼠(P < 0.05),具体数据见表 1所示,免疫组化分析结果见图 4所示。
| 组别 | 阳性 | 阴性 |
| 苦参素组 | 8(80.00) | 2(20.00) |
| 顺铂组 | 7(70.00) | 3(30.00) |
| 联合组 | 2(20.00)a | 8(80.00) |
| 对照组 | 10(100.00) | 0(0.00) |
| a:联合组VEGF阳性检出率与苦参素组比较χ2=7.200;P=0.007,与顺铂组比较χ2=5.051;P=0.025,与对照组比较比较χ2=13.333;P=0.000 | ||

|
| A:苦参素组; B:顺铂组; C:联合组; D:对照组 图 4 各组裸鼠皮下移植瘤组织VEGF表达的免疫组化观察 (×200) |
2.3 四组裸鼠皮下移植瘤组织中CD31的表达情况
联合组裸鼠的CD31阳性表达率明显低于其他3组裸鼠(P < 0.05),具体数据见表 2所示,免疫组化分析结果见图 5所示。
| 组别 | 阳性 | 阴性 |
| 苦参素组 | 9(90.00) | 1(10.00) |
| 顺铂组 | 7(70.00) | 3(30.00) |
| 联合组 | 3(30.00)a | 7(70.00) |
| 对照组 | 10(100.00) | 0(0.00) |
| a:联合组CD31阳性检出率与苦参素组比较χ2=7.500;P=0.006,与顺铂组比较χ2=4.967;P=0.031,与对照组比较比较χ2=10.769;P=0.001 | ||
|
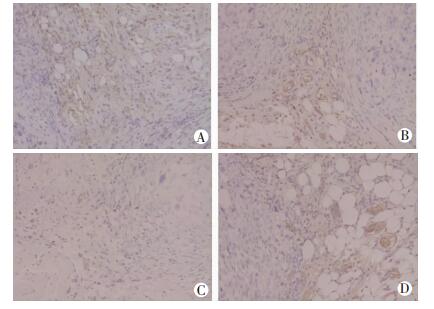
| A:苦参素组; B:顺铂组; C:联合组; D:对照组 图 5 各组裸鼠皮下移植瘤组织CD31表达的免疫组化观察 (×200) |
3 讨论
虽然世界各国医疗领域在肝癌方面已经取得了可喜的研究进展,但现阶段肝癌仍是危害人类生命健康的主要恶性肿瘤疾病,距统计全球范围内每年约有69万人死于肝癌,其中约有50%的患者在我国[5-6]。目前,被世界广泛认可的肝癌治疗方式为手术、放疗、化疗等。由于受多种因素的影响,一部分患者难以耐受手术,多选择接受化疗,常用的药物包括顺铂、苦参素等[7-9]。
顺铂是现阶段我国临床上应用较广泛的一线抗癌药物,抗癌功效可靠,当大剂量使用易发生毒副反应。苦参素为从中药中提取的以红车轴草苷、黄酮类化合物、氧化苦参碱为主要成分的生物碱。大量药理研究已经证实,该药物对直肠癌、肝癌、胃癌等细胞均具有较强的杀伤力,且与顺铂联合应用能够发挥中和药性的效果,在不影响患者化疗疗效的同时,能够减轻顺铂的毒副作用。
本研究分析苦参素与顺铂合用对人肝癌裸鼠皮下移植瘤组织VEGF、CD31表达的影响。我国医疗领域关于VEGF的研究较多,关于CD31的研究相对较少。VEGF是血管生成过程中的主要促进因子,肿瘤细胞产生的VEGF能够以自分泌的方式作用于肿瘤细胞半身,促进肿瘤细胞增生,或通过旁分泌的方式促进血管内皮分裂,增加血管通透性。研究证实该因子在多种恶性肿瘤病理组织有表达,其阳性表达率升高往往代表恶性肿瘤细胞的血管生成能增强,发生细胞转移的风险增大[10-11]。CD31主要分布在脉管细胞上,既往研究证实CD31与内皮细胞运动及血管生成均存在密切关系,参与和介导了多种肿瘤细胞黏附在内皮细胞上的过程,其阳性表达能够促进恶性肿瘤细胞的转移[12-13]。多数研究学者认为,两者的表达变化能够在一定程度上反映肿瘤在机体内的生长情况[14-15]。为进一步验证苦参素与顺铂联合对肝癌细胞的作用,并初步探讨其机制是否是通过影响肿瘤血管生成而发挥,明确两者在肿瘤组织中表达的临床意义,我院开展了动物研究。
本研究结果显示联合组裸鼠的给药15 d后的移植瘤体积明显小于其他3组裸鼠,VEGF、CD31阳性表达率均较苦参素组、顺铂组和对照组裸鼠低,存在的差异具有统计学意义。分析得到上述研究结果的原因可能为:顺铂对肿瘤DNA的复制作用并无特异性,在发挥抑制肿瘤增殖作用的同时,也会造成正常细胞的死亡,故VEGF、CD31的阳性表达率仍然较高。苦参素的肿瘤抑制作用不及顺铂,但两者联合应用能够发挥协同作用。对上述研究结果进行分析和总结,本研究得出苦参素与顺铂联合应用,能够有效抑制VEGF、CD31的表达,发挥良好的抗肝癌效果。
| [1] |
张中林, 毛晓雯, 张吉发, 等. 人促血管生成素2单链抗体对裸鼠人肝癌血管生成及肿瘤生长的作用[J].
中华实验外科杂志, 2013, 30(8): 1642–1645.
ZHANG Z L, MAO X W, ZHANG J F, et al. Effects of angiopoietin 2 single-chain antibody on human hepatocellular carcinoma in nude mice[J]. Chin J Exp Surg, 2013, 30(8): 1642–1645. DOI:10.3760/cma.j.issn.1001-9030.2013.08.028 |
| [2] |
周佳美, 向慧玲, 朱争艳, 等. 大鼠CBRH-7919肝癌细胞诱导大鼠骨髓间充质干细胞向血管内皮细胞分化的初步研究[J].
中国现代医学杂志, 2012, 22(29): 21–25.
ZHOU J M, XIANG H L, ZHU Z Y, et al. Differentiation of bone marrow mesenchymal stem cells into endothelial cells induced by rat CBRH-7919 hepatoma cells in vitro[J]. Chin J Mod Med, 2012, 22(29): 21–25. DOI:10.3969/j.issn.1005-8982.2012.29.005 |
| [3] | Cristina C, Perez-Millan MI, Luque G, et al. VEGF and CD31 association in pituitary adenomas[J]. Endocr Pathol, 2010, 21(3): 154–160. DOI:10.1007/s12022-010-9119-6 |
| [4] |
徐昊平, 郭睿, 金冶宁, 等. 肺腺癌靶向基因放射治疗的体内研究及小动物正电子发射计算机体层摄影评价疗效的可行性[J].
中华肿瘤杂志, 2014, 36(5): 329–334.
XU H P, GUO R, JIN Y Y, et al. Gene-targeted radiation therapy mediated by radiation-sensitive promoter in lung adenocarcinoma and the feasibility of micro-PET/CT in evaluation of therapeutic effectiveness in small animals[J]. Chin J Oncol, 2014, 36(5): 329–334. DOI:10.3760/cma.j.issn.0253-3766.2014.05.003 |
| [5] |
刘翠云, 董惠, 成慧, 等. 探讨nm23-H1、VEGF-C和CD31在甲状腺乳头状癌中表达的相关性[J].
诊断病理学杂志, 2017, 24(4): 284–287.
LIU C Y, DONG H, CHENG H, et al. Correlation between VEGF-C, nm23-H1 and CD31 in papillary thyroid carcinoma[J]. Chin J Diagn Pathol, 2017, 24(4): 284–287. DOI:10.3969/j.issn.1007-8096.2017.04.013 |
| [6] |
李明琰, 何文凯, 陈建威, 等. Ad-HIF-1α-Trip肌肉注射对大鼠缺血肢体血管新生和血液灌注的影响[J].
第三军医大学学报, 2012, 34(15): 1518–1522.
LI M Y, HE W K, CHEN J W, et al. Effects of Ad-HIF-1α-Trip transfer on angiogenesis and blood perfusion in a rat model of hind limb ischemia[J]. J Third Mil Med Univ, 2012, 34(15): 1518–1522. |
| [7] | Kasprzak A, Surdacka A, Tomczak M, et al. Expression of angiogenesis-stimulating factors (VEGF, CD31, CD105) and angiogenetic index in gingivae of patients with chronic periodontitis[J]. Folia Histochem Cytobiol, 2012, 50(4): 554–564. DOI:10.5603/20324 |
| [8] |
符黄德, 罗起胜, 邓元央, 等. 肝癌衍生生长因子和血管内皮生长因子在脑胶质瘤中的表达及其与肿瘤微血管密度的相关性研究[J].
中国全科医学, 2016, 19(17): 2019–2023.
FU H D, LUO Q S, DENG Y Y, et al. Expression of Hepatoma-derived Growth Factor and Vascular Endothelial Growth Factor and Their Correlation With Tumor Microvessel Density in Gliomas[J]. Chin Gen Pract, 2016, 19(17): 2019–2023. DOI:10.3969/j.issn.1007-9572.2016.17.008 |
| [9] |
司春枫, 鲁美钰, 王巧云, 等. VEGF融合蛋白疫苗联合环磷酰胺抗小鼠H22肝癌实验研究[J].
中国药理学通报, 2017, 33(5): 617–621.
SI C F, LU M Y, WANG Q Y, et al. Improved antitumor efficacy by combinationtreatment with recombined VEGF protein vaccineand cyclophosphamide in H22 hepatocellular carcinoma bearing-mice[J]. Chin Pharmacul Bull, 2017, 33(5): 617–621. DOI:10.3969/j.issn.1001-1978.2017.05.006 |
| [10] |
耿良, 范敬, 高启龙, 等. 人参皂苷Rg3和PEG-PLGA-Rg3纳米微粒对Lewis肺癌小鼠的作用及其机制[J].
北京大学学报(医学版), 2016, 48(3): 496–501.
GENG L, FAN J, GAO Q L, et al. Preliminary study for the roles and mechanisms of 20(R)-ginsenoside Rg3 and PEG-PLGA-Rg3 nanoparticles in the Lewis lung cancer mice[J]. J Peking Univy(Health Sci), 2016, 48(3): 496–501. DOI:10.3969/j.issn.1671-167X.2016.03.021 |
| [11] |
胡哲, 王培恩, 瞿海江. TACE联合索拉菲尼治疗晚期肝癌患者的疗效及对血清VEGF、CTGF、HIF-1α及OPN水平的影响[J].
中国生化药物杂志, 2017, 38(4): 345–347, 350.
HU Z, WANG P E, QU H J. The dynamic changes of serum VEGF, CTGF, HIF-1 and OPN levels in patients with advanced liver cancer treated with Sola Feeney combined with TACE[J]. Chin J Biochem Pharm, 2017, 38(4): 345–347, 350. DOI:10.3969/j.issn.1005-1678.2017.04.114 |
| [12] |
王启船, 王青, 万里新, 等. 食管鳞癌中T淋巴瘤侵袭转移诱导基因1、血管内皮生长因子和CD31的表达及其相关性研究[J].
中国医药导报, 2012, 9(23): 95–96.
WANG Q C, WANG Q, WAN L X, et al. The study of expression of Tiam1, VEGF and CD31 in esophageal squamous cell carcinoma and their correlations of them[J]. Chin Med Herald, 2012, 9(23): 95–96. DOI:10.3969/j.issn.1673-7210.2012.23.040 |
| [13] |
王刚, 程雪, 张祥林, 等. shRNA-CXCR7联合TRAIL对人肝癌SMMC-7721细胞裸鼠皮下移植瘤生长的影响[J].
中国生化药物杂志, 2016, 37(1): 28–31.
WANG G, CHENG X, ZHANG X L, et al. Effect of shRNA-CXCR7 combined with TRAIL on subcutaneous transplantation tumor of SMMC-7721 cell line in nude mice[J]. Chin J Biochem Pharm, 2016, 37(1): 28–31. |
| [14] |
高军, 祝小英, 石庆芳, 等. 沙利度胺联合表阿霉素对小鼠H22肝癌移植瘤的生长抑制研究[J].
中国临床药理学杂志, 2016, 32(2): 170–173.
GAO J, ZHU X Y, SHI Q F, et al. Mechanism and inhibition of thalidomide combined with epirubicine on the growth of transplanted H22 hepatocellular carcinoma in mice[J]. Chin J Clin Pharmacol, 2016, 32(2): 170–173. DOI:10.13699/j.cnki.1001-6821.2016.02.024 |
| [15] |
方蕾, 赵展, 吴乾能, 等. 恩度联合TACE术治疗肝癌对患者血清VEGF、HIF-1A、OPN、MMP-9的影响及意义[J].
中华全科医学, 2016, 14(3): 412–414.
FANG L, ZHAO Z, WU Q N, et al. Influence and significance of hepatic transcatheter arterial chemoembolization combime with endostar on levels of serum VEGF, HIF-1A, OPN and MMP-9 in patients with hepatocellular carcinoma[J]. Chin J Gen Pract, 2016, 14(3): 412–414. DOI:10.16766/j.cnki.issn.1674-4152.2016.03.025 |



