2. 610064 成都,四川大学国家生物医学材料工程技术研究中心
2. National Engineering Research Center of Biomaterials, Sichuan University, Chengdu, Sichuan Province, 610064, China
创面是由物理或热等因素导致的皮肤或黏膜损伤。理想的创面敷料应具有多孔结构、良好的力学性能、高持水性、无毒、良好的组织相容性和抗菌活性等特点[1]。细菌纤维素膜(bacterial cellulose membrane,BCM)具有良好的力学性能、高持水性和组织相容性等优点,在组织工程支架、人工皮肤等方面具有广泛的应用前景,是目前生物医用材料研究的热点领域[2-3]。纳米氧化锌(zinc oxide nanoparticles,nZnO)具有抗菌活性强和细胞毒低等特点[4],同时锌也是创面愈合的必需微量营养元素,在组织再生方面具有重要作用[5-7]。本研究探讨nZnO/BCM的原位合成,评价其物理特性与抗菌性能,旨在研发一种具有抗感染作用的新型复合敷料nZnO/BCM,以期最终作为新型医用敷料应用于创面治疗。
1 材料与方法 1.1 主要材料BALB/c小鼠(第三军医大学实验动物中心),金黄色葡萄球菌(ATCC25923, 美国典型菌种保藏中心), 大肠杆菌(ATCC25923, 美国典型菌种保藏中心), 细菌纤维素膜(海南光宇生物科技有限公司), 无水醋酸锌(上海Aladdin公司),氯化锂(成都科隆化学品有限公司),扫描电子显微镜(S-3000N型,日本HITACHI公司), 动态机械分析仪(Q800型, 美国TA公司)。
1.2 nZnO/BCM复合膜的制备采用两步法进行nZnO/BCM复合膜的制备(专利号:ZL201510301459.X)。第一步,BCM的化学修饰改性,即在BCM分子侧链上引入羧基以增强后续nZnO原位合成过程中nZnO与BCM结合的稳定性。将BCM在室温下浸泡于溶胀溶液(含5.0%氯化锂的二甲基乙酰胺)中8~12 h,使BCM溶胀。然后,将量浓度为细菌纤维素中羟基7.5倍的马来酸加入体系中,60 ℃下磁力搅拌反应3 h。反应结束后,以无水乙醇充分洗涤,然后冷冻干燥,得到改性后的BCM。第二步,nZnO的原位合成。以改性后的BCM为反应模板,将其浸入0.02 mol/L醋酸锌无水乙醇溶液中,于50 ℃下反应1 h,使醋酸锌渗入细菌纤维素三维网架中;然后将0.08 mol/L氢氧化钠乙醇溶液缓慢加入反应体系,于50 ℃下温和搅拌反应2 h。反应结束后,用去离子水彻底冲洗并进行冷冻干燥,于120 ℃烤箱中继续干燥1 h,最终制备出nZnO/BCM复合膜。采用原子吸收光谱法测定nZnO/BCM复合膜的nZnO含量。
1.3 扫描电子显微镜观察将合成的nZnO/BCM复合膜切割成3 mm×3 mm小片,在真空中涂覆金钯,然后于扫描电子显微镜下观察nZnO/BCM复合膜的纤维网络、孔隙以及nZnO颗粒分布与尺寸大小等。
1.4 nZnO结合稳定性检测以BCM为对照,采用先高压灭菌后浸提的方法评价nZnO/BCM复合膜中nZnO的结合稳定性。将样品浸泡在PBS中,置于高压灭菌器中121 ℃灭菌30 min。然后,将样品置于恒温振荡器中37 ℃下振荡24 h。采用原子吸收光谱法测定并对比处理前后样品中氧化锌含量,评估nZnO的结合稳定性。
1.5 力学性能检测以BCM为对照,将样品切成哑铃形,采用动态机械分析仪进行拉伸试验,测量样品的力学性能,包括抗张强度、杨氏模量以及断裂伸长率。
1.6 水蒸气透过率检测水蒸气透过率检测实验方法参考美国材料和试验协会标准进行测量。以BCM为对照,将样品切成直径为35 mm的圆形,置于直径为34 mm的含有10 mL去离子水的圆筒形杯的口部。用特氟龙胶带密封样品与杯口接触边缘,置于37 ℃、50%相对湿度的培养箱中24 h,然后测量去离子水含量变化。
1.7 抗菌活性评价实验采用振荡抑菌实验评价nZnO/BCM的抗菌活性。将金黄色葡萄球菌和大肠杆菌接种于灭菌的LB肉汤,于振荡培养箱中培养过夜(37 ℃)。调整细菌悬液浓度至106 CFU/mL,按3 cm2 nZnO/BCM :1 mL细菌悬液(106 CFU/mL),于37 ℃、180 r/min条件下振荡培养24 h,然后将细菌悬液倍比稀释,取不同稀释后的细菌悬液100 μL涂布于LB琼脂平板,37 ℃培养24 h,进行菌落计数并按以下公式计算抗菌率。以LB培养基正常培养的细菌为空白对照组。抑菌率=(空白对照组菌液浓度-实验组菌液浓度)/空白对照组菌液浓度×100%。
1.8 统计学分析采用SPSS 17.0统计软件,数据以x±s表示,结合稳定性、水蒸气透过率力学性能检测组间比较行t检验,抑菌作用评价组间比较行单因素方差分析。检验水准:α=0.05。
2 结果 2.1 nZnO/BCM复合膜的形态及nZnO分布扫描电子显微镜结果显示:BCM干膜的纤维排列紧密,形成网络结构,纤维之间孔隙小、孔隙密度低。制备的nZnO/BCM经冷冻干燥后,其纤维呈立体网络结构,孔隙大小和密度均显著大于BCM;可见球状nZnO附于纤维,形成独特的串珠形态,nZnO直径为30~90 nm(图 1)。

|
| A:BCM箭头示细菌纤维素;B:nZnO/BCM箭头示氧化锌纳米颗粒 图 1 扫描电子显微镜下观察nZnO/BCM复合膜的形态和nZnO分布 |
2.2 nZnO/BCM复合膜中nZnO的结合稳定性
高压蒸汽灭菌后浸提实验检测nZnO/BCM复合膜的结合稳定性,结果显示:处理前nZnO/BCM复合膜中nZnO的含量为(40.07±0.21)%,处理后nZnO/BCM复合膜中nZnO的含量为(36.47±1.79)%, 处理后nZnO/BCM仅有8.98%的nZnO脱失(P=0.375)。提示采用的二步法原位合成的nZnO/BCM具有良好的结合稳定性。
2.3 nZnO/BCM复合膜的透气性以BCM为对照,对nZnO/BCM复合膜的透气性进行检测。结果显示:nZnO/BCM复合膜的水蒸气透过率为2 856.60 g/(m2·d),高于BCM[2 506.56 g/(m2·d),P < 0.05]。
2.4 nZnO/BCM复合膜的力学性能动态机械分析仪检测样品力学性能,结果显示:nZnO/BCM复合膜的平均抗张强度为(29.68±4.82)MPa,显著高于BCM[(23.17±1.81)MPa, P < 0.05];nZnO/BCM复合膜的杨氏模量为(2 387.41±507.17)MPa,显著高于BCM[(1 280.28±595.49)MPa, P < 0.05];nZnO/BCM复合膜和BCM的断裂伸长率差异无统计学意义,均约为1.30%(P=0.889)。
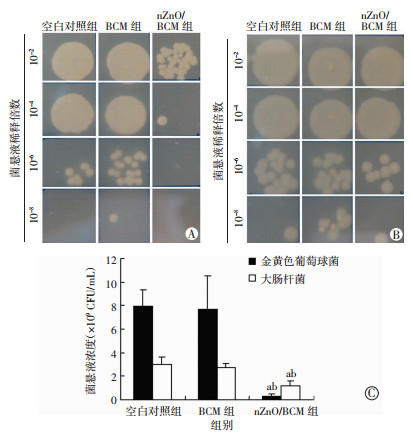
2.5 nZnO/BCM复合膜的抗菌性能nZnO/BCM组的金黄色葡萄球菌、大肠杆菌浓度显著低于空白对照组和BCM组(P < 0.05,图 2)。nZnO/BCM组对金黄色葡萄球菌的抑菌率为96.72%,对大肠杆菌的抑菌率为60.14%。而BCM组对金黄色葡萄球菌和大肠杆菌均无抗菌活性。
|
| A:与样品混合培养后的金黄色葡萄球菌;B:与样品混合培养后的大肠杆菌;C:nZnO/BCM抗菌性能分析a:P < 0.05,与空白对照组比较;b:P < 0.05,与BCM组比较 图 2 nZnO/BCM复合膜对金黄色葡萄球菌和大肠杆菌的体外抑菌作用 |
3 讨论
BCM由于其良好的性能,已作为原材料被应用于医疗产品开发,包括医用敷料[8-10]。然而,BCM以及目前基于BCM开发的医用敷料均无抗菌性能。本研究将具有抗菌活性的nZnO与BCM结合形成具有抗菌活性的nZnO/BCM复合膜,为开发具有抗菌活性的BCM功能性新型医用敷料奠定基础。
以BCM为模板原位合成nZnO是制备nZnO/BCM复合膜的方法之一[11]。为提高nZnO在BCM上的结合稳定性,本研究在进行nZnO的原位合成前,先对BCM进行化学修饰改性,即通过一定的反应体系,在BC分子的侧链上引入羧基。根据分析计算,引入的羧基与nZnO的结合能力约为BC分子上羟基与nZnO的结合能力的5倍。因此,本研究采用先对BCM进行化学改性,然后再进行nZnO原位合成的方法(即二步法),理论上有利于提高nZnO与BCM的结合稳定性。本研究检测了nZnO含量为40%的nZnO/BCM复合膜的物理特性、nZnO与BCM结合的稳定性和抗菌性能。电镜观察显示,BCM干膜的纤维束排列紧密,孔隙小且密度低;通过二步法获得的nZnO/BCM复合膜的孔隙大小和密度均显著增强。这主要与对BCM进行化学改性时的溶胀处理能打断BCM纤维之间氢键,从而有效降低BCM的结晶度有关。进一步研究发现:纳米尺度的球状nZnO附着于BCM纤维,形成独特的串珠形态,提示nZnO在BCM上的原位合成取得成功。我们采用二步法制备的nZnO/BCM复合膜,其nZnO的脱失率小于10%,显著低于文献[12]报道的方法,表明本研究制备nZnO/BCM复合膜的方法有利于稳定维持nZnO的含量,从而有利于其作用的持续发挥。研究表明医用敷料较适合的水蒸气透过率为2 500~3 000 g/(m2·d)[13]。本研究制备的nZnO/BCM复合膜具有高孔隙率的三维立体空间结构,该结构有利于提高复合膜的透气性。nZnO/BCM复合膜(含40% nZnO)的水蒸气透过率为2 856.60 g/(m2·d),高于单纯BCM的水蒸气透过率,提示nZnO/BCM复合膜有利于维持创面愈合所需要的湿润微环境。进一步分析nZnO/BCM复合膜的物理特性,发现nZnO/BCM复合膜的抗张强度和杨氏模量较单纯BCM明显提高,而断裂伸长率无明显变化,提示nZnO/BCM复合膜的物理特性得到进一步改善,可能与nZnO/BCM复合膜上nZnO沿附于BCM纤维呈串珠状排列有关。该排列结构使得BCM的纤维结构对抗拉伸的能力得到增强,从而表现出物理力学特性的改善。nZnO/BCM复合膜的抗张强度(29.68 MPa)、杨氏模量(2 387.41 MPa)也显著高于现有商品化的创面敷料。如IntegraTM(抗张强度:0.63 MPa,杨氏模量:1.56 MPa)[14]和KaltostatTM(抗张强度:0.9 MPa,杨氏模量:1.3 MPa)[15]。这提示本研究合成的nZnO/BCM复合膜具有良好的物理力学性质。nZnO通过产生ROS,具有广谱的抗菌活性[16]。本研究制备的nZnO/BCM复合膜具有的高孔隙率三维空间结构也有利于细菌与nZnO的充分接触,从而有利于nZnO/BCM抗菌作用的发挥。本研究结果显示:nZnO/BCM复合膜(含40% nZnO)对创面感染的常见细菌金葡菌和大肠杆菌的抑菌率分别为96.72%、60.14%,证明其良好的抗菌性能。本研究发现nZnO对金葡菌的抑菌率显著高于大肠杆菌,与已有文献[17]报道一致,但其机制有待进一步探讨。
综上所述,本研究采用二步法制备的nZnO/BCM复合膜具有良好的nZnO结合稳定性、孔隙率、水蒸气透过率和物理力学性能,对常见的革兰阳性菌金黄色葡萄球菌和革兰阴性菌大肠杆菌具有较好的抗菌活性。下一步,我们将评估nZnO/BCM复合膜的生物安全性及其促进感染创面愈合的作用,旨在为其临床转化与应用奠定坚实基础。
| [1] | DHIVYA S, PADMA V V, SANTHINI E. Wound dressings:a review[J]. Biomedicine(Taipei), 2015, 5(4): 22. DOI:10.7603/s40681-015-0022-9 |
| [2] | LEE K Y, BULDUM G, MANTALARIS A, et al. More than meets the eye in bacterial cellulose: biosynthesis, bioprocessing, and applications in advanced fiber composites[J]. Macromol Biosci, 2014, 14(1): 10–32. DOI:10.1002/mabi.201300298 |
| [3] | FU L, ZHANG J, YANG G. Present status and applications of bacterial cellulose-based materials for skin tissue repair[J]. Carbohydr Polym, 2013, 92(2): 1432–1442. DOI:10.1016/j.carbpol.2012.10.071 |
| [4] | MOHANDAS A, KUMAR P T S, RAJA B, et al. Exploration of alginate hydrogel/nano zinc oxide composite bandages for infected wounds[J]. Int J Nanomedicine, 2015, 10(Suppl 1): 53–66. DOI:10.2147/IJN.S79981 |
| [5] | LANSDOWM A B, SAMPSON B, ROWE A. Sequential changes in trace metal, metallothionein and calmodulin concentrations in healing skin wounds[J]. J Anat, 1999, 195(Pt 3): 375–386. DOI:10.1046/j.1469-7580.1999.19530375.x |
| [6] | BERGER MM, BINNERT C, CHIOLERO RL, et al. Trace element supplementation after major burns increases burned skin trace element concentrations and modulates local protein metabolism but not whole-body substrate metabolism[J]. Am J Clin Nutr, 2007, 85(5): 1301–1306. |
| [7] | BERGER M M, BAINES M, RAFFOUL W, et al. Trace element supplementation after major burns modulates antioxidant status and clinical course by way of increased tissue trace element concentrations[J]. Am J Clin Nutr, 2007, 85(5): 1293–1300. |
| [8] | LEE K Y, BULDUM G, MANTALARIS A, et al. More than meets the eye in bacterial cellulose: biosynthesis, bioprocessing, and applications in advanced fiber composites[J]. Macromol Biosci, 2014, 14(1): 10–32. DOI:10.1002/mabi.201300298 |
| [9] | CHANG W S, CHEN H. Physical properties of bacterial cellulose composites for wound dressings[J]. Food Hydrocolloids, 2016, 53: 75–83. DOI:10.1016/j.foodhyd.2014.12.009 |
| [10] | FU L, ZHANG J, YANG G. Present status and applications of bacterial cellulose-based materials for skin tissue repair[J]. Carbohydr Polym, 2013, 92(2): 1432–1442. DOI:10.1016/j.carbpol.2012.10.071 |
| [11] | WANG P, ZHAO J, XUAN R, et al. Flexible and monolithic zinc oxide bionanocomposite foams by a bacterial cellulose mediated approach for antibacterial applications[J]. Dalton Trans, 2014, 43(18): 6762–6768. DOI:10.1039/c3dt52858h |
| [12] | SHAHMOHAMMADI JEBEL F, ALMASI H. Morphological, physical, antimicrobial and release properties of ZnO nanoparticles-loaded bacterial cellulose films[J]. Carbohydr Polym, 2016, 149: 8–19. DOI:10.1016/j.carbpol.2016.04.089 |
| [13] | LI J, WAN Y, LI L, et al. Preparation and characterization of 2, 3-dialdehyde bacterial cellulose for potential biodegradable tissue engineering scaffolds[J]. Mater Sci Eng C, 2009, 29(5): 1635–1642. DOI:10.1016/j.msec.2009.01.006 |
| [14] | MADHUMATHI K, SUDHEESH KUMAR P T, ABHILASH S, et al. Development of novel chitin/nanosilver composite scaffolds for wound dressing applications[J]. J Mater Sci Mater Med, 2010, 21(2): 807–813. DOI:10.1007/s10856-009-3877-z |
| [15] | KUMAR P T, LAKSHMANAN V K, BISWAS R, et al. Synthesis and biological evaluation of chitin hydrogel/Nano ZnO composite bandage as antibacterial wound dressing[J]. J Biomed Nanotechnol, 2012, 8(6): 891–900. DOI:10.1166/jbn.2012.1461 |
| [16] | STANKIC S, SUMAN S, HAQUE F, et al. Pure and multi metal oxide nanoparticles: synthesis, antibacterial and cytotoxic properties[J]. J Nanobiotechnology, 2016, 14(1): 73. DOI:10.1186/s12951-016-0225-6 |
| [17] | FU F, LI L, LIU L, et al. Construction of Cellulose Based ZnO Nanocomposite Films with Antibacterial Properties through One-Step Coagulation[J]. ACS Appl Mater Interf aces, 2015, 7(4): 2597–2606. DOI:10.1021/am507639b |



