2.400047 重庆,重庆师范大学教育科学学院, 特殊教育系;
3.400038 重庆,第三军医大学, 西南医院输血科;
4.400038 重庆,第三军医大学, 基础医学部生物化学与分子生物学教研室
2. Faculty of Education for Children with Special Needs, College of Education Science, Chongqing Normal University, Chongqing, 400047;
3. Department of Blood Transfusion, Southwest Hospital, College of Basic Medical Sciences, Third Military Medical University, Chongqing, 400038, China;
4. Department of Biochemistry and Molecular Biology, College of Basic Medical Sciences, Third Military Medical University, Chongqing, 400038, China
孤独症(autism)又称儿童自闭症,是一种脑发育障碍综合征,主要发病对象为儿童,病征包括语言障碍、交往障碍、重复刻板行为等。孤独症的发病率约为2 /1 000~6/1 000[1],男孩高于女孩,我国目前约有60多万孤独症儿童,且发病率呈上升趋势[2]。孤独症的发病原因复杂,涉及免疫、遗传、环境、教育、饮食等诸多方面,至今尚未完全阐明[3]。
研究表明,细胞自噬水平的降低是导致孤独症发病的重要原因[4-5]。在神经组织中条件性敲除自噬关键基因ATG7会导致出生幼鼠的孤独症行为[4],而使用自噬的诱导剂雷帕霉素预处理则会改善大鼠的孤独症病症[5]。我们的前期研究也发现,雷帕霉素预处理可增强大鼠脑组织中的自噬水平,明显改善孤独症大鼠的病症行为[6]。由于白藜芦醇是一种存在于多种植物如葡萄、花生、桑葚、虎杖等中的天然多酚类物质,具有预防多种疾病的药用功能[7],且它在多种细胞中可增强细胞的自噬水平[8-10],因此本研究拟以孤独症大鼠为模型,观察白藜芦醇是否能够通过增强脑组织中细胞自噬水平来改善孤独症大鼠的病症行为。
1 材料与方法 1.1 实验动物成年清洁级雌、雄Wistar大鼠各12只,雄性体质量300~350 g,雌性体质量200~250 g,由第三军医大学实验动物中心提供并饲养。
1.2 药品及试剂丙戊酸钠(sodium valproate,VPA)为Sigma公司产品,SIRT1、LC3抗体、GAPDH抗体为Cell Signaling公司产品,细胞裂解液与BCA蛋白浓度测定试剂盒为江苏碧云天生物技术公司产品,蛋白分子量标准为北京中衫公司产品,PVDF膜为Bio-Rad公司产品。
1.3 动物模型制备与分组按照Schneider等[11]的方法,雌、雄大鼠合笼过夜后发现阴栓者记为妊娠第1天(E1)。把孕鼠分为4组,即对照组、VPA组(即模型组)、白藜芦醇组及VPA联合白藜芦醇组,每组3只。白藜芦醇组与VPA联合白藜芦醇组从E6天开始按照3.6 mg/kg体质量在孕鼠皮下注射白藜芦醇,持续注射13 d,其他两组注射等量生理盐水。VPA组与VPA联合白藜芦醇组在E12.5 d按600 mg/kg剂量一次性腹腔注射VPA;同时给对照组与白藜芦醇组注射等量生理盐水。对照组孕鼠所产仔鼠为正常对照组,而VPA组孕鼠所产仔鼠即为孤独症模型鼠。幼鼠出生的第1天记为P1。各组幼鼠均在出生后23d(P23) 断奶。
1.4 重复行为检测幼鼠出生后35 d,分别从各组选择6只雄性幼鼠进行检测。测试在洁净的旷场箱内进行。被测试鼠首先进行10 min的适应环境,然后摄像记录10 min内测试鼠的行为,再借助Any-Maze软件系统统计分析测试期内被测试鼠用于整理身体毛发的累积时间。
1.5 社会交往行为检测幼鼠出生后35 d,分别从各组选择6只雄性幼鼠进行检测。以大小为60 cm×60 cm×60 cm的透明三室箱为检测场所。被检测鼠于实验前1 d放入检测场所适应环境。检测时被测鼠先在中间小室适应10 min。左侧小室放置空铁丝笼子,右侧小室放置装有陌生幼鼠铁丝笼子。然后打开从中间小室进入左、右小室的隔板,通过摄像记录被检测鼠行为,时间为10 min,然后借助Any-Maze软件系统统计分析被检测鼠嗅陌生鼠(社交行为)的时间。
1.6 神经行为学检测幼鼠出生后35 d进行检测,从对照组与模型组各选5只检测,被检测鼠的选择标准同1.4。检测场地为25 cm×25 cm×38 cm的封闭箱,箱子中央区大小为12 cm×12 cm。检测前1d,被检测鼠放入检测场地适应环境。实验时将被检测鼠置于检测箱中央,摄像记录被检测鼠行为,时间为5 min,然后借助Any-Maze软件系统统计分析被检测鼠直立次数及在中央区活动时间及活动的总路程。
1.7 Western blot检测取出生后35 d的幼鼠,断颈处死,然后立即分离海马、前额叶皮层和小脑组织。将各组织用组织裂解液进行匀浆,然后以12 000 r/min在4 ℃离心30 min。分离上清,测量蛋白浓度后放置于-80 ℃冰箱备用。取总蛋白量为50 μg的组织样品,在SDS-PAGE电泳分离后电转移至PVDF膜上。再用5%脱脂奶粉封闭2 h后加入一抗,于4 ℃孵育过夜,经PBST漂洗后再加入二抗,于室温孵育1 h。再经PBST洗涤后加入化学发光液进行显影曝光。
1.8 统计学分析采用SPSS 20.0统计软件进行数据统计分析,所有数据均采用x±s表示,统计方法为单因素方差分析,检验水准α=0.05。
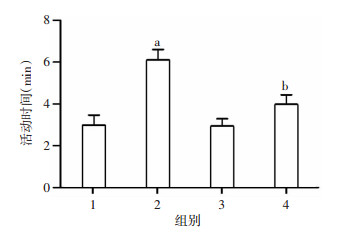
2 结果 2.1 白藜芦醇显著改善孤独症大鼠的重复行为重复行为实验结果显示,与对照组相比,VPA组累计梳理毛发时间显著增加(P < 0.05,图 1),提示VPA组大鼠出现刻板、重复行为;白藜芦醇单独处理变化不明显,而白藜芦醇联合处理显著改善了VPA处理引起的自疏理重复行为(P < 0.05,图 1)。
|
| 1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组 a: P < 0.05,与对照组比较;b: P < 0.05,与VPA组比较 图 1 各组大鼠的重复行为分析 |
2.2 白藜芦醇显著改善孤独症大鼠的社会交往能力
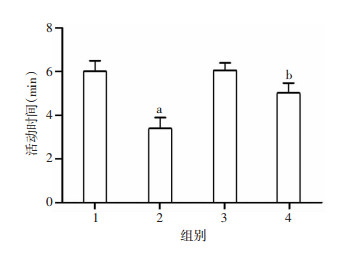
社会交往能力障碍是孤独症儿童的行为特点,这一特点在VPA处理组的幼鼠体现的比较明显,表现为不愿意与陌生幼鼠交往,社会交往能力显著下降(P < 0.05)。与对照组相比,白藜芦醇单独处理组幼鼠的社会交往能力无显著变化;但白藜芦醇联合处理显著改善了VPA处理引起的社会交往能力下降(P < 0.05,图 2)。
|
| 1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组 a: P < 0.05,与对照组比较;b: P < 0.05,与VPA组比较 图 2 各组大鼠的社会交往能力分析 |
2.3 白藜芦醇明显改善孤独症大鼠的神经病征行为 2.3.1 白藜芦醇减少孤独症幼鼠在中央区活动时间
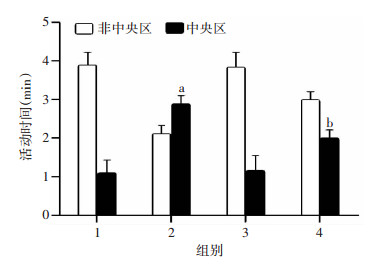
正常幼鼠活动范围大,在中央区活动时间较短,而孤独症模型鼠(VPA处理组)活动范围窄,在中央区活动时间明显增加(图 3,P < 0.05)。与对照组相比,白藜芦醇单独处理组幼鼠活动方式无显著差异;但白藜芦醇联合处理组幼鼠在中央区活动时间显著减少(P < 0.05),活动方式得到明显改善。
|
| 1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组 a: P < 0.05,与对照组比较;b:P < 0.05,与VPA组比较 图 3 各组大鼠在中央区活动时间分析 |
2.3.2 白藜芦醇增加孤独症大鼠站立次数
正常幼鼠比较活跃,站立次数较多,而孤独症模型鼠(VPA处理组)不喜活动,站立次数显著减少(P < 0.05,图 4)。与对照组相比,白藜芦醇单独处理组幼鼠站立次数差异无统计学意义;但白藜芦醇联合处理组幼鼠站立次数显著增加(P < 0.05)。

|
| 1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组 a:P < 0.05,与对照组比较;b: P < 0.05,与VPA组比较 图 4 各组大鼠站立次数分析 |
2.3.3 白藜芦醇增加孤独症大鼠活动距离
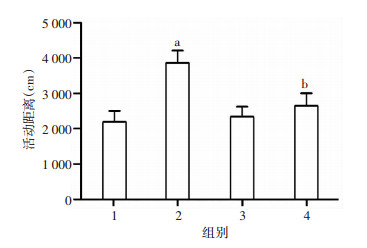
与对照组相比,孤独症模型鼠(VPA组)活动距离明显增加(P < 0.05,图 5),而白藜芦醇组差异无统计学意义,但白藜芦醇联合处理组较VPA组的活动距离显著减少(P < 0.05)。
|
| 1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组 a:P < 0.05,与对照组比较;b: P < 0.05,与VPA组比较 图 5 各组大鼠活动距离分析 |
2.4 白藜芦醇增强孤独症大鼠海马、前额叶皮层和小脑组织自噬标志蛋白LC3-Ⅱ的表达
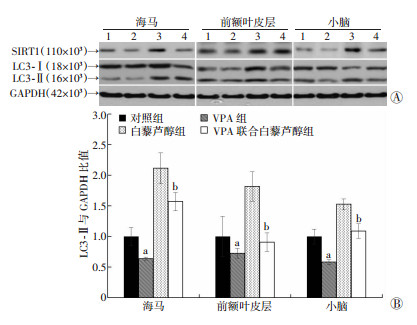
分离幼鼠的海马、前额叶皮层和小脑组织进行Western blot分析。结果如图 6所示,与对照组相比,VPA组孤独症幼鼠的海马、前额叶皮层和小脑组织中的SIRT1蛋白表达水平明显减弱,而白藜芦醇可以增强SIRT1蛋白表达。对自噬信号标志性蛋白LC3-Ⅱ的水平检测发现,VPA组LC3-Ⅱ水平显著降低(P < 0.05),说明孤独症幼鼠脑组织中的自噬信号被抑制,而使用白藜芦醇后,可明显增加孤独症幼鼠海马、前额叶皮层和小脑组织中LC3-Ⅱ的表达水平(P < 0.05),增强自噬信号。对LC3-Ⅱ表达水平的定量分析进一步支持了这一结果。
|
| A:Western blot检测结果1:对照组;2:VPA组;3:白藜芦醇组;4:VPA联合白藜芦醇组;B:半定量分析结果a:P < 0.05,与对照组比较;b: P < 0.05,与VPA组比较 图 6 Western blot检测白藜芦醇对孤独症大鼠脑组织中自噬相关蛋白表达水平的影响 |
3 讨论
白藜芦醇是一种广泛存在于植物性食物或药物中的非黄酮类多酚小分子化合物,具有抗氧化、抗感染、神经保护和抗肿瘤等多种生物学活性。由于白藜芦醇具有多种生物和药理活性,目前已广泛应用于食品、医药、保健品、化妆品等领域,已有大部分国家和地区都开发了白藜芦醇及其制品[12]。研究表明,白藜芦醇对于中风、缺血等引起的脑损伤均具有重要的保护作用[13]。但白藜芦醇是否具有改善孤独症模型大鼠病症行为的作用,国内尚少见报道。本研究结果表明,白藜芦醇可以显著改善孤独症模型大鼠的社会交往能力,主要体现为对陌生鼠代表的新伙伴兴趣增加,接触时间增长;同时,白藜芦醇改善了孤独症模型大鼠的重复刻板行为,体现为自我梳理时间减少;白藜芦醇还明显改善了孤独症模型大鼠的神经行为,体现为对新环境认知与探索能力增强,焦虑感下降,体现为停留在中央区的时间减少,活动距离减少,站立次数增加。重复刻板行为、社会交往障碍和焦虑水平增加是孤独症患者的典型行为特征。在本实验中,VPA模型组幼鼠表现出自我梳理时间增加所代表的重复刻板行为,与陌生鼠接触减少所代表的社会交往障碍及在中央区活动时间与距离增加所代表焦虑水平增强,符合孤独症的行为特征。白藜芦醇减少了孤独症幼鼠的焦虑水平,增强了其探索能力,这可能在一定程度上有助于改善其社会交往障碍与重复刻板的行为特征。
细胞自噬是维持细胞自我平衡的一种自我保护机制,是细胞内降解受损细胞器、长周期性蛋白质及蛋白聚集物的重要途径,与个体的生长、发育与疾病的发生中发挥重要作用[13]。组织免疫化学分析发现,在孤独症患者的颞叶皮层细胞自噬水平显著降低,表现为自噬标志蛋白LC3-Ⅱ水平明显下降而p62水平则显著升高[4]。在自噬阳性调节基因Ambra1杂合性突变的小鼠,表现出认知障碍、社交损害、行为刻板等孤独症的病症行为[14]。通过对全外显子测序数据进行分析发现,在部分孤独症患者体内的自噬信号通路因拷贝数变异而被阻断[15]。而使用自噬的诱导增强剂雷帕霉素可以显著改善大鼠的孤独症病症行为[6]。研究表明,白藜芦醇可以增强小脑神经细胞[16]、海马神经元细胞[17]、前额皮质神经细胞[18]、星形胶质细胞[19]、胶质瘤细胞等多种神经细胞的自噬水平。但白藜芦醇能否改善孤独症大鼠神经细胞的自噬水平尚少见报道。本研究证实,白藜芦醇预处理可显著增强孤独症大鼠海马、前额叶皮质与小脑组织中的自噬水平,纠正VPA引起的自噬水平下调。
研究表明,白藜芦醇可通过多种信号通路诱导细胞自噬,包括AKT/MTOR、AMPK/SIRT1、ROS、P38/MAPK、JNK等多条信号通路[20],其中SIRT1在白藜芦醇诱导神经细胞自噬发生过程中发挥着关键作用。组蛋白脱乙酰酶sirtuin 1(SIRT1) 是组织细胞自我保护的一种重要分子,它在机体细胞周期、细胞衰老、凋亡和新陈代谢等方面的调节中发挥重要作用[21]。研究表明,SIRT1可通过多种信号通路激活细胞自噬。SIRT1可以使转录因子FOXO1与FOXO3去乙酰化而激活,进而转录上调多个自噬相关蛋白,如Rab7、ULK2、Beclin1、VPS34、Bnip3、ATG12、ATG4B等[21]。SIRT1也可以直接使自噬相关蛋白ATG5、ATG7、LC3去乙酰化而表达上调[21]。因此,SIRT1激活后可借助多种途径上调细胞中的自噬水平。由于VPA具有脱乙酰酶抑制剂的作用,很可能在幼鼠脑发育过程中通过抑制SIRT1表达而引起孤独症发病,本研究结果也证实VPA可下调孤独症幼鼠脑组织中的SIRT1表达水平。与VPA的作用恰恰相反,白藜芦醇是SIRT1的直接激活剂,可在细胞中激活并上调SIRT1的表达。因此,白藜芦醇可纠正孤独症幼鼠脑组织中SIRT1表达下调的这一缺陷。本实验的结果也证实了这一点。另外,研究表明,氧化应激在VPA诱导的孤独症发病中也发挥着重要的作用[22],而白藜芦醇则是一类重要的抗氧化剂,因此,白藜芦醇的抗氧化作用也可能在改善孤独症的病症行为中发挥一定作用,具体机制尚需进一步研究探讨。
总之,本研究证实白藜芦醇可以显著改善孤独症大鼠的病症行为,机制可能与上调孤独症大鼠脑组织中SIRT1表达并增强自噬水平相关。相关结果为孤独症的预防及临床治疗提供了理论依据。
| [1] | NAPOLI E, DUENAS N, GIULIVI C. Potential therapeutic use of the ketogenic diet in autism spectrum disorders[J]. Front Pediatr, 2014, 2: 69. DOI:10.3389/fped.2014.00069 |
| [2] |
陈文雄. 孤独症70年:从Kanner到DSM-Ⅴ[J].
临床儿科杂志, 2013, 31(11): 1001–1004.
CHEN W X. Seventy years autism:From kanner to dsm-v[J]. Journal of Clinical Pediatrics, 2013, 31(11): 1001–1004. DOI:10.3969/j.issn.1000-3606.2013.11.001 |
| [3] | MATSON J L, JANG J. Treating aggression in persons with autism spectrum disorders: a review[J]. Res Dev Disabil, 2014, 35(12): 3386–3391. DOI:10.1016/j.ridd.2014.08.025 |
| [4] | TANG G, GUDSNUK K, KUO S H, et al. Loss of mTOR-dependent macroautophagy causes autistic-like synaptic pruning deficits[J]. Neuron, 2014, 83(5): 1131–1143. DOI:10.1016/j.neuron.2014.07.040 |
| [5] | SAHIN M. Targeted treatment trials for tuberous sclerosis and autism: no longer a dream[J]. Curr Opin Neurobiol, 2012, 22(5): 895–901. DOI:10.1016/j.conb.2012.04.008 |
| [6] |
秦利燕, 戴旭芳. 雷帕霉素对自闭症大鼠病症行为的改善作用[J].
第三军医大学学报, 2015, 37(05): 420–424.
QIN L Y, DAI X F. Role of rapamycin in improvement of autistic rats[J]. J Third Mil Med Univ, 2015, 37(05): 420–424. DOI:10.16016/j.1000-5404.201409094 |
| [7] | DIAZ M, DEGENS H, VANHEES L, et al. The effects of resveratrol on aging vessels[J]. Exp Gerontol, 2016, 85: 41–47. DOI:10.1016/j.exger.2016.09.016 |
| [8] |
张勇, 陈明亮, 高燕翔, 等. 白藜芦醇通过诱导自噬缓解肝细胞脂肪变性[J].
第三军医大学学报, 2014, 36(21): 2178–2182.
ZHANG Y, CHEN M L, GAO Y X, et al. Resveratrol attenuates steatosis in cultured hepatic cells by inducing autophagy[J]. J Third Mil Med Univ, 2014, 36(21): 2178–2182. |
| [9] |
邓皓月, 糜漫天. 白藜芦醇通过上调SIRT1/自噬通路改善Aβ25-35对PC12细胞增殖的抑制作用[J].
第三军医大学学报, 2016, 38(06): 619–622.
DENG H Y, MI M T. Resveratrol attenuates Aβ25-35 induced neurotoxicity via activation of SIRT1/autophagy signaling pathway[J]. J Third Mil Med Univ, 2016, 38(06): 619–622. DOI:10.16016/j.1000-5404.201507141 |
| [10] | CAPUTO M, MATARESE G, PIERANTONI G M, et al. Convergent effects of resveratrol and PYK2 on prostate cells[J]. Int J Mol Sci, 2016, 17(9): E1542. DOI:10.3390/ijms17091542 |
| [11] | SCHNEIDER T, PRZEWŁOCKI R. Behavioral alterations in rats prenatally exposed to valproic acid: animal model of autism[J]. Neuropsychopharmacology, 2005, 30(1): 80–89. DOI:10.1038/sj.npp.1300518 |
| [12] | BORRIELLO A, BENCIVENGA D, CALDARELLI I, et al. Resveratrol: from basic studies to bedside[J]. Cancer Treat Res, 2014, 159: 167–184. DOI:10.1007/978-3-642-38007-5_10 |
| [13] | CHEN W, SUN Y, LIU K, et al. Autophagy: a double-edged sword for neuronal survival after cerebral ischemia[J]. Neural Regen Res, 2014, 9(12): 1210–1216. DOI:10.4103/1673-5374.135329 |
| [14] | DERE E, DAHM L, LU D, et al. Heterozygous ambra1 deficiency in mice: a genetic trait with autism-like behavior restricted to the female gender[J]. Front Behav Neurosci, 2014, 16(8): 181. DOI:10.3389/fnbeh.2014.00181 |
| [15] | POULTNEY C S, GOLDBERG A P, DRAPEAU E, et al. Identification of small exonic CNV from whole-exome sequence data and application to autism spectrum disorder[J]. Am J Hum Genet, 2013, 93(4): 607–619. DOI:10.1016/j.ajhg.2013.09.001 |
| [16] | WANG R, LIU Y Y, LIU X Y, et al. Resveratrol protects neurons and the myocardium by reducing oxidative stress and ameliorating mitochondria damage in a cerebral ischemia rat model[J]. Cell Physiol Biochem, 2014, 34(3): 854–864. DOI:10.1159/000366304 |
| [17] | LIU S, LI T, LIU H, et al. Resveratrol exerts antidepressant properties in the chronic unpredictable mild stress model through the regulation of oxidative stress and mTOR pathway in the rat hippocampus and prefrontal cortex[J]. Behav Brain Res, 2016, 302: 191–199. DOI:10.1016/j.bbr.2016.01.037 |
| [18] | LIN C J, CHEN T H, YANG L Y, et al. Resveratrol protects astrocytes against traumatic brain injury through inhibiting apoptotic and autophagic cell death[J]. Cell Death Dis, 2014, 5: e1147. DOI:10.1038/cddis.2014.123 |
| [19] | WANG F, CUI N, YANG L, et al. Resveratrol rescues the impairments of hippocampal neurons stimulated by microglial over-activation in vitro[J]. Cell Mol Neurobiol, 2015, 35(7): 1003–1015. DOI:10.1007/s10571-015-0195-5 |
| [20] | APPUHAMY J A, NAYANANJALIE W A, ENGLAND E M, et al. Effects of AMP-activated protein kinase (AMPK) signaling and essential amino acids on mammalian target of rapamycin (mTOR) signaling and protein synthesis rates in mammary cells[J]. J Dairy Sci, 2014, 97(1): 419–429. DOI:10.3168/jds.2013-7189 |
| [21] | NG F, TANG B L. Sirtuins'modulation of autophagy[J]. J Cell Physiol, 2013, 228(12): 2262–2270. DOI:10.1002/jcp.24399 |
| [22] |
张应花, 杨彩玲, 崔卫刚, 等. 舒林酸对丙戊酸孤独症动物模型大鼠氧化应激变化的影响[J].
中国病理生理杂志, 2014, 30(12): 2161–2165.
ZHANG Y H, YANG C L, CUI W G, et al. Effects of sulindac on oxidative stress in an autistic model induced by pre-natal exposure to valproic acid[J]. Chinese Journal of Pathophysiology, 2014, 30(12): 2161–2165. DOI:10.3969/j.issn.1000-4718.2014.12.008 |



