随着MRI新技术的开发应用,前列腺多参数磁共振成像(multiparametric magnetic resonance imaging,Mp-MRI)检查已成为公认的诊断前列腺癌(prostate cancer,PCa)的最佳影像学方法[1-2],可用于PCa的检出、分期和预后评估[3-4]。随着前列腺Mp-MRI临床工作深入的同时,影像科医师在Mp-MRI报告中也存在诸多问题,如报告用语不规范,影像诊断结果模糊等,影响临床医师的正确解读和对病情的准确判断。为规范前列腺Mp-MRI报告,欧洲泌尿放射学会(European Society of Uroradiology,ESUR)于2012年发布前列腺影像报告和数据系统第1版(prostate imaging-reporting and data system version 1,PI-RADS V1)[5],旨在通过评分使前列腺影像报告标准化、规范化,减少模糊的影像描述和诊断结果,帮助泌尿科医生更好的依据Mp-MRI检查结果处理病人[6-7]。2014年,为解决前列腺Mp-MRI国际标准化问题,美国放射学院(American College of Radiology,ACR)和ESUR对PI-RADS V1进行修改,制订了PI-RADS V2[8]。之后国内外学者基于PI-RADS V2做了相关研究,证实PI-RADS V2具有较高的诊断效能[9-10]。对于初级、中级、高级这3个不同经验层次的医师来说,PI-RADS V2的应用能否提高其对PCa影像诊断效能,若有影响,影响到底有多大,哪一个层次的诊断医师最应该推荐使用PI-RADS V2,目前尚不清楚。因此,本研究旨在评价PI-RADS V2提高不同层次影像医师对PCa影像诊断效能的应用价值。
1 资料与方法 1.1 一般资料收集本院2016年进行Mp-MRI检查,临床资料及病理结果齐全的前列腺疾病初诊患者76例,年龄52~ 90(71.9±7.4) 岁。Mp-MRI检查包括T2WI、T1WI、弥散加权成像(diffusion weighted imaging,DWI)、动态增强(dynamic contrast-enhanced, DCE)扫描,患者检查前均未接受过内分泌治疗、离子植入、外放射或穿刺活检等临床处理。本研究经重庆医科大学附属第二医院伦理委员会批准[2016年伦审(18) 号]。
1.2 前列腺Mp-MRI检查检查前1 d患者进少渣饮食并口服缓泻剂,以保证直肠内清洁。采用飞利浦3.0T MRI(Achieva/Intera)扫描仪,以体线圈为射频发射线圈,腹部相控阵线圈为接收线圈。轴位扫描范围包括前列腺及精囊腺。轴位T2WI:采用FSE序列,TR 3500 ms,TE 91 ms;回波链长度25;层厚4 mm,层间距1 mm,FOV 260 mm×260 mm,NEX= 2;矩阵304×230。轴位T1WI:采用序列,TR 473 ms,TE 8.0 ms;回波链长度5;层厚4 mm,层间距1 mm,FOV 260 mm×260 mm,NEX=2;矩阵260×224;轴位DWI采用单次激发EPI序列,TR 1 078.81 ms,TE 69.51 ms,层厚4 mm,层间距1 mm,FOV 260 mm×260 mm,NEX=4,矩阵184×183,b值取0、1 000 s/mm2,采集3个方向。通过飞利浦后处理工作站Extended MR Workspace软件获得相应的ADC图。轴位DCE经肘静脉穿刺,高压注射器团注对比剂Gd-DTPA 0.1 mmol/kg,速率2 mL/s。注射对比剂前先扫描1组图像作为蒙片,注射对比剂的同时开始扫描,连续扫描25个周期。DCE扫描采用容积超快速采集序列,TR 3.2 ms;TE 1.46 ms,翻转角15°,FOV 260 mm×260 mm,矩阵164×162。
1.3 影像学评分将影像医师分为3个层次,分别为初级职称、中级职称和高级职称。在3个层次里分别选择3名研究方向为腹部影像的医师,共9名医师。
1.3.1 经验评分按照医师平时积累的知识及经验做出的评分作为经验评分。经验评分前,9名医师均不知晓PI-RADS V2评分标准。9名医师分别对入组的76例患者Mp-MRI图像按5分制进行盲法经验评分。1分:临床显著癌存在可能性极低,2分:临床显著癌存在可能性低,3分:临床显著癌存在可能性中等,4分:临床显著癌存在可能性高,5分:临床显著癌存在可能性极高。当同一层次3名医师经验评分出现不一致的情况,由该层次3名医师共同讨论得出最终评分。最终分别得到初级医师、中级医师、高级医师经验评分结果。
1.3.2 PI-RADS V2评分经验评分完成之后,以讲座及讨论形式组织9名医师一起学习PI-RADS V2,直至充分理解PI-RADS V2评分标准,然后严格按照PI-RADS V2的评分标准对入组的76例患者Mp-MRI图像进行影像学评分,作为PI-RADS V2评分。首先,根据Mp-MRI图像,确定病灶的位置,若病灶位于外周带,进一步看DWI,若DWI评分3分进一步看DCE。移行带病灶进一步看T2WI,若T2WI评分3分进一步看DWI。总体5分制,评分标准见表 1,评分示例见图 1~3。当同一层次3名医师PI-RADS V2评分出现不一致的情况,由该层次3名医师共同讨论得出最终评分。最终分别得到初级医师、中级医师、高级医师PI-RADS V2评分结果1。1周以后9名医师根据PI-RADS V2再次进行评分,过程同前,分别得到初级医师、中级医师、高级医师PI-RADS V2评分结果2。

|
| A:T2WI图右侧移行带见边界不清的不均匀信号强度, 评分3分;B:DWI图显著高信号;C:ADC图局灶显著低信号,最大径线≥1.5 cm,评分5分;D:DCE增强早期图。评分5分,P1-RADS V2最终评分4分。病理结果为PCa 图 1 前列腺右侧移行带癌Mp-MRI图像 |

|
| A:T2WI图;B:DWI图左侧外周带轻度高信号;C:ADC图左侧外周带中度低信号,评分3分;D:DCE增强早期图局灶性强化,且早于邻近前列腺组织,DCE阳性。P1-RADS V2最终评分4分。病理结果为PCa。 图 2 前列腺左侧外周带癌Mp-MRI图像 |

|
| A:T2WI图,评分2分右侧移行带见边界清楚的低信号、不均匀包膜内结节,评分2分;B:DWI图;C:ADC图;D:DCE增强早期图。P1-RADS V2最终评分2分。病理结果为前列腺增生。 图 3 前列腺移行带增生Mp-MRI图像 |
| 病灶位置 | 序列1 | 序列2 | 最终评分 | |||||
| 序列 | 评分标准 | 评分 | 序列 | 评分标准 | 评分 | |||
| 外周带 | DWI | ADC及DWI上无异常 | 1分 | 1分 | ||||
| ADC图模糊不清的低信号 | 2分 | 2分 | ||||||
| ADC图局灶性轻或中度低信号和DWI等信号或轻度高信号 | 3分 | DCE | 无早期强化;或弥漫强化,但T2WI上未见相应局灶病灶 | 阴性 | 3分 | |||
| 局灶强化,且早于或与邻近前列腺组织同步强化,且T2WI有可疑发现 | 阳性 | 4分 | ||||||
| ADC图局灶性显著低信号病灶和DWI显著高信号,最大径线 < 1.5 cm | 4分 | 4分 | ||||||
| 同4,最大径线≥1.5 cm,或有明确前列腺外侵犯行为 | 5分 | 5分 | ||||||
| 移行带 | T2WI | 均匀中等信号强度 | 1分 | 1分 | ||||
| 边界清楚低信号或不均匀包膜内结节 | 2分 | 2分 | ||||||
| 边界不清的不均匀信号强度(包括所有不符合2、4、5的) | 3分 | DWI | 标准同外周带DWI标准 | 1-4分 | 3分 | |||
| 5分 | 4分 | |||||||
| 双凸透镜形、新月形、或边界不清、均匀中等强度低信号,最大径线 < 1.5 cm | 4分 | 4分 | ||||||
| 同4,最大径线≥1.5 cm,或有明确前列腺外侵犯行为 | 5分 | 5分 | ||||||
1.4 病理学检查
Mp-MRI检查后3个月内,以超声引导下经直肠前列腺穿刺活检或前列腺根治性切除术获取病理结果。
1.5 统计学分析采用SPSS 22.0及MedCalc17.1.0统计软件。不同层次医师前后2次PI-RADS V2评分结果分别行Kappa一致性检验。医师第2次PI-RADS V2评分结果两两间分别行Kappa一致性检验。不同层次医师经验评分与PI-RADS V2评分结果进行Spearman相关性分析。以病理结果为金标准,秩和检验分析初级、中级、高级医师经验诊断结果与PI-RADS V2诊断结果的差异,绘制初级、中级、高级医师经验诊断、PI-RADS V2诊断的ROC曲线,计算曲线下面积,并计算各自对于PCa检出的敏感度、特异度、阳性预测值、阴性预测值。
2 结果入组76例患者经病理诊断,PCa34例,非PCa42例。
2.1 医师2次PI-RADS V2评分结果的一致性初级、中级、高级医师前后2次PI-RADS V2评分结果行Kappa一致性检验,Kappa值分别为0.875,0.810,0.878,具有统计学意义(P < 0.01)。表明前后2次结果具有高度一致性。
2.2 不同层次医师PI-RADS V2评分结果的一致性初级、中级、高级医师PI-RADS V2第2次评分结果两两间行Kappa一致性检验,初级-中级医师PI-RADS V2评分结果Kappa值为0.699,中级-高级医师Kappa值为0.766,初级-高级医师Kappa值为0.686,均有统计学意义(P < 0.01)。两两比较评分结果间具有较好一致性。
2.3 不同层次医师经验评分与PI-RADS V2评分的相关性初级、中级、高级医师经验评分与各自第2次PI-RADS V2评分结果行Spearman相关性分析。初级、中级、高级医师经验评分与PI-RADS V2评分正相关,P值均小于0.01,具有显著统计学意义。初级、中级、高级经验评分与PI-RADS V2评分相关系数r值分别为0.672、0.805、0.890,r值呈递增趋势。
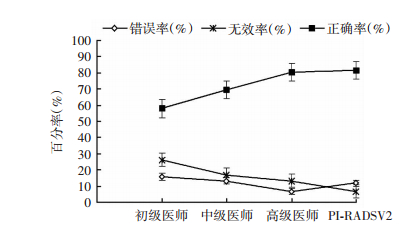
2.4 不同层次医师经验诊断及PI-RADS V2诊断的正确率、无效率及错误率以病理结果作为金标准对初级、中级、高级医师经验诊断(评分1~2分诊断为非癌,4~5分为癌,3分为无效)的正确率、无效率及错误率与PI-RADS V2进行对比(由于PI-RADS V2前后2次评分高度一致,且3个经验层次医师PI-RADS V2评分的较好一致性,折中选择中级医师第2次PI-RADS V2评分结果进行对比):初级医师诊断正确率明显低于PI-RADS V2,错误率和无效率明显高于PI-RADS V2,差异有统计学意义(Z=-8.300, P < 0.01)。中级医师诊断正确率低于PI-RADS V2,错误率和无效率高于PI-RADS V2,差异有统计学意义(Z=-0.63, P < 0.01)。高级医师诊断正确率略低于PI-RADS V2,错误率低于PI-RADS V2,无效率高于PI-RADS V2,差异有统计学意义(Z=-7.145, P < 0.01)。如图 4所示,初级、中级、高级医师及PI-RADS V2诊断正确率呈递增趋势,无效率呈现递减趋势,错误率初级、中级、高级医师递减趋势,PI-RADS V2错误率略高于高级医师。
|
| 图 4 不同层次医师及PI-RADS V2诊断正确率、错误率及无效率 |
2.5 不同层次医师经验诊断及PI-RADS V2诊断效能分析
以病理结果作为金标准,初级、中级、高级医师经验诊断及PI-RADS V2诊断(选择中级医师第2次PI-RADS V2评分结果)的ROC曲线结果见表 2。初级、中级、高级医师及PI-RADS V2对于PCa的检出均有统计学意义,高级医师的诊断准确性最高,然后依次为PI-RADS V2、中级医师及初级医师。
| 评分类别 | 曲线下面积 | 95%CI | P值 |
| 初级医师 | 0.760 | 0.641~0.852 | <0.01 |
| 中级医师 | 0.836 | 0.736~0.908 | <0.01 |
| 高级医师 | 0.912 | 0.841~0.965 | <0.01 |
| PI-RADS V2 | 0.890 | 0.805~0.955 | <0.01 |
以病理结果作为金标准,初级、中级、高级医师经验诊断及PI-RADS V2诊断(选择中级医师第2次PI-RADS V2评分结果)PCa检出效能见表 3。PI-RADS V2诊断敏感度最高,其次为高级医师。高级医师特异度及阳性预测值最高,其次为PI-RADS V2。
| 评分类别 | 敏感度 | 特异度 | 阳性预测值 | 阴性预测值 |
| 初级医师 | 70.48 | 76.22 | 70.48 | 76.22 |
| 中级医师 | 87.25 | 78.46 | 76.81 | 89.08 |
| 高级医师 | 91.12 | 88.27 | 86.33 | 92.42 |
| PI-RADS V2 | 94.11 | 86.69 | 85.02 | 94.61 |
3 讨论
2014年,ACR和ESUR发布PI-RADS V2之后,国内外学者基于PI-RADS V2做了相关研究,研究主要集中于PI-RADS V2与V1的对比,PI-RADS V2用于Mp-MRI不同组合方案诊断效能的评估,不同分区PCa的评估及临床显著癌的评估等[9-15],研究证实PI-RADS V2较V1具有更高的诊断效能,因此本研究选择PI-RADS V2进行研究。关于PI-RADS V2对具有不同诊断能力影像医师的相关研究极少,KASEL-SEIBERT等[16]研究发现具有丰富PCa诊断经验的医师(诊断效能:PI-RADS V1 0.79;PI-RADS V2 0.83) 和没有经验的医师(诊断效能:PI-RADS V1 0.70;PI-RADS V2 0.83) 进行PI-RADS V2诊断具有相同的诊断效能,且高于PI-RADS V1,PI-RADS V2具有良好的重复性。本研究也证实了该观点,且本研究将医师的经验层次进行细分,分为初级、中级、高级3个层次。除此之外,本研究重点分析3个不同经验层次影像医师经验评分与PI-RADS V2评分的相关性,经验诊断与PI-RADS V2诊断结果、诊断效能的差异。
本研究结果发现3个层次医师经验评分与其PI-RADS V2评分均呈正相关,相关系数r随着医师诊断经验的增加而逐渐增加。说明经验更丰富的医师与PI-RADS V2的相关性更高,评分结果更趋于一致。且3个层次医师PI-RADS V2评分具有较高一致性,这也说明了PI-RADS V2重复性良好,在充分理解PI-RADS V2评分标准的基础上,严格按照PI-RADS V2的评分标准进行评分,可提高初级、中级医师的PCa诊断水平,使其接近甚至达到具有丰富诊断经验高级医师的诊断水平。初级、中级、高级医师经验诊断的正确率、无效率及错误率与PI-RADS V2进行对比的结果显示,随着医师的经验增加,诊断PCa的正确率逐渐增加,且PI-RADS V2诊断正确率甚至超过高级职称诊断医师。这说明不同层次医师在学习PI-RADS V2之后,严格按照PI-RADS V2进行评分,能提高3个层次医师诊断正确率,证实PI-RADS V2对于不同层次医师的价值,特别是初级、中级医师,可帮助其提高诊断PCa的正确率、降低错误率。对于评分为3分本研究判定为无效,无效率呈现递减趋势,说明初级、中级医师诊断癌的信心不足,随着经验的增加对于癌及非癌的诊断信心更足。因此,PI-RADS V2的应用能够提高初级、中级医师对于癌及非癌的诊断信心。经验诊断及PI-RADS V2诊断的ROC曲线结果显示高级医师的曲线下面积最大,然后依次为PI-RADS V2、中级及初级医师。高级医师及PI-RADS V2的诊断具有较高准确性,且PI-RADS V2的诊断准确性接近高级职称,对经验不足的初级、中级医师普及应用PI-RADS V2能明显提高其诊断PCa的准确性。本研究关于诊断效能的结果发现,初、中、高级医师诊断PCa的敏感度和特异度逐渐增加,说明随着工作时限的增加、诊断经验的丰富,对于PCa的检出效能逐渐增加。PI-RADS V2的应用可提高不同层次医师的诊断敏感度,提高初级、中级医师的诊断特异度,对于经验不足医师,PI-RADS V2的应用可显著提高其PCa的影像诊断效能。
本研究PI-RADS V2对PCa检出的敏感度为94.11%,特异度86.69%,略低于王蕊等[10]的报道(敏感度96.55%、特异度88.57%),高于牛翔科等[14]的报道(外周带敏感度88.3%、特异度85.6%,移行带敏感度83.4%、特异度63.9%),且高于HAMOEN等[17]的Meta分析报告(敏感度82%、特异度82%)。各个研究者PCa检出效能结果的不一致,可能是因为虽然PI-RADS V2详细制定了评分标准,而不同机构之间对标准的解读存在差异。ROSENKRANTZ等[18]对来自不同机构的6名放射医师的PI-RADS V2评分研究认为,PI-RADS V2具有中等度的可重复性,这6名放射医师都具有丰富经验且对PI-RADS诊断完全熟知,可能是实现较好重复性的原因之一。MULLER等[13]对于同一机构5位诊断医师的评分一致性研究发现PI-RADS V2可重复性好。本研究对同一经验层次医师前后2次PI-RADS V2诊断及3个经验层次医师的PI-RADS V2诊断结果分别进行了一致性分析。同一经验层次医师不同时间点PI-RADS V2诊断高度一致,3个不同经验层次医师的PI-RADS V2诊断结果仍具有较好一致性。这可能是因为同一机构的诊断医师相互交流互动密切,对于PI-RADS V2的解读一致。因此,在以后的工作中,需要进一步开展多中心研究,探讨不同机构PI-RADS V2的诊断效能的重复性与统一方法。
本研究的局限性:① 样本量偏少;② 关于PI-RADS V2评分,虽然3个层次9名医师严格按照评分表打分,仍然存在一定主观性。今后应扩大样本量,并且进行多中心重复性研究。
总之,本研究结果表明PI-RADS V2具有良好重复性,能显著提高经验不足诊断医师的PCa影像诊断效能以及对于癌及非癌的诊断信心,值得推广使用。
| [1] | DELONGCHAMPS N B, ROUANNE M, FLAM T, et al. Multiparametric magnetic resonance imaging for the detection and localizationof prostate cancer: combination of T2-weighted, dynamic contrast-enhanced and diffusion-weighted imaging[J]. BJU Int, 2011, 107(9): 1411–1418. DOI:10.1111/j.1464-410X.2010.09808.x |
| [2] |
中华放射学杂志前列腺疾病诊疗工作组, 中华放射学杂志编辑委员会. 前列腺癌MR检查和诊断共识[J].
中华放射学杂志, 2014, 48(7): 531–534.
Prostate disease diagnosis and treatment working group of Chinese Journal of Radiology, Editorial board of Chinese Journal of Radiology. MR examination and diagnostic consensus of prostate cancer[J]. Chin J Radio, 2014, 48(7): 531–534. DOI:10.3760/cma.j.issn.1005-1201.2014.07.002 |
| [3] | HOEKS C M, BARENTSZ J O, HAMBROCK T, et al. Prostate cancer: multiparametric MR imaging for detection, localization, and staging[J]. Radiology, 2011, 261(1): 46–66. DOI:10.1148/radiol.11091822 |
| [4] | WANG R, WANG H, ZHAO C, et al. Evaluation of multiparametric magnetic resonance imaging in detection and prediction of prostate cancer[J]. PLoS One, 2015, 10(6): e0130207. DOI:10.1371/journal.pone.0130207 |
| [5] | BARENTSZ J O, RICHENBERG J, CLEMENTS R, et al. ESUR prostate MR guidelines 2012[J]. Eur Radiol, 2012, 22(4): 746–757. DOI:10.1007/s00330-011-2377-y |
| [6] | VOURGANTI S, RASTINEHAD A, YERRAM N K, et al. Multiparametric magnetic resonance imaging and ultrasound fusion biopsy detect prostate cancer in patients with prior negative transrectal ultrasound biopsies[J]. J Urol, 2012, 188(6): 2152–2157. DOI:10.1016/j.juro.2012.08.025 |
| [7] | HAFFNER J, LEMAITRE L, PUECH P, et al. Role of magnetic resonance imaging before initial biopsy: comparison of magnetic resonance imaging-targeted and systematic biopsy for significant prostate cancer detection[J]. BJU Int, 2011, 108: E171–E178. DOI:10.1111/j.1464-410X.2011.10112.x |
| [8] | WEINREB J C, BARENTSZ J O, CHOYKE P L, et al. PI-RADS Prostate Imaging-Reporting and Data System: 2015, Version 2[J]. Eur Urol, 2016, 69(1): 16–40. DOI:10.1016/j.eururo.2015.08.052 |
| [9] | PART S Y, JUNG D C, OH Y T, et al. Prostate cancer: PI-RADS Version 2 helps preoperatively predict clinically significant cancers[J]. Radiology, 2016, 280(1): 108–116. DOI:10.1148/radiol.16151133 |
| [10] |
王蕊, 高歌, 王慧慧, 等. 评价第二版前列腺影像报告和数据系统对前列腺临床显著癌的检出效能[J].
中国医学影像技术, 2016, 32(12): 1799–1802.
WANG R, GAO G, WANG H H, et al. Evaluation of diagnostic efficacy of Prostate Imaging and Reporting Data System Version 2 in detection of prostate clinically significant cancer[J]. Chin J Med Imaging Technol, 2016, 32(12): 1799–1802. DOI:10.13929/j.1003-3289.2016.12.002 |
| [11] | BALDISSEROTTO M, NETO E J, CARVALHAL G, et al. Validation of PI-RADS v.2 for prostate cancer diagnosis with MRI at 3T using an external phased-array coil[J]. J Magn Reson Imaging, 2016, 44(5): 1354–1359. DOI:10.1002/jmri.25284 |
| [12] |
姬广海, 孛茹婷, 郑义, 等. 基于第2版前列腺影像报告和数据系统的多参数MRI诊断外周带前列腺癌[J].
中国医学影像技术, 2016, 32(9): 1414–1418.
JI G H, BO R T, ZHENG Y, et al. Multiparametric MRI based on prostate imaging reporting and data system version 2 in diagnosis of peripheral prostate cancer[J]. Chin J Med Imaging Technol, 2016, 32(9): 1414–1418. DOI:10.13929/j.1003-3289.2016.09.025 |
| [13] | MULLER B G, SHIH J H, SANKINENI S, et al. Prostate Cancer: Interobserver Agreement and Accuracy with the Revised Prostate Imaging Reporting and Data System at Multiparametric MR Imaging[J]. Radiology, 2015, 277(3): 741–750. DOI:10.1148/radiol.2015142818 |
| [14] |
牛翔科, 刘伟, 肖建明, 等. PI-RADS v2在前列腺癌中的诊断价值分析[J].
四川大学学报(医学版), 2016, 47(5): 796–799.
NIU X K, LIU W, XIAO J M, et al. Diagnostic Value of PI-RADS v2 in Prostate Cancer[J]. J Sichuan Univ (Med Sci Edi), 2016, 47(5): 796–799. DOI:10.13464/j.scuxbyxb.2016.05.034 |
| [15] | POLANEC S, HELBICH TH, BICKEL H, et al. Head-to-head comparison of PI-RADS v2 and PI-RADS v1[J]. Eur J Radiol, 2016, 85(6): 1125–1131. DOI:10.1016/j.ejrad.2016.03.025 |
| [16] | KASEL-SEIBERT M, LEHMANN T, ASCHENBACH R, et al. Assessment of PI-RADS v2 for the Detection of Prostate Cancer[J]. Eur J Radiol, 2016, 85(4): 726–731. DOI:10.1016/j.ejrad.2016.01.011 |
| [17] | HAMOEN E H, DE ROOIJ M, WITJES J A, et al. Use of the Prostate Imaging Reporting and Data System(PI-RADS) for prostate cancer detection with multiparametric magnetic resonance imaging: A diagnostic meta-analysis[J]. Eur Urol, 2015, 67(6): 1112–1121. DOI:10.1016/j.eururo.2014.10.033 |
| [18] | ROSENKRANTZ A B, GINOCCHIO L A, CORNFELD D, et al. Interobserver Reproducibility of the PI-RADS Version 2 Lexicon: A Multicenter Study of Six Experienced Prostate Radiologists[J]. Radiology, 2016, 280(3): 793–804. DOI:10.1148/radiol.2016152542 |



