先天性肛门直肠畸形(congenital anorectal malformation,ARM)是儿童最常见的消化道畸形,发病率为1/5 000~1/1 500[1]; 其病理类型繁多[2-3],术后排便功能障碍对患儿及家庭生活质量造成严重影响。对于中高位肛门直肠畸形患儿,分期手术能在肛门成形术前确定直肠盲端位置及异常瘘管情况,尽可能恢复肛直肠解剖位置及排便功能[4],且能明显降低肛门成型术后感染的发生[3]。但一直以来国内外学者在造口肠管的位置及方式的选择上有很大的争议,理论上结肠各部分均可行造瘘手术, 其中降结肠和乙状结肠交界处(降乙交界)分离式造口术(即将两分离瘘口置于切口两端,且要求两瘘口之间距离合适)备受国外学者认同,为首选的造瘘方法,但笔者认为该造瘘手术操作复杂,术后切口易感染裂开,分离瘘口间距难以把控,且术后家属护理困难。目前,横结肠袢式造口手术在ARM分期治疗中应用不广,但其操作简单,术后并发症少,护理容易。所以笔者收集了62例ARM横结肠袢式造口术的病例,回顾性分析其临床资料并评价此造口术的优缺点,为该术式应用于复杂肛直肠畸形提供依据。
1 资料与方法 1.1 临床资料收集重庆医科大学附属儿童医院胃肠新生儿外科2013年1月至2016年4月,分期治疗[一期行横结肠袢式造口、二期(行腹腔镜辅助下)经腹骶或骶会阴肛门成形、三期造口还纳]的62例先天性肛门直肠畸形(ARM)患儿的临床资料,其中男性49例,女性13例,男女比例为3.8:1;初诊年龄为生后1~165 d(中位年龄13 d);病理分型见表 1。
| 病理类型 | 例数 | 百分比(%) |
| ARM伴尿道球部瘘 | 17 | 27.4 |
| ARM伴前列腺部瘘 | 19 | 30.6 |
| ARM伴膀胱颈部瘘 | 2 | 3.2 |
| ARM伴无瘘管 | 10 | 16.2 |
| ARM伴舟状窝瘘 | 7 | 11.3 |
| ARM伴复杂会阴瘘 | 5 | 8.1 |
| 一穴肛 | 2 | 3.2 |
| 合计 | 62 | 100.0 |
1.2 方法 1.2.1 术前常规检查 1.2.1.1 贫血状况评估
分别于二期、三期术前采取外周血行血常规检查,了解患儿血红蛋白量评估贫血状况。
1.2.1.2 常规生化检查分别在两次手术前抽取静脉血作肝功能、血清电解质检查,评估血浆蛋白水平及内环境情况。
1.2.1.3 尿液检查分别于二期、三期手术前无菌导尿后收集患儿中段尿液,定量分析尿液中白细胞数量。
1.2.2 经结肠造口远端造影检查将foley尿管放入横结肠袢式造口远端,并注气胀满球囊固定封堵造口,注入欧乃派克造影显示远端直肠盲端并测的与正常肛隐窝位置的距离,与术中直视下测得直肠盲端与正常肛隐窝距离进行比较。
1.2.3 横结肠造口外观随访观察横结肠袢式造口肠管的外观、血供及排便情况,评估造口肠管有无脱垂、回缩、黏膜出血及造口袋安置等情况.
1.3 统计学方法应用SPSS 19.0软件,计量资料以x±s表示,两组数据间比较,采用配对t检验进行统计学分析,计数资料以率表示,检验水准:α=0.05。
2 结果 2.1 各种结肠造口方式比较降乙结肠交界分离式造口术降结肠固定于左侧腹膜后壁,既预留出远端乙状结肠保证二期手术的完成,同时完全阻断远端结肠粪便蓄积。但此术式手术操作较复杂,需做较大切口才能准确判断出降结肠乙状结肠交界位置,并完全离断肠管后缩小远端肠管;且降结肠因腹膜固定而不易拖出或拖出后因张力高而回缩,造口肠管分别位于切口两端,极易污染切口而导致伤口裂开(图 1A)。
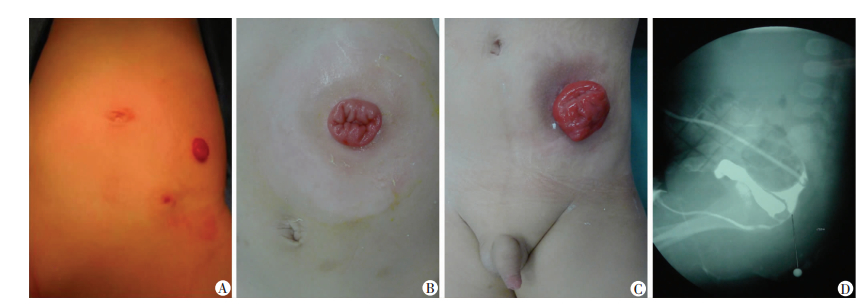
|
| A:降乙结肠交界处分离式造口, 需分别安置两个造口袋,增加护理难度;B:横结肠袢式造口;C:乙状结肠造口体表形态;D:乙状结肠造口造影图像显示预留远端结肠过短,无法拖出成型肛门 图 1 各种结肠造口的体表观和影像学表现 |
横结肠袢式造口术,手术操作简单,左上腹小切口拖出横结肠造口,预留足够远端肠管成型肛门,并借助脾曲部位的韧带对造瘘肠管的固定作用,减少术后造口肠管脱垂;其次左上腹造口更便于造口袋安置和护理;而且也不影响腹腔镜手术操作;再者袢式造口术不需处理血管,手术创伤小,造口还纳手术难度小(图 1B)。
乙状结肠部位的造口能尽可能保留出近端结肠的长度,有利水分的吸收使大便相对成形,方便术后护理;同时乙状结肠在解剖上相对游离,该处造瘘比较容易;但选择位置不当,造口位置过高,可能导致远端肠管预留不够而无法无张力的拖出成型肛门(图 1C、D)。
2.2 贫血状况62例患儿二期手术前血常规检查结果显示,21例(33.9%)血红蛋白含量介于为90~110 g/L,为轻度贫血,其血红蛋白量为(99.17±4.15) g/L,其MCV、MCHC、MCH均低于正常范围(不排除缺铁性贫血可能);而在三期术前,62例患儿复查血常规时仍有22例(35.5%)血红蛋白量为介于90~110 g/L,其血红蛋白量为(97.35±4.71) g/L。但两次结果比较显示,在二期术前轻度贫血的21例患儿中有7例在三期术前贫血状况已恢复正常;9例患儿贫血状况较前明显好转,两者前后分别为(96.79±4.02)、(102.23±3.74) g/L;3例患儿贫血状况无明显变化;只有2例患儿贫血状况加重为中度贫血(60 g/L≤Hb<90 g/L),其血红蛋白量分别为76.2 g/L和70.6 g/L;有8例患儿在二期术前无贫血但在三期术前存在轻度贫血;无重度及极重度贫血患儿。
2.3 血浆蛋白水平62例患儿二期术前肝功能检查结果显示,5例(8.1%)出现轻度低蛋白血症(>30 g/L),其血浆白蛋白量为(32.12±0.93) g/L,但该5例患儿在肛门成型术后伤口愈合良好;在三期术前复查时其中4例患儿恢复正常,1例(1.6%)患儿仍表现为轻度低蛋白血症(血浆蛋白值32.7 g/L)。
2.4 外周血电解质水平62例患儿二期术前外周血电解质检查结果:7例(11.3%)患儿出现电解质紊乱,有2例轻度低钠血症(血钠值分别为122.7 mmol/L和126.4 mmol/L),1例高钾血症(血钾值为5.68 mmol/L),2例轻度低钾血症(血钾值分别为3.15 mmol/L和3.07 mmol/L),2例低氯血症(血氯值分别为95.1 mmol/L和92.3 mmol/L),无高氯血症。7例患儿在行三期手术前检查时,6例患儿电解质紊乱情况均恢复,仍有1例患儿出现轻度低氯血症(血氯值91.7 mmol/L), 无难以纠正的严重电解质紊乱情况发生。
2.5 尿路感染情况62例患儿二期手术前尿常规检查结果显示,19例(30.7%)尿液样本中白细胞数量超过正常范围(0~18) 个/μL,其白细胞数目为(124.42±106.33) 个/μL,其病理类型分别为ARM伴前列腺部瘘7例、伴尿道球部瘘4例、伴膀胱颈部瘘1例、伴舟状窝瘘3例、伴复杂会阴瘘2例、一穴肛2例;其中4例患儿尿液样本明显浑浊;1例ARM伴膀胱颈部瘘患儿出现过发热伴有尿路刺激症状,其余患儿均无明显的尿路感染症状。在行三期手术前因肛门成形术时已经完成异常尿路瘘管的修补,解除了直肠盲端粪便对尿路的污染,再次复查尿常规时,15例患儿恢复正常,仍有4例(6.4%)患儿尿样中白细胞数量(74.75±52.89) 个/μL,大于正常范围,患儿无临床症状。
2.6 经结肠造口造影检查62例患儿中57例在行二期手术前经横结肠造口行欧乃派克远端直肠盲端造影,均能明确异常瘘管位置及病理类型,与术中结果一致(一致率100%),并将术前造影测得直肠盲端与肛隐窝之间的距离(34.63±6.01) mm与术中实际测得距离(37.33±6.17) mm并采用配对t检验统计分析,结果差异无统计学意义(t=0.066,P > 0.05),其中有2例(3.5%)患儿分别为尿道球部瘘和尿道前列腺部瘘,造影时出现远端肠管穿孔,经对症抗感染等保守治疗后治愈,并在三期关瘘手术时证实为乙状结肠继发性闭锁。
2.7 横结肠袢式造瘘术后造瘘口随访62例患儿中无严重的造口肠管脱垂和回缩,9例造口肠管黏膜有息肉样改变,均不影响造口袋的安置及排便。
3 讨论ARM是儿童最常见的消化道畸形,通过手术成型肛门是唯一的治疗手段。对于直肠会阴瘘等低位畸形,出生后即经会阴行肛门成形术可取得满意疗效;而对于伴尿道瘘、阴道瘘、膀胱瘘、一穴肛等中高位肛门直肠畸形,分期手术更安全、可行[3, 5-6]。分期手术第一步即行结肠造口,首先可以解决患儿排便的问题;其次通过造口肠管进行造影检查可明确直肠盲端的位置及异常瘘管的位置,有利于二期手术时选择恰当的手术方式成形肛门并修补异常瘘口;更为重要的是在肛门成型术后,造瘘可有效地降低成型肛门发生严重感染的几率,避免肛管直肠回缩及肛门形成严重瘢痕而影响肛门的外观及功能。但结肠造口除了增加家属护理成本和不便之外,还可能造成造口肠管脱垂、回缩、坏死等严重并发症,故选择合适的造口方式十分关键。一直以来国内外学者对造口的位置及方式的选择上有很大的争议[6],不恰当的造口方式会对整个肛门畸形矫治过程造成严重影响,也会给患儿及家庭带来不必要的痛苦和负担。
文献[3, 7]推荐降乙结肠交界分离式造口术为首选的结肠造口方法。他认为降结肠固定于左侧腹膜后壁,行该处分离式造口优点突出,它既预留出远端乙状结肠保证二期手术的完成,同时完全阻断远端结肠粪便蓄积,降低因异常瘘口所致泌尿生殖道的感染。但此术式手术操作较复杂,需做较大切口才能准确判断出降结肠乙状结肠交界位置,并完全离断肠管后缩小远端肠管;且降结肠因腹膜固定而不易拖出或拖出后因张力高而回缩,造口肠管分别位于切口两端,极易污染切口而导致伤口裂开。国内文献[8]报道在乙状结肠部位的造口能尽可能保留出近端结肠的长度,有利水分的吸收使大便相对成形,方便术后家属护理;同时乙状结肠在解剖上相对游离,该处造瘘比较容易;但选择位置不当[5],造口位置过高,可能导致远端肠管预留不够而无法无张力的拖出成型肛门。而对于横结肠袢式造口术,PENA认为其丢失远端结肠过长、远端结肠粪便容易蓄积从而增加对合并尿道异常瘘口患儿的尿路感染率、且易导致电解质紊乱而不建议采用。但文献[9]报道,选择近脾曲横结肠袢式造口也有明显优点,首先手术操作简单,左上腹小切口拖出横结肠造口,预留足够远端肠管成型肛门,并借助脾曲部位的韧带对造瘘肠管的固定作用,减少术后造口肠管脱垂;其次左上腹造口更便于造口袋安置和护理;而且也不影响腹腔镜手术操作;再者袢式造口术不需处理血管,手术创伤小,造口还纳手术难度小,所以国内仍有不少学者选择此方式。但横结肠袢式造口对ARM患儿术后营养状况、内环境稳定及对二期手术实施的具体影响到底有多大,国内鲜有相关的临床报道。
本组患儿在行结肠造口术后的两次随访中(肛门成形术前及造瘘口还纳术前),贫血的发生率分别为33.9%和35.5%,多为轻度贫血;而贫血患儿的血常规检查中显示MCV、MCHC、MCH提示均低于正常范围(不排除缺铁性贫血可能)。本研究中贫血的发生率略高于该值。相关研究表明造瘘口黏膜出血发生率0.7%~10.3%[10-11],笔者通过详细询问家属造瘘护理情况后认为造瘘术后造瘘口黏膜出血导致患儿慢性失血性贫血,其主要原因是术后结肠造瘘口护理过程中家属护理不当,或者不恰当造口袋与造口肠管黏膜反复摩擦出血,所以造瘘术后对家属的宣教及正确造口护理有可能改善患儿贫血的发生率。
先天性肛门直肠畸形患儿往往在出生后因腹胀、呕吐等影响,患儿容易出现低蛋白血症,严重低蛋白血症可导致手术伤口渗液及组织水肿而影响术后切口愈合。本组研究中结肠造口术后的两次随访患儿出现低蛋血症的发生率为8.1%和1.6%,无严重低蛋白血症发生。发生轻度低蛋白血症的5例患儿术后切口愈合良好,无切口裂开及感染发生。
PENA教授认为存在直肠尿道瘘的患儿预留肠管过长容易导致尿液反流肠管发生尿液二次吸收,增加高氯性酸中毒的发生[5]。本组患儿二期手术前有7例出现电解质紊乱,其中6例患儿分别为轻度低钾血症和低氯低钠血症,1例患儿出现轻度高钾血症。无高氯血症患儿。在三期手术时,7例电解质紊乱患儿均较前明显缓解。出现上述结果分析原因可能为:① 行横结肠造口患儿预留远端结肠相对较长,减少了对水吸收,患儿粪便较稀从而丢失了部分电解质;② 行造口的患儿在造瘘口护理过程中,家属用棉质布料擦拭或造口袋的反复利用导致真菌或细菌的侵入造成反复腹泻所致。本组病例研究显示并无患儿因严重电解质紊乱住院治疗。
直肠肛门畸形伴尿道瘘管的患儿肠道与尿路相通,尿路污染是难以避免的,但PENA等[5]、LIECHTY等[6]认为袢式造口术未能完全隔断造口肠管近远端,导致近端造口的粪便溢向远端结肠,增加了尿路感染的发生率,而本组病例在行肛门成形术前尿常规提示白细胞异常的有16例(30.6%),其中仅有1例伴膀胱瘘的患儿有尿路感染症状,进一步检查后确诊伴有膀胱输尿管反流,其余患儿均无尿路感染的表现。在肛门成型术后12例患儿恢复正常,其余4例尿白细胞异常也较之前好转。说明横结肠袢式造口术后的ARM伴尿道瘘的患儿出现尿路感染的发生率极低,对患儿生活质量并无不利影响;二期肛门成形术时同期修补异常瘘口,患儿尿路污染情况改善明显。但若ARM患儿并发膀胱输尿管反流、先天性肾积水、马蹄肾等泌尿系畸形,术后仍可存在尿路感染,需长期随访治疗。
复杂的先天性肛门直肠畸形患儿在行肛门成形术前行经结肠造口加压造影检查明确有无异常瘘管的存在及直肠盲端位置[12],文献[5, 12]报道在横结肠造口后,远端造口与直肠盲端距离过长,造影检查需要更高的压力注入造影剂才能明确瘘口位置,从而增加了术前漏诊率和肠穿孔的发生率。本研究中62例患儿有57例在二期术前用水溶性造影剂(欧乃派克)加压造影检查,均能准确显示有无异常无瘘口及直肠盲端位置,与术中结果一致。即使发生远端结肠穿孔(本组2例均为继发性乙状结肠狭窄),通过对症抗感染保守治疗均能治愈,无严重并发症。说明只要选择合适的造影剂,足够的造影压力,经横结肠造口造影检查能准确显示直肠盲端和异常瘘管位置;且造影导致肠穿孔的发生率不高。
国外有文献报道袢式造口术后肠管脱垂及回缩的发生率与分离式造口术相当[7],但也有研究表明袢式造口肠管脱垂及回缩发生率为31%~63%,分离式造口的发生率为15%~45%[13-14]。本组病例中造瘘口肠管无严重脱垂及回缩,未导致梗阻及影响造口袋安置,均无需再次手术修复。
综上所述,针对我国目前医疗卫生现状,多数ARM患儿在发现肛门直肠畸形时通常急诊入院,患儿因腹胀呕吐导致严重脱水及电解质紊乱,一般情况较差,对于不能明确ARM具体病理类型及患儿合并其他系统畸形时往往需先行预防性造口术再择期行肛门成型手术,理论上,造口位置可根据临床医师经验选择。笔者认同降结肠分离式造口术的临床应用优点,但临床急诊手术特别在夜班情况下往往缺乏有丰富造口经验的医师,既然横结肠袢式造口术对患儿整个过程中无明显不利影响;且手术操作简单,术后并发症少、方便家属护理等突出优点,横结肠袢式造口术也不失为一种可行、有效的造口选择。
| [1] | LEVITT M A, PEÑA A. Imperforate anus and cloacal malformations[J]. Ashcraft's Pediatric Surgery, 2010: 468–490. DOI:10.1016/b978-1-4160-6127-4.00036-7 |
| [2] | HOLSCHNEIDER A, HUTSON J, PEÑA A, et al. Preliminary report on the International Conference for the development of standards for the treatment of anorectal malformations[J]. J PediatrSurg, 2005, 40(10): 1521–1526. DOI:10.1016/j.jpedsurg.2005.08.002 |
| [3] | LEVITT M A, PENA A. Anorectal malformations[J]. Orphanet J Rare Dis, 2007, 2: 33. DOI:10.1186/1750-1172-2-33 |
| [4] |
吴永隆, 陈思远, 陈秀兰, 等. 男性先天性中高位肛门直肠畸形术后排便功能评估及其影响因素[J].
第三军医大学学报, 2015, 37(21): 2151–2155.
WU Y L, CHEN S Y, CHEN X L, et al. Bowel function and its influencing factors for male children with high and intermediate anorectal malformation after surgical treatment[J]. J Thir Mil Med Univ, 2015, 37(21): 2151–2155. DOI:10.16016/j.1000-5404.201503166 |
| [5] | PENA A, MIGOTTO-KRIEGER M, LEVITT M A. Colostomy in anorectal malformations: a procedure with serious but preventable complications[J]. J PediatrSurg, 2006, 41(4): 748–756. DOI:10.1016/j.jpedsurg.2005.12.021 |
| [6] | LIECHTY S T, BARNHART D C, HUBER J T, et al. The morbidity of a divided stoma compared to a loop colostomy in patients with anorectal malformation[J]. J PediatrSurg, 2016, 51(1): 107–110. DOI:10.1016/j.jpedsurg.2015.10.025 |
| [7] | PATWARDHAN N, KIELY E M, DRAKE D P, et al. Colostomy for anorectal anomalies: high incidence of complications[J]. J PediatrSurg, 2001, 36(5): 795–798. DOI:10.1053/jpsu.2001.22963 |
| [8] | SALEEM M, SAQI Z, SHAIKH A H, et al. Complications of colostomy in infants and children[J]. Ann KE Med Col, 1998, 4: 20–23. |
| [9] |
唐维兵, 徐小群, 耿其明, 等. 新生儿结肠造瘘术165例分析[J].
临床小儿外科杂志, 2008, 7(5): 41–43.
TANG W B, XU X Q, GENG Q M, et al. Neonatal colostomy: report of 32 cases[J]. J Clin Pediatric Surg, 2008, 7(5): 41–43. DOI:10.3969/j.issn.1671-6353.2008.05.014 |
| [10] | CHANDRAMOULI B, SRINIVASAN K, JAGDISH S, et al. Morbidity and mortality of colostomy and its closure in children[J]. J PediatrSurg, 2004, 39(4): 596–599. DOI:10.1016/j.jpedsurg.2003.12.016 |
| [11] | MOLLITT D L, MALANGONI M A, BALLANTINE T V, et al. Colostomy complications in children[J]. Arch Surg, 1980, 115(4): 455–458. DOI:10.1001/archsurg.1980.01380040079014 |
| [12] |
吴永隆, 陈思远, 陈秀兰, 等. 男性先天性中高位肛门直肠畸形的诊断及伴发畸形评估的临床研究[J].
第三军医大学学报, 2015, 37(13): 1349–1352.
WU Y L, CHEN S Y, CHEN X L, et al. Diagnosis for high and intermediate imperforate anus in male neonates and assessment of accompaniedmalformations[J]. J Thir Mil Med Univ, 2015, 37(13): 1349–1352. DOI:10.16016/j.1000-5404.201411030 |
| [13] | ODA O, DAVIES D, COLAPINTO K, et al. Loop versus divided colostomy for the management of anorectal malformations[J]. J PediatrSurg, 2014, 49(1): 87–90. DOI:10.1016/j.jpedsurg.2013.09.032 |
| [14] | VAN DEN HONDEL D, SLOOTS C, MEEUSSEN C, et al. To split or not to split: colostomy complications for anorectal malformations or hirschsprung disease: a single center experience and a systematic review of the literature[J]. Zeitschrift fur Kinderchirurgie, 2014, 24(1): 61–69. DOI:10.1055/s-0033-1351663 |



