2. 400714 重庆,中国科学院重庆绿色智能技术研究院
2. Chongqing Institute of Green and Intelligent Technology, Chinese Academy of Sciences, Chongqing, 400714, China
随着人口老龄化、城市现代化、农村城镇化、环境污染化、生活方式不良化和医学现代化,肺癌的发病人数逐年增多,且呈现年轻化趋势,其发病率及死亡率均为恶性肿瘤的首位[1],约70%的患者确诊肺癌时已为晚期。这与现有的诊断技术水平不高有着密切关系,不论是荧光支气管镜还是超声支气管镜均无法满足临床肺癌早期诊断的需要,故迫切需要开发新的诊断技术用于早期肺癌的诊断,以延长肺癌患者的生存时间[2]。太赫兹波段(0.1~10 THz或30 μm至3 mm)是人类迄今为止尚未完全了解的最后一个电磁波谱“空白”区[3]。由于太赫兹光谱的对非极性材料的特殊穿透性(对不透明的物体进行透视成像)和对生物体组织的无损伤特性[4], 使其在医疗诊断、物理、化学、电子信息、材料科学、天文学、大气与环境监测、通讯雷达、国家安全与反恐等方面具有重大的科学价值和应用前景[5]。目前已有太赫兹光谱技术用于脑胶质瘤[6]、乳腺癌[7]、结肠癌[8]、肝癌[9]、皮肤基底细胞癌[10]等肿瘤检测的相关报道,报道中明确指出肿瘤组织与正常组织的太赫兹光谱存在一定的差异,其中乳腺和皮肤等浅表性器官已经在个体开展应用研究[11-13]。
细胞癌变的病因在于细胞的异常增殖,该过程需要的物质基础首先是细胞中细胞器含量增加,由此带来的细胞中水含量和水状态的变化能被敏感的太赫兹波捕获。肿瘤细胞新陈代谢旺盛,核酸和蛋白质等生物大分子的含量较正常组织多[14],这也是太赫兹能够用于肿瘤诊断的理论基础[15]。
基于上述前期研究,本研究拟通过太赫兹光谱技术检测同一患者来源的肺癌组织、癌旁组织及正常肺组织标本,对比3类组织标本对太赫兹光谱的吸收率,初步探索太赫兹技术对早期肺癌诊断的作用,寻找具有特异性诊断价值的太赫兹频段。
1 对象与方法 1.1 组织标本来源收集2015年6-12月经我院胸外科手术切除、病理明确诊断为非小细胞肺癌患者30例,包括同一患者的肺癌组织标本、癌旁组织(距离瘤体2 cm的组织)标本、正常肺组织(距离瘤体5 cm的肺组织)标本。其中男性23例,女性7例;年龄36~82岁,中位年龄51.8岁;肺癌组织病理类型分别为:腺癌17例、鳞癌10例、大细胞肺癌2例、肉瘤样癌1例。所有组织样本在实验前进行例行组织病理学检查。
1.2 检测标本制作所有30例组织标本均经福尔马林溶液固定、酒精脱水、石蜡包埋,切片厚度为1 mm,切片组织固定于聚乙烯片上。
1.3 检测方法应用重庆中科院太赫兹检测中心的太赫兹时域光谱成像仪对每组组织切片标本进行检测标本进行检测,所采用太赫兹光谱频段为0.2~2.0 THz,检测标本大小25 mm2。
1.4 检测目的对比每组3种类型组织标本对太赫兹光谱的吸收率,寻找其差异,进一步求证太赫兹光谱技术能否应用于肺癌的早期诊断,同时探索可能具有特异性诊断价值的太赫兹频段。
1.5 统计学方法所得数据采用x±s表示,采用SPSS 18.0统计软件进行分析。计量资料比较用t检验,检验水准:α=0.05。
2 结果 2.1 样本收集与处理30例样本中,男性23例,女性7例;年龄小于50周岁的8例,50~60岁12例,60岁以上10例;具有吸烟史20例,不吸烟10例;肺腺癌,肺鳞癌,大细胞肺癌和肺肉瘤样癌各为17、10、2例和1例,其比例分别为56.67%、33.33%、6.67%和0.33%。
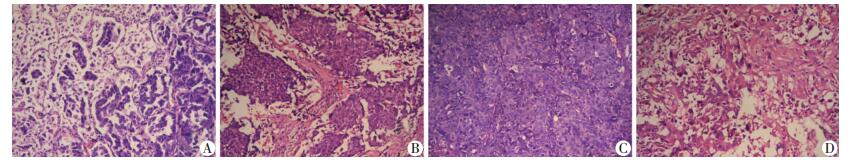
为了准确判定肺癌类型,我们对所有肿瘤组织样本进行病理组织切片分析,如图 1。
|
| A~D:分别代表肺腺癌、鳞癌、大细胞癌和肉瘤样癌组织 图 1 4种不同肺癌类型肿瘤组织病理学变化(HE ×200) |
2.2 特异性诊断价值太赫兹频段的探索 2.2.1 标本检测前处理及检测条件的优化
在太赫兹光谱测定中,很多因素会对影响测量结果。首先,我们测试了不同载玻片材质对测试的影响,结果显示聚乙烯材质玻片明显优于玻璃材质玻片(数据未显示)。为了尽量减少标本中水含量的影响,我们对每一组标本同时进行福尔马林溶液固定、酒精脱水和石蜡包埋等处理。在预实验中,我们探索了不同切片厚度对结果的影响,结果发现1 mm厚度较为理想(数据未显示)。因此在后续研究中,所用标本均采用此标准。此外,我们也探索了检测孔径对结果的影响,预实验中选择了10、5 mm和3 mm三种规格的孔径,结果显示小孔径明显优于大孔径,因考虑到3 mm孔径比较小,覆盖样本面积小,因此本实验最终选择了5 mm孔径。
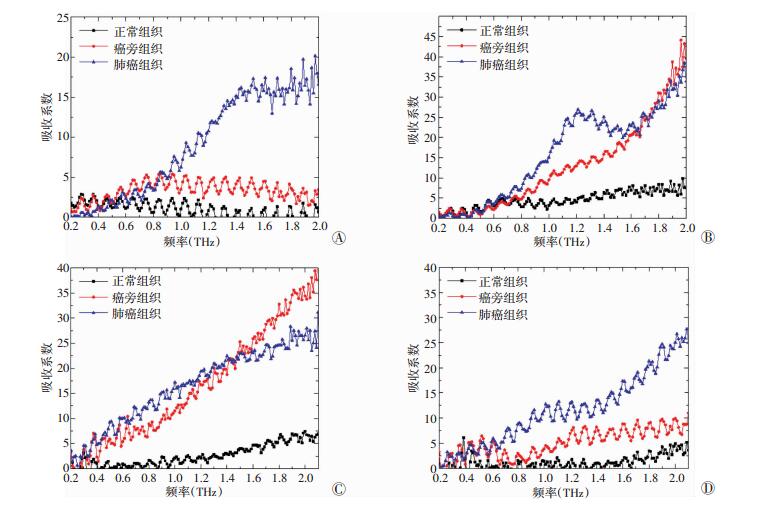
2.2.2 可能具有特异性诊断价值太赫兹频段的探索根据已经优化的测量条件,对4种不同的肺癌类型标本进行太赫兹波谱测定。正常组织标本对不同太赫兹波谱的吸收值均较低,但随着太赫兹波谱频率的增高,吸收值有轻微的增加的趋势。4种不同类型的肺癌组织标本的太赫兹吸收值,随着太赫兹波谱频率的增高,均显著地增强(图 2)。4组肿瘤组织标本的吸收值均明显高于正常组织,且随着波谱频率的增高,其差异越来越大。而癌旁组织标本与肺癌组织一样,总体来说,其太赫兹吸收值随着频率的增高和增大。腺癌和肉瘤样癌组中,癌旁组织吸收值微微高于正常组织,而明显低于肿瘤组织(图 2A、D)。而在鳞癌和大细胞肺癌组中,癌旁组织的吸收值及其变化趋势与肿瘤组织大体相似(图 2B、C)。
|
| A~D:分别代表肺腺癌,肺鳞癌,大细胞肺癌和肺肉瘤样癌;黑色线:正常组织标本(距离瘤体5 cm的肺组织)太赫兹吸收情况;红色线:癌旁组织标本(距离瘤体2 cm的组织);蓝色线:肺癌组织标本 图 2 4种不同肺部组织类型样品的太赫兹吸收效率谱分析 |
利用统计学方法,我们对图 2中的数据进行了统计学分析。我们选取了0.2~0.8 THz,0.8~1.4 THz和1.4~2.0 THz三个不同的太赫兹波段进行分析,评估其差异(表 1)。在0.2~0.8与0.8~1.4波段,结果呈现肿瘤组织>癌旁组织>正常组织的趋势。在1.4~2.0波段,肿瘤组织高于正常组织,且差异具有统计学意义,而且与前两个波段相比,其差异更为明显。在所有波段中,不同样本中癌旁组织的测量结果差异较大,特别是在1.4~2.0波段中(表 1)。综合上述分析数据,我们选择1.4~2.0波段作为后续大规模样本检测。
| 类别 | 0.2~0.8 | 0.8~1.4 | 1.4~2.0 |
| 正常组织 | 1.24±0.96 | 1.91±1.45 | 3.78±2.75 |
| 癌旁组织 | 2.91±1.67a | 8.19±5.16b | 17.29±12.87b |
| 肺癌组织 | 4.07±3.92a | 13.47±6.34b | 21.76±5.58b |
| a:P<0.05, 与正常组织比较; b: P<0.001, 与正常组织比较 | |||
2.2.3 大规模样本检测
根据确定的最佳太赫兹波段,针对前期收集的30例进行了测试和统计分析(表 2)。与正常组织比较,太赫兹波吸收曲线结果显示:肺癌组织标本在1.4、1.5、1.6、1.7、1.8、1.9THz和2.0 THz频率处均出现测量值显著升高的特征,差异具有统计学意义(P<0.001)。其中,在1.9 THz处差异最为显著(表 2)。癌旁组织与正常组织比较,其吸收值在各检测频率上均显著高于正常组(P<0.001)。与癌旁组织相比,在1.4 THz和1.5 THz处,肺癌组织吸收值明显较高,差异具有统计学意义(P<0.05),但在其他频率,因癌旁组织组差异较大,与肺癌组织相比,差异无统计学意义(P>0.05,表 2)。
| 类别 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 |
| 正常组织 | 2.64±2.53 | 2.89±1.98 | 3.19±2.17 | 4.12±2.71 | 4.65±3.02 | 3.54±2.28 | 4.66±3.27 |
| 癌旁组织 | 11.77±4.63a | 12.67±3.43b | 14.95±4.91b | 17.52±5.38b | 19.04±7.82a | 22.35±7.27b | 23.39±9.08a |
| 肺癌组织 | 19.07±5.55bc | 19.82±2.76bc | 19.57±3.67b | 20.35±2.17b | 21.86±2.51b | 23.31±3.15b | 26.55±7.64b |
| a: P<0.01, b: P<0.001, 与正常组织比较; c:P<0.05,与癌旁组织比较 | |||||||
3 讨论
作为最常见的恶性肿瘤,肺癌近年来的发病率和死亡率一直居高不下。肿癌的早期诊断与治疗是提高肺癌患者生存率和改善预后的关键。影像学是肺癌诊断的主要手段之一,也是肺癌早期诊断的重要手段,但各种影像学检测都只能发现“病灶”,而不能最终确诊[16]。病理学检测是现在肺癌诊断的金标准,但该方法需要活检标本,会对患者造成一定程度的伤害,且很大程度上受制于医师经验,因此不能作为肺癌早期诊断与常规体检项目。本研究利用太赫兹光谱技术,对人肺癌组织标本进行检测,并同时比较肺癌组织、癌旁组织及正常肺组织之间的差异,筛选出具有特异性诊断价值的太赫兹频段,初步探索太赫兹光谱技术用于肺癌的早期诊断。
在太赫兹光谱测量过程中,多种因素会影响测量的结果,其中之一就是水含量。水分对太赫兹吸收的影响占据主要地位,在肾癌组织中,新鲜组织的吸收系数明显高于脱水后的组织[17]。与正常组织相比,肿瘤组织的含水量更高,这也是太赫兹光谱技术可以应用于区分肿瘤组织和正常组织的重要原因[15]。研究表明,石蜡包埋是一种能够有效降低水分影响的方法[18],利用该方法,研究人员发现胃癌组织与正常组织相比,太赫兹吸收光谱有明显差异[19]。在本研究中,我们采用石蜡切片的方法,降低水分的影响,以尽量减少不确定因素。
肿瘤组织与其旁边正常组织的自身差异是造成太赫兹光谱吸收差异的另外一个重要因素。与正常细胞相比,肿瘤细胞细胞核具有畸形,体积大,核膜厚,核质比失常以及染色加深等一系列特征。大部分恶性肿瘤细胞代谢率高,增殖快,核酸和蛋白等大分子的含量较正常细胞高[14]。研究表明,在新鲜组织中,水分含量的差异是导致太赫兹吸收率差异的重要原因[20],而脱水后,组织自身组成成分特点,如核酸、蛋白质的含量差异,就成为太赫兹检测的关键因素[21-22]。
在利用太赫兹时域光谱技术检测肿瘤组织与癌旁组织时,发现二者之间差异性较小,且不同患者癌旁组织之间相比差异特别大。总结其原因,可能是由肿瘤的侵袭与转移造成的,收集样本时,距离癌组织2 cm的肺组织被作为癌旁组织。而事实上,肿瘤组织都具有不同程度的侵袭与转移的能力,在收集的癌旁组织中,可能存在一定数量的肿瘤细胞,所以在检测时,部分癌旁组织与肿瘤组织表现出相似的太赫兹光谱吸收能力,也提示太赫兹检测灵敏度较高,可能具有临床应用价值。
本研究利用太赫兹时域光谱技术,尝试对人肺癌进行诊断检测。分别比较了脱水后的肺癌组织、癌旁组织及正常肺组织样本的对太赫兹波的响应。本研究结果表明,太赫兹光谱技术有可能成为肺癌早期诊断的有效技术。下一步,一方面我们将扩大样本量对所获结果进行验证,另外一方面尝试在体外对新鲜肺癌组织标本进行检测,探索有效的太赫兹检测条件及太赫兹频段;同时考虑与相关单位合作,将太赫兹时域光谱技术与纤支镜技术相结合,尝试体内实时检测肺癌,为太赫兹技术在临床医学,特别是肺癌等重大疾病的早期诊断提供新的理论和临床依据。
| [1] | PARKIN D M, PISANI P, FERLAY J. Global cancer statistics[J]. CA Cancer J Clin, 1999, 49(1): 33–64, 1. DOI:10.3322/canjclin.49.1.33 |
| [2] |
刘毅, 初向阳. 多原发非小细胞肺癌诊断、治疗及预后的系统性综述[J].
解放军医学院学报, 2016, 37(8): 901–904.
LIU Y, CHU X Y. Diagnosis, treatment and prognosis of patients with multiple primary non small cell lung cancer: A systematic review[J]. Acad J Chin PLA Med School, 2016, 37(8): 901–904. DOI:10.3969/j.issn.2095-5227.2016.08.022 |
| [3] | DAVIES G, LINFIELD E. Bridging the terahertz gap[J]. Physics World, 2004, 17(4): 37–41. DOI:10.1088/2058-7058/17/4/34 |
| [4] |
FERGUSONB, 张希成. 太赫兹科学与技术研究回顾[J].
物理, 2003, 32(05): 0–0.
FERGUSON B, ZHANG X C. Materials for terahertz science and technology[J]. Physics, 2003, 32(05): 0–0. DOI:10.3321/j.issn:0379-4148.2003.05.002 |
| [5] | OH S J, KANG J, MAENG I, et al. Nanoparticle-enabled terahertz imaging for cancer diagnosis[J]. Opt Express, 2009, 17(5): 3469–3475. DOI:10.1364/oe.17.003469 |
| [6] | MENG K, CHEN T N, CHEN T, et al. Terahertz pulsed spectroscopy of paraffin-embedded brain glioma[J]. J Biomed Opt, 2014, 19(7): 077001. DOI:10.1117/1.JBO.19.7.077001 |
| [7] | TRUONG B C, TUAN H D, FITZGERALD A J, et al. Breast cancer classification using extracted parameters from a terahertz dielectric model of human breast tissue[J]. Conf Proc IEEE Eng Med Biol Soc, 2015, 2015: 2804–2807. DOI:10.1109/EMBC.2015.7318974 |
| [8] | WAHAIA F, VALUSIS G, BERNARDO L M, et al. Detection of colon cancer by terahertz techniques[J]. Journal of Molecular Structure, 2011, 1006(1-3): 77–82. DOI:10.1016/j.molstruc.2011.05.049 |
| [9] | WAHAIA F, VALUSIS G, BERNARDO L M, et al. Detection of colon cancer by terahertz techniques[J]. Journal of Molecular Structure, 2011, 1006(1-3): 77–82. DOI:10.1016/j.molstruc.2011.05.049 |
| [10] | MIURA Y, KAMATAKI A, UZUKI M, et al. Terahertz-wave spectroscopy for precise histopathological imaging of tumor and non-tumor lesions in paraffin sections[J]. Tohoku J Exp Med, 2011, 223(4): 291–296. DOI:10.1620/tjem.223.291 |
| [11] | RAHMAN A, RAHMAN A K, RAO B. Early detection of skin cancer via terahertz spectral profiling and 3D imaging[J]. Biosens Bioelectron, 2016, 82: 64–70. DOI:10.1016/j.bios.2016.03.051 |
| [12] | YU C, FAN S, SUN Y, et al. The potential of terahertz imaging for cancer diagnosis: a review of investigations to date[J]. Quant Imaging Med Surg, 2012, 2(1): 33–45. DOI:10.3978/j.issn.2223-4292.2012.01.04 |
| [13] | FITZGERALD A J, BERRY E, ZINOV'EV N N, et al. Catalogue of human tissue optical properties at terahertz frequencies[J]. J Biol Phys, 2003, 29(2-3): 123–128. DOI:10.1023/A:1024428406218 |
| [14] | JOSEPH C S, YAROSLAVSKY A N, NEEL V A, et al. Continuous wave terahertz transmission imaging of nonmelanoma skin cancers[J]. Lasers Surg Med, 2011, 43(6): 457–462. DOI:10.1002/lsm.21078 |
| [15] | ASHWORTH P C, PICKWELL-MACPHERSON E, PROVENZANO E, et al. Terahertz pulsed spectroscopy of freshly excised human breast cancer[J]. Opt Express, 2009, 17(15): 12444–12454. DOI:10.1364/oe.17.012444 |
| [16] | BRUEHLMEIER M, ROELCKE U, BLÄUENSTEIN P, et al. Measurement of the extracellular space in brain tumors using 76Br-bromide and PET[J]. J Nucl Med, 2003, 44(8): 1210–1218. |
| [17] |
周纯武. 影像学在肿瘤诊治中的作用[J].
癌症进展, 2006, 4(2): 110–110.
ZHOU C W. The role of imaging in the diagnosis and treatment of tumor[J]. Oncol Prog, 2006, 4(2): 110–110. DOI:10.3969/j.issn.1672-1535.2006.02.004 |
| [18] |
李晗, 余晨. 太赫兹波对肾癌组织的光谱检测[J].
红外与激光工程, 2016, 001(5): 160–165.
LI H, YU C. Terahertz spectral detection in human renal tissue[J]. Infrared Laser Eng, 2016, 001(5): 160–165. DOI:10.3788/IRLA201645.0525001 |
| [19] | WAHAIA F, KASALYNAS I, SELIUTA D, et al. Study of gastric cancer samples using terahertz techniques[J]. Second International Conference on Applications of Optics and Photonics, 2014. DOI:10.1117/12.2063463 |
| [20] | HOU D, LI X, CAI J, et al. Terahertz spectroscopic investigation of human gastric normal and tumor tissues[J]. Phys Med Biol, 2014, 59(18): 5423–5440. DOI:10.1088/0031-9155/59/18/5423 |
| [21] | QIAO W, YANG K, THOMA A, et al. Dielectric relaxation of HCl and NaCl solutions investigated by terahertz time-domain spectroscopy[J]. Journal of Infrared Millimeter and Terahertz Waves, 2012, 33(10): 1029–1038. DOI:10.1007/s10762-012-9920-z |
| [22] | KNAB J R, CHEN J Y, HE Y, et al. Terahertz measurements of protein relaxational dynamics[J]. Proceedings of the IEEE, 2007, 95(8): 1605–1610. DOI:10.1109/JPROC.2007.898906 |
| [23] | ZHANG W, BROWN E R, RAHMAN M, et al. Observation of terahertz absorption signatures in microliter DNA solutions[J]. Applied Physics Letters, 2013, 102(2): 023701. DOI:10.1063/1.4775696 |



