腰椎多节段退行性疾病临床发病率高,多发生于老年患者,常合并腰椎退行性侧弯、腰椎后凸、腰椎退行性滑脱等。随着融合技术的发展,融合率已逐渐提高,成为目前治疗腰椎退行性疾病的主要外科治疗方式之一[1]。在早期缓解临床症状方面疗效明确,然而远期可导致邻椎病(adjacent segment disease, ASD)、腰部运动功能受限等并发症[2]。Ghiselli等[3]报道在腰椎融合术后10年的随访中,发生退变的邻近节段数量明显增加。近年,Dynesys动态固定系统逐渐发展,其特点是在稳定病变节段、维持椎间隙高度的同时,保留腰椎部分的运动功能,降低对邻近节段的应力负荷,从理论上可减轻甚至避免ASD的发生[4]。本研究通过随访2013年1月至2014年5月于我科行多节段腰椎Dynesys动态固定术和腰椎融合术的患者,探讨Dynesys动态固定系统在腰椎多节段退行性疾病治疗中的临床疗效及对腰椎运动功能的影响。
1 资料与方法 1.1 临床资料收集2013年1月至2014年5月于我科采用腰椎Dynesys动态固定术治疗腰椎多节段退行性疾病的28例患者,纳入Dynesys动态固定组24例,其中男性9例,女性15例,平均年龄53.8(39~71) 岁。其中腰椎间盘突出症22例,腰椎侧弯7例,腰椎管狭窄症4例,腰椎退行性滑脱5例。同期行多节段内固定融合组根据纳入标准纳入27例,其中男性14例,女性13例,平均年龄53.9(40~67) 岁,其中腰椎间盘突出症24例,腰椎侧弯9例,腰椎管狭窄症3例,腰椎退行性滑脱6例。本研究经本院伦理委员会批准[批件号:2012年伦理科研第(14) 号],患者签署知情同意书。
纳入标准:① 30~75岁;② 多节段腰椎退行性疾病,包括退行性失稳及滑脱、腰椎管狭窄、椎间盘突出、退行性腰椎侧弯等,并持续存在临床症状:腰痛或下肢放射痛,肌力减弱和/或感觉异常;③ 接受腰椎双节段以上动态固定术或融合术并同时行必要的椎管减压和(或)髓核摘除;④ 患者均有至少6、12、24个月随访的完整资料,行VAS评分、ODI评分,有腰椎正侧、过伸过屈位X线片。排除标准:① 脊柱骨折、强直性脊柱炎、脊柱结核、脊柱感染、脊柱肿瘤,伴有颈椎病症状;② 马尾综合征导致完全性大小便功能障碍;③ 合并严重内科疾病及心理障碍。
1.2 手术方式患者均采用静吸复合全麻,C型臂X线透视椎弓根定位。Dynesys动态固定组行腰部后正中切口,采用Wiltse入路,显露椎弓根螺钉进钉点,小心剥离,避免破坏小关节囊,在上关节突外侧缘与横突中线连线的交点行椎弓根螺钉置入,术中C臂X线透视机确认椎弓根螺钉位置良好。根据患者症状体征及影像学资料对责任节段进行开窗潜行扩大减压或髓核摘除。根据Dynesys手术标准行PET连接器和PCU间隔器安装。冲洗创口,双侧放置引流管,逐层缝合。融合手术采用传统TLIF手术后正中入路,对每个责任节段进行减压及椎间植骨融合[5]。
1.3 术后处理术后给予抗感染、抗炎、脱水等治疗,引流液少于10 mL拨出引流管,术后3~5 d下床活动,进行功能锻炼。
1.4 观察指标 1.4.1 临床观察指标根据手术病历记录手术时间、出血量。所有患者在术前及术后6、12、24个月行VAS评分及ODI评分。
1.4.2 影像学观察指标在PACS系统中行3次测量然后取平均值为影像学结果。所有患者在术前及术后6、12、24个月行腰椎正侧位、过伸过屈位X线检查。手术节段椎间活动度:测量固定节段上终板和下终板在过伸过曲位的夹角,夹角差即为手术节段椎间活动度。腰椎整体活动度:测量L1椎体上终板与S1椎体上终板之间的夹角,过伸过屈位该夹角差值为腰椎整体活动度。上一椎间活动度:测量固定节段上终板与上一椎体下终板在过伸过屈位的夹角,夹角差即为上一椎间活动度。上一椎间高度:测量冠状位固定节段上终板与上一椎体下终板椎体前后缘距离之和的平均值。术后影像学提示手术节段或邻近自由节段出现退行性小关节炎、椎间盘骨化、节段性不稳、椎间隙变窄、骨赘形成时,判定为手术节段退变进展或出现ASD。
1.5 统计学分析采用SPSS 20.0统计软件,两组间患者平均年龄、出血量、手术时间的比较进行独立样本t检验,对术前、术后VAS评分,X线测量数据进行重复测量方差分析。检验水准α=0.05。
2 结果 2.1 两组一般资料Dynesys组24例,其中男性9例,女性15例,平均随访25.9(23~30) 个月;融合组27例,其中男性14例,女性13例,平均随访26.5(24~31) 个月。两组患者术后临床症状均得到明显缓解或消失。两组患者基本资料见表 1。
| 组别 | n | 诊断 | 手术节段 | |||||||
| 腰椎间盘突出症 | 腰椎退行性侧弯 | 腰椎管狭窄症 | 腰椎退行性滑脱 | L2~S1 | L3~L5 | L3~S1 | L4~S1 | |||
| Dynesys组 | 24 | 22 | 7 | 4 | 5 | 1 | 4 | 3 | 16 | |
| 融合组 | 27 | 24 | 9 | 3 | 6 | 2 | 4 | 6 | 15 | |
2.2 VAS评分及ODI评分
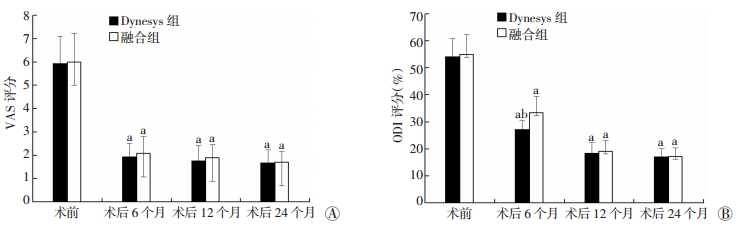
两组VAS评分、ODI评分术后各时间点与同组术前比较,差异有统计学意义(P < 0.01,图 1)。术前及术后6、12、24个月各时间点VAS评分两组间比较差异无统计学意义;术前及术后12、24个月各时间点ODI评分两组间比较差异无统计学意义,术后6个月ODI评分两组间比较差异有统计学意义(P < 0.05)。
|
| A:VAS评分;B:ODI评分a:P < 0.01,与术前比较;b:P < 0.05,与融合组比较 图 1 两组多节段腰椎退行性疾病患者VAS评分及ODI评分比较 |
2.3 手术时间及出血量
Dynesys组、融合组手术时间分别为(207.23±52.53) min和(248.00±57.62) min,差异有统计学意义(P < 0.05);出血量Dynesys组、融合组分别为(408.25±201.6) mL和(625.24±212.9) mL,差异有统计学意义(P < 0.01)。
2.4 腰椎影像学分析两组患者术前腰椎整体活动度、手术节段活动度、邻近上一椎间活动度、邻近上一椎间高度,组间比较差异无统计学意义;而两组患者术后腰椎整体活动度均有明显下降,差异有统计学意义(P < 0.05,表 2)。Dynesys组保留了部分手术节段活动度,术后各时间点与术前相比,差异有统计学意义(P < 0.01);而融合组因术后内固定融合而失去活动度。两组患者邻近上一椎间活动度术前及术后6、12个月组间比较差异无统计学意义,术后24个月组间比较差异有统计学意义(P < 0.05)。Dyensys组邻近上一椎间活动度术前与术后6、12个月比较,差异无统计学意义,与术后24个月比较,差异有统计学意义(P < 0.05);融合组邻近上一节段椎间活动度术前与术后6、12个月比较,差异无统计学意义,与术后24个月比较,差异有统计学意义(P < 0.01)。两组患者各时间点邻近上一椎体椎间高度组间及组内比较差异均无统计学意义(表 3)。
| 组别 | n | 腰椎整体活动度(°) | 手术节段活动度(°) | |||||||
| 术前 | 术后6个月 | 术后12个月 | 术后24个月 | 术前 | 术后6个月 | 术后12个月 | 术后24个月 | |||
| Dynesys组 | 24 | 40.65±12.51 | 25.83±8.36ab | 28.05±10.94ab | 32.63±11.46ab | 20.02±11.03 | 6.60±5.06a | 5.68±4.39a | 9.11±6.81a | |
| 融合组 | 27 | 37.83±16.48 | 21.14±10.19a | 21.73±6.91a | 25.54±4.29a | 17.98±9.10 | 0 | 0 | 0 | |
| a:P < 0.05,与同组术前比较;b:P < 0.05,与融合组比较 | ||||||||||
| 组别 | n | 上一椎体活动度(°) | 上一椎间高度(mm) | |||||||
| 术前 | 术后6个月 | 术后12个月 | 术后24个月 | 术前 | 术后6个月 | 术后12个月 | 术后24个月 | |||
| Dynesys组 | 24 | 7.51±2.54 | 7.92±3.22 | 8.78±2.21 | 9.23±1.97ab | 11.67±2.33 | 11.50±2.34 | 11.22±2.73 | 10.44±2.74 | |
| 融合组 | 27 | 7.97±2.43 | 7.31±2.89 | 9.87±2.08a | 11.22±2.11a | 12.26±2.06 | 11.37±1.24 | 11.80±1.84 | 11.02±1.67 | |
| a:P < 0.05,与同组术前比较;b:P < 0.05,与融合组比较 | ||||||||||
2.5 邻椎病及术后并发症
Dynesys组1例患者出现1枚螺钉的“Halo”征,融合组3例病例出现邻近节段不稳,但无明显临床症状,未行临床干预。
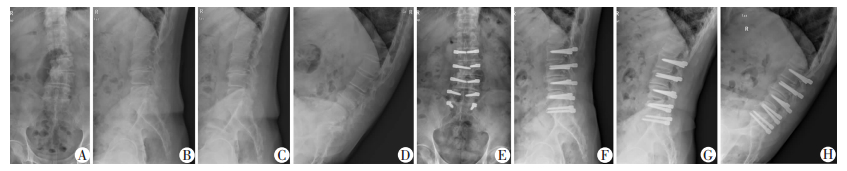
2.6 典型病例典型病例1:老年男性,69岁,因“腰背部疼痛伴间歇性跛行4年,加重2个月”入院,诊断为腰3椎体退行性滑脱(Ⅰ°)伴腰椎管狭窄症,腰2/3、3/4、4/5,腰5骶1椎间盘膨出。行L3/4、L4/5、L5/S1椎间盘摘除、L2~S1 Dynesys动态固定术。术前VAS评分7,ODI评分60.0%;术后6个月VAS评分2,ODI评分20%;术后24个月VAS评分0,ODI评分12%。术后2年随访时手术节段无复发,邻近节段退变未见明显加重(图 2)。
|
| A~D:术前正位、侧位、过伸、过屈位X线片;E~H:术后2年正位、侧位、过伸、过屈位X线片 图 2 腰3椎体退行性滑脱伴腰椎管狭窄症患者多节段Dynesys手术前后X线片表现 |
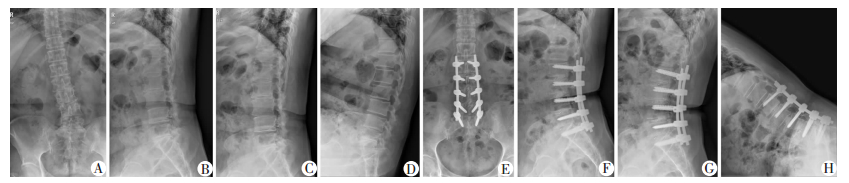
典型病例2:老年女性,66岁,因“腰痛伴双下肢乏力5年,加重伴左下肢放射痛2年”入院,诊断为腰椎管狭窄症,腰椎间盘突出症,腰椎退行性侧弯。行L2/3、L3/4、L4/5、L5/S1椎管减压,植骨融合内固定术。术前VAS评分5,ODI评分65.0%;术后6个月VAS评分3,ODI评分28%;术后24个月VAS评分2,ODI评分17%。术后2年随访时腰椎活动受限(图 3)。
|
| A~D:术前正位、侧位、过伸、过屈位X线片;E~H:术后2年正位、侧位、过伸、过屈位X线片 图 3 腰椎管狭窄症患者多节段融合手术前后X线片表现 |
3 讨论
腰椎多节段退行性疾病多发生于老龄患者,常合并脊柱侧弯、脊柱后凸畸形等[6-7],目前多采用腰椎融合术进行治疗,通过椎间植骨融合达到避免复发、改善临床症状的目的,但同时导致腰椎活动功能的丢失、慢性腰背痛、假关节形成、融合率低、螺钉松动断裂、ASD等,成为影响患者术后远期临床疗效的重要问题[8-9]。Sears等[10]对912例行腰椎融合术患者进行中长期随访研究也证实融合术可加速ASD的发生,融合两个节段ASD发生率分别为5年内(17.2%)、5~10年(30.9%)、10年以上(36.1%),而融合三节段以上ASD的发生率5年内(28.9%)、5~10年(40.2%)、10年以上(40.2%)。尽管随着融合技术的发展,临床融合率显著提高,而患者满意度却未见明显提高。
腰椎融合术后生物力学的改变是导致ASD的主要原因。融合术后椎间盘内压增大、小关节负荷加重、过度活动以及邻近节段应力负荷短期内迅速加大,尤其是术前邻近节段已经存在退变,可加速ASD的发生[11-12]。近年,Dynesys动态固定系统被应用于多节段腰椎退行性疾病的治疗,它在保留固定节段部分活动度的同时,限制不稳定节段的异常活动,降低椎间盘内压、减轻小关节负荷,从而获得较好的临床疗效。Schmoelz等[13]认为Dynesys动态固定技术可以作为融合手术的替代手术方式,并能在维持手术节段稳定的情况下,保留部分椎间活动度,减缓ASD的发生。本研究通过回顾性分析比较Dynesys组和融合组ASD发生率方面未见明显差异,这可能是因为随访时间尚短。有研究表明,Dynesys动态固定系统针对老年患者能取得更好的临床疗效[14],这可能与老年人全身整体关节功能下降,保留更多的运动功能尤其是腰椎的运动功能更有助于生活质量的提高有关。而且,Dynesys动态固定系统可以缩短住院时间、术后早期功能锻炼时间,减少手术时间以及手术出血量等[15],降低手术风险和创伤,还可以有效减缓邻近节段病理进程(ASP)[16]。Payer等[17]对30例腰椎间盘突出症伴椎管狭窄的患者随访发现,Dynesys动态固定系统在早期(尤其是在术后6个月左右)可获得更好的临床疗效。通过本研究我们发现,两组患者VAS评分、ODI评分与术前相比均显著下降,而术后6个月ODI评分两组组间比较差异有统计学意义,这与Payer等[17]的研究结果一致。
目前对于Dynesys动态固定系统是否可以阻止ASD的发生仍存在争议。Vaga等[18]对10例Dynesys动态固定术后患者行糖胺多糖(GAG)测定,发现动态固定可以有效延缓甚至逆转部分椎间盘的退变,同时也会导致邻近节段椎间盘基质成分的改变;而Kumar等[19]对20例Dynesys、12例融合术患者术后2年MRI T2加权相椎间盘Woodend分级进行分析,发现椎间盘的退变及邻椎病的发生是一种自然的病理进程。本研究通过对24例多节段Dynesys、27例融合术后患者进行2年的随访分析,发现两种术式术后腰椎整体活动度均有不同程度的下降,而Dynesys组与融合组比较在术后6、12、24个月保留了更多的活动度,尤其是在术后24个月较融合组多保留约7°的活动度;在手术节段活动度方面,Dynesys组术后24个月仍保留约9°的活动度,这可能是Dynesys组较融合组有更大活动度的原因。两种手术方式术后邻近上一椎间活动度在术后12、24个月较术前增大,而融合组增大的程度较Dynesys动态固定组高。ASD的发生与患者自身的年龄、性别、术前邻近节段退变程度、术后生活方式等密切相关[6, 20],而长节段的固定、矢状面平衡的丢失等也是重要的危险因素[21]。所以,在ASD的发生率方面早期两种手术方式无明显差异,两种手术方式均不能阻止ASD的发生,但融合术较Dynesys动态固定系统更容易导致ASD的发生。
Dynesys动态固定系统在体内长期承受力学作用,且具有部分活动度,可能会增加钉棒断裂及螺钉松动的风险,而且由于对前中椎支撑不够,不适用于腰椎反曲、后凸的患者。本组病例中Dynesys动态固定组发现1例患者出现1枚螺钉的“Halo”征,无螺钉及连接棒断裂,但无明显临床症状,未行临床干预。融合组固定节段未发现内置物并发症,但有3例患者出现邻近节段不稳,这可能与长节段的内固定导致邻近节段的应力负荷增加有关。
综上所述,Dynesys动态固定系统和融合术均能较好地缓解临床症状。与融合术相比,Dynesys动态固定系统保留了更多的活动度、降低了ASD的发生风险,可以作为一种较好的手术治疗选择。由于本研究样本量较小、随访时间较短,远期临床疗效及相关临床并发症亟待进一步长期随访观察。
| [1] | Zeng Z Y, Wu P, Sun D T, et al. Two different fixation methods combined with lumbar interbody fusion for the treatment of two-level lumbar vertebra diseases: a clinical comparison study[J]. Zhongguo Gu Shang, 2015, 28(10): 903–909. |
| [2] | Stoffel M, Behr M, Reinke A, et al. Pedicle screw-based dynamic stabilization of the thoracolumbar spine with the Cosmic-system: a prospective observation[J]. Acta Neurochir(Wien), 2010, 152(5): 835–843. DOI:10.1007/s00701-009-0583-z |
| [3] | Ghiselli G, Wang J C, Bhatia N N, et al. Adjacent segment degeneration in the lumbar spine[J]. J Bone Joint Surg Am, 2004, 86-A(7): 1497–1503. |
| [4] | Zhang Y, Shan J L, Liu X M, et al. Comparison of the Dynesys Dynamic Stabilization System and Posterior Lumbar Interbody Fusion for Lumbar Degenerative Disease[J]. PLoS One, 2016, 11(1): e0148071. DOI:10.1371/journal.pone.0148071 |
| [5] | Mobbs R J, Phan K, Malham G, et al. Lumbar interbody fusion: techniques, indications and comparison of interbody fusion options including PLIF, TLIF, MI-TLIF, OLIF/ATP, LLIF and ALIF[J]. J Spine Surg, 2015, 1(1): 2–18. DOI:10.3978/j.issn.2414-469X.2015.10.05 |
| [6] | Lazennec J Y, Pouzet B, Ramare S, et al. Anatomic basis of minimal anterior extraperitoneal approach to the lumbar spine[J]. Surg Radiol Anat, 1999, 21(1): 7–15. DOI:10.1007/BF01635046 |
| [7] | Wang Q, Liu J, Shi Y, et al. Short-term effects of a dynamic neutralization system (Dynesys) for multi-segmental lumbar disc herniation[J]. Eur Spine J, 2016, 25(5): 1409–1416. DOI:10.1007/s00586-015-4307-1 |
| [8] | Ekman P, Möller H, Shalabi A, et al. A prospective randomised study on the long-term effect of lumbar fusion on adjacent disc degeneration[J]. Eur Spine J, 2009, 18(8): 1175–1186. DOI:10.1007/s00586-009-0947-3 |
| [9] |
徐灿华, 吴增晖, 郑轶, 等. 腰椎极外侧入路椎间融合术在腰椎融合术后邻近节段病变中的初步应用[J].
第三军医大学学报, 2014, 36(17): 1837–1841.
Xu C H, Wu Z H, Zheng Y, et al. Extreme lateral intervertebral fusion in treatment of adjacent segment deterioration after lumbar fusion:report of 9 cases[J]. J Third Mil Med Univ, 2014, 36(17): 1837–1841. |
| [10] | Sears W R, Sergides I G, Kazemi N, et al. Incidence and prevalence of surgery at segments adjacent to a previous posterior lumbar arthrodesis[J]. Spine J, 2011, 11(1): 11–20. DOI:10.1016/j.spinee.2010.09.026 |
| [11] | Liao J C, Chen W J, Chen L H, et al. Surgical outcomes of degenerative spondylolisthesis with L5-S1 disc degeneration: comparison between lumbar floating fusion and lumbosacral fusion at a minimum 5-year follow-up[J]. Spine(Phila Pa 1976), 2011, 36(19): 1600–1607. DOI:10.1097/BRS.0b013e3181f99e11 |
| [12] | Park P, Garton H J, Gala V C, et al. Adjacent segment disease after lumbar or lumbosacral fusion: review of the literature[J]. Spine(Phila Pa 1976), 2004, 29(17): 1938–1944. DOI:10.1097/01.brs.0000137069.88904.03 |
| [13] | Schmoelz W, Huber J F, Nydegger T, et al. Dynamic stabilization of the lumbar spine and its effects on adjacent segments: an in vitro experiment[J]. J Spinal Disord Tech, 2003, 16(4): 418–423. DOI:10.1097/00024720-200308000-00015 |
| [14] | Gédet P, Haschtmann D, Thistlethwaite P A, et al. Comparative biomechanical investigation of a modular dynamic lumbar stabilization system and the Dynesys system[J]. Eur Spine J, 2009, 18(10): 1504–1511. DOI:10.1007/s00586-009-1077-7 |
| [15] | Lee C H, Jahng T A, Hyun S J, et al. Dynamic stabilization using the Dynesys system versus posterior lumbar interbody fusion for the treatment of degenerative lumbar spinal disease: a clinical and radiological outcomes-based meta-analysis[J]. Neurosurg Focus, 2016, 40(1): E7. DOI:10.3171/2015.10.FOCUS15426 |
| [16] | Lee S E, Jahng T A, Kim H J, et al. Clinical Experiences of Non-fusion Dynamic Stabilization Surgery for Adjacent Segmental Pathology after Lumbar Fusion[J]. Int J Spine Surg, 2016, 10: 8. DOI:10.14444/3008 |
| [17] | Payer M, Smoll N R, Oezkan N, et al. Dynamic transpedicular stabilisation and decompression in single-level degenerative anterolisthesis and stenosis[J]. Acta Neurochir (Wien), 2014, 156(2): 221–227. DOI:10.1007/s00701-013-1956-x |
| [18] | Vaga S, Brayda-Bruno M, Perona F, et al. Molecular MR imaging for the evaluation of the effect of dynamic stabilization on lumbar intervertebral discs[J]. Eur Spine J, 2009, 18(Suppl 1): 40–48. DOI:10.1007/s00586-009-0996-7 |
| [19] | Kumar A, Beastall J, Hughes J, et al. Disc changes in the bridged and adjacent segments after Dynesys dynamic stabilization system after two years[J]. Spine (Phila Pa 1976), 2008, 33(26): 2909–2914. DOI:10.1097/BRS.0b013e31818bdca7 |
| [20] | Kaito T, Hosono N, Mukai Y, et al. Induction of early degeneration of the adjacent segment after posterior lumbar interbody fusion by excessive distraction of lumbar disc space[J]. J Neurosurg Spine, 2010, 12(6): 671–679. DOI:10.3171/2009.12.SPINE08823 |
| [21] | Tang S, Rebholz B J. Does lumbar microdiscectomy affect adjacent segmental disc degeneration? A finite element study[J]. J Surg Res, 2013, 182(1): 62–67. DOI:10.1016/j.jss.2012.09.012 |



