2. 400038 重庆,第三军医大学西南医院:放射科;
3. 重庆,第三军医大学西南医院:老年科
2. Department of Radiology, Southwest Hospital, Third Military Medical University, Chongqing, 400038, China;
3. Department of Geriatrics, Southwest Hospital, Third Military Medical University, Chongqing, 400038, China
我国肺癌的发病率和病死率均居恶性肿瘤的首位[1],其中非小细胞肺癌 (non-small cell lung cancer,NSCLC) 占80%~90%。近年来,肺癌的分子生物学指标作为评估肺癌患者预后相关信息的方法之一,越来越受到重视[2-5]。磁共振弥散加权成像 (diffusion weighted imaging, DWI) 利用质子成像原理,能反映肿瘤内部更多的生理病理学特点,为肺癌的诊断、治疗评估及预后提供相关信息,因而逐渐应用于临床研究[6-8]。表观弥散系数 (apparent diffusion coefficient, ADC) 是DWI中反映水分子运动的指标,能反映肿瘤细胞排列致密程度、细胞基质、细胞膜的完整性。有研究指出[9-10],ADC值与肺癌病理分级、细胞密度、EGFR及Ki67等预后病理分子生物学指标密切相关,但相关研究仍较少,且其对于肺癌预后的临床意义及应用价值需要更多研究加以证实。因此,本研究选取了常见的肺癌预后分子生物学指标 (CEA、Ki67、TTF-1及EGFR),进一步探索弥散加权磁共振ADC值与NSCLC的生物学预后指标之间的相关性,为肺癌的诊治提供更多参考信息。
1 资料与方法 1.1 临床资料收集2015年4月至2016年9月期间在第三军医大学西南医院呼吸内科门诊及住院部符合纳入排除标准的NSCLC患者共39例,其中男性31例,女性8例,年龄42~74(58.00±8.36) 岁。纳入标准:① 经纤支镜活检或穿刺活检等方式病理证实为NSCLC;② 患者均能耐受MRI检查且无相关禁忌证;③ 在检查前均未行肿瘤相关治疗;④ 取得患者知情同意并配合行DWI检查。排除标准:① 患者临床病历资料及免疫组化相关信息不全;② 术后复发的患者;③ DWI图像上伪影较重无法测量相关参数者。该研究已通过我院伦理委员会审查 (2014年9月),入组患者均签署知情同意书。对入选者行DWI检查 (诊断后1周以内),并对其临床特点、血CEA水平和病理切片中组织的免疫组化结果作回顾性分析。
1.2 方法 1.2.1 MRI检查及图像分析采用西门子SIEMENS Trio 3.0T磁共振成像设备, 患者采取仰卧体位,先行常规横轴位T1WI、T2WI扫描后行横轴位DWI扫描,DWI采用平面回波序列成像横断位扫描 (echo-planar MR):TR 3 000 ms,TE 68 ms,FOV 380 mm,b值= 50/400/800 mm2/s,层厚5 mm,层间距1 mm,扫描层数18层。扫描时患者自由均匀呼吸, 采用置于膈肌位置的导航条门控,平均扫描时间3~4 min。扫描结束后在SIEMENS的后处理工作站上对ADC图进行图像后处理并测量ADC值。由两位高年资放射科医师采用双盲法统一进行图像测量,取均值为最终ADC值。病变感兴趣区ROI选取病灶信号强度最大的层面及其上下2个层面共3个层面测量其均值,对于含空洞和毛玻璃成分的不均匀病灶,ROI需包括最大信号强度中心的区域[11]。
1.2.2 病理分析及临床相关资料所有标本经石蜡包埋、切片、常规HE染色以及免疫组化染色,由本院病理科高年资医师诊断得出病理结果。Ki67、TTF-1及EGFR均采用国际标准的免疫组化二步法进行检验,Ki67、TTF-1及EGFR以细胞核染成棕黄色或者褐色为阳性细胞。Ki67在低倍至高倍镜下观察、计数并做好记录染色阳性的肿瘤细胞百分数 (%)。TTF-1、EGFR表达情况的检测根据切片中阳性细胞数定义,阳性细胞数<10%为表达阴性,阳性细胞数≥10%为表达阳性。患者均系在治疗前空腹抽取静脉血测量CEA,使用Roche公司生产的Modular E170电化学发光免疫分析系统和配套试剂测定患者血CEA水平。
1.3 统计学分析采用SPSS 17.0统计软件。不同生物学预后相关指标之间ADC值的差异采用两独立样本t检验及单因素方差分析;ADC值与不同生物学预后相关指标之间的相关性采用Spearman相关分析。P < 0.05为差异有统计学意义。
2 结果 2.1 基本情况39例病理证实为NSCLC的患者接受了DWI检查,其中腺癌22例,鳞癌17例,不同性别、年龄、吸烟史、病理类型及分期情况见表 1。结果显示,在不同性别、年龄、吸烟史、病理类型及分期中,ADC值的差异无统计学意义 (P>0.05)。不同血CEA、Ki67、TTF-1、EGFR之间的ADC值差异有统计学意义,较低血CEA (正常值<5 ng/mL) 的ADC值较高 (P < 0.01),Ki67>10%的ADC值较低 (P < 0.01),TTF-1阳性的ADC值较低 (P < 0.01),而EGFR突变型的ADC值比野生型低 (P=0.01)。
| 项目 | n(%) | ADC值 (mm2/s) | P值 |
| 性别 | 0.220 | ||
| 男 | 31(79.5) | 1.09±0.25 | |
| 女 | 8(20.5) | 0.92±0.28 | |
| 年龄 (岁) | 0.230 | ||
| >65 | 9(23.0) | 1.15±0.26 | |
| ≤65 | 30(73.0) | 1.03±0.26 | |
| 吸烟史 | 0.050 | ||
| 有 | 28(71.8) | 1.11±0.26 | |
| 无 | 11(28.2) | 0.92±0.24 | |
| 病理类型 | 0.120 | ||
| 鳞癌 | 17(43.6) | 1.13±0.18 | |
| 腺癌 | 22(56.4) | 1.00±0.30 | |
| 分期 | 0.870 | ||
| Ⅰ | 2(5.1) | 1.08±0.12 | |
| Ⅱ | 4(10.3) | 1.00±0.28 | |
| Ⅲ | 19(48.7) | 1.09±0.22 | |
| Ⅳ | 14(35.9) | 1.02±0.26 | |
| CEA (ng/mL) | <0.01 | ||
| ≥5 | 11(28.2) | 0.73±0.16 | |
| <5 | 28(71.8) | 1.18±0.16 | |
| Ki67(%) | <0.01 | ||
| >10 | 26(66.7) | 0.94±0.23 | |
| ≤10 | 13(33.3) | 1.28±0.16 | |
| TTF-1 | <0.01 | ||
| + | 25(64.1) | 0.96±0.25 | |
| - | 14(35.9) | 1.22±0.20 | |
| EGFR | 0.010 | ||
| 突变型 | 12(30.8) | 0.87±0.26 | |
| 野生型 | 27(69.2) | 1.14±0.22 |
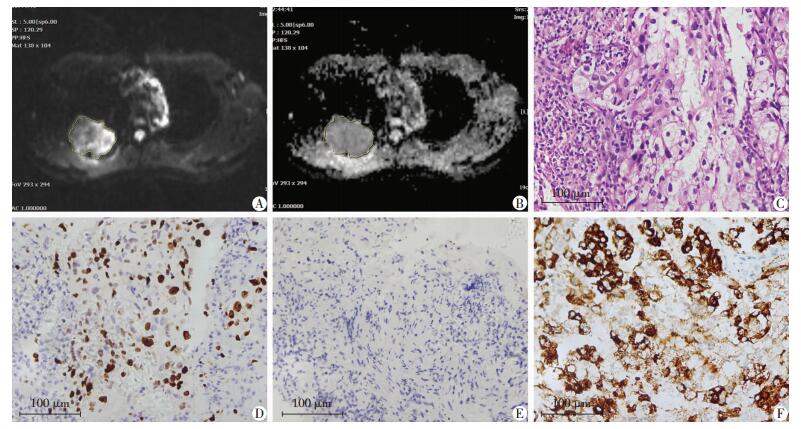
典型病例:患者男性,57岁,行经皮肺穿刺活检病理证实为右上肺腺癌,评估其分期为T3N3M0 ⅢB期。DWI、ADC图像及免疫组化观察结果见图 1。
|
| A:治疗前DWI检查示右上肺团块影,显示为高信号;B:ADC图像示右上肺团块影呈现不均质低信号影,描绘病灶区ROI,测得其ADC值为1.084×10-3 mm2/s;C~F:肺癌组织病理学观察;C:HE染色;D:Ki67>10%;E:TTF-1(-);F:EGFR (+);血CEA为36.82 ng/mL 图 1 NSCLC患者胸部MRI表现及肺组织病理学观察 |
2.2 ADC值与各指标的相关性
Spearman相关分析显示,ADC值与不同生物学指标之间均存在负相关性 (表 2),提示较高CEA、Ki67、TTF-1阳性以及EGFR突变均有较低ADC值 (P < 0.05)。
| 指标 | r | P |
| CEA | -0.77 | <0.001 |
| Ki67 | -0.58 | <0.001 |
| TTF-1 | -0.47 | 0.003 |
| EGFR | -0.40 | 0.012 |
3 讨论
本研究通过对肺癌患者ADC值与分子生物学指标进行相关性分析,发现低ADC值与高CEA、Ki67、TTF-1(+) 及EGFR (+) 密切相关 (r分别为-0.77、-0.58、-0.47、-0.40)。这与文献[10]报道结果一致,进一步证实了ADC值与预后病理分子指标的密切联系,同时关于PET/CT与相关病理分子生物学指标相关性研究已有报道[12]。这均表明功能影像学检查对病灶内部生理学改变监测比既往传统的影像学检查手段更有优势[13]。
本研究所采用的DWI是目前唯一能够活体检测水分子微观运动的功能成像技术。在宫颈癌、肾癌、神经胶质细胞瘤等恶性肿瘤中,不同病理类型、细胞密度、肿瘤分期分级中DWI上ADC值均有明显差异[14-16]。有研究发现,ADC值对于肺部肿瘤良恶性评估、诊断及鉴别诊断、早期治疗的监测等均较常规CT及PET/CT更有优势[17-18]。研究表明,核仁形成区相关蛋白、Ki67、癌基因及抑癌基因等生物学因素的异常与肺癌预后明显相关,有可能作为预后因子识别出早期肺癌术后复发的高危患者[9-10, 19]。本研究选取了对预后有重要意义的常见生物学指标与ADC值的相关性进行分析,以期利用病理生理学成像技术DWI为临床提供更多信息。
CEA存在于肺癌、肝癌及乳腺癌等多种肿瘤组织中,是目前应用最广泛的非特异性肿瘤标记物之一。研究表明[2, 20],17%~80%的肺癌患者血CEA高于正常值。血中CEA浓度越高,肿瘤细胞密度往往越高,分化程度亦越低。治疗前后血CEA值的变化可作为肺癌预后指标之一,治疗后CEA降低常提示预后较好,且血CEA的变化情况与影像学疗效也密切相关[21]。本研究证实了血CEA水平与ADC值之间存在负相关,较高的CEA水平提示较低ADC值;但前期有研究表明,ADC值与CEA之间不存在相关性[10]。这可能与前期试验样本量偏少,试验数据采集方法差异有关。本研究初步探索了这两种临床指标相关性,有待后期大样本量进一步明确。
Ki67是一种细胞核抗原,存在于绝大部分增殖细胞中。其标记指数的高低与肿瘤增殖的活跃程度呈正相关,是目前检测肿瘤细胞增殖状态最准确、可靠的指标之一。Wen等[5]Meta分析表明,Ki67低组较高组生存率好,证实了Ki67作为肺癌预后因子的重要作用。同样,研究表明ADC值可以作为肺癌预后分析的影像学指标之一,较低的ADC值往往预示着不良结局[22-23]。本研究发现Ki67(以10%为分界点) 与ADC之间存在负相关,可能由于增殖活跃的肿瘤细胞密集,肿瘤内部水分子弥散运动受到限制所致,因此,肺癌ADC值的测量有可能为NSCLC评估肿瘤细胞增殖及预后提供一个新途径,对临床治疗方案的制订提供一定的参考[10]。
TTF-1编码的核蛋白相对分子量为38×103,含有371个氨基酸,生理情况分布于甲状腺、呼吸道上皮的Ⅱ型Clara细胞以及部分大脑前腹侧核等,具有调控甲状腺、肺及中枢神经系统中基因的选择性表达的作用[24]。高宗炜等[4]证实了在不同病理类型、分化程度的肺癌组织中,TTF-1的DNA结合活性明显不同,在腺癌、高分化肺癌组织中的TTF-1 DNA结合活性较高,且TTF-1 DNA结合活性水平与肺癌患者生存情况呈负相关,可作为肺癌患者转移及生存情况的潜在预测因子。本研究发现,不同TTF-1的表达状态的ADC值差异有统计学意义,TTF-1表达与ADC值呈负相关,TTF-1阳性的患者病灶ADC值较低,表明ADC值能为临床提供相应预后相关信息。
EGFR是一种具有酪氨酸激酶活性的糖蛋白,是肿瘤细胞增殖、分化和抗凋亡过程中的重要调节因子[25-26]。研究表明,EGFR作为肺癌的独立预后指标之一,临床上使用酪氨酸激酶抑制剂 (TKI) 针对EGFR突变靶点对NSCLC的患者进行一线治疗取得了较好的效果,EGFR突变型往往比野生型有更长的生存时间[3]。EGFR高表达可以促使肿瘤细胞的增殖、黏附、侵袭和转移,诱导肿瘤新生血管形成[27]。Ko等[28]研究发现,结合PET/CT上SUVmax、血清CEA水平、吸烟状态以及肿瘤边缘形态可能预测EGFR突变状态 (AUC=0.82)。因此,PET/CT用于判定EGFR突变状态有一定临床意义。本研究初步探索了ADC值与不同EGFR突变状态之间的相关性,结果发现,ADC值较低的患者往往EGFR存在突变。这表明若在无法获取组织及血标本EGFR突变检测结果的情况下,可以初步估计EGFR的突变状态,相对于PET/CT而言,DWI具有无辐射、多参数扫描等优势,能为临床治疗、预后提供一种新的评估方法。
综上所述,本研究进一步证实了ADC值与CEA、Ki67、TTF-1、EGFR这些生物学预后指标均存在负相关,利用DWI测量肿瘤ADC值有可能为在体判断肺癌的预后等提供了新方法,为临床上评估肺癌的侵袭性、评估预后及制定科学的治疗方案提供了一定的依据。但是,由于目前尚未发现肺癌特异性抗原,且肺部质子含量少,DWI成像受到限制,使得本研究具有一定局限性。同时,本研究仍存在许多不足,尤其是样本量较少,仅初步探索了ADC值与常见预后分子生物学指标之间的相关性,针对ADC值提示临床预后的作用,需今后进一步扩大样本量进行前瞻性研究。
| [1] | Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115–132. DOI:10.3322/caac.21338 |
| [2] |
周崧雯, 周彩存, 李爱武, 等. 多基因表达对非小细胞肺癌术后预后的评价[J].
同济大学学报 (医学版), 2006, 27(1): 73–75.
Zhou S W, Zhou C C, Li A W, et al. The prognostic value of expression of multiple genes on resected non-small cell lung cancer tissues[J]. Journal of Tongji University (Medical Science), 2006, 27(1): 73–75. DOI:10.3969/j.issn.1008-0392.2006.01.022 |
| [3] |
韩宇, 徐建明, 段海清, 等. EGFR基因突变与吉非替尼治疗晚期非小细胞肺癌的疗效和预后的关系[J].
中华肿瘤杂志, 2007, 29(4): 278–283.
Han Y, Xu J M, Duan H Q, et al. EGFR mutation predicts response and prognosis in iressa-treated advanced-stage non-small cell lung cancer[J]. Chinese Journal of Oncology, 2007, 29(4): 278–283. DOI:10.3760/j.issn:0253-3766.2007.04.010 |
| [4] |
高宗炜, 郭春宝, 金先庆. 人肺癌中甲状腺转录因子-1DNA结合活性的意义[J].
中国肺癌杂志, 2009, 12(2): 127–130.
Gao Z W, Guo C B, Jin X Q. The role of thyroid transcription factor-1 DNA binding activity in lung cancer[J]. Chinese Journal of Lung Cancer, 2009, 12(2): 127–130. DOI:10.3779/j.issn.1009-3419.2009.02.06 |
| [5] | Wen S, Zhou W, Li C M, et al. Ki-67 as a prognostic marker in early-stage non-small cell lung cancer in Asian patients: a meta-analysis of published studies involving 32 studies[J]. BMC Cancer, 2015, 15: 520. DOI:10.1186/s12885-015-1524-2 |
| [6] | Zheng Y, Sun X, Wang J, et al. FDG-PET/CT imaging for tumor staging and definition of tumor volumes in radiation treatment planning in non-small cell lung cancer[J]. Oncol Lett, 2014, 7(4): 1015–1020. DOI:10.3892/ol.2014.1874 |
| [7] | Zhang Y, Qin Q, Li B, et al. Magnetic resonance imaging for N staging in non-small cell lung cancer: A systematic review and meta-analysis[J]. Thorac Cancer, 2015, 6(2): 123–132. DOI:10.1111/1759-7714.12203 |
| [8] | Sudarski S, Hagelstein C, Weis M, et al. Dual-energy snap-shot perfusion CT in suspect pulmonary nodules and masses and for lung cancer staging[J]. Eur J Radiol, 2015, 84(12): 2393–2400. DOI:10.1016/j.ejrad.2015.09.024 |
| [9] | Liu H, Liu Y, Yu T, et al. Evaluation of apparent diffusion coefficient associated with pathological grade of lung carcinoma, before therapy[J]. J Magn Reson Imaging, 2015, 42(3): 595–601. DOI:10.1002/jmri.24823 |
| [10] |
陈爱萍, 刘士远, 于红, 等. 表观扩散系数预测非小细胞肺癌预后的初探[J].
医学影像学杂志, 2014, 24(9): 1499–1503.
Chen A P, Liu S Y, Yu H, et al. Preliminary study on predicting the prognosis of non-small-cell lung carcinoma (NSCLC) using apparent diffusion coefficient[J]. Journal of Medical Imaging, 2014, 24(9): 1499–1503. |
| [11] | Priola A M, Priola S M, Parlatano D, et al. Apparent diffusion coefficient measurements in diffusion-weighted magnetic resonance imaging of the anterior mediastinum: inter-observer reproducibility of five different methods of region-of-interest positioning[J]. Eur Radiol, 2017, 27(4): 1386–1394. DOI:10.1007/s00330-016-4527-8 |
| [12] |
张亚锐, 张旭, 胡莹莹, 等. 非小细胞肺癌18F-FDG摄取与EGFR突变的关系[J].
中山大学学报 (医学科学版), 2011, 32(5): 674–678.
Zhang Y R, Zhang X, Hu Y Y, et al. Relationship between 18F-FDG uptake and EGFR mutations in non-small cell lung cancer[J]. Journal of Sun Yat-sen University (Medical Sciences), 2011, 32(5): 674–678. |
| [13] | Eisenhauer E A, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228–247. DOI:10.1016/j.ejca.2008.10.026 |
| [14] | Lee E J, Lee S K, Agid R, et al. Preoperative grading of presumptive low-grade astrocytomas on MR imaging: diagnostic value of minimum apparent diffusion coefficient[J]. AJNR Am J Neuroradiol, 2008, 29(10): 1872–1877. DOI:10.3174/ajnr.A1254 |
| [15] | Yu X, Lin M, Ouyang H, et al. Application of ADC measurement in characterization of renal cell carcinomas with different pathological types and grades by 3.0T diffusion-weighted MRI[J]. Eur J Radiol, 2012, 81(11): 3061–3066. DOI:10.1016/j.ejrad.2012.04.028 |
| [16] | Liu Y, Ye Z, Sun H, et al. Clinical Application of Diffusion-Weighted Magnetic Resonance Imaging in Uterine Cervical Cancer[J]. Int J Gynecol Cancer, 2015, 25(6): 1073–1078. DOI:10.1097/IGC.0000000000000472 |
| [17] |
周荣超, 于铁链, 冯长超, 等. 扩散加权成像在评估肺癌化疗效果中的应用价值[J].
中国肺癌杂志, 2011, 14(3): 256–260.
Zhou R C, Yu T L, Feng C C, et al. Diffusion-weighted imaging for assessment of lung cancer response to chemotherapy[J]. Chinese Journal of Lung Cancer, 2011, 14(3): 256–260. DOI:10.3779/j.issn.1009-3419.2011.03.20 |
| [18] | Ohno Y, Koyama H, Yoshikawa T, et al. Diffusion-weighted MRI versus 18F-FDG PET/CT: performance as predictors of tumor treatment response and patient survival in patients with non-small cell lung cancer receiving chemoradiotherapy[J]. AJR Am J Roentgenol, 2012, 198(1): 75–82. DOI:10.2214/AJR.11.6525 |
| [19] |
周宓, 孙婷婷, 邢晓波, 等. 非小细胞肺癌FDG PET/CT显像与分子指标的相关性研究[J].
中国肺癌杂志, 2009, 12(2): 172–175.
Zhou M, Sun T T, Xing X B, et al. The correlation between FDG PET/CT imaging and molecule makers in non-small cell lung cancer[J]. Chinese Journal of Lung Cancer, 2009, 12(2): 172–175. DOI:10.3779/j.issn.1009-3419.2009.02.17 |
| [20] | Hilbe W, Dirnhofer S, Oberwasserlechner F, et al. Immunohistochemical typing of non-small cell lung cancer on cryostat sections: correlation with clinical parameters and prognosis[J]. J Clin Pathol, 2003, 56(10): 736–741. DOI:10.1136/jcp.56.10.736 |
| [21] |
李玲, 宋丽华, 丁士超, 等. 癌胚抗原和细胞角蛋白19片段作为晚期非小细胞肺癌疗效评价指标的临床价值[J].
中华肿瘤杂志, 2010, 32(11): 850–854.
Li L, Song L H, Ding S C, et al. Clinical value of CEA and CYFRA21-1 as an assessment indicator of therapeutic efficacy in advanced non-small cell lung cancer patients[J]. Chinese Journal of Oncology, 2010, 32(11): 850–854. DOI:10.3760/cma.j.issn.0253-3766.2010.11.011 |
| [22] | Reischauer C, Froehlich J M, Pless M, et al. Early treatment response in non-small cell lung cancer patients using diffusion-weighted imaging and functional diffusion maps—a feasibility study[J]. PLoS One, 2014, 9(10): e108052. DOI:10.1371/journal.pone.0108052 |
| [23] |
蒋洁智, 李鹍, 封俊, 等. ADC直方图评估肺癌化疗早期疗效的应用初探[J].
影像诊断与介入放射学, 2016, 25(1): 13–16.
Jiang J Z, Li K, Feng J, et al. Adc histogram analysis of the early response to chemotherapy in lung cancer[J]. Diagnostic Imaging & Interventional Radiology, 2016, 25(1): 13–16. DOI:10.3969/j.issn.1005-8001.2016.01.003 |
| [24] | Bingle C D. Thyroid transcription factor-1[J]. Int J Biochem Cell Biol, 1997, 29(12): 1471–1473. DOI:10.1016/S1357-2725(97)00007-1 |
| [25] | Tamás P, Solti Z, Bauer P, et al. Mechanism of epidermal growth factor regulation of Vav2, a guanine nucleotide exchange factor for Rac[J]. J Biol Chem, 2003, 278(7): 5163–5171. DOI:10.1074/jbc.M207555200 |
| [26] |
许学亮, 邵红玲. STAT5、VEGF和EGFR在非小细胞肺癌中表达的相关性研究[J].
中国免疫学杂志, 2012, 28(6): 555–559.
Xu X L, Shao H L. Expression of STAT5, VEGF and EGFR in NSCLC and their correlation[J]. Chinese Journal of Immunology, 2012, 28(6): 555–559. DOI:10.3969/j.issn.1000-484X.2012.06.017 |
| [27] | Jimeno A, Hidalgo M. Blockade of epidermal growth factor receptor (EGFR) activity[J]. Crit Rev Oncol Hematol, 2005, 53(3): 179–192. DOI:10.1016/j.critrevonc.2004.10.005 |
| [28] | Ko K H, Hsu H H, Huang T W, et al. Value of 18F-FDG uptake on PET/CT and CEA level to predict epidermal growth factor receptor mutations in pulmonary adenocarcinoma[J]. Eur J Nucl Med Mol Imaging, 2014, 41(10): 1889–1897. DOI:10.1007/s00259-014-2802-y |



