2. 621900 四川 绵阳,工程物理研究院流体物理研究所;
3. 400038 重庆,第三军医大学西南医院神经外科;
4. 646000 四川 泸州,西南医科大学第一附属医院神经外科
2. Institute of Fluid Physics, Chinese Academy of Engineering Physics, Mianyang, Sichuan Province, 621900;
3. Department of Neurosurgery, Southwest Hospital, Third Military Medical University, Chongqing, 400038;
4. Department of Neurosurgery, the First Affiliated Hospital, Southwest Medical University, Luzhou, Sichuan Province, 646000, China
感染是造成战时伤病员和平时重症监护患者死亡的主要原因之一。接触伤员的器械和其他物品进行快速、严格的消毒灭菌是挽救伤员生命和防止院内交叉感染的重要措施。现有常规成熟的消毒灭菌方法虽然均有操作规程[1],但这些方法各有优缺点。常见的化学、紫外光消毒灭菌方法虽然范围广、价格低,但是时间长效果较差[2-3]。而高温高压消毒灭菌方法,安全、有效、无污染,但是消毒时间较长,能耗较高,应用条件要求较多,不便战伤前沿救治及监护室使用频率高的移动物品消毒[4]。为了弥补传统消毒方法的不足,需要将新物理技术引入传统的医疗消毒领域,寻找新的消毒灭菌方法。激光是一种高亮度、相干性和单色性好的光源,利用激光进行消毒灭菌是一种新思路。激光灭菌基于多种效应[5-6],主要有:① 激光的热效应,激光被细菌、培养液或细菌粘着物所吸收,造成温度急剧上升,破坏细菌组织结构;② 激光的力学效应,光被细菌组织中的水分吸收,水分蒸发引起的内应力会导致细菌的破坏和凋亡;③ 激光的电离效应也对细菌有一定的灭杀效果。激光的功率、波段和模式也对灭菌效果有不同的影响。前期国内外部分学者陆续做过一些激光灭菌研究[5-8],但要在这些研究基础上,实现可靠、实用的激光消毒灭菌设备还远远不够,还需进一步对医疗器械表面的细菌进行激光灭杀研究,确定灭菌效果与激光功率、辐照时间之间的关系。基于上述目的,本研究以980 nm波长红外连续激光为实验工具,对手术刀表面金黄色葡萄球菌和大肠杆菌进行灭杀实验并探讨相关问题,继而讨论红外连续激光高效消毒灭菌的优缺点。
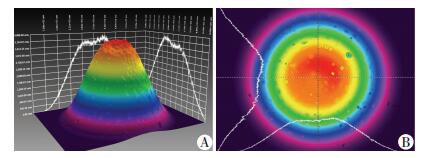
1 材料与方法 1.1 材料半导体单模光纤耦合激光器:波长为980 nm,激光束张角18 mrad,光纤出口直径为4.8 mm,光束束腰与光纤出口直径相同,最大输出功率为10.89 W,测定出的激光能量的三维和二维分布见图 1。
|
| A:三维立体图;B:二维平面图 图 1 980 nm激光的能量分布 |
实验用细菌:金黄色葡萄球菌 (BNCC186335) 和大肠杆菌 (BNCC337357) 由第三军医大学西南医院检验科提供。
细菌LB培养基:体积为1 L,主要由胰蛋白胨10 g、酵母提取物5 g、氯化钠10 g、琼脂粉15 g和蒸馏水配比而成。
实验用金属器件:钢制手术刀。为避免外界影响,将手术刀装入6孔板 (纯聚苯乙烯制成,光透过率约为90%),为了能将手术刀放入无菌6孔板内,截取其一半。在实验时,6孔板中,放置1片未染菌的刀片,5片刀片染菌,对其中4片染菌刀片进行激光辐照,保留1片未染菌刀片和1片染菌刀片作为对照组,制作好的封装刀片的6孔板见图 2A。

|
| A:6孔板内的手术刀;B:激光辐照实验装置;C:980 nm激光辐照到刀片上的情景 图 2 980 nm连续激光辐照装置刀片及实验平台 |
1.2 方法
实验平台见图 2B,6孔板竖直放在升降台上,光纤激光器出光口用支架固定。为了将激光尽可能地辐照在刀片表面,而且要考虑刀片表面的反射光不能反馈到光纤内损伤激光器。通过调试,确定出光口到6孔板的距离为18.3 cm,由于6孔板厚度约为2 cm,因此出光口到刀片的距离为20.3 cm,在此距离,激光光斑直径和刀片宽度基本一致,激光能全部辐照在刀片表面,且覆盖面积较大,刀片表面反射光对激光器无影响。如图 2C所示,实验时,可利用升降台将待测刀片调整至激光辐照光斑上,红外激光辐照在刀片表面时被刀片吸收而快速提升表面温度[9]用于灭菌。
实验过程:激光辐照带菌刀片时,功率分别取5.24、6.87、8.33、10.11 W。先进行大量的尝试实验,确定这4个功率灭菌时间阈值的大致范围。在此基础上,每个功率在大致的灭菌时间阈值范围内,进行4次不同时间的多轮辐照实验,通过灭菌效果的观察,最终确定该功率下的灭菌时间阈值。
灭菌效果的观察方法:用细菌培养基清洗6孔板内的刀片后,放在原孔板中,放入培养箱经过8 h培养,见图 3。每个6孔板的第1个孔内为无菌涂抹刀片清洗下来的培养基,该孔内应该无细菌菌株;第2个孔内为有菌刀片清洗下来的培养基,可见大量的细菌菌株长成;第1、2孔分别作为无菌和有菌对照组,在实验时不进行激光辐照。第3~6孔是用细菌培养基清洗同一激光功率不同时间辐照的刀片之后的培养结果,可见在辐照时间较短时,8 h培养之后有菌株长成,但随着辐照时间增加,到了某一辐照时间阈值时,由于激光灭杀效果达到100%,无细菌菌株出现,可以认为细菌已经被灭杀,由此可以确定这一功率下的灭菌时间阈值。图 3A中激光功率较小时,3、4孔的刀片由于辐照时间较短,培养基中有大量细菌菌株长成,当辐照时间增大,如5、6孔中的培养基中已经看不到细菌菌株长出,表示在5孔对应的辐照时间就已经达到了灭菌时间阈值了。图 3B中,由于功率增大,时间阈值明显降低,只在3孔中形成1个很小的菌株。

|
|
A:小激光功率 (5.24 W);B:大激光功率 (8.33 W) (1):无菌对照;(2):有菌对照;(3)~(6):分别为不同辐照时间 图 3 不同功率、时间条件下980 nm激光辐照后金黄色葡萄球菌培养情况 |
动力学分析方法:外界条件对微生物群落的生长或衰亡的动力学过程有多种模型来描述[10]。本实验中,两种细菌在不同功率980 nm激光辐照下的存活率η随辐照时间t的变化属于一种失活过程,按照微生物学的普遍观点[11],这种失活过程应当满足于一阶反应动力学的指数规律:η=Ae-kt。这里k可以看做是激光辐照灭活反应的速率。类似于薄层菌液受到紫外光辐照时的情况,参数A与通过薄层菌液的紫外光平均强度是相关联的,具有自然对数关系[12]。我们也引入这样一个的“平均强度”物理量,用来表征在某一功率下灭杀细菌时金属医疗器械表面所吸收的激光功率密度,则参数A与这个平均强度I的关系表示为:I=lnA。
2 结果 2.1 细菌在980 nm连续激光辐照下的灭杀效果表 1为金黄色葡萄球菌和大肠杆菌在980 nm波长激光辐照下的灭菌实验结果。其中,金黄色葡萄球菌在5.24 W功率下的辐照存活率是在不同辐照时间下各完成6次实验统计的结果;其他功率下的辐照存活率是在不同辐照时间下各完成7次实验统计的结果;大肠杆菌在5.24 W和6.87 W功率下的辐照存活率都是在不同辐照时间下各完成8次实验统计的结果;8.33 W和10.11 W是在不同时间下各完成7次和5次实验统计的结果。在10.11 W功率辐照条件下,灭杀时间较短,大肠杆菌灭杀时间阈值有一定波动。
| 功率 (W) | 金黄色葡萄球菌 | 大肠杆菌 | |||
| 辐照时间 (s) | 存活率 (%) | 辐照时间 (s) | 存活率 (%) | ||
| 5.24 | 23 | 83.3 | 16 | 62.5 | |
| 25 | 83.3 | 18 | 12.5 | ||
| 27 | 50.0 | 20 | 12.5 | ||
| 29 | 0.0 | 22 | 0.0 | ||
| 6.87 | 18 | 42.9 | 8 | 75.0 | |
| 20 | 28.6 | 10 | 12.5 | ||
| 22 | 14.3 | 12 | 0.0 | ||
| 24 | 0.0 | 14 | 0.0 | ||
| 8.33 | 8 | 100.0 | 5 | 85.7 | |
| 10 | 14.3 | 7 | 14.3 | ||
| 12 | 14.3 | 9 | 28.6 | ||
| 14 | 0.0 | 11 | 0.0 | ||
| 10.11 | 10 | 83.3 | 5 | 0.0 | |
| 12 | 16.7 | 7 | 20.0 | ||
| 14 | 0.0 | 9 | 0.0 | ||
| 16 | 0.0 | 11 | 0.0 | ||
很明显,在相同激光功率下,金黄色葡萄球菌和大肠杆菌的存活率都是随着辐照时间降低的。随着激光功率增大,两种细菌的灭杀时间阈值都呈现下降趋势。
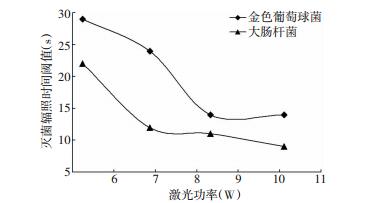
图 4为激光功率和灭菌时间阈值关系。从中可见,在相同激光功率下,杀灭金黄色葡萄球菌的时间要比大肠杆菌的时间长,表明金黄色葡萄球菌的耐热性要比大肠杆菌强。
|
| 图 4 金黄色葡萄球菌和大肠杆菌在不同激光功率条件下的灭菌时间 |
2.2 细菌存活率的动力学分析
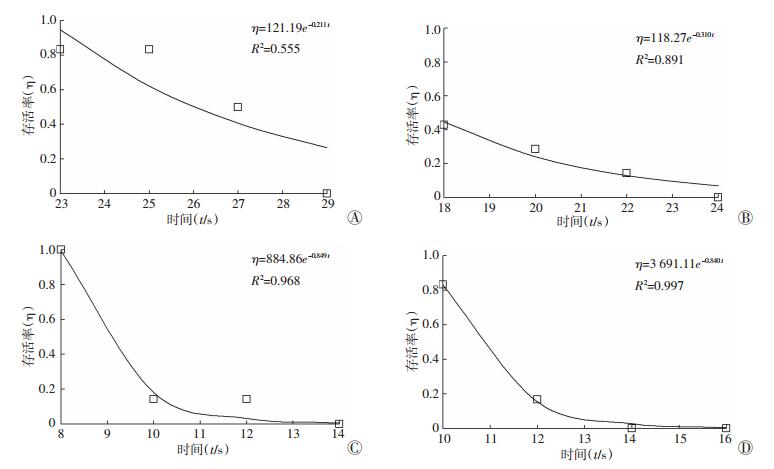
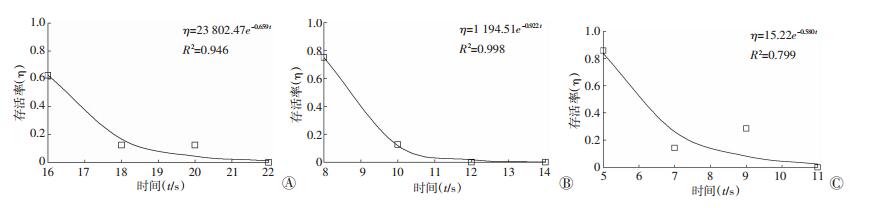
图 5、6分别是金黄色葡萄球菌和大肠杆菌在不同激光功率下的失活动力学过程。从图中的拟合结果可以看出本实验结果基本符合指数规律,其中金黄色葡萄球菌比大肠杆菌的失活规律更接近理想的指数规律。因此,本实验激光灭菌反应确实属于一阶反应动力学过程。
|
| A:5.24 W;B:6.87 W;C:8.33 W;D:10.11 W 图 5 金黄色葡萄球菌在不同激光功率下的失活动力学过程 |
|
| A:5.24 W;B:6.87 W;C:8.33 W 图 6 大肠杆菌在不同激光功率下的失活动力学过程 |
根据本实验数据计算出刀片上获得的平均强度 (表 2)。可以看出金黄色葡萄球菌的平均强度随激光功率增加而增大,大肠杆菌的情况则与之相反。
| 功率 (W) | 金黄色葡萄球菌 | 大肠杆菌 | |||
| 参数A | 平均强度 (W/m2) | 参数A | 平均强度 (W/m2) | ||
| 5.24 | 121.19 | 4.80 | 23 802.47 | 10.08 | |
| 6.87 | 118.27 | 4.77 | 1 194.51 | 7.09 | |
| 8.33 | 884.86 | 6.79 | 15.22 | 2.72 | |
| 10.11 | 3 691.11 | 8.21 | - | - | |
从灭菌角度而言,如果细菌热致衰亡阈值是一定的,且刀片表面的细菌分布均匀,那么激光随着输出功率的增加也就代表着刀片表面吸收的平均强度也应该随之增大,从表 2的结果来看,金黄色葡萄球菌的动力学过程基本呈现出如此变化规律。但大肠杆菌的动力学规律与金黄色葡萄球菌的相反,说明大肠杆菌的热致衰亡阈值可能和红外激光功率相关。激光功率越大,则大肠杆菌的热致衰亡阈值越低,因此平均强度越小。
3 讨论本实验结果表明,红外激光辐照金属医疗器械表面上能在很短的时间内达到灭菌的目的。其灭菌反应动力学过程满足一阶指数关系。激光功率越高,灭菌辐照时间越短,可以在10 s内完成金属医疗器械表面的灭菌工作。当然,本实验用的刀片质量和体积都较小,如果是较大的手术医疗器械,要想达到有效的消毒灭菌效果可以采用增加激光功率和快速扫描等方法。
本实验中激光功率和灭菌时间阈值关系与杭峰等[12]研究结果类似,因此本实验的方法也可以表征不同细菌的耐热特性。事实上,Woo等[13]用微波也对大肠杆菌和金黄色葡萄球菌进行过辐照灭杀研究,发现强微波对大肠杆菌的损伤有多重累积效果,除了热效应之外,强微波同时还易使大肠杆菌的细胞膜上的蛋白质变性、脱落,细胞膜变得更加粗糙而且通透性增大。本实验结果与Woo等的实验结果是相似的,可以推测受到激光作用时,大肠杆菌细胞膜的通透性和上面的蛋白质更易受到激光的影响,其红外激光热致衰亡阈值应随着激光功率增大而减小,红外激光对大肠杆菌细菌灭杀除了有热效应之外,还应有这种非热效应。
红外激光对金属类器械等非透明且具有一定热耐受医用器具的消毒灭菌是有效的,但是对于透明材料的消毒灭菌效果尚欠缺,是由于透明材料无法吸收激光的能量,在辐照时无法产生高温、高热,但是可以采用紫外激光和红外激光协同消毒灭菌。紫外激光要比一般的紫外灯产生的紫外光的功率高得多,因此利用紫外激光直接破坏微生物DNA分子键的特点,结合红外激光的非热效应,能更加快速、彻底地达到消毒灭菌效果。
将红外激光灭菌方法实现工程化,可以制成小型便携式的激光灭菌设备,可用于野外灭菌或重症监护室不便移动的实心金属医疗器械表面灭菌,将是我们后续工作的主要目标。
| [1] |
中华人民共和国卫生部. 医疗机构消毒技术规范: GB/T1. 1-2009[S]. 北京: 中国标准出版社, 2012: 25-41.
The Ministry of Health of the People's Republic of China. Regulation of disinfection technique in healthcare settings: GB/T1.1-2009[S]. Beijing: Standards Press of China, 2012: 25-41. |
| [2] |
黄秋华, 涂慧慧, 吴莉. 三种消毒液对硅胶气管套管消毒效果比较[J].
中国消毒学杂志, 2012, 29(3): 192–193.
Huang Q H, Tu H H, Wu L. Comparison of disinfection efficacy of three liquid disinfectants on silicone tracheal cannula[J]. Chinese Journal of Disinfection, 2012, 29(3): 192–193. |
| [3] |
李钟响, 吴红映, 金美琴. 常见细菌对紫外线敏感性试验观察[J].
中华医院感染学杂志, 2012, 22(1): 121–122.
Li Z X, Wu H Y, Jin M Q. Experimental observation of ultraviolet light sensitivity effect on common bacteria[J]. Chinese Journal of Nosocomiology, 2012, 22(1): 121–122. |
| [4] |
周逞丽. 快速生物监测法对高压蒸汽灭菌效果监测的评价[J].
实用预防医学, 2008, 15(3): 885–886.
Zhou C L. Effect Evaluation of a Rapid Biological Monitoring Method in High—Pressure Sterilization[J]. Practical Preventive Medicine, 2008, 15(3): 885–886. DOI:10.3969/j.issn.1006-3110.2008.03.120 |
| [5] | Deppe H, Horch H H, Schrödl V, et al. Effect of 308-nm excimer laser light on peri-implantitis-associated bacteria: an in vitro investigation[J]. Lasers Med Sci, 2007, 22(4): 223–227. DOI:10.1007/s10103-007-0441-2 |
| [6] | Mohaidat Q I. Laser-induced breakdown spectroscopy (LIBS): an innovative tool for studying bacteria[D]. Detroit:Graduate Schoolof Wayne State University, 2011. |
| [7] | Ando Y, Aoki A, Watanabe H, et al. Bactericidal effect of erbium YAG laser on periodontopathic bacteria[J]. Lasers Surg Med, 1996, 19(2): 190–200. DOI:10.1002/(ISSN)1096-9101 |
| [8] |
李若兰, 任煜光, 孙风阳. 脉冲Nd:YAG激光对几种细菌杀菌作用的实验研究[J].
口腔医学, 2000, 20(1): 16–17.
Li R L, Ren Y G, Sun F Y. Experimental study on bactericidal effects of pulsed nd:YAg laser[J]. Stomatology, 2000, 20(1): 16–17. DOI:10.3969/j.issn.1003-9872.2000.01.008 |
| [9] |
胡鹏, 陈发良. 重复频脉冲激光辐照金属材料热效应模拟分析[J].
中国激光, 2016, 43(10): 1001006.
Hu P, Chen F L. Simulation of thermal effects in repetitive pulsed laser irradiation on metals[J]. Chinese Journal of Lasers, 2016, 43(10): 1001006. DOI:10.3788/cjl201643.1001006 |
| [10] | Ongeng D, Haberbeck L U, Mauriello G, et al. Modeling the Fate of Escherichia coli O157:H7 and Salmonella enterica in the Agricultural Environment: Current Perspective[J]. J Food Sci, 2014, 79(4): R421–R427. DOI:10.1111/1750-3841.12392 |
| [11] | Hiatt C W. Kinetics of the inactivation of viruses[J]. Bacteriol Rev, 1964, 28(2): 150–163. |
| [12] |
杭锋, 陈卫, 陈帅, 等. 微波加热对大肠杆菌与金黄色葡萄球菌蛋白质与核酸变性的影响[J].
食品与机械, 2008, 24(5): 12–15.
Hang F, Chen W, Chen S, et al. The effect of microwave heating on the denaturation of E.coli and S.aureus intracelluar protein and nucleic acid[J]. Food and Machinery, 2008, 24(5): 12–15. |
| [13] | Woo I S, Rhee I K, Park H D. Differential Damage in Bacterial Cells by Microwave Radiation on the Basis of Cell Wall Structure[J]. Appl Environ Microbiol, 2000, 66(5): 2243–2247. DOI:10.1128/aem.66.5.2243-2247.2000 |



