肝性脑病(hepatic encephalopathy,HE)是一种由肝功能不全和(或)门体静脉分流(PSS)引起的大脑功能障碍,表现为从亚临床改变到昏迷的广谱的神经或精神异常[1]。目前主流观点仍认为肝性脑病的主要发病机制是由于循环血内血氨持续升高造成的。人体血氨最主要的来源是肠道细菌已成共识。因此近年来,关于肠道细菌在肝性脑病病程发展中的作用引起重视。虽然人们很早就认识到肠道与肝性脑病的紧密联系,并发现了许多有效的治疗措施,但仍未达到人们的预期。即使是目前最有效的药物—Rifaximin也有其难以避免的并发症[2-3]。
粪便细菌移植(fecal microbiota transplantation, FMT)是近年来应用于治疗伪膜性肠炎及艰难梭菌感染等消化道疾病的新兴且有效的治疗方法[4]。结合对肝性脑病的初步分析,我们推测对肝性脑病采用FMT也可以达到类似的效果。
因此,我们肝性脑病大鼠进行了FMT,对其肝功能及血氨进行了研究,以期了解FMT是否可作为一种有效的治疗肝性脑病的方法。
1 材料及方法 1.1 实验动物及分组选择雄性SD大鼠32只,体质量(250±50) g,随机数字法分为4组,每组8只(A组:正常对照组;B组:肝性脑病模型组;C组:益生菌组;D组:FMT组)。
1.2 肝性脑病大鼠模型建立大鼠购回后适应性饲养1周,保持自由饮水、饮食及通风,12~12 h明暗交替。对正常大鼠颈背部皮下注射生理盐水(首次5 μL/g,而后3 μL/g),每周注射两次,持续9周。对B~D组大鼠,将CCL4、大豆油按2 :3比例混合后于大鼠颈背部皮下注射(首次5 μL/g,而后3 μL/g),每周注射两次,同时5%乙醇自来水自饮,持续9周。
1.3 模型验证大鼠持续造模9周后,对模型组大鼠进行EEG测试,B~D组全部出现肝性脑病典型高频慢波;再随机取模型组大鼠5只,正常对照组大鼠1只,然后以7%水合氯醛麻醉,暴露肝脏,可见B~D组大鼠相比正常对照组大鼠明显,显示造模成功(图 1、2)。

|
| 图 1 正常大鼠肝脏 |

|
| 图 2 肝性脑病模型大鼠肝脏 |
1.4 特殊药品
VSL#3益生菌购于美国VSL公司,每粒含细菌112.5×109,溶于8.333 mL PBS溶液,即13.5×109/mL,4 ℃保存。
1.5 粪便细菌的提取本实验选择一非月经期女性健康志愿者,33岁,既往史无特殊,无巨细胞病毒感染史,无肝炎等传染病史,无吸毒史及HIV感染,无高血压及糖尿病等;近期内无发热、无腹痛、腹泻及便秘等一切消化道症状及感染症状;近期内未服用任何抗生素、抗病毒药物以及一切可能影响肠道功能及细菌的药物。于提取细菌前1 d,嘱该志愿者流质饮食。参考SATOKARI及HAMILTON等[5-6]的方法,提取、过滤并保存粪便细菌。
1.6 差异化处理A组:不进行任何处理;B组:肠道埋管,通过管道向肠道每天注射生理盐水200 μL/d;C组:肠道埋管,参照DAI等[7]的方法,每天注射VSL#3益生菌溶液200 μL/d (200 μL益生菌溶液中含益生菌2.7×109), 持续2周。D组:首先采用紫外分光光度计法计数所提取的粪便细菌的浓度,测得菌液离心后的浓度大约为40.515×109 cfu/mL,调整至13.5×109/mL,然后200 μL/d经肠道埋管注入大鼠肠道,持续2周(图 3)。

|
| 图 3 肠道埋管 |
1.7 标本采集
分别于益生菌移植及FMT后1周及2周行内眦采血:用于肝功检测(主要指标:谷丙转氨酶,谷草转氨酶、白蛋白、总胆红素及直接胆红素)。门静脉采血:用于门静脉血氨检测。尾静脉采血:用于尾静脉血氨检测。以上指标均采用常规生化检测仪测定。
1.8 统计学方法所有数据采用SPSS 19.0中文版进行处理。对于各组移植后1周及移植后2周肝功能各指标和移植后2周门静脉血氨及尾静脉血氨采用配对t检验;其他各指标组间均数比较采用单因素方差分析,组间两两比较采用LSD检验;P < 0.05有统计学意义。
2 结果 2.1 大鼠一般生存情况及大便情况所有实验大鼠均未出现死亡。所有模型大鼠以后均出现嗜睡、活动减少及反应迟钝等情况,偶有厌食及消瘦。移植后1周B组大鼠仍以上述表现为主,而C组开始出现自主活动增多,饮食增加,且大便正常,D组也开始出现自主活动增多及饮食增加,但大便呈湿软状态,并有2只出现腹泻现象。移植后2周,B组仍然表现为嗜睡及活动减少、C及D组大鼠行为与移植后1周无特殊变化,C组大便仍正常,D组大便明显好转呈正常状态。
2.2 移植前后大鼠体重比较移植前各组大鼠之间体质量无明显统计学差异;1周后,B组与其他各组相比,具有统计学差异(P < 0.05),而A组、C组及D组之间无统计学差异;2周后,B组与C组之间具有统计学差异(P < 0.05),而与A、D组之间没有统计学差异;A组、C组及D组移植后2周体重较移植前明显增加,且有统计学意义(P < 0.05),而B组与移植前比较没有统计学差异(表 1)。
| 组别 | 移植前 | 移植后1周 | 移植后2周 |
| A组 | 242.33±27.15 | 262.52±31.24a | 271.95±31.39c |
| B组 | 231.80±35.46 | 224.90±10.99 | 237.90±29.84b |
| C组 | 234.65±27.10 | 284.85±4.29a | 290.58±1.82c |
| D组 | 225.18±14.81 | 259.30±12.86a | 266.83±33.40c |
| a:P < 0.05,与B组比较;b: P < 0.05,与C组比较;c: P < 0.05,与移植前比较 | |||
2.3 各组大鼠肝功能比较
1周后,各组ALT、AST、ALB、TB及DB之间均有统计学差异(P < 0.05) B组与A组比较肝功能明显变差,且有统计学意义;而经过益生菌移植或FMT后移植后1周肝功能主要指标均较前明显好转,且有统计学差异(P < 0.05)(表 2)。
| 组别 | ALT(U/L) | AST(U/L) | ALB(g/L) | TB(μmol/L) | DB(μmol/L) |
| A组 | 216.06±3.38a | 29.25±1.23a | 40.13±0.05a | 6.90±3.69a | 3.33±0.42a |
| B组 | 884.45±5.95 | 92.52±2.85 | 17.33±0.39 | 26.05±1.67 | 13.38±1.36 |
| C组 | 562.22±7.44 | 52.13±1.82 | 26.37±2.17 | 13.45±0.46 | 7.59±0.10 |
| D组 | 776.60±7.92 | 74.38±1.98 | 20.80±0.34 | 17.15±0.46 | 10.10±0.05 |
| a: P < 0.05,与B、C、D组比较 | |||||
2周后,各组ALT、AST、ALB、TB及DB之间均有统计学差异(P < 0.05) B组与A组比较肝功能明显变差,且有统计学意义;而经过益生菌移植或FMT后移植后2周肝功能主要指标均较前明显好转,且有统计学差异(P < 0.05)(表 3)。
| 组别 | ALT(U/L) | AST(U/L) | ALB(g/L) | TB(μmol/L) | DB(μmol/L) |
| A组 | 220.90±5.08a | 30.29±1.40a | 41.26±0.45a | 3.50±1.88a | 2.98±0.34a |
| B组 | 990.07±4.80 | 101.58±2.19 | 17.53±0.53 | 27.20±0.77 | 16.04±0.51 |
| C组 | 380.59±5.12 | 40.46±0.83 | 31.07±0.12 | 8.80±1.00 | 5.96±0.23 |
| D组 | 610.49±4.98 | 72.46±4.42 | 24.48±0.12 | 13.45±0.77 | 10.04±0.09 |
| a: P < 0.05,与B、C、D组比较 | |||||
2.4 移植后1周与移植后2周肝功能比较
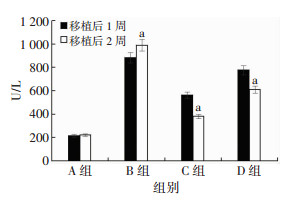
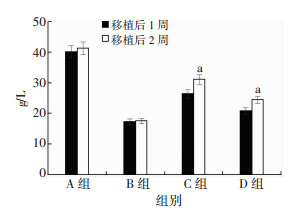
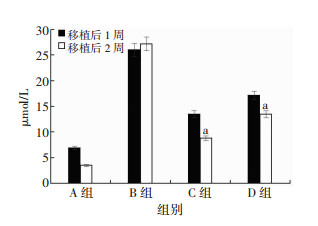
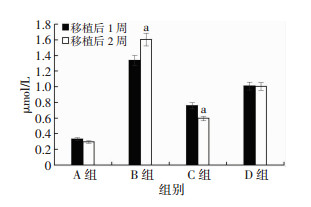
结果表明,A组大鼠肝功移植前后相比没有统计学差异;B组在造模后1周及2周相比,ALT及DB具有统计学差异(P < 0.05),而AST、ALB及TB没有统计学差异(P>0.05);C组大鼠肝功移植后较移植前所有指标均有好转,且有统计学差异(P < 0.05);D组移植后ALT、ALB及TB较前有所好转,且有统计学意义(P < 0.05),而AST和DB没有明显好转(P>0.05)(图 4~8)。
|
| a: P < 0.05,与移植后1周比较 图 4 移植后1周及2周ALT变化情况 |

|
| a: P < 0.05,与移植后1周比较 图 5 移植后1周及2周AST变化情况 |
|
| a: P < 0.05,与移植后1周比较 图 6 移植后1周及2周ALB变化情况 |
|
| a: P < 0.05,与移植后1周比较 图 7 移植后1周及2周TB变化情况 |
|
| a: P < 0.05,与移植后1周比较 图 8 移植后1周及2周DB变化情况 |
2.5 各组大鼠门静脉及尾静脉血氨情况比较
移植后2周B组大鼠与A组比较门静脉血氨明显升高,且有统计学差异(P < 0.05);而经过益生菌移植或FMT后,门静脉血氨明显降低,且有统计学差异(P < 0.05);而C组及D组之间也有统计学差异(P < 0.05)。
移植后2周B组大鼠与A组比较尾静脉血氨明显升高,且有统计学差异(P < 0.05);而经过益生菌移植或FMT后,尾静脉血氨明显降低,且有统计学差异(P < 0.05);而C组及D组之间也有统计学差异(P < 0.05)。
移植后2周所有大鼠尾静脉血氨较门静脉血氨降低,且有统计学差异(P < 0.05)(表 4)。
| (μmol/L,x±s) | |||
| 组别 | 门静脉血氨 | 尾静脉血氨 | P |
| A组 | 12.37±0.73 | 8.52±0.53 | 0.008 |
| B组 | 36.28±1.32 | 32.90±0.35 | 0.032 |
| C组 | 22.05±0.70 | 17.62±0.40 | 0.003 |
| D组 | 26.26±0.30 | 23.10±0.35 | 0.002 |
3 讨论
肝性脑病作为肝硬化最严重的并发症,其治疗手段一直比较局限,到目前为止仍缺乏一个比较理想的方法。如今肠道细菌在肝性脑病病程中的作用受到了重视。目前为止多数指南均将肠道菌群作为治疗目标。例如美国肝病学会和欧洲肝病学会就将乳果糖导泻列为治疗肝性脑病的必要手段[1]。而我国也将乳果糖列为肝性脑病的一线治疗药物[8]。同时抗生素例如新霉素及甲硝唑也被列为治疗肝性脑病的备选药物,以达到清除肠道细菌的目的进而减少血氨。但上述几种药物均不可避免的会出现副作用,特别是抗生素的应用。
因此迫切需要寻找一种新的、安全的治疗方式来重建肠道的正常“全谱系微生物群”达到治疗肝性脑病的目的[9-10]。到目前为止,国际上仅有1例应用FMT治疗肝性脑病的个案报告[11]。因此该方法能否用于治疗肝性脑病仍是一个值得探讨的问题。所以我们将FMT作为研究对象,以期初步了解其是否可用于治疗肝性脑病。
对于建模动物,相对于c57/BL6和BALB/C而言,SD大鼠死亡率低、可重复性高且易于观察[12],因此我们选择SD大鼠进行建模。对于移植途径有三种方法可选择:经口,经小肠及经结肠,考虑到胃液可能会对肠道细菌产生影响,以及通过结肠可能肠道细菌滞留时间较短,因此我们选择了经小肠埋管的方式。但上述方法的优劣性仍需进一步研究。
对于肝性脑病模型,目前尚无能够完全模拟肝性脑病的成熟方法。多采用硫代乙酰胺进行建模,但主要应用于A型肝性脑病,对于C型肝性脑病多采用CCL4联合酒精的方法进行建模。本实验中采用后者进行建模取得了较好的效果。
在本实验中,考虑到男性的生活习惯可能较女性差,因此选择女性作为提供肠道细菌的志愿者,目前尚无动物或临床研究表明不同性别的志愿者提供的肠道细菌会引起不同的影响。由于生物种属不同,可能大鼠肠道细菌和人体肠道细菌存在着较大的差异,因此能否将人体肠道细菌移植并产生一定的治疗效果是未知的。2016年,Nature发表了一篇来自华盛顿大学的论文,研究人员成功的对小鼠进行了人体粪便细菌的移植[13]。其实早在2013年,RIDAURA等[14]进行了一项肥胖研究,他们分别将体型不同的双胞胎志愿者粪便细菌移植入大鼠体内,发现移植同一对双胞胎中较肥胖志愿者的粪便细菌的大鼠体质量体型纤瘦志愿者体质量增加更加明显。因此,对大鼠移植人体粪便细菌是可操作的。结果证明,对肝性脑病大鼠进行人体肠道细菌FMT后,不仅仅使肝性脑病大鼠体质量增加,而且的确改善了肝性脑病大鼠的肝功能,同时明显降低了门静脉及尾静脉的血氨含量。但不能明确的是,如果对大鼠移植同种属正常大鼠的肠道细菌是否更有效。
本实验中还观察到对大鼠进行FMT后1周,大鼠大便性状发生了改变,出现了腹泻及大便湿软等状况,2周后大便又恢复正常,而益生菌却没有类似现象。我们推测可能在此过程中,人体粪便细菌对大鼠肠道细菌进行了一次置换,重新建立了新的肠道微环境从而造成上述情况。
目前,血氨仍被认为是肝性脑病的主要病因。因此我们分别观察了门静脉及尾静脉的血氨含量,发现经过益生菌和FMT后门静脉及尾静脉的血氨含量均明显降低,但益生菌和FMT之间也存在明显的统计学差异,说明FMT可以达到降低循环内血氨的效果,但似乎仍未达到和益生菌相似的效果。而在对门静脉和尾静脉之间的血氨进行比较时不论是模型组还是益生菌或FMT组发现门静脉血氨在经过肝脏进入体循环以后明显下降,但进入体循环以后血氨发生了何种作用仍有待研究,因为在临床实际工作中可能会出现典型肝性脑病的症状而血氨却正常的现象。
总体而言,FMT在治疗肝性脑病上有一定的临床意义,但似乎尚未达到和益生菌相似的效果,这可能和移植入肠道内的粪便细菌存在一定数量的非益生菌或者死菌有一定关系。需进一步研究如何提高其治疗效果。
| [1] | American Association for the Study of Liver Diseases, Euro-pean Association for the Study of the Liver. Hepatic encephalopathy in chronic liver disease: 2014 practice guideline by the European Association for the Study of the Liver and the American Association for the Study of Liver Diseases[J]. J Hepatol, 2014, 61(3): 642–659. DOI:10.1016/j.jhep.2014.05.042 |
| [2] | PATIDAR K R, BAJAJ J S. Antibiotics for the treatment of hepatic encephalopathy[J]. Metab Brain Dis, 2013, 28(2): 307–312. DOI:10.1007/s11011-013-9383-5 |
| [3] | HUANG E, ESRAILIAN E, SPIEGEL B M R. The cost-effectiveness and budget impact of competing therapies in hepatic encephalopathy-a decision analysis[J]. Alimentary Pharmacology & Therapeutics, 2007, 26(8): 1147–1161. DOI:10.1111/j.1365-2036.2007.03464.x |
| [4] | BERG A M, FARRAYE F A. Duodenal infusion of stool is more effective than vancomycin in patients with recurrent Clostridium difficile[J]. Evid Based Med, 2013, 18(6): 220–221. DOI:10.1136/eb-2013-101308 |
| [5] | SATOKARI R, MATTILA E, KAINULAINEN V, et al. Simple faecal preparation and efficacy of frozen inoculum in faecal microbiota transplantation for recurrent Clostridium difficile infection—an observational cohort study[J]. Aliment Pharmacol Ther, 2015, 41(1): 46–53. DOI:10.1111/apt.13009 |
| [6] | HAMILTON M J, WEINGARDEN A R, SADOWSKY M J, et al. Standardized frozen preparation for transplantation of fecal microbiota for recurrent Clostridium difficile infection[J]. Am J Gastroenterol, 2012, 107(5): 761–767. DOI:10.1038/ajg.2011.482 |
| [7] | DAI C, GUANDALINI S, ZHAO D H, et al. Antinociceptive effect of VSL#3 on visceral hypersensitivity in a rat model of irritable bowel syndrome: a possible action through nitric oxide pathway and enhance barrier function[J]. Mol Cell Biochem, 2012, 362(1-2): 43–53. DOI:10.1007/s11010-011-1126-5 |
| [8] |
中华医学会消化病学分会, 中华医学会肝病学分会. 中国肝性脑病诊治共识意见(2013)[J].
中国医学前沿杂志(电子版), 2014, 6(2): 81–93.
Digestive Disease Association of Chinese Medical Association, Liver Disease Association of Chinese Medical Association. Chinese consensus on the medical diagnosis and treatment of hepatic encephalopathy(2013)[J]. Chin J Front Med Sci(Elect Ver), 2014, 6(2): 81–93. DOI:10.3760/cma.j.issn.0254-1432.2013.09.002 |
| [9] | PETROF E O, KHORUTS A. From stool transplants to next-generation microbiota therapeutics[J]. Gastroenterology, 2014, 146(6): 1573–1582. DOI:10.1053/j.gastro.2014.01.004 |
| [10] | VRIEZE A, VAN NOOD E, HOLLEMAN F, et al. Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with metabolic syndrome[J]. Gastroenterology, 2012, 143(4): 913–916. DOI:10.1053/j.gastro.2012.06.031 |
| [11] | KAO D, ROACH B, PARK H, et al. Fecal microbiota transplantation in the management of hepatic encephalopathy[J]. Hepatology, 2016, 63(1): 339–340. DOI:10.1002/hep.28121 |
| [12] | FARJAM M, DEHDAB P, ABBASSNIA F, et al. Thioacetamide-induced acute hepatic encephalopathy in rat: behavioral, biochemical and histological changes[J]. Iranian Red Crescent medical journal, 2012, 3: 164–170. |
| [13] | PLANER J D, PENG Y, KAU A L, et al. Development of the gut microbiota and mucosal IgA responses in twins and gnotobiotic mice[J]. Nature, 2016, 534(7606): 263–266. DOI:10.1038/nature17940 |
| [14] | RIDAURA V K, FAITH J J, REY F E, et al. Gut microbiota from twins discordant for obesity modulate metabolism in mice[J]. Science, 2013, 341(6150): 1241214. DOI:10.1126/science.1241214 |



