2. 746500 甘肃 康县,康县第一人民医院消毒供应室
2. Disinfection and Supply Room, First People's Hospital of Kang County, 746500, Kang County, Gansu Province, China
腹腔镜外科的飞速发展得益于其微创技术的普及,术后快速康复和相对较低的疼痛程度,使得围术期并发症显著降低。然而,术后疼痛仍然是影响该类手术患者整体转归中的主要因素[1]。多模式镇痛是目前腹部外科手术术后镇痛的较佳选择,除了传统的经静脉自控镇痛技术,其他镇痛方法的应用也日趋广泛。近年来,罗哌卡因腹横肌平面 (transversus abdominis plane,TAP) 阻滞用于腹部手术术后镇痛的报道日益增多[2],超声引导下的TAP阻滞进一步提高了该技术的有效性和安全性。但是局麻药的不同剂量和浓度对于TAP阻滞时效的影响迄今尚无定论;而合适的局麻药剂量和浓度为当前研究的方向之一。本研究拟对比两种较低浓度的罗哌卡因在腹腔镜胆囊切除术 (laparoscopic cholecystectomy,LC) 后镇痛的效果,以便更好地掌握局麻药的用药剂量和浓度,为临床疼痛治疗的选择提供依据。
1 资料与方法 1.1 一般资料选择兰州大学第二医院2015年11月至2016年5月择期行LC患者60例 (>18岁),ASA分级Ⅰ~Ⅱ级。排除慢性心血管或内分泌疾病失代偿或术前控制不佳、出凝血功能障碍、进针部位皮肤感染、体质量指数>30、慢性疼痛病史以及对任何药物有过敏史者。纳入研究的患者按照随机数字表法分成两组。0.375%的罗哌卡因由于其起效快,阻滞较完善,在临床上应用较多,而在很多区域麻醉临床实践中发现,0.250%的浓度同样可以达到有效的阻滞,故本研究选择0.250%浓度的罗哌卡因和0.375%浓度的罗哌卡因 (每组30例)。本研究经我院伦理委员会审查批准 (2013092),并与所有参与患者签署麻醉知情同意书及试验知情同意书。所有纳入患者给予数字疼痛强度量表 (numeric rating scale,NRS) 以便熟悉评分,更好地描述疼痛程度 (11个分级中,0级为无痛,10则提示无法忍受的剧烈疼痛)。
1.2 方法 1.2.1 麻醉方法麻醉诱导采用咪达唑仑0.05 mg/kg静脉缓慢推注后,给予2%得普利麻注射液和瑞芬太尼注射液靶控输注 (target controlled infusion,TCI) 诱导。待得普利麻有效血浆浓度达到3.0 μg/mL,瑞芬太尼达到2.5 ng/mL时,患者意识模糊至不清,静脉推注维库溴铵注射液0.1 mg/kg 2 min后行气管插管。PETCO2波形和听诊器听诊确定无误,用容量控制模式行机械通气。手术中,有效得普利麻血浆浓度维持在2 μg/mL,瑞芬太尼在3 ng/mL左右。术中血压借助TCI System的调整维持在诱导前基础血压的±20%, PETCO2维持在30~45 mmHg,脑电双频指数 (bispectral index,BIS) 在40~60范围内以维持麻醉平稳,手术进程顺利。根据术中情况和手术时间间断给予肌松剂。
1.2.2 镇痛方法由有实际操作经验20例以上的麻醉医师为患者实施双侧TAP阻滞。患者和术者术前均不知晓患者的组别且按照0.5 mL/kg计算罗哌卡因的总量。采用肋缘下入路阻滞。超声直视下采用短轴的平面内技术,19G贝朗穿刺针在探头内侧缘2 cm处由内向外,抵达腹直肌和腹横肌之间的TAP。确定针尖位置后回抽无血,缓慢注入15 mL 0.375%或0.250%的罗哌卡因,注射过程中超声下实时看见TAP区低回声区逐渐增大,腹横肌和腹膜因为局麻药重力的缘故下移。对侧采取同样的技术并由同一麻醉医师操作,每例患者共计推注总量30 mL的局麻药。
手术结束前20 min,舒芬太尼注射液按0.1 μg/kg剂量静脉缓慢推注,增强术后镇痛效果并预防瑞芬太尼停药后产生的痛觉敏化现象。肌松拮抗剂视具体情况给予。待苏醒完全,拔除气管导管后,患者常规转运至麻醉后恢复室 (postanesthesia care unit,PACU) 以平稳过渡。
1.2.3 观察指标 1.2.3.1 疼痛评估① 各组患者术中瑞芬太尼和舒芬太尼总用量。②各组患者术后首次使用额外镇痛药 (帕瑞昔布钠) 的时间。③术后转入PACU即刻 (T0),转入病房即刻 (T1),术后6(T2)、12(T3)、18 h (T4) 以及术后24 h (T5) 由同一助理实验员采用NRS进行评分。NRS评分在3~5分之间的患者可给予帕瑞昔布钠40 mg静脉注射,未缓解患者可重复给予帕瑞昔布钠20~40 mg,24 h总量不超过80 mg。术后疼痛剧烈不能用帕瑞昔布钠缓解的患者 (NRS评分在6~10分),给予舒芬太尼5~10 μg缓慢静脉注射。④术后24 h的帕瑞昔布钠和舒芬太尼的总用量。
1.2.3.2 镇静指数评估和不良反应 1.2.3.2.1 镇静指数镇静指数采用Ramsay镇静评分系统,分为以下阈值:①患者焦虑,不能休息,烦躁或兼有上述症状;②患者合作,定向力良好,安静;③对于言语指令配合;④只有在亮光或较大的听觉刺激下才有瑞敏反应;⑤对于大的听觉刺激反应迟钝;⑥对于外界刺激没有反应。
1.2.3.2.2 不良反应术后恶心、呕吐 (postoperative nausea and vomiting,PONV)、寒颤、瘙痒、术后伤口渗血等。
1.3 统计学分析采用SPSS 20.0统计软件,计量资料以 x±s表示,行t检验;分类资料如ASA评分、手术史及术后不良反应发生率,行χ2检验;NRS评分用于比较同时段内休息与活动时得分,行t检验。采用双侧检验,检验水准:α=0.05。
2 结果 2.1 一般情况两组患者ASA分级、年龄、身高、体质量、体质量指数及手术史比较,差异均无统计学意义 (P>0.05,表 1)。
| 组别 | ASA分级 (Ⅰ/Ⅱ级) | 年龄 (岁) | 身高 (cm) | 体质量 (kg) | 体质量指数 (kg/m2) | 手术史 (例) |
| 0.250%罗哌卡因组 | 18/12 | 35.1±7.8 | 168.2±12.2 | 79.4±11.4 | 24.2±3.3 | 4 |
| 0.375%罗哌卡因组 | 21/9 | 35.2±9.8 | 170.4±13.6 | 79.0±12.4 | 23.7±3.1 | 7 |
| P值 | 0.42 | 0.95 | 0.51 | 0.91 | 0.57 | 0.32 |
2.2 疼痛评估
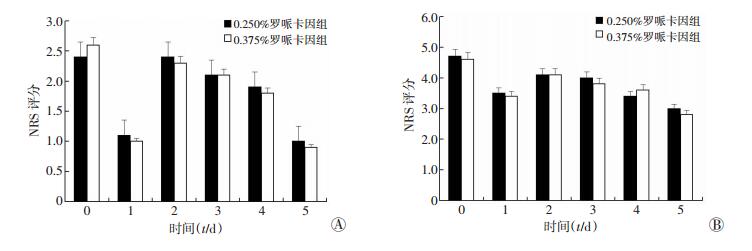
两组患者术中的瑞芬太尼使用量比较,差异有统计学意义 (P=0.03);其他指标两组比较,差异无统计学意义 (P>0.05,表 2,图 1)。
| 组别 |
住院日 (d) |
手术时间 (min) |
术后首次使用镇 痛药时间 (min) |
围术期舒芬太 尼使用量 (μg) |
术中瑞芬太尼 使用量 (μg) |
术后帕瑞昔布钠 使用情况 (例) |
术后不良反应 发生情况 (例) |
||||
| 40 mg | 60 mg | 80 mg | PONV | 异常镇静 | |||||||
| 0.250%罗哌卡因组 | 4.6±1.1 | 47.5±11.7 | 401.0±144.1 | 11.8±1.1 | 1 787.7±171.3 | 10 | 6 | 2 | 3 | 0 | |
| 0.375%罗哌卡因组 | 4.3±0.9 | 49.4±9.3 | 423.0±144.5 | 11.4±1.4 | 1 027.4±148.8 | 12 | 5 | 2 | 2 | 1 | |
| P值 | 0.25 | 0.50 | 0.56 | 0.22 | 0.03 | 0.96 | 0.69 | ||||
|
| 图 1 两组患者休息 (A) 和运动 (B) 时NRS评分比较 (n=30) |
3 讨论
与开腹胆囊切除术相比,LC是一种创伤较小的手术方式,但很多患者仍抱怨有轻至中度的术后疼痛。LC术后疼痛主要由内脏疼痛、腹壁切口疼痛和右肩部疼痛组成,而研究发现,最严重的疼痛发生在术后24 h内,主要是右季肋区和切口痛,以切口痛最为明显[3]。外科切口介导了术后躯体疼痛的所有病理生理过程[4]。LC术后腹壁切口痛为创伤后躯体痛表现,与机械敏或热敏刺激后皮肤初级伤害性传入纤维特性的改变或机械性、伤害性刺激所致的中枢神经系统的功能改变有关[5]。为了减轻患者术后疼痛,促进患者早日康复,多模式镇痛越来越广泛地应用于术后镇痛中。腹横肌平面阻滞被视作腹腔镜手术后非常有效的镇痛方式[2, 6],尤其是随着可视化技术的快速发展,超声引导下的TAP阻滞又进一步提高了其安全性和有效性。然而,Champaneria等[7]的研究却发现TAP阻滞常规使用存在很多弊端。有研究发现目前对于TAP阻滞的认识仍然是非常有限的,需要进一步的研究来指导其合理应用[8]。超声引导TAP阻滞分为肋缘下入路和侧路两种阻滞途径,有研究认为肚脐以上切口的腹腔镜手术,肋缘下入路是更好的选择,T6~T10平面呈现有效的感觉平面阻滞效应 (脐以上手术);侧路技术对T10以上腹部前、外侧腹壁的感觉支阻滞效果差,而肋缘下入路的阻滞平面在T6~T10之间,对于上腹部手术镇痛效果良好[1, 9-12]。据此,本研究采用超声引导下的肋缘下TAP阻滞。但是不同剂量和浓度对于TAP阻滞时间的影响迄今尚无定论。局麻药的神经毒性主要因其吸收入血所致,与浓度和剂量相关[13]。目前认为,罗哌卡因低于3 mg/kg的剂量属于安全阈值。为了缩短局麻药的起效时间,延长术后镇痛时间,临床上经常使用较高浓度或剂量,其安全性存在很大争议。关于罗哌卡因的阻滞浓度,在各种区域麻醉的临床实践中,0.200%以上的浓度被认为是术后镇痛中有效的浓度选择[14];国内关于超声引导区域神经阻滞的第一部专著中,作者建议为0.500%的罗哌卡因浓度[15];而在临床上,0.375%的罗哌卡因由于其起效快,阻滞完善,经常应用于许多高龄患者。因此,本研究拟对比两种较低浓度的罗哌卡因在LC手术镇痛的效果,以便更好掌握其用药剂量和浓度。
本研究结果显示,两组不同浓度的罗哌卡因阻滞组围术期使用舒芬太尼的量、术后各时段的NRS评分差异没有统计学意义;相同的结果也体现在术后两组患者使用帕瑞昔布钠的例数和剂量、术后两组患者首次需要额外镇痛药的时间、不良反应及副作用上。值得注意的是,全身麻醉和手术期间瑞芬太尼输注量在两组间差异有统计学意义,但对术后额外镇痛药使用和疼痛评分的影响没有显著临床价值,该结果与一项随机对照的研究[16]结果相似。LC手术中,对于机体较强的刺激多为手术开始5 min以内Trocar置入前后。本研究中全麻手术后不能客观界定其阻滞平面是否与较高浓度的TAP阻滞导致术中应激反应轻,从而导致术中瑞芬太尼总量下降有关,需要进一步的研究来证实。之前的研究发现3.0 mg/kg和2.5 mg/kg的罗哌卡因行TAP阻滞都能引起明显神经毒性[13, 17]。目前TAP阻滞中最低的有效罗哌卡因浓度仍无明确标准,但能起到有效阻滞效果的局麻药最低浓度的研究势必具有良好的研究前景。本研究中两组患者在术后各时段休息和活动状态下NRS评分差异无统计学意义,排除偏差因素,也可作为低浓度局麻药拥有良好临床镇痛效果的另一佐证。两组患者与局麻药相关的不良反应和毒副作用的发生率差异无统计学意义,TAP阻滞的相关损伤大多发生在盲法穿刺过程中。超声引导进行TAP阻滞以来,穿刺造成的肝脏损伤、脾脏损伤、肾脏损伤、肠管粘连等并发症的发生率显著降低,也更凸显了超声引导下神经阻滞的优势。本研究中两组患者术后PONV的发生率无明显差异,既往研究大多也认为TAP的实施可以有效减少围术期阿片类药物使用,降低PONV的发生。有趣的是,有研究指出,术后PONV的发生可能与TAP阻滞本身相关[18],试验各组纳入标准的差异、手术种类和部位可能导致这一结果,需要更多的临床研究进一步证实。
本研究不足之处在于没有对血浆有效局麻药浓度进行检测。既往关于局麻药剂量和浓度的推荐用法,多为经验之谈或基于循证医学的研究,其准确性需要进一步的临床研究来证实,而局麻药血药浓度的检测目前应该是判定用药安全性的更好指标。其次,双侧的TAP阻滞均在患者全身麻醉后,手术开始之前进行操作,无从判断药物扩散后相关神经分支的起效时间、阻滞范围以及阻滞效果,有其局限性。值得一提的是,腹部手术患者在术后的疼痛来源多为躯体痛和内脏痛[19],纳入本试验的患者均接受LC手术,应该还有牵涉痛的成分。全麻患者术后,因为机体残留药物的影响,患者代谢的个体差异,多数患者在术后早期可能不能正确区分疼痛来源,疼痛描述的程度亦具有一定的偏差。TAP阻滞只是对躯体痛传入神经通路的阻断,并未对内脏痛有良好作用,因此疼痛评分,如VAS和NRS,仍然有相当的偏倚因素存在。
综上所述,LC的患者实施术前的双侧TAP阻滞具有良好的术后镇痛作用。按照0.5 mL/kg的总量计算,0.250%和0.375%两种不同浓度的罗哌卡因作用时效相当。因此,建议使用较低浓度的局麻药,以提高TAP阻滞时的安全性。
| [1] | De-Oliveira G S Jr, Fitzgerald P, Streicher L F, et al. Systemic lidocaine to improve postoperative quality of recovery after ambulatory laparoscopic surgery[J]. Anesth Analg, 2012, 115(2): 262–267. DOI:10.1213/ANE.0b013e318257a380 |
| [2] | De-Oliveira G S Jr, Castro-Alves L J, Nader A, et al. Transversus abdominis plane block to ameliorate postoperative pain outcomes after laparoscopic surgery: a meta-analysis of randomized controlled trials[J]. Anesth Analg, 2014, 118(2): 454–463. DOI:10.1213/ANE.0000000000000066 |
| [3] | Ure B M, Troidl H, Spangenberger W, et al. Pain after laparoscopic cholecystectomy. Intensity and localization of pain and analysis of predictors in preoperative symptoms and intraoperative events[J]. Surg Endosc, 1994, 8(2): 90–96. |
| [4] | McDonnell J G, Curley G, Carney J, et al. The analgesic efficacy of transversus abdominis plane block after cesarean delivery: a randomized controlled trial[J]. Anesth Analg, 2008, 106(1): 186–191. DOI:10.1213/01.ane.0000290294.64090.f3 |
| [5] | Koltzenaurg M. Neural mechanisms of cutaneous nociceptive pain[J]. Clin J Pain, 2000, 16(3 Suppl): S131–138. |
| [6] | De Oliveira G S Jr, Milad M P, Fitzgerald P, et al. Transversus abdominis plane infiltration and quality of recovery after laparoscopic hysterectomy: a randomized controlled trial[J]. Obstet Gynecol, 2011, 118(6): 1230–1237. DOI:10.1097/AOG.0b013e318236f67f |
| [7] | Champaneria R, Shah L, Geoghegan J, et al. Analgesic effectiveness of transversus abdominis plane blocks after hysterectomy: a meta-analysis[J]. Eur J Obstet Gynecol Reprod Biol, 2013, 166(1): 1–9. DOI:10.1016/j.ejogrb.2012.09.012 |
| [8] | Abdallah F W, Chan V W, Brull R. Transversus abdominis plane block: a systematic review[J]. Reg Anesth Pain Med, 2012, 37(2): 193–209. DOI:10.1097/AAP.0b013e3182429531 |
| [9] | Bhatia N, Arora S, Jyotsna W, et al. Comparison of posterior and subcostal approaches to ultrasound-guided transverse abdominis plane block for postoperative analgesia in laparoscopic cholecystectomy[J]. J Clin Anesth, 2014, 26(4): 294–299. DOI:10.1016/j.jclinane.2013.11.023 |
| [10] | El-Dawlatly A A, Turkistani A, Kettner S C, et al. Ultrasound-guided transversus abdominis plane block: description of a new technique and comparison with conventional systemic analgesia during laparoscopic cholecystectomy[J]. Br J Anaesth, 2009, 102(6): 763–767. DOI:10.1093/bja/aep067 |
| [11] | Shibata Y, Sato Y, Fujiwara Y, et al. Transversus abdominis plane block[J]. Anesth Analg, 2007, 105(3): 883. DOI:10.1213/01.ane.0000268541.83265.7d |
| [12] | Niraj G, Kelkar A, Jeyapalan I, et al. Comparison of analgesic efficacy of subcostal transversus abdominis plane blocks with epidural analgesia following upper abdominal surgery[J]. Anaesthesia, 2011, 66(6): 465–471. DOI:10.1111/j.1365-2044.2011.06700.x |
| [13] | Griffiths J D, Barron F A, Grant S, et al. Plasma ropivacaine concentrations after ultrasound-guided transversus abdominis plane block[J]. Br J Anaesth, 2010, 105(6): 853–856. DOI:10.1093/bja/aeq255 |
| [14] | Kuthiala G, Chaudhary G. Ropivacaine: A review of its pharmacology and clinical use[J]. Indian J Anaesth, 2011, 55(2): 104–110. DOI:10.4103/0019-5049.79875 |
| [15] |
田玉科, 梅伟. 超声定位神经阻滞图谱[M]. 北京: 人民卫生出版社, 2011: 184-189.
Tian Y K, Mei W. Atlas of Ultrasound Guided Nerve Block[M]. People's Medical Publishing House, 2011: 184-189. |
| [16] | Abdul Jalil R M, Yahya N, Sulaiman O, et al. Comparing the effectiveness of ropivacaine 0.5% versus ropivacaine 0.2% for transabdominis plane block in providing postoperative analgesia after appendectomy[J]. Acta Anaesthesiol Taiwan, 2014, 52(2): 49–53. DOI:10.1016/j.aat.2014.05.007 |
| [17] | Griffiths J D, Le N V, Grant S, et al. Symptomatic local anaesthetic toxicity and plasma ropivacaine concentrations after transversus abdominis plane block for Caesarean section[J]. Br J Anaesth, 2013, 110(6): 996–1000. DOI:10.1093/bja/aet015 |
| [18] | Xiang Z, Yao T, Hao R, et al. Transversus abdominis plane block for postoperative analgesia after laparoscopic surgery: a systemic review and meta-analysis[J]. Int J Cin Exp Med, 2014, 7(9): 2966–2975. |
| [19] | Akkaya A, Yildiz I, Tekelioglu U Y, et al. Dexamethasone added to levobupivacaine in ultrasound-guided tranversus abdominis plain block increased the duration of postoperative analgesia after caesarean section: a randomized, double blind, controlled trial[J]. Eur Rev Med Pharmacol Sci, 2014, 18(5): 717–722. DOI:10.5455/gulhane.206518 |



