2. 400038 重庆,第三军医大学:生物医学分析测试中心
2. Biomedical Analysis Center, Third Military Medical University, Chongqing, 400038, China
复发性流产 (recurrent spontaneous abortion,RSA) 定义为孕妇2次或更多次20周前的流产,国外发病率为1%[1],国内发病率4.26%[2]。女性复发性流产病因复杂,常见原因为免疫因素、遗传染色体异常、凝血异常、子宫解剖结构异常、内分泌紊乱及感染等[3]。但临床观察发现仍有50%左右复发性流产原因不明,定义为不明原因复发性流产 (unexplained recurrent spontaneous abortion, URSA)[4]。目前对于不明原因复发性流产的病因仍未完全知晓,缺乏有效干预。近年来,环境中具有激素活性的物质是否与女性复发性流产相关,引起了学者的广泛关注,但尚无定论。
环境内分泌干扰物 (endocrine-disrupting chemicals,EDCs) 是天然或合成的化合物,能够干扰内源性激素合成、存储、释放、运输和/或结合内源性激素受体, 最终干扰激素功能的物质[5],其中以双酚A (bisphenol A) 最多见。全世界双酚A年产量约60亿磅,其产品广泛用于婴儿奶瓶、塑料饮料瓶、罐装饮料和食品包装、玩具、医疗设备等[6],人类几乎普遍接触。双酚A具有弱雌激素和抗雄激素活性,流行病学及动物模型研究已经证实其生殖、胚胎毒性[7]。有研究发现在妊娠妇女血液,羊水、胎盘、脐带血检测到双酚A[8], 提示双酚A可以通过胎盘使胎儿在子宫内接受暴露。因此,本研究检测复发性流产患者及正常对照血清游离双酚A,旨在探讨双酚A与复发性流产之间的关系,为复发性流产临床合理干预提供依据。
1 资料与方法 1.1 研究对象纳入2014年10月至2016年4月我科门诊就诊并被诊断为不明原因复发性流产 (胚胎停育) 的患者80例,同时在我院门诊选取80例正常妊娠妇女作为对照组。设计标准结构式调查表,采用个人访谈的方法调查研究对象的人口学资料、流行病学资料、妊娠史、月经史、不良孕产史、家族史等。因年龄>35岁妇女由于卵巢衰退增加流产概率[1], 故以35岁为界进行分层比较,体质量指数 (BMI):24~ < 28为超重、≥28为肥胖[9]。
病例纳入标准:妊娠20周前流产 (胚胎停育)≥2次、最近一次流产在1周内、年龄 < 45岁。排除标准:有职业 (塑料、化工厂等) 暴露史,凝血异常 (抗磷脂抗体阳性),子宫解剖结构异常 (B超检查),内分泌因素 (促卵泡生成素、促黄体生成素、催乳素、雌二醇、孕酮、睾酮、促甲状腺激素异常),免疫因素 (抗核抗体阳性),遗传染色体异常 (核型分析),经过临床抗凝、免疫治疗成功怀孕者。
对照选择:同一地区、相似孕周 (±1周) 已婚健康妊娠女性,既往无死胎、先天畸形、早产和低出生体质量婴儿等不良妊娠结局者。研究对象纳入及生物样本检测均得到本人或家属的知情同意。
1.2 方法 1.2.1 样品收集及处理取流产后1周内空腹静脉血4 mL。胚胎停育患者于清宫术前手术室收取。置玻璃管中低速离心后取血清移至-80 ℃冰箱保存,对照组样品同样处理。分别取血清500 μL,置于编号的玻璃试管中,加入双酚A内标 (美国Sigma公司) 后震荡混匀。2 mL甲醇、1 mL纯水活化固相萃取柱。血清样品过柱,1 mL 5%甲醇,1 mL 40%柱洗涤后氮气吹干,甲醇复溶后进样。色谱条件:液相色谱条件,色谱柱为C18柱,采用甲醇-水梯度洗脱;连续自动进样,流量0.3 mL/min,柱温35 ℃。质谱条件:在负离子电喷雾 (ESI-) 模式电离、多反应监测 (multiple reaction monitoring, MRM) 模式进行测定。双酚A的保留时间为5.06 min。双酚 A 的MRM监测母离子为227.2 m/z,子离子为212.1、133.0 m/z。
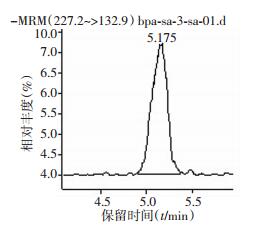
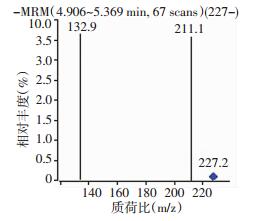
1.2.2 标准曲线及血清双酚A浓度计算取甲醇配制成内标浓度为13.33 ng/mL的7个双酚A标准溶液浓度梯度:0.5、1.0、10.0、25.0、50.0、100.0、200.0 ng/mL,按1.2.1方法衍生并进样,用质谱联用法对双酚A标准溶液测得的面积对应相应的浓度绘制标准曲线并求出回归方程,即可由样品双酚A的峰面积计算浓度。血清双酚A色谱图、质谱图见图 1、2。
|
| 图 1 双酚A色谱图 |
|
| 图 2 双酚A质谱图 |
标准曲线为:y=0.100 116x+0.014 417,R2=0.998 8, 根据3倍信噪比计算最低检测限 (LOD) 为0.10 ng/mL, 10倍信噪比计算定量 (LOQ) 限为0.4 ng/mL。回收率为97.1%~108.2%,精密度为5.1%~10.5%。
1.3 统计学分析使用SPSS 20.0统计软件,符合正态分布的指标,组间比较使用独立样本t检验,非正态分布组间比较采用Wilcoxon秩和检验。采用单因素和多因素非条件logistic回归模型分析双酚A与复发性流产关联。P < 0.05表示差异具有统计学意义。
2 结果 2.1 一般人口学资料病例组、对照组年龄比较差异无统计学意义[(30.01±5.03) vs(30.36±5.60) 岁,P=0.330]。两组间比较,超重和肥胖、初潮年龄提前差异无统计学意义,妊娠合并症及并发症差异有统计学意义 (P=0.040,表 1)。
| 组别 | BMI (kg/m2) | 初潮年龄a(岁) | 孕周 | 妊娠并发症及 合并症c |
||||||
| <24 | 24~ < 28 | ≥28 | ≤12.29b | >12.29岁 | ≤10周 | >10周 | ||||
| 病例组 | 61(76.25) | 18(22.50) | 1(1.25) | 14(17.50) | 66(82.50) | 48(60.00) | 32(40.00) | 8(10.00) | ||
| 对照组 | 64(80.00) | 10(12.50) | 6(7.50) | 6(7.50) | 74(92.50) | 45(56.25) | 35(43.75) | 1(1.25) | ||
| P值 | 0.566 | 0.096 | 0.122 | 0.056 | 0.056 | - | - | 0.040 | ||
| a:初潮平均年龄见文献[10];b:初潮年龄提前;c:病例组4例甲状腺囊肿、1例卵巢囊肿、3例妊娠滋养细胞疾病,对照组1例甲状腺囊肿 | ||||||||||
2.2 两组孕妇年龄、BMI、孕周、初潮年龄与血清双酚A浓度的关系
对照组血清双酚A检出率是81.25%(65/80),病例组检出率是89.47%(68/76),两组间差异无统计学意义 (P=0.184);两组血清双酚A浓度分布呈非正态分布,病例组和对照组分别为39.51(19.72,57.13)、3.56(2.46,6.88) ng/mL,病例组明显高于对照组 (P < 0.01)。剔除激素相关病例后经秩和检验发现:病例和对照组双酚A浓度在年龄≤35岁、BMI、孕周和初潮年龄差异均具有统计学意义 (P < 0.001, 表 2)。
| 组别 | n | 年龄 (岁) | BMI (kg/m2) | 孕周 | 初潮年龄 (岁) | |||||||||||||||||||
| ≤35 | >35 | <24 | ≥24 | ≤10 | >10 | ≤12.29 | >12.29 | |||||||||||||||||
| 双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
双酚A检出 [例 (%)] |
双酚A浓度 (ng/mL) |
|||||||||
| 病例组 | 76 | 57/64 (89.06) |
43.32 (20.38, 62.35) |
11/12 (91.67) |
37.37 (13.38, 52.97) |
52/57 (91.23) |
45.07 (24.48, 65.47) |
16/19 (84.21) |
46.05 (21.20, 61.26) |
42/45 (93.33) |
38.06 (19.96, 53.79) |
26/31 (83.87) |
47.85 (15.82, 64.14) |
14/14 (100.00) |
56.67 (36.09, 71.61) |
54/63 (85.71) |
37.00 (5.73, 55.52) |
|||||||
| 对照组 | 80 | 56/69 (79.71) |
3.67 (2.40, 6.87) |
9/11 (81.81) |
3.27 (2.65, 21.23) |
53/64 (82.81) |
3.56 (2.40, 5.56) |
12/16 (75.00) |
5.16 (2.79, 14.90) |
39/45 (86.67) |
3.70 (2.69, 6.87) |
26/35 (74.29) |
3.23 (2.18, 9.15) |
5/6 (83.33) |
4.43 (2.38, 5.97) |
60/74 (81.08) |
3.56 (2.43, 7.03) |
|||||||
| P值 | 0.720 | < 0.001 | 0.720 | 0.069 | 0.454 | < 0.001 | 0.454 | < 0.001 | 0.708 | < 0.001 | 0.708 | < 0.001 | 0.067 | < 0.001 | 0.067 | < 0.001 | ||||||||
2.3 血清双酚A与复发性流产的多因素非条件logistic回归分析
结果显示:血清双酚A是复发性流产的危险因素 (P<0.01),年龄≤35岁为保护因素 (P<0.01,表 3)。
| 变量 | β | S.E | Wals | df | P | OR | 95%CI |
| 双酚A | 0.904 | 0.155 | 34.217 | 1 | 0.001 | 2.469 | 1.824~3.343 |
| 年龄≤35岁 | -2.314 | 0.616 | 14.124 | 1 | 0.001 | 0.099 | 0.441~3.095 |
| BMI≥24 | 0.190 | 0.472 | 0.161 | 1 | 0.668 | 1.209 | 0.479~3.050 |
| 孕周>10周 | 0.001 | 0.430 | 0.000 | 1 | 0.999 | 1.001 | 0.431~2.324 |
3 讨论
双酚A是酚类环境雌激素的一种,是塑料工业生产聚碳酸酯、环氧树脂、酚醛树脂等物质的前体物质,广泛应用于染料、罐头内包装、食品包装材料、婴儿用瓶等塑料工业,这些物品反复使用及暴露于高热环境会导致双酚A的浸出。近10年来,国内外已有大量体内外动物实验报告证实双酚A对生殖的影响。双酚A作为雌激素受体激动剂及雄激素拮抗剂通过模拟体内激素分泌干扰正常细胞功能[6]。双酚A在生殖系统中有着复杂的影响,动物实验结果显示:双酚A可引起雌性哺乳动物的阴道、子宫及卵巢等的形态学改变[5];体外斑马鱼实验表明5 ng/mL双酚A水平即可抑制卵母细胞成熟表达信号[11]。有研究观察双酚A暴露对生殖的影响发现:血清双酚A与早期胚胎发育异常、复发性流产、子宫内膜增生、多囊卵巢有关,同时也发现双酚A干扰精子功能,降低精子数量,导致男性不育等[7]。不良围产期双酚A暴露与童年和成人健康状况有关联, 包括对生殖和发育的影响、代谢性疾病的发生、潜在的致癌风险和其他健康影响。双酚A与肥胖和糖尿病有关,国外已有大样本文献报道肥胖与反复流产的关系[12]。肥胖与流产、双酚A与肥胖,仍然需要更多的研究来解释其中的关系。有研究报道双酚A通过激活氧化物酶体增殖物激活型受体影响脂肪代谢导致肥胖的发生[5],动物实验及临床研究表明:青春期前环境内分泌干扰物暴露可能会导致激素水平及性成熟改变[13]。
美国一项研究报道双酚A在正常人群体液和组织中不同地区检出率为52%~100%[6],本研究结果与其一致。本研究中对照组血清双酚A浓度 (M=2.91 ng/mL) 与2006年美国专家提出的血清未结合活性双酚A浓度相近 (0.3~4.4 ng/mL)[14],略高于2015年一项关于国内健康成年人尿液中双酚A浓度的研究数据 (M=2.33 ng/mL)[15]。本研究中病例组血清游离双酚A浓度明显高于对照组,也明显高于国内一项关于复发性流产尿液检测研究数据 (M=1.66 ng/mL)[16],这可能与不同地区目标人群的选择及检测方法有关, 但两组间检出率相似。本研究中病例组血清游离双酚A浓度低于国内一项双酚A环境污染研究结果 (198.7 ng/mL)[17]。本研究发现两组中超重肥胖者双酚A浓度差异有统计学意义,但两组超重肥胖者检出率差异无统计学意义,与国外研究结果有差异,可能与饮食习惯不同有关。而病例组妊娠期并发症及合并症高于对照组,应引起我们的注意。早期动物实验研究表明:双酚A在体内快速生物转化及排泄不会蓄积,不会对人体有影响[18],人体接触双酚A后经肝脏代谢后很快排出体外。但是,近年来越来越多的证据表明:游离性双酚A即使在低剂量也可以作为一个强有力的内分泌干扰物导致持久的不良后果[19]。
本研究采用固相萃取-同位素内标-液相色谱质谱联用检测血清游离双酚A,比普通液相色谱方法在一定程度上提高了检测的准确性及精密度,增加了结果的准确性,适用于血清中双酚A的检测。复发性流产的病因无疑是多方面和复杂的,本研究就双酚A对其影响进行了初步分析,结果提示:双酚A浓度在两组间差异具有统计学意义,其可能是不明原因反复自然流产 (胚胎停育) 的高危因素之一,可增加复发性流产的风险。为了排除年龄、BMI等混杂因素影响,本研究进行了双酚A与复发性流产的多因素非条件logistic回归分析,结果显示双酚A是复发性流产的危险因素,提示围产期妇女需要优先避免双酚A暴露。
本研究检测了复发性流产孕妇血清双酚A浓度,但没有检测患者怀孕前和怀孕期间的样本,单一检测结果可能不能完全体现复发性流产患者暴露水平。下一步研究将会设置多指标的前瞻性研究,并检测胚胎组织及不同时间点双酚A浓度,为临床工作提供更多依据。
| [1] | Vitale J. Recurrent miscarriage[J]. N Engl J Med, 2011, 364(8): 783–784. DOI:10.1056/NEJMc1014103#SA2 |
| [2] |
刘宝, 高尔生. 中国已婚育龄妇女自然流产的危险因素分析[J].
中国公共卫生, 2002, 18(7): 890–892.
Liu B, Gao E S. Risk factors for spontaneous abortion of Chinese married women at reproductive age[J]. China Public Health, 2002, 18(7): 890–892. DOI:10.3321/j.issn:1001-0580.2002.07.048 |
| [3] | Rai R, Regan L. Recurrent miscarriage[J]. Lancet, 2006, 368(9535): 601–611. DOI:10.1016/S0140-6736(06)69204-0 |
| [4] | Ford H B, Schust D J. Recurrent pregnancy loss: etiology, diagnosis, and therapy[J]. Rev Obstet Gynecol, 2009, 2(2): 76–83. |
| [5] | Diamanti-Kandarakis E, Bourguignon J P, Giudice LC, et al. Endocrine-disrupting chemicals: an Endocrine Society scientific statement[J]. Endocr Rev, 2009, 30(4): 293–342. DOI:10.1210/er.2009-0002 |
| [6] | Vandenberg L N, Hauser R, Marcus M, et al. Human exposure to bisphenol A (BPA)[J]. Reprod Toxicol, 2007, 24(2): 139–177. DOI:10.1016/j.reprotox.2007.07.010 |
| [7] | Rochester J R. Bisphenol A and human health: a review of the literature[J]. Reprod Toxicol, 2013, 42: 132–155. DOI:10.1016/j.reprotox.2013.08.008 |
| [8] | Schönfelder G, Wittfoht W, Hopp H, et al. Parent bisphenol A accumulation in the human maternal-fetal-placental unit[J]. Environ Health Perspect, 2002, 110(11): A703–A707. DOI:10.1289/ehp.021100703 |
| [9] |
中国成人血脂异常防治指南制订联合委员会. 中国成人血脂异常防治指南[J].
中华心血管病杂志, 2007, 35(5): 390–419.
Committee on prevention and control of dyslipidemia in Chinese adults. Guideline for management of dyslipidemia in China[J]. Chinese Journal of Cardiology, 2007, 35(5): 390–419. |
| [10] |
方琪, 王宏, 曹型远, 等. 重庆城区儿童青春期发动时相现况及与肥胖的相关研究[J].
卫生研究, 2012, 41(4): 562–565.
Fang Q, Wang H, Cao X Y, et al. Puberty timing status and its correlation with childhood obesity in Chongqing city[J]. Journal of Hygiene Research, 2012, 41(4): 562–565. |
| [11] | Santangeli S, Maradonna F, Gioacchini G, et al. BPA-Induced Deregulation Of Epigenetic Patterns: Effects On Female Zebrafish Reproduction[J]. Sci Rep, 2016(6): 21982. DOI:10.1038/srep21982 |
| [12] | Metwally M, Ong K J, Ledger W L, et al. Does high body mass index increase the risk of miscarriage after spontaneous and assisted conception? A meta-analysis of the evidence[J]. Fertil Steril, 2008, 90(3): 714–726. DOI:10.1016/j.fertnstert.2007.07.1290 |
| [13] | Watkins D J, Téllez-Rojo M M, Ferguson K K, et al. In utero and peripubertal exposure to phthalates and BPA in relation to female sexual maturation[J]. Environ Res, 2014, 134: 233–241. DOI:10.1016/j.envres.2014.08.010 |
| [14] | vom Saal F S, Welshons W V. Evidence that bisphenol A (BPA) can be accurately measured without contamination in human serum and urine, and that BPA causes numerous hazards from multiple routes of exposure[J]. Mol Cell Endocrinol, 2014, 398(1/2): 101–113. DOI:10.1016/j.mce.2014.09.028 |
| [15] | Gao C, Liu L, Ma W, et al. Bisphenol A in Urine of Chinese Young Adults: Concentrations and Sources of Exposure[J]. Bull Environ Contam Toxicol, 2016, 96(2): 162–167. DOI:10.1007/s00128-015-1703-5 |
| [16] | Shen Y, Zheng Y, Jiang J, et al. Higher urinary bisphenol A concentration is associated with unexplained recurrent miscarriage risk: evidence from a case-control study in eastern China[J]. PLoS One, 2015, 10(5): e0127886. DOI:10.1371/journal.pone.0127886 |
| [17] | Huang Y Q, Wong C K, Zheng J S, et al. Bisphenol A (BPA) in China: a review of sources, environmental levels, and potential human health impacts[J]. Environ Int, 2012, 42: 91–99. DOI:10.1016/j.envint.2011.04.010 |
| [18] | Dekant W, Völkel W. Human exposure to bisphenol A by biomonitoring: methods, results and assessment of environmental exposures[J]. Toxicol Appl Pharmacol, 2008, 228(1): 114–134. DOI:10.1016/j.taap.2007.12.008 |
| [19] | Mileva G, Baker S L, Konkle A T, et al. Bisphenol-A: epigenetic reprogramming and effects on reproduction and behavior[J]. Int J Environ Res Public Health, 2014, 11(7): 7537–7561. DOI:10.3390/ijerph110707537 |



