2. 400038 重庆,第三军医大学:生物医学工程系生物医学材料学教研室;
3. 400038 重庆,第三军医大学:生物医学工程系数学与生物数学教研室
2. Department of Biomedical Materials Sciences, College of Biomedical Engineering, Third Military Medical University, Chongqing, 400038, China;
3. Department of Mathematics and Biomathematics, College of Biomedical Engineering, Third Military Medical University, Chongqing, 400038, China
轻度认知功能障碍(mild cognitive impairment,MCI)也称早期老年痴呆症(incipient dementia,ID),是一种介于正常衰老和老年痴呆症之间的一个过渡阶段,主要表现为一种认知功能障碍症候群,其核心症状是认知功能的减退,根据病因和损害部位不同,可以累及记忆、执行功能、语言、运用、视空间结构技能等一项或以上,并产生相应的临床症状,而日常能力没有受到明显影响[1-3]。
根据Grundman等[4]的研究发现,主要表现为记忆丧失的遗忘型MCI (amnestic MCI,aMCI)患者,将有10%~15%的可能性进展为阿尔茨海默病(Alzheimer’s disease,AD)。2013年的一项回顾性研究表明,医院内MCI或aMCI患者进展为AD的转化率为7.5%~16.5%,而社区内MCI或aMCI患者进展为AD的转化率为5.4%~11.5%[5]。由于检测程度不同、人种差异以及MCI诊断标准的更新,社区内MCI或aMCI患者进展为AD的转化率往往低于医院内的转化率[6-8],这对临床医师在鉴别MCI和AD,并决定是否对MCI患者提供早期干预提出了极大的挑战。因此本研究拟通过数学模型的方式,寻找MCI或aMCI患者进展为AD可能的危险因素,建立有效判别MCI或aMCI患者预后效果的数学模型,旨在通过对MCI或aMCI患者在24个月之后的预后效果进行预测,以便临床医师对具有较高转化风险的MCI或aMCI患者进行早期干预,延缓MCI或aMCI患者进展为AD提供依据。
1 资料与方法 1.1 临床资料选用数据来自美国阿尔茨海默病影像中心(Alzheimer’s Disease Neuroimaging Initiative,ADNI, https://ida.loni.ucla.edu/login.jsp)的免费公用数据库,由阿尔茨海默病的代谢组学协会(Alzheimer’s Disease Metabolomics Consortium)搜集并分享。选择包括患者ID号、性别、受教育程度、临床诊断、核磁共振检查结果等指标齐全的样本,共包括MCI患者152例,其中随访24个月之后诊断为正常人11例,MCI患者93例,AD患者48例。数据矩阵的维度为152×27,其中每个样本的指标包括性别(x1)、基线诊断年龄(x2)、受教育时间(x3)、基线简易智力状况检查量表得分(minimum mental state examination score,MMSE,x4)、随访24个月简易智力状况检查量表得分(x5)等25项指标,最后两列分别为基线诊断(x26)、随访24个月后诊断(x27),定义为“1=正常组(healthy control,HC)、2=MCI组、3=AD组”。根据随访24个月后的诊断结果,将基线诊断为MCI的152名患者分为两类:稳定组(MCI not converted to AD,MCInc)104例,依据为随访24个月后诊断x27=1或x27=2;和进展组(MCI converted to AD,MCIc)48例,随访24个月x27=3。
1.2 方法 1.2.1 差异性检验筛选判别指标对于连续型变量,采用独立样本t检验的方法进行均值比较;对于离散型变量采用非参数χ2检验进行差异性比较,根据显著性差异指标P < 0.05或P < 0.01,选择对诊断敏感的指标。
1.2.2 判别分析诊断将总体数据中152例MCI患者按照随机数字表法分为训练样本和检测样本,其中两组样本均包括MCInc 52例、MCIc 24例,分别为训练样本和检测样本,且两样本相互独立。为减少随机抽样的的系统误差,本研究通过计算机程序按照上述要求,完成100次随机模拟分组,并针对每次分组条件下的训练样本和检测样本,分别采用贝叶斯判别分析(Bayes discriminant analysis,BDA)、决策树(decision tree)、BP神经网络(back propagation neural networks,BPNN)、模糊C均值聚类(fuzzy c-means algorithm,FCM)以及K均值聚类(k-means algorithm,K-means)的方法进行判别诊断,并以“诊断准确率”为评价模型指标,对5种方法的诊断效果进行评价。
1.3 统计学分析指标筛选通过独立样本t检验、非参数χ2检验完成,指标筛选水准为P < 0.01。指标筛选及ROC曲线在SPSS 19.0中完成,其余模型实现及数据处理用数学软件MATLAB R2014a编程完成。
2 结果 2.1 差异性检验对每项指标进行差异性检验,首先根据显著性差异指标P < 0.05,选择基线MMSE得分(x4)、随访24个月后MMSE得分(x5)、ADAST (x7)、ADASM (x8)、左海马体积(x12)、右海马体积(x13)、海马体积比率(x14)、PRT (x15)、TMP (x16)、PCING (x19)、MPRT (x22),共11项指标。表 1给出了2组样本全部指标的均值、标准差和差异性检验结果。
| 组别 | 例数 | x1 | x2 | x3 | x4 | x5 | x6 | x7 |
| 性别 | 年龄 | 受教育程度 | 基线时 | 24个月后 | 载脂蛋白ε4等位基因 | 阿尔茨海默病认知 | ||
| (男性比例) | MMSE得分 | MMSE得分 | 阳性率(AOPE4, %) | 行为评分(ADAST) | ||||
| MCInc组 | 104 | 67.31 | 75.69±7.12 | 15.85±2.87 | 27.40±1.59 | 27.19±2.54 | 49.04 | 9.62±3.90 |
| MCIc组 | 48 | 64.58 | 75.00±7.30 | 15.96±2.75 | 26.83±1.59 | 22.98±3.36 | 60.42 | 12.71±4.11 |
| 统计量 | - | χ2=0.109 | t=0.553 | t=-0.227 | t=2.055 | t=8.554 | χ2=1.705 | t=-4.459 |
| P值 | - | 0.741 | 0.581 | 0.821 | 0.042 | < 0.001 | 0.192 | < 0.001 |
| 组别 | x8 | x9 | x10 | x11 | x12 | x13 | ||
| 阿尔茨海默病认知行为 | 大脑容积 | 心室容积 | 大脑与心室容积比 | 左海马体积 | 右海马体积 | |||
| 评分修正值(ADASM) | ||||||||
| MCInc组 | 16.17±5.97 | 1 062.95±114.07 | 43.66±23.31 | 0.04±0.02 | 3 260.69±534.95 | 3 316.62±532.57 | ||
| MCIc组 | 20.46±5.57 | 1 052.25±110.28 | 49.57±26.44 | 0.05±0.02 | 3 028.90±552.71 | 3 093.71±555.49 | ||
| 统计量 | t=-4.202 | t=0.543 | t=-1.391 | t=-1.517 | t=2.457 | t=2.366 | ||
| P值 | < 0.001 | 0.588 | 0.166 | 0.131 | 0.015 | 0.019 | ||
| 组别 | x14 | x15 | x16 | x17 | x18 | x19 | ||
| 海马体积比率 | 左右半脑顶叶皮质 | 左右半脑颞叶皮质 | 左右半脑额叶皮质 | 左右半脑枕叶皮质 | 左右半脑后扣带回皮质 | |||
| (×1 000) | 灰度平均值(PRT) | 灰度平均值(TMP) | 灰度平均值(FRT) | 灰度平均值(OCT) | 灰度平均值(PCING) | |||
| MCInc组 | 6.21±0.87 | 1.06±0.05 | 1.01±0.08 | 1.10±0.04 | 1.11±0.07 | 1.00±0.07 | ||
| MCIc组 | 5.83±0.93 | 0.98±0.04 | 0.96±0.05 | 1.08±0.04 | 1.10±0.07 | 0.96±0.07 | ||
| 统计量 | t=2.408 | t=3.654 | t=2.494 | t=1.935 | t=1.343 | t=3.028 | ||
| P值 | 0.017 | 0.001 | 0.014 | 0.055 | 0.181 | 0.003 | ||
| 组别 | x20 | x21 | x22 | x23 | x24 | x25 | ||
| 左右半脑前扣带回皮 | 左右半脑额叶中区皮 | 左右半脑顶叶中区皮 | 左右半脑感觉运动皮 | 左右半脑尾状核皮 | 左右半脑丘脑皮质 | |||
| 质灰度平均值(ACING) | 质灰度平均值(MFRT) | 质灰度平均值(MPRT) | 质灰度平均值(SMC) | 质灰度平均值(CAD) | 灰度平均值(THL) | |||
| MCInc组 | 0.81±0.07 | 1.03±0.05 | 1.11±0.07 | 1.13±0.05 | 1.25±0.10 | 1.10±0.08 | ||
| MCIc组 | 0.83±0.06 | 1.03±0.05 | 1.08±0.08 | 1.13±0.05 | 1.25±0.09 | 1.13±0.07 | ||
| 统计量 | t=-1.213 | t=-0.446 | t=2.780 | t=0.085 | t=0.305 | t=-1.932 | ||
| P值 | 0.227 | 0.656 | 0.006 | 0.932 | 0.760 | 0.055 | ||
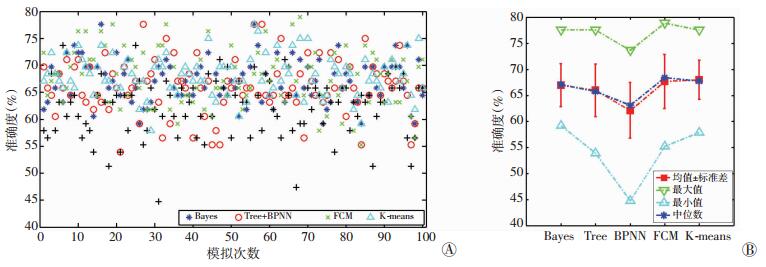
根据上述11个判别指标,分别采用贝叶斯判别分析(BDA)、决策树、BP神经网络(BPNN)、模糊C均值聚类(FCM)以及K均值聚类(K-means)的方法进行诊断,得到100次模拟分组条件下的诊断正确率如图 1A所示,5种数学模型的预测准确率的均值、方差、中位数及最值如图 1B所示。
|
| A:100次模拟诊断正确率分布图;B:诊断正确率的统计学描述 图 1 5种诊断模型随机模拟100次的准确率(P < 0.05) |
根据5种数学模型得到的判别诊断准确率的均值分别为66.97%、66.00%、62.13%、67.70%以及68.01%,可见选用差异性指标水平在P < 0.05情况下的判别模型并不恰当,因此本研究提高差异性指标水平,选择P < 0.01作为指标筛选标准,筛选得到随访24个月后MMSE得分(x5)、ADAST (x7)、ADASM (x8)、PRT (x15)、PCING (x19)、MPRT (x22)6项指标,并通过ROC曲线分析对上述6项指标进行敏感度及特异性分析。
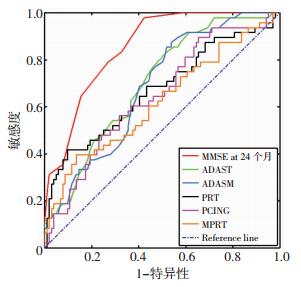
图 2给出了6项指标的ROC曲线,其相应的指标ROC曲线下面积(area under the curve,AUC)均与参考面积(AUC=0.5)差异存在统计学意义(P < 0.05)。因此,结合以上两项检验结果,可以认为这6项指标在MCInc组和MCIc组的判别中有较强的作用,从而将筛选出的6项指标作为诊断模型的自变量。表 2给出了6项指标的ROC曲线下面积值。
|
| 图 2 MCInc组和MCIc组6项指标的ROC曲线图 |
| 序号 | 指标 | AUC | 95% CI | P值a |
| x5 | 24个月后MMSE得分 | 0.854 | 0.796~0.912 | < 0.001 |
| x7 | AD认知行为评分 | 0.701 | 0.616~0.785 | < 0.001 |
| x8 | AD认知行为评分修正值 | 0.685 | 0.599~0.771 | < 0.001 |
| x15 | PRT | 0.671 | 0.573~0.768 | 0.001 |
| x19 | PCING | 0.647 | 0.554~0.740 | 0.004 |
| x22 | MPRT | 0.622 | 0.523~0.721 | 0.016 |
| a:与AUC=0.5比较 | ||||
2.2 诊断模拟的准确率比较
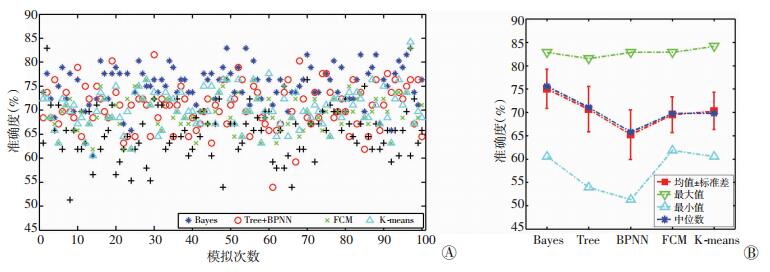
根据选择的6项诊断指标,分别采用贝叶斯判别分析(BDA)、决策树、BP神经网络(BPNN)、模糊C均值聚类(FCM)以及K均值聚类(K-means)的方法进行诊断。通过对原始数据进行100次随机化分组进行诊断训练和模拟,较好地减少单次随机分组造成的系统误差,图 3A显示了100次随机分组模拟条件下,5种诊断模型在MCInc组与MCIc组分类诊断中的准确率;图 3B显示了5种诊断模型准确率的均值、标准差、中位数、最值的大小关系。
|
| A:100次模拟诊断正确率分布图;B:诊断正确率的统计学描述 图 3 5种诊断模型随机模拟100次的准确率(P < 0.01) |
根据图 3显示的数据,可以发现BDA模型的准确率明显高于其他4种模型。为进一步比较BDA模型与其他4种模型判别诊断准确率的差异,将100次模拟获得5种模型的准确率作配对样本t检验,得到检验结果如表 3所示。BDA模型的准确率明显高于其他4种模型(P < 0.01)。
| 模型 | 均值检验 | t值 | P值 | |
| x±s | 95%CI | |||
| 决策树 | 4.421±5.702 | 3.290~5.552 | 7.754 | 8.054×10-12 |
| BP神经网络 | 9.868±6.385 | 8.602~11.135 | 15.456 | 3.850×10-28 |
| 模糊C均值聚类 | 5.566±3.740 | 4.824~6.908 | 14.883 | 5.327×10-27 |
| K均值聚类 | 4.789±3.585 | 4.078~5.501 | 13.359 | 6.958×10-24 |
在100次判别模拟中,5种模型的平均判别准确例数和准确率见表 4。可知,当进行MCInc组与MCIc组分类诊断时,BDA模型和决策树模型对于MCInc组的诊断准确率较高,而FCM模型和K-means模型对于MCIc组的诊断准确率较高,就综合判别诊断效果而言,BDA模型的判别准确率明显高于其他4种模型,其平均判别准确率达到74.86%(56/76)。
| 模型 | 判别诊断 | 平均值 | 最大值 | 最小值 | |
| MCInc组 | MCIc组 | ||||
| 贝叶斯判别分析 | 42.64(82.00) | 14.25(59.38) | 74.86 | 84.21 | 64.47 |
| 决策树 | 41.59(79.98) | 12.34(51.42) | 70.96 | 81.58 | 56.58 |
| BP神经网路 | 37.22(71.58) | 11.73(48.87) | 64.41 | 76.32 | 48.68 |
| 模糊C均值聚类 | 34.69(66.71) | 18.05(75.21) | 69.39 | 77.63 | 59.21 |
| K均值聚类 | 36.15(69.52) | 17.52(73.00) | 70.62 | 81.58 | 59.21 |
3 讨论
本研究对象是ADNI提供的152例明确诊断的MCI患者,根据其在24个月后的随访诊断结果,将全部152例患者分为MCInc患者和MCIc患者。为减少模拟模型的抽样误差,本研究采用随机数字表法将152例MCI患者分为2组,每组均包括52例MCInc患者和24例MCIc患者,得到的两组分别为本研究模型的训练样本和检测样本。为减少随机抽样的系统误差,本研究通过计算机程序进行100次随机分组。首先通过差异性检验的方法,以P < 0.01作为差异性评价指标,共筛选出包括随访24个月后MMSE得分(x5)、阿尔茨海默病评估量表-认知行为评分ADAST (x7)、阿尔茨海默病评估量表-认知行为评分修正值ASASM (x8)、左右半脑顶叶皮质灰度平均值PRT (x15)、左右半脑颞叶皮质灰度平均值PCING (x19)、左右半脑顶叶中区皮质灰度平均值MPRT (x22)6项指标,再采用贝叶斯判别分析、决策树、BP神经网络、模糊C均值聚类、K均值聚类等判别模型对每1次随机分组条件下检测样本中76例MCI患者的预后诊断(24个月后)进行判别评估,最终得到上述5种判别模型在100次随机分组条件下的平均准确率分别为74.86%、70.96%、64.41%、69.39%、70.62%。
根据既往研究来看,国内外的研究重点主要在于如何根据现有的分子生物学指标、影像学指标,利用数学模型对MCI患者及AD患者进行诊断[9-12],其研究成果为临床医师在实际临床工作中鉴别诊断认知功能障碍类疾病提供了新的思路和方法。然而也有研究发现:由于MCI患者的诊断标准尚不明确,特别是其中aMCI患者的诊断更为困难[2, 4],因此提出一个能够有效判别MCI患者预后效果的数学模型成为新的研究重点。本研究通过对152例MCI患者的预后进行评估,在所提出的5种判别模型中,贝叶斯判别分析模型(BSA)的平均准确率最高,达到74.86%(56/76),明显高于本研究中的其他数学模型,能够较为有效地对MCI患者的预后效果进行评估,达到了本研究的研究目的,能够为临床医师在是否对MCI患者进行早期干预问题上提供理论依据。
当然,本研究中得到的准确率尚不能令人满意,分析其原因主要包括两个方面:一方面,目前MCI患者的鉴别诊断仍存在较大争议,通过常规的生化学、影像学指标诊断仍较为困难,本研究提出的MCI患者在24个月后预后效果的判别更是困难;另一方面,由于本研究采用的数据样本较少,评价指标较为单一,模型方法也相对简单。因此今后从两个方面进行研究改进:一是收集更多数据样本,综合多种临床上的检验检查指标,尽可能较少样本中的异常值数据;二是研究探索判别效果更好的数学模型,或通过改进现有模型提高判别准确率。
| [1] | Petersen R C, Smith G E, Waring S C, et al. Mild cognitive impairment: clinical characterization and outcome[J]. Arch Neurol,1999, 56 (3) : 303 –308. DOI:10.1001/archneur.56.3.303 |
| [2] | Panza F, Capurso C, D'Introno A, et al. Mild cognitive impairment: risk of Alzheimer disease and rate of cognitive decline[J]. Neurology,2007, 68 (12) : 964 –965. DOI:10.1212/01.wnl.0000259691.26674.d3 |
| [3] | Cheng G, Huang C, Deng H, et al. Diabetes as a risk factor for dementia and mild cognitive impairment: a meta-analysis of longitudinal studies[J]. Intern Med J,2012, 42 (5) : 484 –491. DOI:10.1111/j.1445-5994.2012.02758.x |
| [4] | Grundman M, Petersen R C, Ferris S H, et al. Mild cognitive impairment can be distinguished from Alzheimer disease and normal aging for clinical trials[J]. Arch Neurol,2004, 61 (1) : 59 –66. DOI:10.1001/archneur.61.1.59 |
| [5] | Ward A, Tardiff S, Dye C, et al. Rate of Conversion from Prodromal Alzheimer's Disease to Alzheimer's Dementia: A Systematic Review of the Literature[J]. Dement Geriatr Cogn Dis Extra,2013, 3 (1) : 320 –332. DOI:10.1159/000354370 |
| [6] | Busse A, Hensel A, Gühne U, et al. Mild cognitive impairment: long-term course of four clinical subtypes[J]. Neurology,2006, 67 (12) : 2176 –2185. DOI:10.1212/01.wnl.0000249117.23318.e1 |
| [7] | Manly J J, Tang M X, Schupf N, et al. Frequency and course of mild cognitive impairment in a multiethnic community[J]. Ann Neurol,2008, 63 (4) : 494 –506. DOI:10.1002/ana.21326 |
| [8] | Ganguli M, Snitz B E, Saxton J A, et al. Outcomes of mild cognitive impairment by definition: a population study[J]. Arch Neurol,2011, 68 (6) : 761 –767. DOI:10.1001/archneurol.2011.101 |
| [9] | Graña M, Termenon M, Savio A, et al. Computer aided diagnosis system for Alzheimer disease using brain diffusion tensor imaging features selected by Pearson's correlation[J]. Neurosci Lett,2011, 502 (3) : 225 –229. DOI:10.1016/j.neulet.2011.07.049 |
| [10] | McEvoy L K, Holland D, Hagler D J Jr, et al. Mild cognitive impairment: baseline and longitudinal structural MR imaging measures improve predictive prognosis[J]. Radiology,2011, 259 (3) : 834 –843. DOI:10.1148/radiol.11101975 |
| [11] | 罗万春. 阿尔茨海默病和轻度认知损伤诊断的建模分析[J]. 第三军医大学学报,2013, 35 (15) : 1613 –1615. |
| [12] | 马翠, 周先东, 罗万春. 阿尔茨海默病和轻度认知损伤诊断的逐步Fisher判别模型[J]. 第三军医大学学报,2016, 38 (13) : 1501 –1505. DOI:10.16016/j.1000-5404.201509138 |



