毒蛇咬伤是常见急症。目前抗蛇毒血清的使用被认为是毒蛇咬伤的特效治疗[1],其能与毒液中参与病理生理反应的游离毒素结合并中和,使之失去毒性。但毒素一旦与组织细胞产生效应,抗蛇毒血清也无法产生作用[2]。已经发生的局部毒性损伤若不及时处理,患者极易出现肿胀、骨筋膜室综合征等局部并发症,常常导致组织坏死、甚至截肢[3]。而且蛇毒毒素吸收至全身后极易造成多器官功能受损[4]。快速有效减轻局部组织反应、减少毒素吸收对控制局部和全身并发症,减少致残率尤为重要。目前针对肿胀的治疗措施极为有限,大多采用传统综合治疗和中西医结合治疗,但效果并不明显。负压创面治疗技术(negative pressure wound therapy, NPWT)由德国Ulm大学创伤外科的Fleischmann博士首创,是近年来新兴的减轻组织水肿、促进创面愈合的治疗技术[5],目前极少用于毒蛇咬伤治疗。我们自2015年来采用皮肤多个小切口后联合NPWT治疗早期毒蛇咬伤患者,现报告如下。
1 资料与方法 1.1 研究对象选取2015年4月至2016年7月西南医院急救部收治的29例蝮蛇咬伤住院患者,男性18例,女性11例,平均年龄48.4岁。纳入标准:①年龄:18~70岁;②明确为毒蛇咬伤48 h内;③伤情按Downey分级为2~3级者(Downey分级:0级:肿胀范围小于2.5 cm,无全身中毒症状;1级:肿胀范围2.5~15 cm,没有全身中毒表现;2级:肿胀范围15~40 cm,有轻微全身中毒表现;3级:肿胀范围超过40 cm,有明显全身中毒表现;4级:严重全身中毒表现如昏迷、休克等[6-7]);④无心、肝、肾及血液系统等重要脏器疾病,来院时凝血3项各指标在正常范围内,未发生骨筋膜室综合征。签署参加临床试验知情同意书和手术知情同意书。此研究已通过中国注册临床试验伦理审查委员会审查(注册号:ChiCTR-TRC-14004189),符合医学研究伦理。
1.2 分组与治疗方法用SPSS 13.0软件产生随机数字的方法将患者随机分为观察组和对照组,观察组14例,对照组15例。
对照组给予常规综合治疗,包括伤口清创、“十”字切开、抗蛇毒血清治疗、破伤风抗毒素注射、甲强龙抗过敏治疗、甘露醇脱水、季德胜蛇药片内服外敷、抗感染以及补液等治疗。
观察组除上述综合治疗外,在患肢伤处近心端15~20 cm皮肤张力较高且避开大血管神经处(下肢一般为胫骨近端胫腓两侧,上肢一般为肱骨外侧)皮肤。常规消毒后在局麻下行6个小切口,切口分2行纵行排列,每行3个,长度1.5 cm,间距1 cm,两行间隔2 cm,深达皮下;确定无活动性出血后,以一次性负压引流护创材料(山东创康生物技术有限公司)覆盖创面,透明透气胶黏贴膜粘贴,确保密闭性后,给予125 mmHg持续负压吸引。肿胀消退后拆除负压引流材料,切口清创缝合。
1.3 观察指标设置6个抽血与指标观察的时间点:治疗前0 h,治疗后6、12、24、48、72 h。①按时间节点记录患者的近、中、远3个部位患肢周径:上肢分别记录腕横纹上10、20 cm及鹰嘴上10 cm平面;下肢记录内踝上15、25 cm及股骨内侧髁上15 cm平面。同时测量健侧肢体对应部位肢体周径,每次测量后计算患肢周径与相应健侧肢体周径差值,读数保留小数点后1位。②按上述时间点抽取静脉血,离心分离血清后于-70 ℃低温保存,收齐血标本后统一检测IL-6、TNF-α,检测方法采用ELISA法。③以全身及局部症状及体征消失,无明显后遗症为出院标准,记录观察组和对照组出院时的住院天数。
1.4 统计学方法采用SPSS 13.0统计软件进行统计学分析,计数资料采用χ2检验;计量资料用x±s或Md±Q表示,采用独立样本t检验和两组的重复测量设计的方差分析。检验水准α=0.05。
2 结果 2.1 两组患者的一般资料比较两组患者均以男性居多,最小年龄16岁,最大年龄70岁。平均就诊时间为19.1 h,多数患者在受伤后24 h内就诊,最早伤后5 h,最晚为伤后48 h。对照组与观察组的性别比、年龄、受伤部位、伤情分级差异无统计学意义(P>0.05,表 1)。
| 组别 | 例数 | 年龄 | 性别比男/女 | 受伤部位上肢/下肢 |
| 观察组 | 14 | 49.1±18.2 | 9/5 | 5/9 |
| 对照组 | 15 | 47.8±19.3 | 9/6 | 3/12 |
| χ2或t | t=-182 | 0.558 | 0.298 | |
| P | 0.875 | 0.812 | 0.344 |
2.2 两组患者入院不同部位各时间点肢体周径差
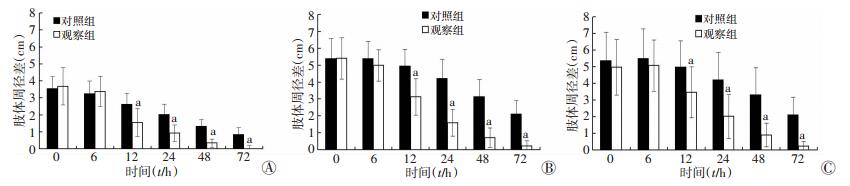
两组患者入院时均已出现患肢肿胀,以患肢中部肿胀明显。两组病例肢体远端、中部、近端周径差基线值差异均无统计学意义(P=0.648、0.964、0.555)。各时间点两组肢体周径差值变化曲线如图 1。经治疗后,在不同测量时间下对照组与观察组肢体远端周径差差异有统计学意义(F=10.884,P=0.03,图 1A);对照组与观察组肢体中部周径差差异有统计学意义(F=25.374,P=0.000,图 1B);对照组与观察组肢体近端周径差差异有统计学意义(F=8.946,P=0.006,图 1C)。
|
| A:肢体远端周径差变化曲线;B:肢体中部周径差变化曲线;C:肢体近端周径差变化曲线;a: P < 0.05,与对照组比较 图 1 两组患者入院不同部位各时间点肢体周径差(x±s) |
2.3 两组患者入院后IL-6与TNF-α浓度变化 2.3.1 入院时(0 h)两组血清IL-6和TNF-α浓度比较
两组患者入院时(0 h)血清IL-6和TNF-α浓度均升高,对IL-6浓度基线水平采用独立样本t检验结果显示,观察组与对照组差异无统计学意义(t=-0.040,P=0.968);对TNF-α浓度基线水平采用两独立样本比较的秩和检验,结果显示观察组与对照组差异无统计学意义(W=-1.091,P=0.290,表 2)。
| 组别 | IL-6浓度 | TNF-α浓度 |
| 观察组 | 15.64±15.50 | 370.72±341.46 |
| 对照组 | 11.18±23.84 | 270.30±250.52 |
| t/W | -0.040 | -1.091 |
| P | 0.968 | 0.290 |
2.3.2 经治疗后两组血清IL-6和TNF-α浓度比较
经治疗,两组患者血清IL-6和TNF-α浓度逐渐下降,在不同测量时间下对照组与观察组IL-6浓度存在统计学差异(F=5.115,P=0.032),观察组IL-6浓度低于对照组(表 3);在不同测量时间下对照组与观察组TNF-α浓度存在统计学差异(F=4.516,P=0.043),观察组TNF-α浓度低于对照组(表 4)。
| 组别 | 0 h | 6 h | 12 h | 24 h | 48 h | 72 h |
| 观察组 | 15.64±15.50 | 11.39±5.46a | 6.56±3.12a | 4.07±2.92a | 1.89±1.81a | 0.58±0.93a |
| 对照组 | 11.18±23.84 | 9.39±19.16 | 8.61±12.87 | 7.05±7.61 | 5.23±4.09 | 2.04±2.51 |
| a:P < 0.05,与对照组比较 | ||||||
| 组别 | 0 h | 6 h | 12 h | 24 h | 48 h | 72 h |
| 观察组 | 370.72±341.46 | 176.38±291.53a | 103.49±138.29a | 60.73±70.66a | 32.47±50.19a | 15.69±20.98a |
| 对照组 | 270.30±250.52 | 355.26±250.72 | 296.79±224.34 | 208.09±224.37 | 117.70±115.16 | 57.11±50.72 |
| a:P < 0.05,与对照组比较 | ||||||
2.4 两组患者住院时间比较
观察组住院时间(5.43±1.07) d,最短住院4 d,最长7 d;对照组住院时间(7.67±1.95) d,最短住院5 d,最长12 d。平均住院时间两组差异有统计学意义(P=0.001),观察组较对照组少。
3 讨论在本研究中,我们观察到几乎所有患者均出现了局部肢体肿胀,患者入院时下肢最高肿胀平面至腹股沟,上肢最高肿胀平面至肩关节。可见毒蛇咬伤后局部并发症极高,这与文献[8]报道相符。全球范围内,至少有40万毒蛇咬伤患者有明确的并发症发生,以蝮蛇咬伤较明显[9]。因蛇毒中含有各种酶类,蛋白水解酶可损害血管壁内皮细胞,可增加管壁通透性,导致血浆外渗,组织水肿,透明质酸酶可溶解细胞与纤维间质,破坏结缔组织完整性,且蛇毒作用于机体后可使机体释放出激肽、组胺和5-羟色胺等物质而引起肿胀。足见毒蛇咬伤后局部肢体损害严重性,因此针对患肢局部肿胀的治疗应该被足够重视,且应采取积极可行的治疗手段。
我们观察到治疗6 h内肿胀消退不明显,尤其表现在肢体近端,治疗早期肿胀仍有向上发展趋势,说明早期毒素吸收至全身组织后,前述毒性效应继续存在。究其原因,蛇毒通过毒牙刺破皮肤后注入皮下或者肌内,然后扩散至组织间隙,大多数均通过淋巴系统吸收,血液中1.5~5 h达最大浓度[10]。所以部分患者入院时,仍有部分毒液残留于局部组织,肿胀未达高峰,以致后续向近心端发展。可以看出即便两组患者均已在入院后使用抗蛇毒血清治疗,但肿胀曲线显示观察组从治疗12 h开始肿胀消退速度明显快于对照组。且从两组多个测量部位多个时间点比较均有统计学差异。我们认为,使用抗蛇毒血清后仍有必要采用负压引流治疗。因为在咬伤部位的近心端皮肤上做皮肤小切口,首先起到皮肤减张的目的,减轻了持续肿胀对患者局部的进一步损害,同时为水肿液的引流和毒素的排出提供了快速通道。在小切口上采用持续负压吸引,加速了水肿液排出,阻断了毒液的物理吸收过程,减轻了毒素吸收后对全身组织器官产生的反应,起到了减轻肿胀同时又引流毒液的双重作用。可见小切口负压治疗在加速肿胀消退方面有明显作用。负压治疗技术既往主要应用于急、慢性创口的治疗[11],通过本研究我们认为负压治疗技术可能会成为毒蛇咬伤后的一种创新应用,或可进一步推广。
通过对两组患者不同时间点IL-6与TNF-α浓度的测量,我们发现大多数毒蛇咬伤患者入院时这两项指标均有不同程度升高,两组无明显差异。这些变化与以往文献[12]报道类似。众所周知,IL-6与TNF-α同是早期炎症反应的经典促炎因子,能在细胞核等亚细胞水平上,诱导包括自身在内的多种炎性因子表达上调,从而激发一系列级联反应或瀑布效应,IL-6水平与炎症反应强度呈正相关[13]。TNF-α可激活巨噬细胞和中心粒细胞并影响它们的吞噬作用和细胞毒作用。且蛇毒可使前体TNF-α转化为活化的TNF-α从而导致全身和局部损伤[12]。由此可见,毒蛇咬伤后,两组患者机体均有不同程度的炎症反应存在。但是我们发现,经治疗后两组IL-6、TNF-α水平下降,通过多次测量比较显示,观察组IL-6水平和TNF-α低于对照组,差异有统计学意义,说明小切口负压治疗后全身炎症反应可迅速缓解。我们认为,采用小切口负压治疗使肢体肿胀得到明显控制的同时减轻了局部炎症反应,控制了炎症介质的持续表达引起的级联反应,使得全身性炎症反应也迅速缓解。由于负压吸引可引流毒液,减少毒素进一步吸收,减轻毒素对全身各组织器官的作用,使全身炎症反应得到控制。所以正是由于观察组局部水肿减轻速度和全身炎症缓解速度明显优于对照组,其平均住院天数明显减少。观察组最短住院日仅为4 d,而对照组最长住院日为12 d。
本研究也存在一些不足,由于病例数有限,我们并没有设计受伤部位以及就诊时间对消肿速度的相关性分析,以及受伤程度与治疗效果的相关性分析。
总之,我们认为在毒蛇咬伤治疗中,在传统综合治疗基础上,需重视患肢局部的积极处理。给予伤情Downey分级为2~3级的患者患肢皮肤多个小切口联合负压治疗,较单独采用传统综合治疗可在短时间内控制患肢肿胀发展,明显加速肿胀消退,并且可以有效加速缓解全身炎症反应,缩短住院时间,近期疗效明显。针对小切口负压治疗技术减轻肿胀和全身炎症反应的作用机制,我们还将在下一步临床和基础研究中做进一步探索。
| [1] | Warrell D A. WHO/SEARO Guidelines for the clinical management of snake bites in the Southeast Asian region[J]. Southeast Asian J Trop Med Public Health,1999, 30 (Suppl 1) : 1 –85. |
| [2] | Gutiérrez J M, León G, Burnouf T. Antivenoms for the treatment of snakebite envenomings: the road ahead[J]. Biologicals,2011, 39 (3) : 129 –142. DOI:10.1016/j.biologicals.2011.02.005 |
| [3] | Gay C C, Maruñak S L, Teibler P, et al. Systemic alterations induced by a Bothrops alternatus hemorrhagic metalloproteinase (baltergin) in mice[J]. Toxicon,2009, 53 (1) : 53 –59. DOI:10.1016/j.toxicon.2008.10.010 |
| [4] | Karabuva S, Vrkiç I, Briziç I, et al. Venomous snakebites in children in southern Croatia[J]. Toxicon,2016, 112 : 8 –15. DOI:10.1016/j.toxicon.2016.01.057 |
| [5] | Daeschlein G, Napp M, Lutze S, et al. Comparison of the effect of negative pressure wound therapy with and without installation of polyhexanide on the bacterial kinetic in chronic wounds[J]. Wound Medicine,2016, 13 : 5 –11. DOI:10.1016/j.wndm.2016.02.001 |
| [6] | 章均, 王珊, 李长春, 等. Downey分级在儿童毒蛇咬伤诊治中的应用[J]. 中华实用儿科临床杂志,2013, 28 (20) : 1592 –1595. DOI:10.3969/cma.j.issn.2095-428X.2013.20.021 |
| [7] | Downey D J, Omer G E, Moneim M S. New Mexico rattlesnake bites: demographic review and guidelines for treatment[J]. J Trauma,1991, 31 (10) : 1380 –1386. DOI:10.1097/00005373-199110000-00011 |
| [8] | Lavonas E J, Kokko J, Schaeffer T H, et al. Short-term outcomes after Fab antivenom therapy for severe crotaline snakebite[J]. Ann Emerg Med,2011, 57 (2) : 128 –137. DOI:10.1016/j.annemergmed.2010.06.550 |
| [9] | Gutiérrez J M, Williams D, Fan H W, et al. Snakebite envenoming from a global perspective: Towards an integrated approach[J]. Toxicon,2010, 56 (7) : 1223 –1235. DOI:10.1016/j.toxicon.2009.11.020 |
| [10] | Paniagua D, Jiménez L, Romero C, et al. Lymphatic route of transport and pharmacokinetics of Micrurus fulvius (coral snake) venom in sheep[J]. Lymphology,2012, 45 (4) : 144 –153. |
| [11] | Salman A E, Yetişir F, Aksoy M, et al. Use of dynamic wound closure system in conjunction with vacuum-assisted closure therapy in delayed closure of open abdomen[J]. Hernia,2014, 18 (1) : 99 –104. DOI:10.1007/s10029-012-1008-0 |
| [12] | Açıkalın A, Gökel Y. Serum IL-6, TNFα levels in snakebite cases occurring in Southern Turkey[J]. Emerg Med J,2011, 28 (3) : 208 –211. DOI:10.1136/emj.2009.078428 |
| [13] | Guisasola M C, Ortiz A, Chana F, et al. Early inflammatory response in polytraumatized patients: Cytokines and heat shock proteins. A pilot study[J]. Orthop Traumatol Surg Res,2015, 101 (5) : 607 –611. DOI:10.1016/j.otsr.2015.03.014 |



