2. 615000 四川 西昌,中国人民解放军第519医院:检验科;
3. 615000 四川 西昌,中国人民解放军第519医院:医务处;
4. 615000 西昌,西昌市人民医院检验科
2. Department of Clinical Laboratory, No. 519 Hospital of PLA, Xichang, Sichuan Province, 615000;
3. Department of Medical Affairs, No. 519 Hospital of PLA, Xichang, Sichuan Province, 615000;
4. Department of Clinical Laboratory, Xichang People ' s Hospital, Xichang, Sichuan Province, 615000, China
结核病是由结核分枝杆菌(Mycobacterium tuberculosis, MTB)感染引起的传染性疾病,并以肺结核(pulmonary tuberculosis, PTB)最为常见,占80%~90%。全球约有1/3人口为MTB感染者,但仅有近1/10的感染者发展成结核病[1];同卵双胞胎同患肺结核的几率明显大于异卵双胞胎[2];不同种系小鼠感染MTB后出现不同的MTB免疫反应[3],这些均表明MTB感染及其感染后的临床转归存在个体间差异,基因多态性在肺结核发生发展中起重要作用。并且不同地域不同种族人群的肺结核易感基因及其对应的单核苷酸多态性(single nucleotide polymorphisms, SNP)均存在差异[4],但目前仅有关于基因多态性与维吾尔族[5-6]、哈萨克族[7]、藏族[8-9]等少数民族肺结核发病风险的文献报道,而凉山彝族人群肺结核发病率高,却缺乏相关的研究报道。
SOCS1基因位于16p13.13,所编码的细胞因子信号传导抑制因子1(suppressor of cytokine signaling1, SOCS1)是MTB感染时宿主巨噬细胞中调节细胞因子信号通路的一个关键分子。SOCS1基因在肺结核患者外周血单个核细胞及结核淋巴结中均表达增加[10-11],其差异性表达对鉴别活动性肺结核和潜伏性肺结核具有辅助诊断作用[12]。我们课题组前期实验还发现miR-155能通过靶向作用SOCS1参与调控结核早期分泌抗原ESAT-6介导的MTB感染时机体巨噬细胞凋亡发生[13]。故我们推测SOCS1基因SNP可能与肺结核发生风险存在关联性,且未见有关文献报道。因此为证实这一推测,本研究试图在凉山彝族人群中研究SOCS1基因-3969 C/T位点(rs243327)[14](位于5′端启动子区,等位基因C→T突变会引起SOCS1基因转录因子结合位点的改变,影响SOCS1基因表达,进而影响机体抗MTB免疫反应)、+1125G/C位点(rs33932899)[15](位于3′端非翻译区,可影响机体血清IgE水平)与肺结核发生风险之间的关联性,为预测肺结核发生风险,提高肺结核的预防、诊断水平奠定理论基础。
1 材料与方法 1.1 研究对象2015年3月至2016年6月在凉山州传染病医院招募肺结核患者188例,同时在解放军第519医院和西昌市人民医院招募健康对照229例。所有研究对象均为常年居住凉山彝族自治州境内的彝族同胞,且相互之间无生物学亲缘关系。肺结核确诊严格按照中华人民共和国卫生和计划生育委员会制定的诊断标准。188名肺结核患者年龄为(36.96±17.32)岁,64.4%是男性。229名健康对照年龄为(37.68±13.45)岁,54.1%是男性。作为健康对照,应排除肺部、肾脏、心脏、脑部及尿路等脏器感染,无高血压、糖尿病、甲状腺疾病、恶性肿瘤、慢性消耗性疾病及其他传染病病史,且HIV抗体阴性。所有受试人员均签署知情同意书。本研究获第三军医大学大坪医院野战外科研究所伦理委员会批准。
1.2 基因组DNA提取采集肘静脉全血2 mL/例,EDTA抗凝,颠倒混匀,置于-20 ℃冰箱保存。所有标本冷链运输回重庆第三军医大学大坪医院检验科。按照全血基因组DNA提取试剂盒(TIANGEN生产,北京)操作指南提取基因组DNA,经Nanodrop ND1000(ThermoFisher Scientific生产,美国)检测DNA浓度和纯度后,置于-80 ℃冰箱,备用。
1.3 SNP分型利用primer 6.0软件设计rs243327、rs33932899两个位点PCR扩增引物(rs243327上游引物:5′-TCTTGGGACCTGATTTGCCC-3′,下游引物:5′-CGGTCAGCAG-AATCCACACT-3′,PCR产物长度480 bp;rs33932899上游引物:5′-GGAAATAAGAGCCCGTGCCT-3′,下游引物:5′-CCCTGGTTGTTGTAGCAGCT-3′,PCR产物长度510 bp)。所有引物均由成都擎科合成。
PCR总反应体积为50 μL,含有2×I-5TMMix (MCLAB Inc,美国)25 μL,上、下游引物(浓度为10 pmol/μL)各1 μL,基因组DNA 1 μL,双蒸水22 μL。采用Touch Down PCR扩增方法:在98 ℃下进行4 min的预变性,接下来98 ℃下变性10 s,退火温度从59 ℃降至50 ℃,72 ℃下延伸15 s (共10个循环,每个循环降1 ℃),然后再进行20个循环的98 ℃下10 s变性,55 ℃下15 s退火和72 ℃下15 s延伸,最后在72 ℃下延长5 min。所有PCR扩增产物均用ABI 3730XL测序仪(Applied Biosystems,美国)直接测序,Chromas基因序列分析软件对rs243327、rs33932899两个位点进行基因型的辨别和判读。
1.4 统计学分析计数肺结核患者和健康对照组rs243327、rs33932899两个位点的基因型和等位基因,利用Mann-Whitney U秩和检验比较肺结核组和健康对照组之间的年龄差异,利用χ2检验判断肺结核组和健康对照组的基因型分布是否符合哈-温平衡,采用χ2检验分析分类变量的统计学变化,非条件Logistic回归分析计算比值比(OR)和95%可信区间(CI)评价相关性。检验水准α=0.05。所有数据均采用SPSS19.0统计软件(SPSS Inc,美国)进行分析。
2 结果 2.1 凉山彝族人群肺结核患者与健康对照人群的社会人口学和临床特征首先对凉山彝族人群肺结核患者与健康对照人群的性别、年龄、有无吸烟史、痰涂片抗酸染色是否阳性、是否合并肺外结核感染及是否患有HIV共感染等情况进行统计分析(表 1)。肺结核组和健康对照组研究对象分别为188例和229例,总计417例。两组间年龄差异采用Mann-Whitney U秩和检验,性别、有无吸烟史的差异采用χ2检验,结果表明凉山彝族人群肺结核发病风险与年龄无相关性(P=0.139,表 1),但与性别、是否有吸烟史有显著相关性(P=0.035,P=0.009,表 1),这可能与吸烟能降低机体肺泡巨噬细胞抗MTB免疫力,且在凉山地区烟草种植范围广,吸烟人数较多,彝族男性吸烟人数显著多于女性有关。
| 组别 | n | 性别(男/女) | 年龄 | 有吸烟史[例数(%)] | 痰涂片AFS阳性(%) | 合并肺外结核感染[例数(%)] | 合并HIV共感染[例数(%)] | ||
| x±s | 最小值 | 最大值 | |||||||
| 肺结核组 | 188 | 121/67a | 36.96±17.32 | 13 | 76 | 79(42.0)b | 29.90 | 102(54.2) | 48(25.5) |
| 健康对照组 | 229 | 124/105 | 37.68±13.45 | 14 | 81 | 68(29.6) | - | - | - |
| a:P=0.035, b:P=0.009, 与健康对照组比较;AFS:抗酸染色,HIV:人类免疫缺陷病毒 | |||||||||
2.2 凉山彝族人群肺结核组-健康对照组rs243327、rs33932899基因型分布
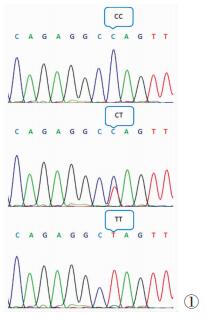
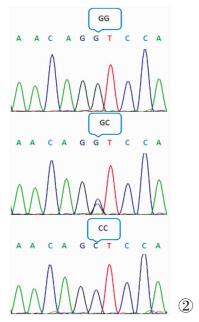
运用测序法对188例肺结核患者和229例健康对照人群进行rs243327、rs33932899基因分型,基因分型成功率100%。如图 1所见,rs243327存在C→T多态性。如图 2所见,rs33932899存在G→C多态性。在肺结核组和健康对照组中,rs243327位点基因型分布如表 2所示,rs33932899位点基因型分布表 3所示,均符合Hardy-Weinberg遗传平衡定律,这提示所选研究人群具有较好的群体代表性。rs243327最小等位基因频率分别为19.1%、26.4%,与dbSNP数据库中国北京汉族人群中的最小等位基因频率存在差异(T等位基因:30.5%)。rs33932899最小等位基因频率分别是21.0%、25.5%,由于dbSNP数据库未见报道有关中国北京汉族人群中rs33892899最小等位基因频率数据,故无法比较。
|
| 图 1 rs243327 C/T基因分型结果 |
|
| 图 2 rs33932899 G/C基因分型结果 |
| 组别 | rs243327 | MAF (%) | HWE P值 | ||
| CC | CT | TT | |||
| 肺结核组 | 125 | 54 | 9 | 19.1 | 0.321 |
| 健康对照组 | 125 | 87 | 17 | 26.4 | 0.728 |
| 总计 | 250 | 142 | 26 | 23.2 | 0.338 |
| MAF:最小等位基因频率;HWE:哈-温遗传平衡 | |||||
| 组别 | rs33932899 | MAF (%) | HWE P值 | ||
| GG | GC | CC | |||
| 肺结核组 | 116 | 65 | 7 | 21.0 | 0.568 |
| 健康对照组 | 129 | 83 | 17 | 25.5 | 0.475 |
| 总计 | 245 | 148 | 26 | 23.9 | 0.566 |
| MAF:最小等位基因频率;HWE:哈-温遗传平衡 | |||||
2.3 rs243327、rs33932899与凉山彝族人群肺结核发生风险的关联性分析
如表 4所示,通过卡方检验发现,在rs243327位点处肺结核组CC基因型频率显著高于健康对照组(CC vs CT:OR=1.611,95% CI=1.058-2.453,P=0.026;CC vs CT+TT:OR=1.651,95% CI=1.107-2.461,P=0.014),提示rs243327 CC基因型可能增加凉山彝族人群肺结核的发生风险,可能是凉山彝族人群肺结核的易感基因型;C等位基因频率亦显著高于健康对照组(C vs T:OR=1.516,95%CI=1.089-2.109,P=0.013),提示rs243327 C等位基因可能增加凉山彝族人群肺结核的发生风险,可能是凉山彝族人群肺结核的易感等位基因。在rs33932899位点处GG、CG、CC基因型分布在两组间无统计学差异(GG vs CG:OR=1.148,95% CI=0.762-1.731,P=0.436;GG vs CC:OR=2.184,95% CI=0.874-5.454,P=0.088;GG/CG+CC:OR=1.229,95% CI=0.875-1.928,P=0.193),rs33932899 G等位基因与C等位基因在肺结核组和健康对照组之间亦无统计学差异(G vs C:OR=1.290,95% CI=0.932-1.785,P=0.124),提示rs33932899位点可能与凉山彝族人群肺结核发生风险无相关性。
| SOCS1 SNP | 肺结核组[例数(%)] | 健康对照组[例数(%)] | χ2 | P | OR(95%CI) |
| rs243327基因型 | |||||
| CC | 125(66.5) | 125(54.6) | 1(参考) | ||
| CT | 54(28.7) | 87(38.0) | 4.974 | 0.026 | 1.611(1.058-2.453) |
| TT | 9(4.8) | 17(7.4) | 2.232 | 0.135 | 1.899(0.811-4.398) |
| CT+TT | 63(33.5) | 104(45.4) | 6.094 | 0.014 | 1.651(1.107-2.461) |
| 等位基因 | |||||
| C | 304(80.9) | 337(73.6) | 1(参考) | ||
| T | 72(19.1) | 121(26.4) | 6.136 | 0.013 | 1.516(1.089-2.109) |
| rs33932899基因型 | |||||
| GG | 116(61.7) | 129(56.4) | 1(参考) | ||
| CG | 65(34.6) | 83(36.2) | 0.436 | 0.509 | 1.148(0.762-1.731) |
| CC | 7(3.7) | 17(7.4) | 2.911 | 0.088 | 2.184(0.874-5.454) |
| CG+CC | 72(38.3) | 100(43.6) | 1.692 | 0.193 | 1.229(0.875-1.928) |
| 等位基因 | |||||
| G | 297(79.0) | 341(74.5) | 1(参考) | ||
| C | 79(21.0) | 117(25.5) | 2.362 | 0.124 | 1.290(0.932-1.785) |
3 讨论
单核苷酸多态性是指由于单个核苷酸变异而产生的一种DNA序列多态性,属于第三代遗传标记。近些年来,探讨基因单核苷酸多态性在宿主结核病发生和发展中的重要作用备受关注,已有研究表明[5]人类白细胞抗原(HLA)基因、自然抗性相关性巨噬细胞蛋白1 (NRAMP1)基因、核体蛋白SP110基因、维生素D受体(VDR)基因、嘌呤受体PX27基因、肝X受体(LXR)基因、干扰素-γ(IFN-γ/IFNG)基因及干扰素-γ受体1(IFNGR1)基因等的SNP与不同地区、不同人群肺结核的发生发展相关联。
鉴于SOCS1在肺结核患者外周血单个核细胞和淋巴结中高表达,并能负反馈调节IL-2、IL-6、IL-12、IFN-γ等多种细胞因子JAK/STAT通路的信号转导,是MTB感染时机体巨噬细胞中调节细胞因子信号通路的一个关键分子,并且我们课题组前期实验还发现miR-155能通过靶向作用SOCS1参与调控结核早期分泌抗原ESAT-6介导的MTB感染时机体巨噬细胞凋亡发生,故选取SOCS1基因作为本研究的候选基因。然后通过SOCS1基因的tagSNP网上系统(Hapmap数据库、dbSNP数据库)分析和相关文献查阅,选取-3969 C/T位点(rs243327)[14]:位于SOCS1基因5′端启动子区,等位基因C→T的突变会引起转录因子结合结合位点(transcription factor binding site, TFBS)的改变,转录因子ICSBP[即干扰素调控因子8(interferon regulation factor, IRF8)]与等位基因C结合,与等位基因T不结合,进而改变SOCS1基因的表达,影响机体抗结核杆菌的免疫力,最终导致不同基因型人群对肺结核易感性的不同;+1125G/C位点(rs33932899)[15](位于SOCS1基因3′UTR,与机体血清IgE水平有关)作为本研究的tagSNP。最后选择结核病高发、却缺乏相关的研究报道的凉山彝族人群作为研究对象,以此探讨SOCS1基因单核苷酸多态性与肺结核发生风险的关联性。本研究在凉山彝族人群中共选取了188例肺结核患者和229例健康对照者,经过基因组DNA提取、PCR扩增后直接测序法SNP分型和统计学分析,发现SOCS1基因Tag SNP rs243327位点等位基因C可能增加凉山彝族人群肺结核的发生风险,而rs33932899位点可能与凉山彝族人群肺结核的发生风险无显著相关性。综上所述,本研究在凉山彝族人群中初步验证了SOCS1基因5′端启动子区的tagSNP rs243327位点与肺结核易感性具有关联性,而3′端非翻译区的tagSNP rs33932899位点与肺结核易感性无显著相关性。但由于肺结核发病机制复杂,是基因与环境(如吸烟、卫生条件差、营养条件差及HIV感染等)交互作用的结果,后期我们将进一步扩大样本量,并且设计分子学实验深入探讨rs243327 C/T不同等位对SOCS1基因表达的影响及调控机制,进一步了解rs243327等位基因C增加凉山彝族人群肺结核发生风险的SNP功能学原因。
| [1] | Nair N, Cooreman E. Working towards TB elimination the WHO Regional Strategic Plan (2006-2015)[J]. J Commum Dis,2006, 38 (3) : 185 –190. |
| [2] | Comstock G W. Tuberculosis in twins: a re-analysis of the prophit survey[J]. Am Rew Respir Dis,1978, 117 (4) : 621 –624. DOI:10.1164/arrd.1978.117.4.621 |
| [3] | Di Pietrantonio T, Schurr E. Host-pathogen specificity in tuberculosis[J]. Adv Exp Med Biol,2013, 783 : 33 –44. DOI:10.1007/978-1-4614-6111-1_2 |
| [4] | 周莹, 高琪乐, 黄华艺, 等. 宿主基因多态性与结核易感性研究进展[J]. 中华医院感染学杂志,2016, 26 (2) : 477 –480. DOI:10.11816/cn.ni.2016-150859 |
| [5] | 周江, 张万江. 甘露聚糖结合凝集素基因A/B位点与新疆维吾尔族结核病的相关性研究[J]. 中国防痨杂志,2012, 34 (7) : 445 –451. |
| [6] | 王喜, 任玲君, 李秀玲, 等. 新疆维吾尔族人群HLA-DR、DQ基因多态性与结核病易感性的研究[J]. 中国防痨杂志,2011, 33 (4) : 197 –203. |
| [7] | 吴芳.结核易感基因多态性与新疆哈萨克族结核病易感性的相关性研究[D].武汉:华中科技大学, 2014. |
| [8] | 陈雪融, 冯玉麟, 马玙, 等. 维生素D受体基因多态性与中国藏族结核病的关联研究[J]. 四川大学学报(医学版),2006, 37 (6) : 847 –851. |
| [9] | 李素芝, 蒋亚建, 谢本维, 等. 中国藏族人群HLA-DRB1、-DQA1、-DQB1等位基因多态性与肺结核易感性的关联性研究[J]. 第三军医大学学报,2011, 33 (12) : 1254 –1257. DOI:10.16016/j.1000-5404.2011.12.007 |
| [10] | Masood K I, Rottenberg M E, Carow B, et al. SOCS1 gene expression is increased in severe pulmonary tuberculosis[J]. Scand J Immunol,2012, 76 (4) : 398 –404. DOI:10.1111/j.1365-3083.2012.02731.x |
| [11] | Nicol A F, Nuovo G J, CoelhoJ M, et al. SOCS in situ expression in tuberculous lymphadenitis in an endemic area[J]. Exp Mol Pathol,2008, 84 (3) : 240 –244. DOI:10.1016/j.yexmp.2008.04.001 |
| [12] | Masood K I, Hussain R, Rao N, et al. Differential Early Secreted Antigen Target (ESAT) 6 kDa-induced IFN-gamma and SOCS1 expression distinguishes latent and active tuberculosis[J]. J Infect Dev Ctries,2014, 8 (1) : 59 –66. DOI:10.3855/jidc.3412 |
| [13] | Yang S, Li F, Jia S, et al. Early secreted antigen ESAT-6 of Mycobacterium Tuberculosis promotes apoptosis of macrophages via targeting the microRNA155-SOCS1 interaction[J]. Cell Physiol Biochem,2015, 35 (4) : 1276 –1288. DOI:10.1159/000373950 |
| [14] | Vargas-Alarcon G, Posadas-Sanchez R, Posadas-Romero C, et al. Association of the suppressor of cytokine signaling 1 (SOCS1) gene polymorphisms with acute coronary syndrome in Mexican patients[J]. Mol Immunol,2014, 62 (1) : 137 –141. DOI:10.1016/j.molimm.2014.06.019 |
| [15] | Zhang P, Li F, Li N, et al. Genetic variations of SOCS1 are associated with chronic hepatitis B virus infection[J]. Human Immunology,2014, 75 (8) : 709 –714. DOI:10.1016/j.humimm.2014.04.010 |



