胶质瘤是成人颅内最常见的恶性肿瘤之一,其恶性程度高、预后差,常规行放、化疗的胶质瘤患者的中位生存期仅为12~18个月 [1]。肿瘤新生血管是胶质瘤重要组织学特征之一,大量新生血管参与了胶质瘤微环境的构筑,与肿瘤生物学行为的演进密切相关 [2]。肿瘤微血管密度(microvessel density,MVD)描述了肿瘤微血管的数量分布特点,但是存在样本获取有创、取材范围较小等局限性,无创监测肿瘤新生血管的影像学技术有望弥补这些不足。磁共振灌注成像技术可以实现肿瘤血管的定量研究:DSC-MRI可以有效地测量肿瘤组织血流量、血流速率;DCE-MRI参数Ktrans直接反映组织血管通透性;VSI-MRI则可以较好地无创测量肿瘤组织的微血管管径等 [3-5]。磁共振灌注成像技术已经广泛用于胶质瘤的分级诊断、预后评估及疗效监测等领域,然而灌注技术强烈依赖人工对比剂的使用,有潜在的诱导受检者肾功能不全及对比剂残留在脑组织的风险 [6]。
弥散加权磁共振成像(diffusion weighted imaging,DWI)是唯一可以活体描述水分子自由扩散运动的磁共振成像方式,该过程不依赖任何外源性或内源性对比剂,真正实现了“无创”检测活体组织的功能信息。定量DWI或(和)非定量DWI已经广泛用于检测肿瘤组织细胞密度、鉴别肿瘤组织学分级等方面 [7-8]。 Le Bihan 等 [9-10]采用双指数模式从弥散信号中分离出微循环灌注的信息。目前的研究集中在验证DWI微循环灌注信号与DSC-MRI、DCE-MRI一致性方面,其组织学证据,特别是新生血管类型的研究有待进一步探讨。本研究立足DWI对胶质瘤新生血管的研究,重点探讨肿瘤新生血管类型与DWI的相关性,为DWI实现活体肿瘤新生血管动态检测提供实验依据。
1 材料与方法 1.1 C6胶质瘤原位移植模型的建立将C6细胞(购自中科院上海细胞库)接种于培养瓶中,加入适量含有10%FBS的DMEM高糖培养基(Hyclone公司),放置于37 ℃、5% CO2培养箱中培养。待细胞生长至接近90% 融合时,收集细胞用于建立胶质瘤原位移植模型。
取30只体质量150~180 g清洁级成年雄性SD大鼠(购自第三军医大学大坪医院野战外科研究所实验动物中心),随机数字表法分成6组,每组5只。大鼠麻醉后,取俯卧位将其头部固定于脑立体定位仪的大鼠适配器上。于前囟前1 mm,正中线右旁3 mm处,用直径为2 mm的牙科钻钻穿表面颅骨。量程为20 μL的微量进样器吸取10 μL胶质瘤细胞悬液,微量注射器固定于脑立体定位仪上,垂直进入脑实质中,控制进针深度为 5 mm,再回退1 mm,手动将胶质瘤细胞悬液缓慢注入脑实质内,控制注射时间为10 min。注射细胞悬液完毕后,留针5 min后退出,骨蜡封口,缝合皮肤切口,做好标记后分笼饲养。
1.2 C6胶质瘤原位模型MR扫描和数据处理采用Bruker 7.0 T小动物磁共振成像仪Biospin 70/20(德国Bruker公司),将其固定于磁共振动物专用扫描床内进行扫描。分别在接种肿瘤细胞后4、8、12、16、20、24 d进行MR扫描。扫描过程中持续使用2%异氟烷维持荷瘤鼠的麻醉状态。
MR扫描参数如下:TurboRARE-T2WI,TR/TE= 3 000 ms/50 ms,FOV=35 mm×35 mm,层厚0.5 mm;DWI-MRI,TR/TE=3 000 ms/50 ms,FOV=35 mm× 35 mm,层厚0.5 mm,b=0,500,1 000 s/mm2。
扫描完成后将DWI原始数据导入Bruker Biospin软件中进一步分析处理。分别测量肿瘤、对侧脑组织ADC值,取二者比值计算相对ADC(relative ADC,rADC)。
1.3 C6胶质瘤肿瘤组织学染色荷瘤鼠行MR扫描完成后,立即注射过量水合氯醛处死,经左心室灌注4%多聚甲醛,获取脑组织。组织经石蜡包埋,行组织学染色,抗体为兔抗大鼠CD34、Tenascin-C(英国Abcam公司)。免疫组化简要步骤如下,荷瘤鼠脑组织以2 μm的厚度行连续切片,65 ℃高温熔蜡后,置于二甲苯中脱蜡,脱蜡完成后,切片浸入pH=6.0的枸橼酸溶液中高压锅煮沸2 min,自然冷却后PBS冲洗,置于10%H2O2溶液中封闭内源性过氧化物酶。用山羊血清封闭非特异性抗原10 min后,滴加50 μL相应一抗4 ℃过夜。PBS冲洗孵育了一抗的切片,37 ℃孵育标记了辣根过氧化物酶的山羊抗兔二抗30 min,DAB系统显色。
1.4 统计学方法采用SPSS 24.0统计软件。计量资料以x±s表示,采用单因素方差分析,分别比较MRI与组织学定量参数的组间差异,Spearman相关性分析分别比较rADC与MVD、新生血管类型的相关性并计算相应的相关系数,P<0.05认为差异有统计学意义。
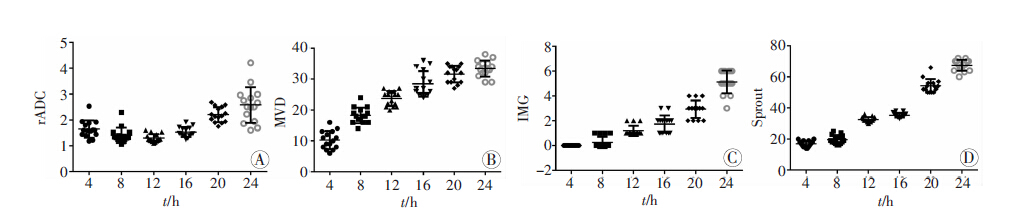
2 结果 2.1 大鼠C6胶质瘤磁共振成像特点30只荷瘤鼠常规T2加权MRI均显示为右侧基底节区类圆形高信号,肿瘤边界显示不清楚;随着移植时间的推移,肿瘤的体积越来越大,内部信号也越来越混杂,代表大片状坏死的T2WI低信号区亦开始出现并逐渐增大范围(图 1)。DWI显示肿瘤组织较对侧脑组织明显的弥散受限,表现为显著弥散高信号。定量测量肿瘤及对侧脑组织ADC并计算肿瘤组织rADC发现随着肿瘤的进展,rADC不断升高,伪彩图也相应越亮(图 2A)。

|
| 图 1 大鼠C6胶质瘤第8、16、24天MRI影像表现 |
|
| A:rADC值;B:MVD值;C:血管套叠情况;D:血管出芽情况 图 2 大鼠C6胶质瘤不同观察时间MR及组织学定量参数的变化 |
2.2 大鼠C6胶质瘤新生血管特点
采用Weidner的“Hotspot”方法计数并定量肿瘤组织MVD,发现C6胶质瘤新生血管密度异常丰富,MVD随着肿瘤的增长不断升高(图 2B)。HE染色显示,30只荷瘤鼠组织学表现均符合WHO高级别胶质瘤特征;CD34染色显示MVD随肿瘤的生长不断增大。进一步分析肿瘤组织中新生血管的类型,发现血管出芽(TNC)、血管套叠(CD34高倍镜)参与了C6胶质瘤血管新生的过程,是两种主要的新生血管类型( 图 3)。定量血管出芽及血管套叠各观察点的数量发现二者随肿瘤移植时间的延长亦不断升高(图 2C、D)。

|
| 图 3 大鼠C6胶质瘤组织学及新生血管观察 |
2.3 DWI与肿瘤新生血管相关性分析
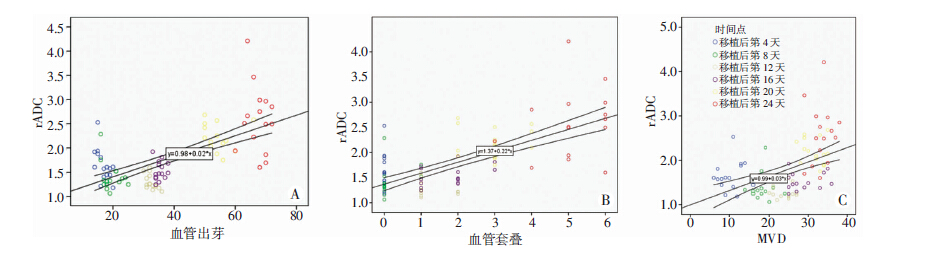
为了探讨DWI对肿瘤血管的检测能力,比较了各观察点内DWI定量参数rADC与MVD的相关性,发现两者均有较好相关性。同时非参数相关分析比较整个观察时间点rADC与MVD,二者亦表现出较好相关性(图 4A)。进一步探讨DWI对肿瘤新生血管类型的显示能力,比较了rADC与肿瘤新生血管类型的关系,发现rADC与血管出芽、血管套叠均表现出较好相关性(图 4B、C)。
|
| A:血管出芽;B:血管套叠;C:MVD 图 4 MR 定量参数与组织学指标相关性分析 |
3 讨论
胶质瘤是成人富血供的肿瘤之一,异常增殖的新生血管参与了肿瘤微环境的构筑 [11]。研究显示,胶质瘤新生血管与肿瘤级别有明显的相关性。无创在体显示肿瘤新生血管对肿瘤分级、分期、乃至临床预后的判断有巨大临床价值。本实验分析比较了弥散加权磁共振成像技术显示大鼠C6胶质瘤肿瘤新生血管的价值,发现DWI与活体荷瘤鼠不同观察时间点MVD有显著相关性,同时对新生血管类型亦有较好的预测价值,为DWI活体显示胶质瘤肿瘤新生血管提供了实验证据。
新生血管在供给肿瘤细胞养分的同时,也受到肿瘤细胞及其代谢产物直接或间接的影响。胶质瘤细胞在低氧环境下产生的VEGF形成了一个环路,VEGF可以刺激内皮细胞不断增殖、分化甚至极化形成新生的血管;相应地,这些新生血管的参与亦对肿瘤细胞的生物学行为、肿瘤的微环境产生了影响 [12]。研究证实,新生血管与肿瘤等级、药物敏感性、临床预后等有直接关联。长期以来肿瘤新生血管的检测依赖组织病理学的证据,MVD已经成为检测肿瘤新生血管的金标准。磁共振灌注成像技术可以无创、重复检测组织血管灌注状态,同时与MVD等组织新生血管指标具有良好相关性,因此越来越受到人们的关注。然而大量磁共振对比剂的运用可能给患者造成不同程度的对比剂不良反应,轻者局部组织水肿,重者可能会出现不良性肾小球纤维化 [13-14]。同时人工对比剂在患者体内的代谢方式存在不同的差异,对比剂可以在部分患者脑组织出现沉积,在引起信号“失真”的同时也留下了诱导产生对比剂不良反应的隐患。本实验证实不依赖对比剂的弥散加权磁共振成像技术与胶质瘤组织MVD及新生血管类型有较强的相关性,可以对胶质瘤组织新生血管进行成像。
DWI是唯一活体显示水分子扩散运动的磁共振技术,其信号变化反映了水分子的自由扩散程度。研究证实,组织中水分子扩散程度及微血管灌注直接影响DWI定量参数ADC值的变化 [15]。肿瘤组织细胞密度越大,水分子扩散越受限;微血管灌注越强,水分子扩散的距离越远,相应组织ADC值升高越明显。经证实体素内不相干运动(intravoxel incoherent motion,IVIM) DWI模型可以利用低b值(<200 s/mm2)将微血管中血液的流动模拟成水分子的扩散运动 [16]。Bai等通过比较高、低b值条件下(b=100 s/mm2、3 000 s/mm2)ADC的差异(ADC difference),将微血管灌注引起的DWI信号变化分离出来,发现ADC difference的最大值与宫颈癌组织MVD有较好相关性 [17]。本实验结果也表现出了相似的结果:C6胶质瘤各观察时间点rADC与相应组织MVD呈现显著正相关。
不同于结肠癌、肾透明细胞癌等其他富血供肿瘤,多种不同类型的血管参与了胶质瘤微血管的新生,已经阐述清楚的有血管出芽、血管套叠、血管共生、血管拟态、马赛克样血管生成以及肿瘤细胞转分化血管生成等 [18]。本次实验在C6胶质瘤组织中发现血管套叠、血管出芽等血管新生类型的存在,并且两者组织学定量与ADC有显著正相关。血管套叠与血管出芽均属于血管生成(angiogenesis),二者受到VEGF的直接调节。VEGF及其受体VEGFR的参与激活了Notch-DLL信号通路,该通路直接诱导内皮细胞特化成“柄细胞”和“尖细胞”,参与微血管的新生 [19]。针对VEGF及其受体VEGFR的抗血管生成药物延长了胶质瘤患者的无进展生存期,改善患者的生活质量。胶质瘤患者抗血管生成精准化治疗方案的制定需要实时、准确的检测出组织中血管新生类型。本次实验结果发现DWI与血管套叠及血管出芽等血管新生类型有较好相关性,提示DWI在制定胶质瘤患者抗血管生成治疗的个体化方案及疗效监测等领域可以提供更多地活体组织及新生血管相关的功能信息。
本次实验描述了C6胶质瘤组织肿瘤新生血管及DWI动态变化,验证了rADC值与MVD、血管套叠、血管出芽有显著正相关,证实了DWI可以活体显示肿瘤组织新生血管,为DWI实时定量进行肿瘤新生血管显像提供实验依据。
| [1] | Reardon D A, Wen P Y. Glioma in 2014: unravelling tumour heterogeneity-implications for therapy[J]. Nat Rev Clin Oncol,2015, 12 (2) : 69 –70. DOI:10.1038/nrclinonc.2014.223 |
| [2] | Soda Y, Myskiw C, Rommel A, et al. Mechanisms of neovascularization and resistance to anti-angiogenic therapies in glioblastoma multiforme[J]. J Mol Med (Berl),2013, 91 (4) : 439 –448. DOI:10.1007/s00109-013-1019-z |
| [3] | Li X, Zhu Y, Kang H, et al. Glioma grading by microvascular permeability parameters derived from dynamic contrast-enhanced MRI and intratumoral susceptibility signal on susceptibility weighted imaging[J]. Cancer Imaging,2015, 15 (1) : 1 –9. DOI:10.1186/s40644-015-0039-z |
| [4] | Kang H Y, Xiao H L, Chen J H, et al. Comparison of the Effect of Vessel Size Imaging and Cerebral Blood Volume Derived from Perfusion MR Imaging on Glioma Grading[J]. AJNR Am J Neuroradiol,2016, 37 (1) : 51 –57. DOI:10.3174/ajnr.A4477 |
| [5] | 黄杰, 李晓光, 康厚艺, 等. DSC-MRI和DCE-MRI定量分析在脑胶质瘤分级诊断中的应用[J]. 第三军医大学学报,2015, 37 (7) : 672 –677. DOI:10.16016/j.1000-5404.201410173 |
| [6] | McDonald R J, McDonald J S, Kallmes D F, et al. Intracranial Gadolinium Deposition after Contrast-enhanced MR Imaging[J]. Radiology,2015, 275 (3) : 772 –782. DOI:10.1148/radiol.15150025 |
| [7] | Surov A, Gottschling S, Mawrin C, et al. Diffusion-Weighted Imaging in Meningioma: Prediction of Tumor Grade and Association with Histopathological Parameters[J]. Transl Oncol,2015, 8 (6) : 517 –523. DOI:10.1016/j.tranon.2015.11.012 |
| [8] | Xiao H F, Chen Z Y, Lou X, et al. Astrocytic tumour grading: a comparative study of three-dimensional pseudocontinuous arterial spin labelling, dynamic susceptibility contrast-enhanced perfusion-weighted imaging, and diffusion-weighted imaging[J]. Eur Radiol,2015, 25 (12) : 3423 –3430. DOI:10.1007/s00330-015-3768-2 |
| [9] | Lee E Y, Hui E S, Chan K K, et al. Relationship between intravoxel incoherent motion diffusion-weighted MRI and dynamic contrast-enhanced MRI in tissue perfusion of cervical cancers[J]. J Magn Reson Imaging,2015, 42 (2) : 454 –459. DOI:10.1002/jmri.24808 |
| [10] | Zhou Y, Liu J, Liu C, et al. Intravoxel incoherent motion diffusion weighted MRI of cervical cancer—Correlated with tumor differentiation and perfusion[J]. Magn Reson Imaging,2016, 34 (8) : 1050 –1056. DOI:10.1016/j.mri.2016.04.009 |
| [11] | Xia S, Lal B, Tung B, et al. Tumor microenvironment tenascin-C promotes glioblastoma invasion and negatively regulates tumor proliferation[J]. Neuro Oncol,2015, 18 (4) : 507 –517. DOI:10.1093/neuonc/nov171 |
| [12] | Xu R, Shimizu F, Hovinga K, et al. Molecular and Clinical Effects of Notch Inhibition in Glioma Patients: A Phase 0/I Trial[J]. Clin Cancer Res,2016, 22 (19) : 4786 –4796. DOI:10.1158/1078-0432.CCR-16-0048 |
| [13] | He A, Kwatra S G, Zampella J G, et al. Nephrogenic systemic fibrosis: fibrotic plaques and contracture following exposure to gadolinium-based contrast media[J]. BMJ Case Rep,2016, 22 (19) : 4786 –4796. DOI:10.1136/bcr-2016-214927 |
| [14] | Soulez G, Bloomgarden D C, Rofsky N M, et al. Prospective Cohort Study of Nephrogenic Systemic Fibrosis in Patients With Stage 3-5 Chronic Kidney Disease Undergoing MRI With Injected Gadobenate Dimeglumine or Gadoteridol[J]. AJR Am J Roentgenol,2015, 205 (3) : 469 –478. DOI:10.2214/AJR.14.14268 |
| [15] | Jin N, Deng J, Zhang L, et al. Targeted single-shot methods for diffusion-weighted imaging in the kidneys[J]. J Magn Reson Imaging,2011, 33 (6) : 1517 –1525. DOI:10.1002/jmri.22556 |
| [16] | Suzuki K, Igarashi H, Watanabe M, et al. Separation of perfusion signals from diffusion-weighted image series enabled by independent component analysis[J]. J Neuroimaging,2011, 21 (4) : 384 –394. DOI:10.1111/j.1552-6569.2010.00514.x |
| [17] | Liu Y, Ye Z, Sun H, et al. Grading of uterine cervical cancer by using the ADC difference value and its correlation with microvascular density and vascular endothelial growth factor[J]. Eur Radiol,2013, 23 (3) : 757 –765. DOI:10.1007/s00330-012-2657-1 |
| [18] | Jain R K, Carmeliet P. SnapShot: Tumor angiogenesis[J]. Cell,2012, 149 (6) : 1408 –1408. DOI:10.1016/j.cell.2012.05.025 |
| [19] | Yahyanejad S, King H, Iglesias V S, et al. NOTCH blockade combined with radiation therapy and temozolomide prolongs survival of orthotopic glioblastoma[J]. Oncotarget, 2016. [Epub ahead of print],2016 . DOI:10.18632/oncotarget.9275 |



