2. 610041 成都,四川大学华西医院放射科
2. Department of Radiology, West China Hospital of Sichuan University, Chengdu, Sichuan Province, 610041, China
脑胶质瘤与脑炎是发病率较高的中枢神经系统疾病。这两类疾病在临床症状、体征及常规辅助检查存在部分重叠,甚至于常规头部影像学检查亦不易区分,误诊率极高。由于对脑胶质瘤与脑炎的治疗方法和措施迥异,因而病变的定性对于治疗方案的制定和选择具有至关重要的意义。CT功能成像如CT灌注成像(CT perfusion imaging,CTP),磁共振功能成像如扩散加权成像(diffusion weighted imaging,DWI)、扩散张量成像(diffusion tensor imaging,DTI)、灌注加权成像(perfusion weighted imaging,PWI)、磁共振波谱成像(proton MR spectroscopy,H-MRS)、动脉自旋标记成像(arterial spin labeling,ASL)等技术在大脑病变的定性诊断、肿瘤复发等方面的研究已经取得一定进展和较为广泛的应用 [1]。而BOLD-fMRI技术在临床的研究和应用,目前仍主要集中在脑功能区的定位和显示,脑功能区及其附近肿瘤性病变对脑功能区的影响,保留脑功能区的肿瘤全切,疾病预后判断,以及神经环路、静息态脑神经功能 [2-3]等方面的研究,而运用功能磁共振静息态fMRI-BOLD信号改变,如进行ALFF(amplitude of low-frequencyfluctuation,ALFF)值的测量,进行脑内病变的定性诊断却鲜有报道。因此,本研究纳入脑胶质瘤30例、脑炎30例及40名志愿者,进行BOLD-fMRI静息态低频振荡振幅ALFF值测量和统计分析,探讨BOLD技术在脑胶质瘤与脑炎的诊断与鉴别诊断的潜在价值。
1 材料与方法 1.1 研究对象对于常规T1平扫、T1增强和T2平扫、T2-FLAIR序列进行检查,预览发现单侧大脑实质异常信号病变,拟诊断为脑胶质瘤或脑炎,在获得患者知情同意的情况下,使用3D-T1和SE-EPI序列采集高分辨率结构图像及BOLD-fMRI图像,然后进行术后病理、临床辅助检查以及治疗后随访复查的追踪。收集2014年8月至2016年5月西藏自治区人民政府驻成都办事处医院收治的脑胶质瘤、脑炎患者。纳入标准:①出现神经系统症状与体征。②单侧大脑实质异常信号病变。③对侧大脑实质形态、结构、信号正常。④胶质瘤患者经手术病理证实,脑炎患者经手术病理、临床辅助检查或抗炎治疗后复查等方式证实。排除标准:①双侧大脑实质出现异常信号病变。②中线结构明显移位,导致对侧大脑实质形态、结构、信号改变。③诊断结果未经术后病理、临床辅助检查或抗炎治疗后复查证实。
共收集患者60例,其中男36例,女24例,年龄 19~82(47.6±3.4)岁。脑胶质瘤30例,其中12例经活检后病理诊断,18例经开颅手术病灶切除后病理诊断证实;一、二级胶质瘤21例,三级胶质瘤6例,四级胶质瘤3例。脑炎30例,其中7例经活检后病理诊断证实,18例经临床表现、体征结合血常规、脑脊液常规和生化检查以及C反应蛋白等临床辅助检查综合诊断,5例经诊断性抗炎治疗后复查等方式证实;其中细菌感染(脑脓肿)4例,脑结核8例,寄生虫感染6例,病毒性脑炎5例,非感染性脑炎7例。临床表现为头痛48例,头痛伴呕吐11例,头痛伴视物模糊6例,癫痫6例,运动障碍16例。
另征集同期40名志愿者作为正常对照,与患者种族、性别、年龄进行匹配。志愿者纳入标准:①无神经系统症状与体征。②大脑实质形态、结构、信号正常。③血常规正常。④与患者种族、性别、年龄相匹配。
1.2 研究方法本研究采用前瞻性病例-对照研究,分别测量脑胶质瘤与脑炎患者的患侧、健侧ALFF值,设置为胶质瘤患侧组(ipsilateral glioma group,IGG)、胶质瘤健侧组(contralateral glioma group,CGG)、脑炎患侧组(ipsilateral encephalitis group,IEG)、脑炎健侧组(contralateral encephalitis group,CEG),从40个正常对照分别选取30个与胶质瘤患者、脑炎患者的种族、性别、年龄配对的被试进行病变相应区域的ALFF值测量,组成胶质瘤的正常对照组(corresponding areas of glioma in healthy control group,CAGHCG)和脑炎的正常对照组(corresponding areas of encephalitis in healthy control group,CAEHCG)。进行统计分析时,为了尽量减轻患者种族、性别、年龄、个体差异以及正常生理活动诸如呼吸、心跳等干扰因素对测量结果的影响,增加了脑胶质瘤、脑炎的患侧和健侧ALFF值的差与患侧ALFF值的比值[(IGG-CGG)/IGG]、[(IEG-CEG)/IEG]作为统计分析参数。
1.3 检查方法与数据采集磁共振设备为PHLIPS公司3.0T MRI机,使用头部8通道线圈,所有被试带隔音耳塞,由海绵垫固定头部,采集BOLD信号。扫描参数如下:采用SE-EPI序列,b=1 000 s/mm2,TR 2 000 ms,TE 30 ms,视野240×240(3),层厚3.75 mm,层间距0 mm,激励次数2。
1.4 数据预处理首先将BOLD-fMRI所采集的图像原始数据进行时间层校正,空间标准化和头动校正,对未超出头动校正标准(三维平移<1 mm,三维旋转度<1°)的数据进行数据测量和分析。采用DPARSF软件对ALFF进行计算,具体的计算步骤如下:①在经过rfMRI原始数据的预处理之后,对图像中每个体素的时间序列进行带通滤波(bandpass filtered),其频率在0.01~0.08Hz,研究表明此频率范围内的信号可以去除低频漂移和呼吸、心跳等产生的高频噪声。②然后采用傅立叶转换(fast Fourier transform,FFT)将滤波后的时间序列转换到频域范围,计算并得到信号在0.01~0.08 Hz下的功率谱。③由于信号在某一频率范围内的能量与该时间序列的信号功率谱幅度的平方成正比,将由FFT得到的能量谱开平方,然后平均到0.01~0.08 Hz,从而得到每个体素的低频振荡振幅,即ALFF值。
1.5 统计学分析采用SPSS 17.0统计软件,各组ALFF测量值比较应用秩和检验;应用受试者工作特征(receiver operator characteristic curve,ROC)曲线计算各组ALFF值的组间曲线下面积(area under the curve,AUC)、诊断阈值、灵敏度、特异度。以P<0.05为差异有统计学意义。
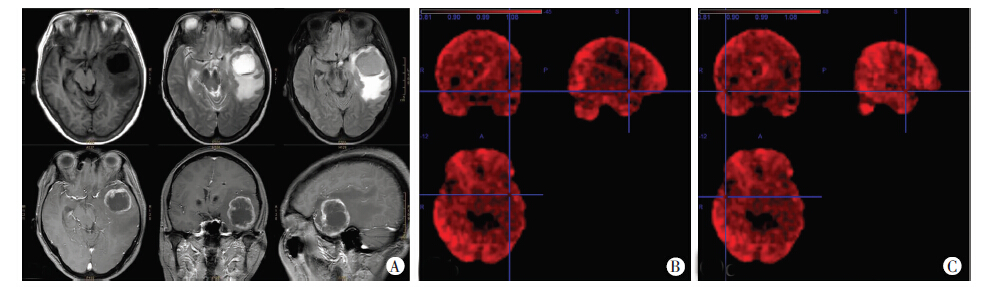
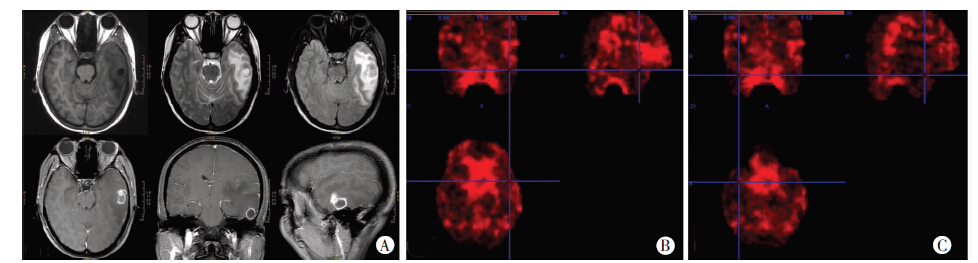
2 结果 2.1 ALFF值的测量将预处理后的数据导入工具MRIcroN,进行脑胶质瘤、脑炎的患侧病变区域、健侧对应区域和正常对照相应区域的ALFF值测量。为了保证患侧测量区为病变的有效活性成分区域,需要结合、对照常规检查 T1WI 增强序列图像,选择病变内增强后强化的实性区域为测量目标区域;健侧则选择病变对应区域的脑实质进行测量;正常对照则选择对应病变所在解剖结构区域进行测量。测量时需要注意避开坏死囊变区、水肿区、出血灶及钙化灶,避开脑室、脑池、脑沟及大血管,还需要避开颅底、鼻窦及头皮等。每个测量目标区域分别选取6个测量点进行测量,取其平均值作为该区域的ALFF测量值(图 1、2)。
|
| A:左侧颞叶类圆形长T1长T2信号,T2FLAIR序列为稍高信号,外周大片状水肿灶 上排从左到右为T1WI、T2WI、T2FLAIR图像,下排从左到右为T1WI增强的轴位、冠状位、矢状位图像,示病灶明显环状强化,壁厚薄不均,并多发强化壁结节;B:在左侧颞叶病变强化区域进行ALFF值测量 上左为冠状位,上右为矢状位,下为轴位图像;C:在右侧颞叶与病变对应区域脑实质进行ALFF值测量 上左为冠状位,上右为矢状位,下为轴位图像 图 1 左侧颞叶脑胶质瘤的常规MRI图像及患侧与健侧ALFF值测量图 |
|
| A:左侧颞叶类圆形等长T1等长T2信号,T2FLAIR序列为稍高、稍低信号,外周大片状水肿灶 上排从左到右为T1WI、T2WI、T2FLAIR图像;下排从左到右依次为T1WI增强的轴位、冠状位、矢状位图像,示病灶明显多发环状强化,病灶内前份局部结节状强化;B:在左侧颞叶病变强化区域进行ALFF值测量 上左为冠状位,上右为矢状位,下为轴位图像;C:在右侧颞叶与病变对应区域脑实质进行ALFF值测量 上左为冠状位,上右为矢状位,下左为轴位图像 图 2 左侧颞叶脑炎的常规MRI图像及患侧与健侧ALFF值测量图 |
2.2 各组ALFF测量值
结果见表 1。胶质瘤患侧(IGG)与胶质瘤健侧(CGG)、胶质瘤患侧(IGG)与胶质瘤正常对照(CAGHCG)的ALFF值组间差异均具有统计学意义(P<0.01)。脑炎患侧(IEG)与脑炎健侧(CEG)、正常对照(CAEHCG)的ALFF值组间差异无统计学意义(P>0.05)。IGG与IEG的ALFF测量值组间差异具有统计学意义(P<0.01);(IGG-CGG)/IGG与(IEG-CEG)/IEG组间差异也具有统计学意义(P<0.01)。
| 组别 | 患侧 | 健侧 | 对照 | (患侧-健侧)/患侧 |
| 脑胶质瘤 | 0.969 8±0.012 3a | 1.041 4±0.002 3 | 1.049 2±0.004 6 | -0.079 3±0.015 0 |
| 脑炎 | 1.043 8±0.001 7 | 1.049 2±0.004 2 | 1.041 4±0.004 1 | -0.005 4±0.003 5 |
| Z值 | -6.568 | -2.286 | -1.539 | -5.337 |
| P值 | <0.01 | 0.022 | 0.124 | <0.01 |
| a: P<0.01,与胶质瘤健侧(CGG)、胶质瘤正常对照(CAGHCG)比较 | ||||
2.3 ALFF测量值对IGG与CGG、IGG与IEG、IEG与CEG组间诊断效能
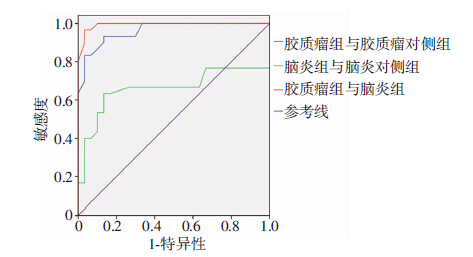
结果见图 3。由ROC曲线可知,IGG与CGG的ROC曲线下面积为0.962,诊断阈值为1.024,灵敏度0.933,特异度0.867。IEG与CEG的ROC曲线下面积为0.661,诊断阈值为1.051,灵敏度0.633,特异度0.867。IGG与IEG的ROC曲线下面积为0.993,诊断阈值为1.032,灵敏度0.967,特异度0.967。
|
| 图 3 胶质瘤患侧与健侧、脑炎患侧与健侧、胶质瘤患侧与脑炎患侧组间诊断效能比较ROC曲线 |
2.4 IGG与CGG、IEG与CEG、IGG与IEG的ALFF测量值的诊断范围
结合IGG与CGG诊断阈值为1.024,IGG与IEG诊断阈值为1.032,得出IGG的ALFF测量值<1.024,1.024<IEG的ALFF测量值<1.032,即IGG<IEG。而IEG与CEG没有组间差异,且ROC曲线下面积<0.7,组间诊断效能低下,因而脑炎的ALFF值测量不能与对侧及正常对照区别。
3 讨论静息态功能磁共振BOLD-fMRI低频振幅技术探测大脑自发活动产生的BOLD信号,可反映局部脑活动强度 [4]。这种技术采用一个低频频段(0.01~ 0.08 Hz)内所有频点上幅值的平均值来代表一个体素自发神经元活动的强弱,从能量的角度反应各个神经元体素在静息状态下自发活动水平的高低,进行量化测量即得到ALFF测量值。
3.1 脑胶质瘤患侧的ALFF值减低,提示脑胶质瘤的BOLD信号降低本研究结果显示,IGG与CGG、IGG与CAGHCG的ALFF值组间差异具有统计学意义,(IGG-CGG)/IGG与(IEG-CEG)/IEG组间差异亦具有统计学意义,脑胶质瘤患侧的ALFF测量值比健侧和正常对照均减低,即脑胶质瘤病变的BOLD信号降低。Holodny等 [5-6]及Cui等 [7]认为多形性胶质母细胞瘤造成的BOLD-fMRI信号降低与肿瘤的占位效应相关,而另有研究认为该结果更多的与肿瘤的生物学相关因素如肿瘤的血容量、瘤内毛细血管密度、肿瘤摄氧指数以及瘤内动静脉分流有关 [8]。Ludemann等 [9]认为肿瘤平均BOLD-fMRI信号改变与肿瘤内血容量有关,肿瘤周围BOLD-fMRI信号下降是由于肿瘤盗血现象引起瘤周低灌注所致。Holodny等 [6]发现胶质瘤或非胶质瘤均可引起BOLD-fMRI信号降低,在胶质母细胞瘤更明显,因而认为肿瘤血管系统的调节功能异常和引流静脉回流障碍是BOLD-fMRI信号减低的主要原因。Schreiber等 [10]观察到在胶质瘤周围BOLD-fMRI信号下降,而在非胶质瘤周围BOLD-fMRI信号未受明显影响,因而将胶质瘤的侵袭性和产生神经递质归结为造成BOLD-fMRI信号降低的主要原因。Chen等 [11]认为,对于Ⅰ、Ⅱ级胶质瘤,老年人由于年龄增长导致血管壁弹性降低,脑血管系统对神经系统刺激的反应性下降,因而BOLD-fMRI信号随着年龄增长降低,年龄成为主导因素;而对于Ⅲ级胶质瘤,则因为高级别肿瘤的异常新生血管对脑血管系统刺激不敏感,导致BOLD-fMRI信号减低,因而BOLD-fMRI信号与肿瘤分级相关。
也有研究 [12]认为颅脑肿瘤导致局部神经功能紊乱的方式分两种:一种是肿瘤占位效应推挤血管使其暂时性失去血液供应造成的生理性供血障碍,流经功能区血流量减少 [13],静脉回流障碍,造成脱氧血红蛋白浓度的差异程度发生变化,被激活的脑功能区体积减小,BOLD-fMRI信号降低。另一种是肿瘤侵犯神经组织,发生破坏性解剖性供血障碍,并诱导异常肿瘤血管生成,改变肿瘤周围生物化学环境 [10],产生血管性水肿,分泌神经递质,改变皮层代谢状态及神经血管结合状态,或者肿瘤异常新生血管丧失自我调节功能,导致功能区激活体积减小,BOLD-fMRI信号降低。
本研究认为,人体细胞发生基因变异,大量的肿瘤细胞快速增多,在有限的空间内形成排列密集、紊乱的瘤巢,必然导致氧气和养分严重供应不足,形成一个高度缺血乏氧的微环境,尤其在病变中心区域,病变范围微循环中脱氧血红蛋白的浓度比例增高,造成静息态BOLD信号减低,ALFF测量值减低。高度缺血乏氧的微环境一方面造成部分肿瘤细胞出现坏死 [14],另一方面刺激肿瘤细胞产生促血管生成素,通过内皮依赖性血管、马赛克血管及血管生成拟态等多种方式 [15],促进肿瘤血管生成 [16],而且发育成熟的正常血管和发育不成熟的异质性肿瘤血管的构成比例处于不断变化中 [17]。这些不成熟的肿瘤血管在结构和功能上具有高度的异质性,致病变外周代谢旺盛与中心区域缺血缺氧、酸中毒等并存 [18],其管壁缺乏血管周细胞及平滑肌细胞,对氧的缩血管效应和二氧化碳的舒血管效应均不敏感 [19],丧失自我调节功能,肿瘤内微循环的血容量、血流量及氧合血红蛋白与脱氧血红蛋白的浓度比例不能及时调整、变化,造成BOLD信号减低。脑肿瘤的占位效应,以及对周围脑组织结构、生理学状态、脑组织代谢、神经递质传递和神经血管结合状态产生影响,诱导周围脑组织血管病理性增生,引起血管性水肿等因素,导致毛细血管数量减少和血流量减少,从而降低了肿瘤微循环中氧合血红蛋白浓度,脱氧血红蛋白浓度相对升高,造成BOLD信号减低 [12]。
3.2 脑炎的BOLD信号没有明显变化本研究结果显示IEG与CEG的ALFF值没有组间差异,脑炎的BOLD信号没有明显变化。脑炎的病理基础以脑组织及脑膜充血肿胀、血管扩张、炎性渗出和肉芽组织增生为主 [20],可生成增多、增粗的新生毛细血管网,其细胞结构组成与排列分布相对正常,血管结构与功能以及病变区域血液供应和血管自我调节能力与正常脑实质相似,仅仅表现为病变区域细胞肿胀,血管网密集、扩张,血液供应更丰富,血容量、血流量虽然有所增加,但其血液中氧合血红蛋白与脱氧血红蛋白的浓度比例没有发生明显变化,因而BOLD信号没有明显变化。
3.3 ALFF测量值对胶质瘤、脑炎的诊断与鉴别诊断的效能及意义本研究中IGG与IEG、IGG与CGG、(IGG-CGG)/IGG与(IEG-CEG)/IEG具有组间差异,IGG与IEG、IGG与CGG的ROC曲线下面积很大,分别为0.993和0.962,说明ALFF值对脑胶质瘤与脑炎的鉴别诊断效能很高,对胶质瘤的诊断效能亦较高。而IEG与CEG没有组间差异,ROC曲线下面积<0.7,因而ALFF测量值对脑炎的诊断效能低下,不能与健侧及正常对照区别。胶质瘤ALFF值减低是由于肿瘤细胞堆积、肿瘤血管的异质性,以及神经血管结合状态异常、肿瘤占位等因素,造成病变区域脱氧血红蛋白浓度比例相对升高,BOLD信号减低。脑炎患侧ALFF值与健侧、正常对照没有差异,是因为脑实质炎症所造成的炎性肿胀、渗出与肉芽肿增生,虽然引起病变血流量、血容量的增加,但其血管床的氧合血红蛋白、脱氧血红蛋白浓度比例没有改变,故BOLD信号无明显差异。
3.4 本研究的局限性与展望ALFF测量值对胶质瘤的诊断、胶质瘤与脑炎的筛查和区分具有一定的临床应用价值。然而,胶质瘤及脑炎造成ALFF测量值改变的具体病理生理学机制尚不清楚,未来结合更多的脑影像指标,如血流,灌注以及波谱信息,有望能进一步揭示其潜在机制。结合常规磁共振检查序列,MRI多模态检查方式,以及翔实的临床病史、辅助检查等,进行全面、客观的综合分析,才能相对准确的进行胶质瘤与炎症的诊断和鉴别诊断。同时由于胶质瘤、脑炎的异质性较大,对于脑胶质瘤的分级 [21-23]以及对炎性病变的病因分析等更深层次的探讨,则有待于收集更多的病案数据、病种细化,作进一步分层研究。
| [1] | Lagaru A, Mosci C, Mittra E, et al. Glioblastoma Multiforme Recurrence: An Exploratory Study of 18F FPPRGD2 PET/CT[J]. Radiology,2015, 277 (2) : 497 –506. DOI:10.1148/radiol.2015141550 |
| [2] | Luo S, Qi R F, Wen J Q, et al. Abnormal Intrinsic Brain Activity Patterns in Patients with End-Stage Renal Disease Undergoing Peritoneal Dialysis: A Resting-State Functional MR Imaging Study[J]. Radiology,2016, 278 (1) : 181 –189. DOI:10.1148/radiol.2015141913 |
| [3] | Zhang L J, Wen J, Liang X, et al. Brain Default Mode Network Changes after Renal Transplantation: A Diffusion-Tensor Imaging and Resting-State Functional MR Imaging Study[J]. Radiology,2016, 278 (2) : 485 –495. DOI:10.1148/radiol.2015150004 |
| [4] | Auer D P. Spontaneous low-frequency blood oxygenation level-dependent fluctuations and functional connectivity analysis of the 'resting' brain[J]. Magn Reson Imaging,2008, 26 (7) : 1055 –1064. DOI:10.1016/j.mri.2008.05.008 |
| [5] | Holodny A I, Schulder M, Liu W C, et al. Decreased BOLD functional MR activation of the motor and sensory cortices adjacent to a glioblastoma multiforme: implications for image-guided neurosurgery[J]. AJNR Am J Neuroradiol,1999, 20 (4) : 609 –612. |
| [6] | Holodny A I, Schulder M, Liu W C, et al. The effect of brain tumors on BOLD functional MR imaging activation in the adjacent motor cortex: implications for image-guided neurosrugery[J]. AJNR Am J Neuroradiol,2000, 21 (8) : 1415 –1422. |
| [7] | Cui Y, Tha K K, Terasaka S, et al. Prognostic Imaging Biomarkers in Glioblastoma: Development and Independent Validation on the Basis of Multiregion and Quantitative Analysis of MR Images[J]. Radiology,2016, 278 (2) : 546 –553. DOI:10.1148/radiol.2015150358 |
| [8] | 肖炳祥. BOLD-fMRI在脑肿瘤临床应用中的研究进展[J]. 中国临床神经外科杂志,2010, 15 (4) : 211 –214. DOI:10.3969/j.issn.1009-153X.2010.04.007 |
| [9] | Ludemann L, Forschler A, Grieger W, et al. BOLD signal in the motor cortex shows a correlation with the blood volume of brain tumors[J]. Magn Reson Imaging,2006, 23 (4) : 435 –443. DOI:10.1002/jmri.20530 |
| [10] | Schreiber A, Hubbe U, Ziyeh S, et al. The influence of gliomas and nonglica space-occupying lesions on blood-oxygen-level-dependent contrast enhancement[J]. AJNR Am J Neuroradiol,2000, 21 (6) : 1055 –1063. |
| [11] | Chen C M, Hou B L, Holodny A I. Effect of age and tumor grade on BOLD functional MR imaging in preoperative assessment of patients with glioma[J]. Radiology,2008, 248 (3) : 971 –978. DOI:10.1148/radiol.2483071280 |
| [12] | 刘浩, 林青, 徐文坚, 等. 血氧水平依赖功能磁共振成像评价脑肿瘤恶性程度与脑皮层功能区距离和激活体积的相关性[J]. 中国医学影像学杂志,2012, 20 (2) : 97 –102. DOI:10.3969/j.issn.1005-5185.2012.02.007 |
| [13] | Krings T, Topper R, Willmes K, et al. Activation in primary and secondary motor areas in patients with CNS neoplasms and weakness[J]. Neurology,2002, 58 (3) : 381 –390. DOI:10.1212/WNL.58.3.381 |
| [14] | Colen R R, Wang J, Singh S K, et al. Glioblastoma: Imaging Genomic Mapping Reveals Sex-specific Oncogenic Associations of Cell Death[J]. Radiology,2015, 275 (1) : 215 –227. DOI:10.1148/radiol.14141800 |
| [15] | 乐晓峰, 孙彬佳, 郭斯翊, 等. 血管生成拟态在肿瘤研究中的现状与展望[J]. 现代肿瘤医学,2014, 22 (9) : 2204 –2208. DOI:10.3969/j.issn.1672-4992.2014.09.64 |
| [16] | Louis Gagnon, Sava Sakadzilc, Frédéric Lesage, et al. Quantifying the Microvascular Origin of BOLD-fMRI from First Principles with Two-Photon Microscopy and an Oxygen-Sensitive Nanoprobe[J]. J Neurosci,2015, 35 (8) : 3663 –3675. DOI:10.1523/JNEUROSCI.3555-14.2015 |
| [17] | 何慧瑾, 冯晓源. 重视MRI新技术在脑肿瘤诊断中的合理应用[J]. 磁共振成像,2012, 3 (1) : 4 –7. DOI:10.3969/j.issn.1674-8034.2012.01.002 |
| [18] | 陈波. 肿瘤血管生成的影像学评价[J]. 医学研究生报,2011, 24 (2) : 196 –202. DOI:10.3969/j.issn.1008-8199.2011.02.021 |
| [19] | 刘丽. 肿瘤血管生成的影像学评价及新进展[J]. 医学研究生报,2012, 25 (10) : 1102 –1108. DOI:10.3969/j.issn.1008-8199.2012.10.025 |
| [20] | 冯少仁, 刘国辉, 邹国荣, 等. 肿瘤样脑炎的MRI表现分析[J]. 放射学实践,2012, 27 (7) : 739 –741. DOI:10.3969/j.issn.1000-0313.2012.07.009 |
| [21] | Sui Y, Wang H, Liu G, et al. Differentiation of Low-and High-Grade Pediatric Brain Tumors with High b-Value Diffusion-weighted MR Imaging and a Fractional Order Calculus Model[J]. Radiology,2015, 277 (2) : 489 –496. DOI:10.1148/radiol.2015142156 |
| [22] | Bai Y, Lin Y, Tian J, et al. Grading of Gliomas by Using Monoexponential, Biexponential, and Stretched Exponential Diffusion-weighted MR Imaging and Diffusion Kurtosis MR Imaging[J]. Radiology,2016, 278 (2) : 496 –504. DOI:10.1148/radiol.2015142173 |
| [23] | Park J E, Kim H S, Park K J, et al. Pre-and Posttreatment Glioma: Comparison of Amide Proton Transfer Imaging with MR Spectroscopy for Biomarkers of Tumor Proliferation[J]. Radiology,2016, 278 (2) : 514 –523. DOI:10.1148/radiol.2015142979 |



