2. 730030 兰州, 甘肃省人民医院西院消化科 ;
3. 730030 兰州, 甘肃省消化系肿瘤重点实验室
2. Department of Gastroenterology, West Branch of Gansu Provincial People's Hospital, Lanzhou, Gansu Province, 730030, China ;
3. Key Laboratory of Digestive Tumors of Gansu Province, Lanzhou, Gansu Province, 730030, China
炎症性肠病(inflammatory bowel disease,IBD)是一种病因未明的累积胃肠道的慢性非特异性炎症疾病,主要包括了克罗恩病(Crohns disease,CD)和溃疡性结肠炎(ulcerative colitis,UC),在我国发病率逐年提升。由于其发病机制仍不清楚 ,可能与免疫、遗传、感染及精神因素有关 [1],目前尚缺少有效地治疗药物。因此,临床仍致力于开发安全高效的新药物。
中药或天然产物因安全性高、副作用小,一直是当前IBD研究的热点。二氢杨梅素(dihydromyricelin,DHM)又称蛇葡萄素,是一种二氢黄酮醇类黄酮化合物。其广泛存在于蛇葡萄科蛇葡萄属植物中,在藤茶中的量可以达到30%[2]。近年来,药理实验研究证实二氢杨梅素具有抗自由基、抗氧化、抗肿瘤、广谱抗菌、解酒保肝及降低血糖 、血脂等多方面的药理作用。新近的研究显示二氢杨梅素还可以抑制核因子κB(nuclear factor κβ,NF-κB)的活性。
本实验以4%葡聚糖硫酸钠(dextran sulfate salt,DSS)诱导小鼠急性溃疡性结肠炎模型,通过给予不同剂量的DHM灌胃治疗,并与治疗溃疡性结肠炎传统药物5-氨基水杨酸(5-aminosalicylic acid,5-ASA)做对照,观察结肠炎小鼠的一般情况、结肠长度、病理损伤程度,肠组织中Toll样受体(Toll-like receptor,TLR)2、TLR4、NF-κB的表达,炎性因子如IL-1β、TNF-α、IL-6水平,以及肠组织中髓过氧化物酶(myeloperoxidase,MPO)、一氧化氮(nitric oxide,NO)及超氧化物歧化酶(superoxide dismutase,SOD)的变化,探讨DHM对小鼠溃疡性结肠炎的作用及可能机制。
1 材料与方法 1.1 动物SPF级BALB/c雌鼠60只,体质量17~22 g,8周龄,购于中国农业科学院兰州兽医研究所。
1.2 药物二氢杨梅素(批号:MUST-15010908),由成都曼斯特生物科技有限公司提供;葡聚糖硫酸钠(DSS)由Sigma公司提供;5-氨基水杨酸 (美沙拉嗪肠溶片)由葵花药业集团佳木斯鹿灵制药有限公司生产。
1.3 主要试剂Anti-TLR2、Anti-TLR4由艾博抗(上海)贸易有限公司提供;IL-1β、TNF-α、IL-6检测ELISA试剂盒由武汉博士德生物工程有限公司提供。 MPO、NO、SOD检测ELISA试剂盒由南京建成科技有限公司提供;NF-κB 非放射性EMSA检测试剂盒由微奥基因科技常州有限公司提供。
1.4 UC模型的建立与处理小鼠采用随机数字表法分为6组:正常组,模型组,DHM低剂量组[50 mg/(kg·d)]、中剂量组[100 mg/(kg·d)]、高剂量组[200 mg/(kg·d)]及5-氨基水杨酸组[50 mg/(kg·d)],每组10只小鼠。分组当日给予正常组小鼠蒸馏水自行饮用,其余组小鼠给予4%DSS水溶液自行饮用(记为第1天),连续饮用7 d。于饮用4%DSS水溶液当日开始,对DHM低、中、高剂量组及5-氨基水杨酸组按各组拟定剂量分别进行灌胃治疗,连续给药14 d后采用颈椎脱位法处死小鼠,游离结肠及远端回肠,取出肛门至盲肠末端的整个结肠和直肠段,对其进行肉眼观察,并测量长度。摘取小鼠脾脏称量。以PBS溶液将小鼠结肠内容物及管壁冲洗干净,于病变部位取材,置于4%多聚甲醛溶液中固定,留待进行常规石蜡包埋切片,HE染色。剩余肠段封存于EP管中,迅速转移到-80 ℃冰箱中冷冻保存,留待下一步提取肠组织蛋白。
1.5 疾病活动指数每日对各组小鼠进行体质量测量,观察小鼠的活动、毛色、精神状态以及大便性状、颜色等。参照文献[4],结合小鼠体质量下降百分率(体质量不变为0,1~5 为1分,6~10为2分,11~15为3分,大于15为4分)、大便黏稠度(正常为0,松散的大便为2分,腹泻为4分)和便血(正常0分,隐血阳性为2分,显性出血为4分)3种情况进行疾病活动指数(disease activity index,DAI)评分,即DAI=(体质量指数+大便形状+出血情况)/3。
1.6 光镜下病理组织学观察小鼠结肠组织病理切片观察用常规HE染色法。光镜下观察结肠组织损伤情况,结肠病灶病理组织显微镜检查并评分(CMDI),评分标准如下,①溃疡,0-无,1-小溃疡(<3 mm),2-大溃疡(>3 mm); ②炎症0-无,1-轻度,2-重度; ③肉芽组织:0-无,1-有; ④病变深度:0-无,1-黏膜下层,2-肌层,3-浆膜层; ⑤纤维化:0-无,1-轻度,2-重度,各项相加即为总分。
1.7 脾脏指数根据公式计算:脾脏指数(mg/g)=脾脏质量/小鼠体质量。
1.8 ELISA检测用ELISA测定DHM治疗前后肠组织细胞因子IL-1β、TNF-α、IL-6含量以及治疗前后肠组织MPO、NO、SOD的活性变化,分别按照相应的ELISA试剂盒说明书进行测定。
1.9 EMSA检测用非放射性EMSA测定通用试剂盒检测治疗前后肠组织NF-κB的活性。
1.10 Western blot检测采用Western blot检测DHM治疗前后肠组织TLR2、TLR4含量的表达。
1.11 统计学分析采用SPSS 19.0统计软件。正态分布计量资料数据以x±s表示,两组间均数比较采用t检验。P<0.05为差异有统计学意义。
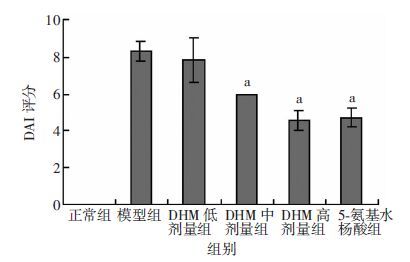
2 结果 2.1 小鼠DAI结果统计结果显示,除正常组外,其余各组小鼠从饮用4%DSS 3 d后,开始出现烦躁不安、精神倦怠、腹泻、血便、毛色黯淡无光泽、消瘦等情况。经过治疗后,各剂量治疗组均有不同程度的改善。药物治疗14 d后,DHM中剂量组、高剂量组、5-氨基水杨酸组DAI均显著低于模型组(P<0.01,图 1),DHM高剂量组与5-氨 基水杨酸组相比差异无统计学意义(P=0.611)。说明中、高剂量DHM对缓解小鼠疾病活动具有显著的抑制作用,高剂量组与5-氨基水杨酸治疗效果相当。
|
| a: P<0.01,与模型组比较 图 1 治疗14 d后各组小鼠DAI评分比较 |
2.2 病理组织学评分
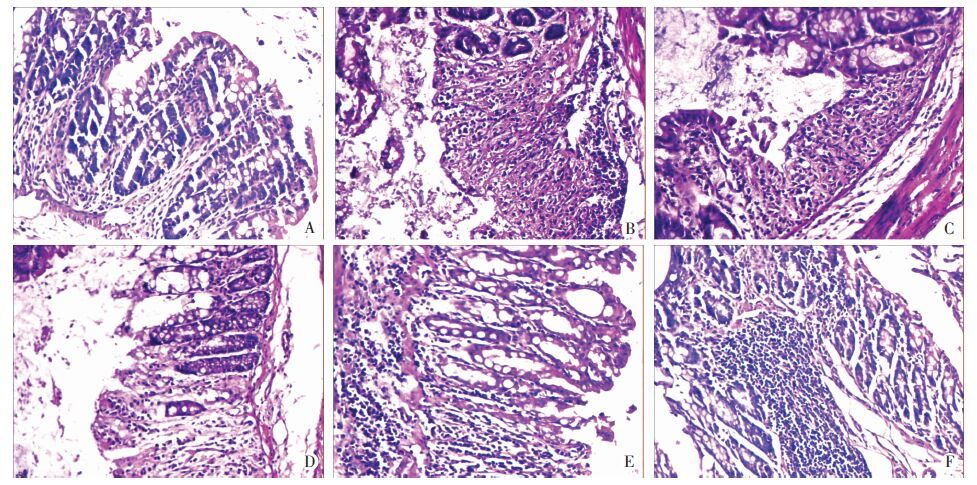
正常组,光镜下可见正常肠道黏膜。模型组,光镜下可见黏膜固有层大量炎性细胞浸润,多灶性大小不一的溃疡,无黏膜覆盖。DHM低剂量组,光镜下可见黏膜固有层可见炎性细胞浸润,多灶性大小不一溃疡,肉芽填充,可见上皮覆盖。DHM中剂量组,光镜下可见多灶性溃疡,但可见肉芽组织填充,腺体增生修复,部分上皮覆盖。DHM高剂量组,光镜下可见溃疡面积较小,肉芽组织修复,可见上皮覆盖,但炎症较重。5-氨基水杨酸组光镜下可见溃疡面积较小,黏膜修复较为完整(图 2)。
|
| A:正常组;B:模型组;C:DHM低剂量组;D:DHM中剂量组;E:DHM高剂量组;F:5-氨基水杨酸组 图 2 光学显微镜观察各组小鼠结肠组织学变化 (HE ×200) |
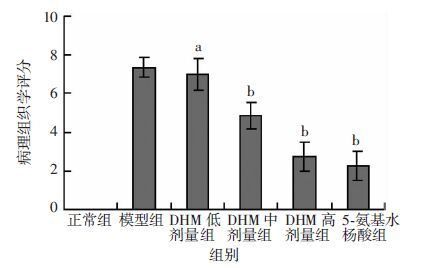
与正常组相比,其余各组的病理组织学评分均显著升高,差异有统计学意义(P<0.01),DHM低、中剂量组与高剂量组相比,差异也有统计学意义(P<0.01),高剂量组与5-氨基水杨酸组差异无统计学意义(P>0.05,图 3)。
|
| a: P<0.05,b: P<0.01,与模型组比较 图 3 光镜下小鼠结肠病理组织学评分 |
2.3 DHM对小鼠结肠长度的影响
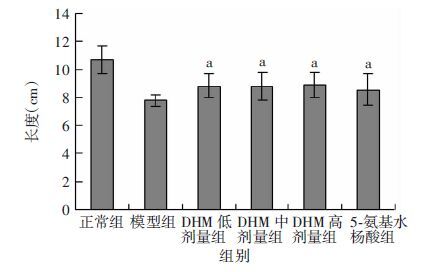
正常组小鼠肠黏膜无充血、水肿,饮用4%DSS 7 d后,模型组小鼠结肠肠壁充血、水肿,严重者自结肠至肛门肠段均可见血性内容物。统计结果显示,各治疗组与模型组相比,均可不同程度的抑制溃疡性结肠炎小鼠结肠缩短(P<0.05,图 4)。
|
| a: P<0.05,与模型组比较 图 4 各组小鼠治疗14 d后结肠长度比较 |
2.4 小鼠脾脏指数
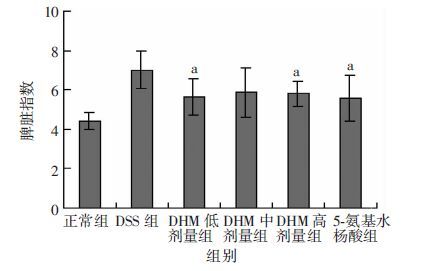
模型组,DHM低、中、高剂量组,5-氨基水杨酸组小鼠脾脏指数较正常组升高,差异有统计学意义(P<0.05)。DHM低剂量组、高剂量组、5-氨基水杨酸组与模型组相比,差异有统计学意义(P<0.05),而DHM中剂量组与模型组比较差异无统计学意义(P>0.05),DHM各剂量组与5-氨基水杨酸组之间差异均无统计学意义(P>0.05,图 5)。
|
| a: P<0.05,与模型组比较 图 5 各组小鼠治疗14 d后脾脏指数比较 |
2.5 Wsetern blot测定小鼠结肠组织中TLR2、TLR4的表达变化
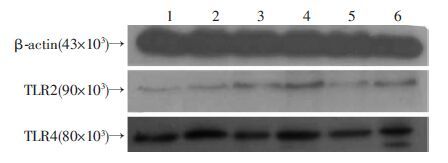
模型组小鼠结肠组织TLR2、TLR4蛋白表达水平较正常组明显升高,给予DHM灌胃治疗后,各剂量组小鼠肠组织TLR2、TLR4蛋白表达水平均有明显降低,其中DHM高剂量治疗组给药后显著抑制了DSS给药后小鼠结肠组织中TLR2、TLR4的高表达(P<0.01),治疗效果与5-氨基水杨酸相当(图 6)。
|
| 1: 正常组; 2: 模型组; 3: DHM低剂量组; 4: DHM中剂量组; 5: DHM高剂量组; 6: 5-氨基水杨酸组 图 6 Wsetern blot检测各组小鼠结肠组织中TLR2、TLR4的表达 |
2.6 EMSA测定NF-κB的表达
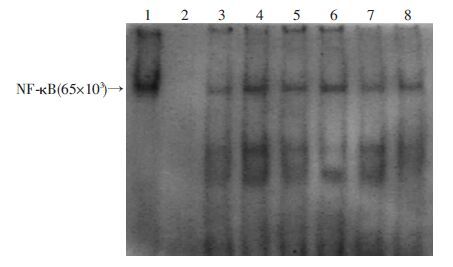
模型组小鼠结肠组织NF-κB表达水平较正常组明显升高,表明溃疡性结肠炎小鼠结肠黏膜中NF-κB信号通路被激活。给予DHM治疗后,明显抑制了NF-κB的高表达。各治疗组对NF-κB 均具有显著的抑制作用(P<0.01),而高剂量组与5-氨基水杨酸组相比,差异有统计学意义(P<0.01,图 7)。
|
| 1~8:NF-κB阳性、NF-κB阴性、正常组、模型组、DHM低剂量组、DHM中剂量组、DHM高剂量组、水杨酸对照组 图 7 各组小鼠NF-κB表达情况比较 |
2.7 ELISA法测定细胞因子IL-1β、TNF-α、IL-6的含量
模型组小鼠组织蛋白中IL-1β、TNF-α、IL-6含量显著升高(P<0.01)。而高剂量组、5-氨基水杨酸组与模型组相比,差异均有统计学意义(P<0.05,表 1)。
| 组别 | n | IL-1β | TNF-α | IL-6 |
| 正常组 | 6 | 138.55±13.13 | 190.47±22.63 | 387.35±34.61 |
| 模型组 | 6 | 321.13±25.10a | 352.40±24.27a | 699.00±81.42a |
| DHM低剂量组 | 7 | 300.79±28.96 | 291.87±31.85 | 560.80±12.44 |
| DHM中剂量组 | 7 | 190.83±18.14b | 254.21±83.47 | 625.79±27.72 |
| DHM高剂量组 | 7 | 178.41±11.47b | 195.99±7.01b | 536.14±40.72b |
| 5-氨基水杨酸组 | 7 | 169.62±18.04b | 218.04±25.84b | 427.19±18.91b |
| a: P<0.01,与正常组比较; b: P<0.05,与模型组比较 | ||||
2.8 ELISA法测定NO、SOD、MPO的活性
模型组小鼠结肠组织中SOD活性明显下降(P<0.01),NO、MPO活性明显升高(P<0.01)。给予药物治疗后,DHM各剂量组及5-氨基水杨酸组小鼠结肠组织中SOD、MPO活性均有不同程度变化,与模型组比较差异均有统计学意义(P<0.05,表 2),但DHM低、中剂量组NO活性与模型组比较,差异无统计学意义(P>0.05);DHM高剂量组、5-氨基水杨酸与模型组比较,差异有统计学意义(P<0.05,表 2)。
| 组别 | n | MPO(U/g) | SOD(U/mg) | NO(μmol/g) |
| 正常组 | 6 | 0.45±13.13 | 33.22±2.72 | 0.82±0.06 |
| 模型组 | 6 | 4.87±0.69a | 7.05±0.06a | 4.76±0.14a |
| DHM低剂量组 | 7 | 2.47±0.18b | 18.86±1.84b | 4.64±0.18 |
| DHM中剂量组 | 7 | 2.31±0.00b | 18.84±1.66b | 4.41±0.29 |
| DHM高剂量组 | 7 | 1.47±0.23b | 29.24±3.97b | 2.01±0.14b |
| 5-氨基水杨酸组 | 7 | 1.41±0.29b | 26.91±1.61b | 2.05±0.11b |
| a: P<0.01,与正常组比较; b: P<0.05,与模型组比较 | ||||
3 讨论
目前,UC的发病机制仍未明确,主要观点认为UC是免疫、遗传、环境、肠道菌群等多种因素共同作用的结果。由于其发病机制不明,所以目前临床上仍缺少有效的治疗药物,因此,开发高效且安全副作用小的药物仍然是目前炎性肠病的研究热点。
5-氨基水杨酸(5-ASA)又名美沙拉嗪,是当前治疗UC的一线药物,能够有效缓解轻度和中毒活动期UC患者的症状。国内外众多研究对5-ASA治疗实验性小鼠结肠炎的机制见解各异,但相关数据对其疗效都是一致的认可[3-4]。DSS诱导的结肠炎动物模型在UC相关研究中应用广泛,病理表现近似于人类UC,可用于评价新的治疗方法对UC的治疗作用[5-6]。
本实验通过DSS诱导建立小鼠的急性UC模型,发现使用不同剂量DHM后,可不同程度缓解DSS诱导的小鼠急性溃疡性结肠炎的疾病活动指数(DAI),结肠长度及脾脏指数变化。镜下可见DHM可以减轻溃疡性结肠炎模型肠黏膜的组织病理炎症改变。说明DHM对急性溃疡性结肠炎小鼠具有一定的干预机制。
近年来,随着对核因子NF-κB结构与功能研究的深入,细胞因子与 NF-κB的关系已引起了人们高度的重视,成为当今研究的热点,而通过激活NF-κB从而释放的如IL-1β、TNF-α、IL-6等炎性刺激因子,越来越多的研究证实,UC患者肠黏膜组织、血清及粪便中肿瘤坏死因子TNF-α、IL-1β、IL-6等多种细胞因子的表达均增强[7-8]。本实验应用EMSA测定NF-κB结果显示出经过DHM治疗的溃疡性结肠炎小鼠与模型组小鼠相比,差异有统计学意义(P<0.05)。通过ELISA法,结果显示出IL-1β、TNF-α、IL-6在模型组小鼠肠黏膜中表达明显升高,经过DHM治疗的溃疡性结肠炎小鼠肠组织中IL-1β、TNF-α、IL-6等炎性刺激因子较模型组相比,均有不同程度的降低,差异有统计学意义(P<0.05)。说明DHM能够降低DSS诱导的小鼠结肠组织中IL-1β、TNF-α、IL-6,具有一定的抗炎作用。
TLRs是一族具有信号转导功能的固有免疫识别受体,其中TLR2主要识别革兰阳性肽聚糖,而TLR4主要识别革兰阴性菌的脂多糖(lipopolysaccharide,LPS) [9-10]。研究表明,TLR2和TLR4在正常的结肠黏膜中呈现低表达,而在溃疡性结肠炎的结肠黏膜中则呈现异常的高表达[11],大量研究表明,TLR4/NF-κB 信号通路在UC中发挥至关重要的作用,因此,TLR2、TLR4受体及其信号传导通路可能是溃疡性结肠炎发病过程中的重要环节。本实验Western blot检测结果显示,溃疡性结肠炎模型组小鼠肠组织TLR2、TLR4表达明显增高,对照组小鼠结肠黏膜TLR2、TLR4表达较少,通过二氢杨梅素治疗的小鼠TLR2、TLR4及NF-κB表达含量明显降低,与模型组相比,差异均有统计学意义(P<0.05)。说明TLR2、TLR4可能参与了溃疡性结肠炎的发生和发展,而DHM可抑制UC模型中TLR2、TLR4的表达,发挥抗炎作用。
免疫因素也被公认为是UC发病机制的重要因素之一。有报道肠黏膜超氧化物歧化酶(SOD)活性降低,髓过氧化物酶(MPO)活性 、一氧化氮(NO) 水平升高与 UC 的发病关系密切[12]。SOD是机体超氧自由基的清除剂,广泛分布于细胞内和各种体液中,机体多种病理过程如缺血性疾病、炎症、肿瘤、损伤、衰老等均与SOD密切相关。SOD活性的高低间接反映了机体清除氧自由基的能力[13]。MPO是中性粒细胞嗜天青颗粒的重要组成部分,是粒细胞聚集的指标,也是炎症和组织损伤的指标。据报道,实验性动物和炎症性肠病患者的MPO活性都会显著增加[14]。NO作为另一种氧自由基也对肠黏膜具有氧化损伤和促炎作用,研究表明 UC病变黏膜中NO浓度的增加与炎症程度呈平行关系[15]。本实验ELISA结果显示,模型组小鼠SOD活性明显下降,NO、MPO活性明显升高,治疗组小鼠SOD活性不同程度升高,NO、MPO活性不同程度降低,与模型组相比具有明显的统计学差异(P<0.05),提示氧化应激在DSS诱导的UC模型中发挥了作用,而DHM具有一定的抗氧化作用,抑制组织的过氧化反应。因此,我们认为二氢杨梅素确实具有一定的抗氧化作用,增加SOD活性,抑制MPO、NO产生可能是其缓解小鼠结肠炎的机制之一。
以上研究结果表明,不同剂量DHM灌胃给药,可以不同程度有效缓解DSS诱导的小鼠结肠炎,对DSS小鼠结肠炎具有良好的保护作用。其作用机制是多方面的,可能通过抑制结肠黏膜组织TLR2、TLR4蛋白的合成,进而阻断了TLR/NF-κB信号通路的转导,使NF-κB的活性受到抑制,减少IL-1β、TNF-α、IL-6等炎性因子的表达、分泌,阻断炎症的放大效应从而有效减轻炎症反应对机体造成的损伤。同时,增加SOD活性,抑制MPO、SOD产生可能是其重要作用机制之一。本实验结果为确定信号通路中的关键分子和DHM最佳治疗剂量以及临床研发治疗UC药物提供了实验依据。
| [1] | Korzenik J R, Podolsky D K. Evolving knowledge and therapy of inflammatory bowel disease[J]. Nat Rev Drug Discov,2006, 5 (3) : 197 –209. DOI:10.1038/nrd1986 |
| [2] | 陈夏静, 姚汉玲, 张秋琼, 等. 大叶蛇葡萄中蛇葡萄素含量的高效液相色谱法测定[J]. 时珍国医国药,2010, 21 (5) : 1053 –1054. DOI:10.3969/j.issn.1008-0805.2010.05.010 |
| [3] | Deng X, Tolstanova G, Khomenko T, et al. Mesalamine restores angiogenic balance in experimental ulcerative colitis by reducing expression of endostatin and angiostatin: novel molecular mechanism for therapeutic action of mesalamine[J]. J Pharmacol Exp Ther,2009, 331 (3) : 1071 –1078. DOI:10.1124/jpet.109.158022 |
| [4] | Kruis W, Kiudelis G, Racz I, et al. Once daily versus three times daily mesalazine granules in active ulcerative colitis: adoube-blind, double-dummy, randomised, non-inferiority trial[J]. Gut,2009, 58 (2) : 233 –240. DOI:10.1136/gut.2008.154302 |
| [5] | 农辉, 黄雪. 葡聚糖硫酸钠诱导结肠炎模型的研究进展[J]. 世界华人消化杂志,2014, 22 (22) : 3245 –3250. |
| [6] | Wirtz S, Neurath MF. Mouse models of inflammatory bowel disease[J]. Adv Drug Deliv Rev,2007, 59 (11) : 1073 –1083. DOI:10.1016/j.addr.2007.07.003 |
| [7] | 甘华田, 欧阳钦, 贾道全, 等. 溃疡性结肠炎患者核因子NF-κB活化与细胞因子基因表达[J]. 中华内科杂志,2002, 41 (4) : 252 –255. |
| [8] | Grivennikov S I, Karin M. Dangerous liaisons: STAT3 and NFKB collaboration and crosstalk in cancer[J]. Cytok Growth Factor Rev,2010, 21 (1) : 11 –19. DOI:10.1016/j.cytogfr.2009.11.005 |
| [9] | Muzio M, Mantovani A. Toll-like receptors[J]. Microbes Infect,2000, 2 (3) : 251 –255. DOI:10.1016/s1286-4579(00)00303-8 |
| [10] | Dogi C A, Galdeano C M, Perdigón G. Gut immune stimulation by non pathogenic Gram(+ )and Gram(-)bacteria. Comparison with a probiotic strain[J]. Cytokine,2008, 41 (3) : 223 –231. DOI:10.1016/j.cyto.2007.11.014 |
| [11] | Szebeni B, Veres G, Dezsfi A, et al. Increased expression of Toll-like receptor(TLR) 2 and TLR4 in the colonic mucosa of children with inflammatory bowel disease[J]. Clin Exp Immunol,2008, 151 (1) : 34 –41. DOI:10.1111/j.1365-2249.2007.03531.x |
| [12] | Mylonas C, Kouretas D. Lipid peroxidation and tissue damage[J]. In Vivo,1999, 13 (3) : 295 –309. |
| [13] | 游宇, 刘玉晖, 卢放根, 等. N-乙酰半胱氨酸对葡聚糖硫酸钠诱导的小鼠溃疡性结肠炎的保护作用[J]. 中南药学,2007, 5 (4) : 295 –299. DOI:10.3969/j.issn.1672-2981.2007.04.003 |
| [14] | Fakhfouri G, Rahimian R, Daneshmand A. et al Granisetron ameliorates acetic acid-induced colitis in rats[J]. Hum Exp Toxicol,2010, 29 (4) : 321 –328. DOI:10.1177/0960327110362702 |
| [15] | 金惠铭. 病理生理学[M]. 5版 北京: 人民卫生出版社, 2000 : 150 . |



