2. 400042 重庆,第三军医大学大坪医院野战外科研究所第三研究室,创伤与烧伤国家重点实验室
2. State Key Laboratory of Trauma, Burns and Combined Injury, Department 3, Institute of Surgery Research, Daping Hospital, Third Military Medical University, Chongqing, 400042, China
脊髓损伤(spinal cord injury,SCI)后产生的运动和感觉功能障碍一直是学者关注的重点,而认知、情绪改变因各种原因容易被忽略[1]。但已有研究表明,SCI患者会出现不同程度的记忆障碍、焦虑、抑郁等情况[2-4]。伴随预防医学、临床医学和康复医学的相互融入,脊髓损伤患者的治疗与康复逐渐成为一个综合的过程。人们也逐渐意识到该问题的重要性[1]。关于脊髓损伤后认知障碍的研究较少,更缺乏对相关机制的探究。我们在既往研究基础上,采用大鼠脊髓挫裂伤模型,观察伤后不同时间点大鼠的认知功能状况以及大鼠脑内的病理变化,并探索其可能机制。
1 材料与方法 1.1 材料雌性成年SD大鼠120只,体质量200~220 g,由第三军医大学大坪医院野战外科研究所实验动物中心提供。动物生产许可:SCXK (渝)2012-0005。动物饲养及实验过程遵守实验动物管理及保护的有关规定。动物分为实验组和对照组(每组60只,每组下设5个时间点,每个时间点12只)。戊巴比妥钠(德国)、快速高尔基体染色试剂盒(FD rapid golgistain kit,美国)、兔抗大鼠葡萄糖调节蛋白78(glucose regulated protein 78 kD,GRP78,Bioworld,美国)、兔抗大鼠Caspase-12(Bioworld,美国),Allen打击器(RM2007,美国),冰冻切片机(Leica CM1900,德国),电泳仪、电泳槽(Bio-Rad,美国)。
1.2 动物模型建立动物术前12 h禁食,以1%戊巴比妥钠(4 mL/kg)腹腔注射麻醉。常规备皮,消毒,咬开T9~T11椎板,显露脊髓。Allen打击器上建立力度为20 g×25 mm的挫裂伤模型。造模以损伤后大鼠后肢发生抽搐后瘫软、尾巴痉挛性摆动为标准。对照组仅显露脊髓,不做损伤处理。分别缝合肌肉和皮肤置于25~28 ℃动物房内。术后护理:每天1次青霉素1.6×105U后腿肌肉丰厚处注射,连续3 d;每天3次按摩膀胱排尿,直到约1周后恢复自主排尿。
1.3 行为学评价 1.3.1 大鼠后肢运动功能(BBB评分)造模后分别于相应时间点评估BBB评分。检测时对偏离平均值2分以上者剔除,之后补充。由1~2名熟悉BBB评分方法的非本组实验人员进行评分。
1.3.2 高架十字迷宫和Morris水迷宫实验SCI后8、12周进行。保持室内适宜温度湿度,调节灯光,测试时间5 min,每只老鼠只测试1次,实验前安抚实验对象,充分适应实验环境,实验过程中从十字迷宫掉下地的老鼠予以剔除。记录开放臂进入次数和在迷宫内行进路程。每次实验后清洁器械表面避免留下气味。用Smart 2.0软件分析数据。
分别在损伤后7、11周进行水迷宫的训练和测试(测试时间正好落在第8周和第12周)。测试分为定位航行测试和空间探索测试。定位航行测试连续4 d,训练依次从迷宫的4个象限入水。每天第1次训练(测试)均从目标象限对侧象限头朝内放入水迷宫。前4 d定位巡航测试大鼠每天第1次找到平台的时间为潜伏期。第5天为空间探索测试,取消平台,在90 s内记录大鼠穿越平台次数。Smart 2.0软件(Panlab)分析数据。
1.3.3 病理染色和快速高尔基体染色相应时间点行为学检测后,灌注动物,OCT冰冻切片包埋剂包埋组织,冰冻切片厚度15 μm行尼氏染色,观察海马皮质区域神经细胞形态。
快速高尔基体染色按说明进行换液染色。每组取4~6只样本,放入-80℃低温速冻后制备60 μm冰冻切片,切至完整海马区域且背景清晰5~10张切片。每张脑片观察海马区域末端树突,在400倍油镜下观察海马区域清晰基树突末端,统计方法以每10 μm树突棘个数反映树突棘密度[5]。
1.3.4 Western blot检测相应时间点取出海马组织冻存于液氮,收集完成各组标本后取出放入PIPA裂解液与蛋白酶抑制剂混合液中。经过研磨、低温超速离心、取上清液等过程,最后BCA试剂盒测蛋白浓度得到各组蛋白。之后进行凝胶电泳, 曝光仪曝光条带并分析各组条带灰度值。
1.4 统计学分析采用SPSS 19.0统计软件进行分析,所有数据以x±s来表示。Morris水迷宫实验潜伏时检测采用单因素方差分析。其余数据均用独立样本t检验,检验水准α=0.05。
2 结果 2.1 一般情况与对照组比较,损伤组大鼠精神萎靡,双下肢软瘫,并且出现尿潴留。1周内部分大鼠出现血尿等现象,随着时间推移好转。10 d左右可基本自主排尿。损伤组手术苏醒后评分均为0,即损伤后后肢完全性瘫痪。术后各时间点损伤组和对照组比较,差异有统计学意义(P < 0.01,图 1)。
|
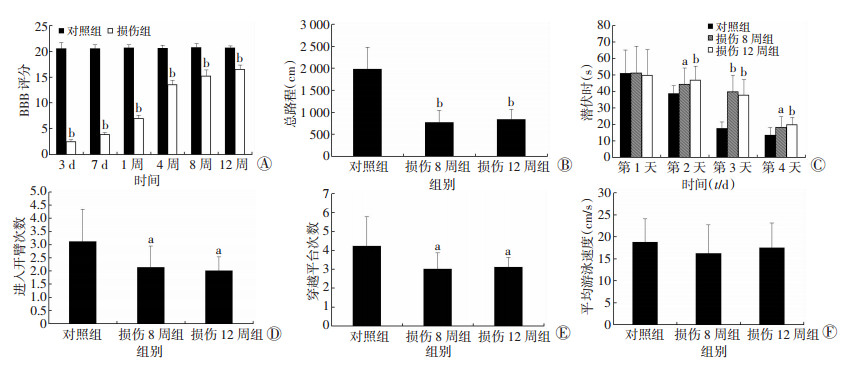
| A:BBB评分;B:高架十字迷宫动物活动路程;C:高架十字迷宫进入开臂平均用时;D:水迷宫测试平均潜伏时;E:水迷宫测试穿越平台次数;F:水迷宫测试平均游泳速度a:P < 0.05,b:P < 0.01,与对照组比较 图 1 各组大鼠BBB评分、高架十字迷宫和Morris水迷宫检测结果 |
2.2 脊髓损伤大鼠高架十字迷宫和Morris水迷宫检测结果
高架十字迷宫检测结果显示,损伤大鼠进入开臂次数减少,相比对照组差异有统计学意义(P < 0.05)。但随着时间的推移,没有更加严重的迹象。动物活动的总路程有显著下降(P < 0.01),对照组大鼠平均活动总路程约为20 m,损伤8周或12周后,大鼠平均活动总路程均在10 m之内。这提示大鼠在SCI后出现探索行为减弱的表现(图 1)。
水迷宫实验中,SCI大鼠的定位巡航潜伏时间均出现下降趋势,结果显示,损伤大鼠潜伏时间在巡航的2~4 d均有所延长,差异具有统计学意义(P < 0.05,P < 0.01)。探索实验结果显示,损伤8周和12周后的动物穿越平台的次数明显低于对照组(P < 0.05),且记录各组平均游泳速度差异无统计学意义(P>0.05)。以上说明大鼠的空间记忆和学习能力在损伤后有所下降,但因损伤造成的运动功能损害对该行为学测试的影响可忽略(图 1)。
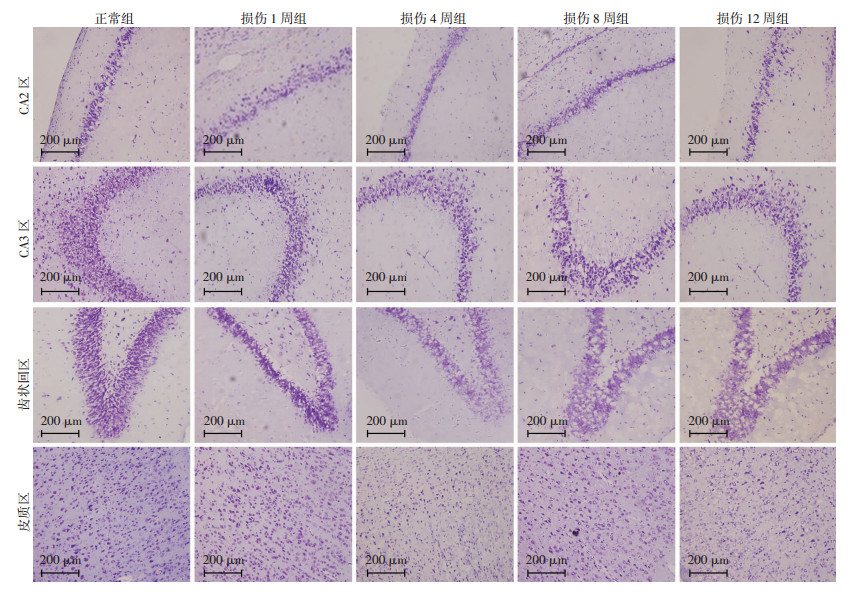
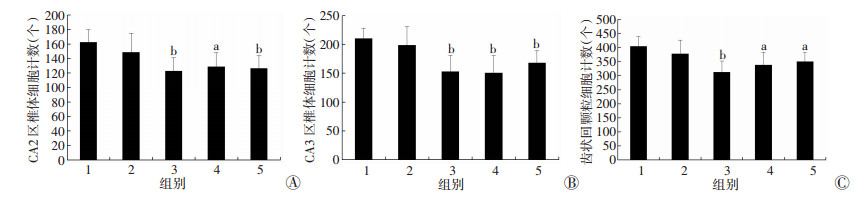
2.3 脊髓损伤大鼠脑组织尼氏染色观察对照组海马与皮质区域椎体细胞排列整齐结构紧密,形态完整。而损伤组大鼠海马各区域以及部分皮质出现了病理改变。其中以齿状回、CA2和CA3区域改变最明显,该区神经元细胞排列稀疏,结构紊乱。在皮质区域也可见锥体细胞减少、染色变浅等现象。这种变化早在SCI后4周即可发现,并持续到损伤后12周(P < 0.05,P < 0.01)皮质区域在SCI后8周起也出现了神经细胞减少(P < 0.05,P < 0.01,图 2、3)。
|
| 图 2 各组大鼠海马与皮质区域尼氏染色结果 |
|
| 1:对照组;2:损伤1周组;3:损伤4周组;4:损伤8周组;5:损伤12周组A:CA2区椎体细胞计数;B:CA3区椎体细胞计数;C:齿状回颗粒细胞计数a:P < 0.05,b:P < 0.01,与对照组比较 图 3 各组大鼠海马皮质各个区域尼氏染色结果定量分析 |
2.4 脊髓损伤大鼠脑组织树突棘染色观察
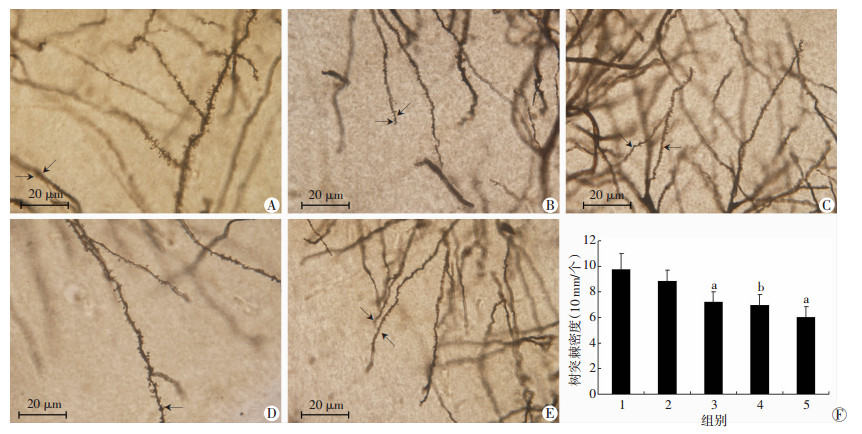
SCI后海马区域4周与8周树突棘数量稀疏,与对照组比较,密度明显减少(P < 0.05,P < 0.01,图 4)。
|
| ↑:示树突棘1:对照组;2:损伤1周组;3:损伤4周组;4:损伤8周组;5:损伤12周组A~E:分别为对照组,损伤1、4、8、12周组a:P < 0.05,b:P < 0.01,与对照组比较 图 4 各组大鼠高尔基体染色结果 |
2.5 脊髓损伤大鼠海马组织GRP78和Caspase-12蛋白的表达情况
GRP78蛋白在SCI后大鼠海马的表达明显高于对照组,且随着时间的推移表达续升高,但在损伤后12周有明显下降(P < 0.01)。Caspase-12蛋白从损伤后1周表达增高,之后持续高表达。伤后各个时间点与对照组相比,差异有统计学意义(P < 0.05,P < 0.01,图 5)。

|
| A:Western blot检测结果;B:半定量分析结果1:对照组;2:损伤1周组;3:损伤2周组;4:损伤4周组;5:损伤8周组;6:损伤12周组a:P < 0.05,b:P < 0.01,与对照组比较 图 5 Western blot检测各组大鼠海马组织GRP78和Caspase-12蛋白表达 |
3 讨论
长期以来,学者们对SCI的研究主要集中在运动、感觉功能的缺失及其自主神经相关的并发症上,而对于损伤后造成的大脑认知障碍的研究较少。考虑到情感、记忆等认知功能在患者治疗和康复过程中的重要意义,研究脊髓损伤后相关问题的发生及可能原因显得尤为重要。
我们的前期研究发现,SCI大鼠在损伤5周后出现齿状回颗粒细胞数量减少,并且损伤后8周动物有学习记忆功能改变[6]。本研究进一步完善了SCI后大鼠认知功能的行为学评价,并增加了焦虑相关的行为学测试。对SCI后大鼠的脑内变化进行了相对系统的观察。我们验证了SCI大鼠8周后会出现学习和空间记忆能力下降。而且,通过高架十字迷宫实验发现,动物还有抑郁、恐惧和明显的探索兴趣减退等情绪障碍。同时,这些种变化会持续到损伤后12周。但是,海马、皮质部位的病理学改变却早于行为学变化。海马多个区域神经细胞在4周后即出线数量减少的情况。快速高尔基体染色结果证实,海马内树突棘密度随着时间推移逐渐减少、稀松,说明海马内部的纤维投射可能受损,也说明海马与皮质或大脑其他部位的信息链接可能不畅。最后,我们发现内质网应激相关蛋白GRP78和Caspase-12在损伤大鼠海马表达明显上调。这提示内质网应激、海马神经元的慢性炎症可能参与了大鼠SCI后的认知、情绪障碍。
脊髓损伤引起海马、皮质区域病理改变和认知障碍、情绪改变的机制尚不完全清楚。综合已有的相关报道,我们发现主要集中在以下两大主要方面:①脊髓损伤伴发有难以察觉脑组织结构损害。Wang等[7]对42只成年雄狗进行了后肢高速冲击实验,发现在损伤仅8 h之后在损伤动物的海马和丘脑等处发生神经元变性和脱髓鞘改变。此外Zhang等[8]对成年白猪行脊柱高速冲击非穿透性钝挫伤的研究中发现,损伤动物的记忆力等行为学方面有异常,动物在损伤后脑电图和脑内也有不同程度改变。②脊髓损伤介导的脑内继发性损伤。有学者发现SCI后大鼠脑内细胞周期激活,并发现了脑内有持续性炎症反应。与神经病理性疼痛密切相关的小胶质细胞在SCI慢性期也处于持续激活状态。通过竞争性抑制脑内IL-6的表达使得炎症减轻,并有助于功能恢复[9]。还有观点认为SCI后到脑海马和皮质区域神经元大量消失与皮质脊髓束联系切断又或是脊髓损伤后上行神经元凋亡有关,但该问题目前仍存在一定的争论[6]。本实验结果显示,SCI后大鼠海马有内质网应激相关蛋白的激活,支持了慢性炎症的观点。
内质网应激(endoplasmic reticulum stress,ERS)是指某种原因导致细胞内质网生理功能发生紊乱的一种亚细胞器病理过程。严重持续的内质网应激可能引起与之有关的炎症和凋亡通路激活与SCI继发性损伤密切相关[10-12]。最近有研究指出,SCI后12周脑内有内质网应激相关蛋白GRP78表达增高[13-14],本研究结果印证了这一观点。使用Western blot检测,我们发现脊髓挫裂伤后1周到3个月GRP78和Caspase-12蛋白总体趋势在海马表达逐渐升高,而8~12周GRP78蛋白表达的下降可能是持续强烈的内质网应激已经引起细胞稳态调节能力减弱,内质网功能失代偿[11]。这些结果说明脊髓损伤后海马可能产生持续严重的ERS,并且参与了炎症和神经细胞凋亡等反应。然而对于内质网应激的发生和发展的具体机制以及是否是影响脊髓损伤后认知障碍等问题我们还不得而知,也需要更多的探索。
| [1] | Wu J, Raver C, Piao C, et al. Cell cycle activation contributes to increased neuronal activity in the posterior thalamic nucleus and associated chronic hyperesthesia after rat spinal cord contusion[J]. Neurotherapeutics,2013, 10 (3) : 520 –538. DOI:10.1007/s13311-013-0198-1 |
| [2] | Davidoff G N, Roth E J, Richards J S. Cognitive deficits in spinal cord injury: epidemiology and outcome[J]. Arch Phys Med Rehabil,1992, 73 (3) : 275 –284. |
| [3] | Davidoff G, Morris J, Roth E, et al. Cognitive dysfunction and mild closed head injury in traumatic spinal cord injury[J]. Arch Phys Med Rehabil,1985, 66 (8) : 489 –491. |
| [4] | Wilmot C B, Cope D N, Hall K M, et al. Occult head injury: its incidence in spinal cord injury[J]. Arch Phys Med Rehabil,1985, 66 (4) : 227 –231. DOI:10.1016/0003-9993(85)90148-0 |
| [5] | 贾贺, 张博爱, 刘宇, 等. 慢性脑缺血大鼠海马CA1区锥体细胞树突形态及树突棘密度的变化[J]. 中国病理生理杂志,2012, 28 (1) : 177 –180. DOI:10.3969/j.issn.1000-4718.2012.01.035 |
| [6] | 冯东亮, 南伟, 伍亚民, 等. 脊髓损伤大鼠的学习记忆功能与海马病理改变[J]. 中国康复理论与实践,2015, 21 (11) : 1267 –1272. DOI:10.3969/j.issn.1006-9771.2015.11.007 |
| [7] | Wang Q, Wang Z, Zhu P, et al. Alterations of myelin basic protein and ultrastructure in the limbic system at the early stage of trauma-related stress disorder in dogs[J]. J Trauma,2004, 56 (3) : 604 –610. DOI:10.1097/01.ta.0000058122.57737.0e |
| [8] | Zhang B, Huang Y, Su Z, et al. Neurological, functional, and biomechanical characteristics after high-velocity behind armor blunt trauma of the spine[J]. J Trauma,2011, 71 (6) : 1680 –1688. DOI:10.1097/TA.0b013e318231bce7 |
| [9] | Guerrero A R, Uchida K, Nakajima H, et al. Blockade of interleukin-6 signaling inhibits the classic pathway and promotes an alternative pathway of macrophage activation after spinal cord injury in mice[J]. J Neuroinflammation,2012, 9 : 40 . DOI:10.1186/1742-2094-9-40 |
| [10] | Hasnain S Z, Lourie R, Das I, et al. The interplay between endoplasmic reticulum stress and inflammation[J]. Immunol Cell Biol,2012, 90 (3) : 260 –270. DOI:10.1038/icb.2011.112 |
| [11] | Penas C, Guzmán M S, Verdú E, et al. Spinal cord injury induces endoplasmic reticulum stress with different cell-type dependent response[J]. J Neurochem,2007, 102 (4) : 1242 –1255. DOI:10.1111/j.1471-4159.2007.04671.x |
| [12] | Liu S, Sarkar C, Dinizo M, et al. Disrupted autophagy after spinal cord injury is associated with ER stress and neuronal cell death[J]. Cell Death Dis,2015, 6 : e1582 . DOI:10.1038/cddis.2014.527 |
| [13] | Yu Z, Luo H, Fu W, et al. The endoplasmic reticulum stress-responsive protein GRP78 protects neurons against excitotoxicity and apoptosis: suppression of oxidative stress and stabilization of calcium homeostasis[J]. Exp Neurol,1999, 155 (2) : 302 –314. DOI:10.1006/exnr.1998.7002 |
| [14] | Wu J, Zhao Z, Kumar A, et al. Endoplasmic Reticulum Stress and Disrupted Neurogenesis in the Brain Are Associated with Cognitive Impairment and Depressive-Like Behavior after Spinal Cord Injury[J]. J Neurotrauma,2016 . DOI:10.1089/neu.2015.4348 |



