2. 100142 北京,解放军空军总医院消化内科/全军小肠疾病内镜诊疗中心 ;
3. 430071 武汉,武汉大学中南医院消化内科 ;
4. 400038 重庆,第三军医大学西南医院全军消化病研究所
2. Department of Gastroenterology, Endoscopic Diagnosis and Treatment Center for Small Bowel Diseases, Air Force General Hospital, Beijing, 100042 ;
3. Department of Gastroenterology, Zhongnan Hospital of Wuhan University, Wuhan, Hubei Province, 430071 ;
4. Institute of Gastroenterology, Southwest Hospital, Third Military Medical University, Chongqing, 400038, China
Zhang Yafei, E-mail: zhangyafei1127@163.com
Barrett食管(barrett’s esophagus,BE)是食管远端复层鳞状上皮被化生的柱状上皮所取代的一种病理现象,是食管腺癌发生最重要的危险因素[1-2]。我国对BE的研究起步较晚,过去认为在临床上较为少见,但近年,随着国人生活方式的日益西化,BE发病率呈上升趋势,其也必将导致相关食管腺癌的发病率迅速提高。因此,应重视BE及相关食管腺癌的研究。
lincRNA (large intergenic noncoding RNA)是一类位于编码蛋白基因之间,长度超过200nt的位于基因间的长链非编码RNA (long non-coding RNA,lncRNA)。Yang等[3]利用新一代高通量RNA测序技术检测了BE及BE相关腺癌组织中lncRNA的表达变化,共发现32种显著上调表达的lncRNA,其中LINC00261在BE组织中较正常食管鳞状上皮组织上调表达48.79倍,在BE相关腺癌组织中较正常食管鳞状上皮组织上调表达181.82倍,其差异性均最为显著。在本研究中,我们利用qRT-PCR技术检测了LINC00261在中国人群正常食管鳞状上皮组织、BE及食管腺癌组织标本中的表达水平变化,并以人胚胎干细胞为细胞模型,初步探讨了LINC00261在BE发生过程中的可能作用机制。
1 资料与方法 1.1 材料本研究由空军总医院伦理委员会批准(2014)。收集第三军医大学西南医院、广州军区武汉总医院、空军总医院病理科石蜡包埋人食管腺癌组织、BE组织及正常食管鳞状上皮组织(食管鳞癌及腺癌术后癌旁正常组织,距离肿瘤边界>2 cm)标本各20例。所有病例均未行术前放化疗,常规石蜡包埋,制备5 μm厚连续切片。
1.2 实验方法 1.2.1 细胞培养正常食管鳞状上皮细胞系(Het-1A)、BE细胞系(BE CP-A)及BE相关腺癌细胞系(OE33和skgt4)接种于含10%胎牛血清的1640培养基中,置37℃、5% CO2培养箱中培养,至对数生长期进行实验。人胚胎干细胞购自上海细胞保藏中心,以人胚胎成纤维细胞作为饲养层细胞。
1.2.2 qRT-PCR利用美国AB公司专门为石蜡组织样本提取核酸(包括DNA、RNA及miRNA)所研发的RecoverAllTM Total Nucleic Acid Isolation Kit for FFPE Tissues试剂盒提取总RNA;利用TaKaRa公司的总mRNA试剂盒提取细胞总RNA。然后利用qRT-PCR法检测LINC00261的表达,以β-actin为内参。引物设计如下:LINC00261:上游,5′-GCATTGTGTTGTCAGC CTCA-3′,下游,5′-AACCTACAAGTGGTCTGGGG-3′;β-actin:上游,5′-ATTGGCAATGAGCGGTTC-3′,下游,5′-GGATGCCACAGGACTCCAT-3′。
1.2.3 酸暴露及胆酸诱导下LINC00261表达水平的变化将人胚胎干细胞培养于人胚胎成纤维细胞饲养层;设置一定的酸暴露及胆酸梯度[4],与处于对数生长期的人胚胎干细胞共孵育24、48、72 h后提取细胞总RNA;qRT-PCR法检测LINC00261的表达,以β-actin为内参。
1.2.4 慢病毒转染我们构建了LINC00261慢病毒表达载体(LV-LINC00261,北京唯尚立德生物科技有限公司),以其转染处于对数生长期的人胚胎干细胞(MOI=20),24 h后更换培养基,继续培养48 h后行qRT-PCR检测(LINC00261)及Western blot检测(FOXA2),以携带无意义序列的重组慢病毒载体LV-NC作为阴性对照;以FOXA2慢病毒表达载体(LV-FOXA2,北京唯尚立德生物科技有限公司)转染处于对数生长期的人胚胎干细胞(MOI=20)24 h后更换培养基,6 h后将其置于酸暴露及胆酸条件培养基内,48 h后提取细胞总蛋白,Western blot检测FOXA2、CDX2及肠型分化标志黏蛋白2(mucin 2,MUC2)蛋白表达水平变化,以β-actin表达水平为内参。
1.3 统计学分析采用SPSS 17.0统计软件进行分析,实验数据以x±s表示,行Student-t检验或ANOVA方差分析,P < 0.05认为差异具有统计学意义。
2 结果 2.1 LINC00261在食管腺癌组织标本及相关细胞系中的表达我们利用qRT-PCR检测了20例正常食管鳞状上皮组织,20例BE组织及20例食管腺癌组织中LINC00261的表达,结果提示在BE及食管腺癌组织标本中,LINC00261表达较正常食管鳞状上皮组织均显著上调(P < 0.01,图 1A);进一步,我们检测了LINC00261在正常食管鳞状上皮细胞系(Het-1A)、BE细胞系(BE CP-A)及BE相关腺癌细胞系(OE33和skgt4)中的表达,结果提示在BE细胞系及BE相关腺癌细胞系中,LINC00261表达水平较正常食管鳞状上皮细胞系显著增高(P < 0.05,图 1B)。

|
| A:LINC00261在正常食管鳞状上皮组织、BE组织及食管腺癌组织中的表达;B:LINC00261在相关细胞系中的表达(以Het-1A表达量为1) a:P < 0.05,与Het-1A比较;b:P < 0.05,与BE CP-A比较 图 1 qRT-PCR检测LINC00261在食管腺癌组织标本及相关细胞系中的表达 |
2.2 酸暴露及胆酸诱导下LINC00261表达水平的变化
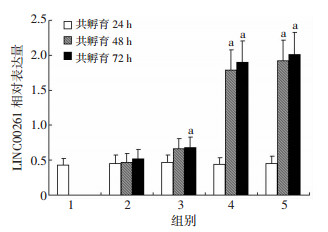
我们以生长于人胚胎成纤维细胞饲养层的人胚胎干细胞为细胞模型,初步证实在酸暴露及胆酸诱导下,其LINC00261表达可显著上调(P < 0.05),并表现出一定的浓度依赖性及时间依赖性(图 2)。
|
| 1:对照组;2:0 μmol/L组;3:100 μmol/L组;4:300 μmol/L组;5:1 000 μmol/L组a:P < 0.05,与对照组比较 图 2 qRT-PCR检测酸暴露及胆酸诱导下人胚胎干细胞LINC00261表达变化 |
2.3 生物信息学分析提示LINC00261参与FOXA2表达调控
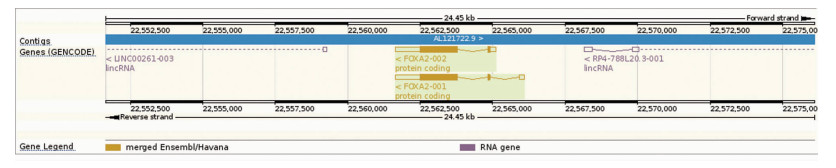
LINC00261全长4 924 bp,定位于染色体20p11.21 (22 541 191~22 559 280),利用生物信息学分析的方法(www.ensembl.org),我们发现其恰好位于叉头框蛋白A2(forkhead box protein A2, FOXA2)(22 561 643~22 566 093)上游启动子区域(图 3)。提示LINC00261可能参与FOXA2表达的负性调控。
|
| 图 3 生物信息学分析提示LINC00261位于FOXA2上游启动子区域 |
2.4 LINC00261慢病毒转染对FOXA2表达的影响
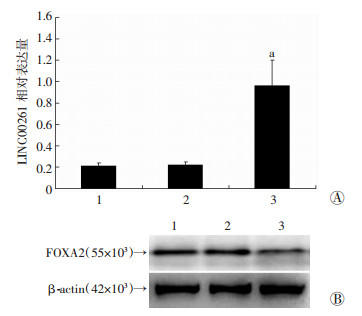
为了证实LINC00261可负性调控FOXA2的表达,我们构建了LINC00261慢病毒载体并转染人胚胎干细胞,结果如图 4所示,LINC00261表达水平的上调可显著抑制FOXA2蛋白的表达水平(P < 0.05)。
|
| 1:对照组;2:LV-NC;3:LV-LINC00261 A:qRT-PCR检测结果;B:Western blot检测结果a:P < 0.05,与对照组及LV-NC比较 图 4 LINC00261慢病毒转染对FOXA2表达的影响 |
2.5 上调FOXA2表达对酸暴露及胆酸诱导下CDX2表达及细胞分化表型等的影响
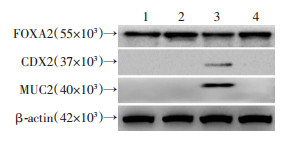
我们利用FOXA2慢病毒表达载体转染人胚胎干细胞,以探讨上调表达FOXA2表达对酸暴露及胆酸诱导下CDX2表达及细胞分化表型等的影响,结果如图 5所示,酸暴露及胆酸可诱导人胚胎干细胞FOXA2表达的下调及CDX2表达的上调(同时可以检测出相应柱状上皮标记物MUC2蛋白的表达);转染FOXA2后的人胚胎干细胞,在酸暴露及胆酸诱导下,其CDX2表达受抑(相应柱状上皮标记物MUC2蛋白表达也未检出),这一结果提示FOXA2上调表达可阻断人胚胎干细胞在酸暴露及胆酸诱导下CDX2表达及细胞分化表型的变化。
|
| 1:对照组;2:LV-FOXA2转染组;3:AB诱导组(AB指acid and bile,A:acid,pH=5;B:bile acid,混合胆酸,总剂量为300 μmol/L);4:LV-FOXA2+AB组 图 5 上调FOXA2表达对酸暴露及胆酸诱导CDX2、MUC2蛋白表达的影响 |
3 讨论
lncRNA是一类转录本长度超过200nt的RNA分子。人体内,lncRNA在数量上占全部ncRNA转录的大部分,它们的编码基因在基因组范围内的分布也非常广泛,它们并不编码蛋白,因而其一度被认为是转录的“噪音”。但近年的研究显示,lncRNA通过表观遗传修饰与转录调控、转录后加工、翻译调控等多种机制,在细胞生命活动中发挥重要作用。
lincRNA是一类位于编码蛋白基因之间,长度超过200nt的长链非编码RNA (位于基因间的lncRNA)[5-6]。人体内有数以千计的lincRNA,但目前已明确具体功能的不足1%。HOX转录反义RNA (HOX transcript antisense RNA,HOTAIR)是第1个被发现具有反式调控作用的lincRNA,定位于人类染色体12q13.13区域HOX基因家族HOXC11基因的反义链,编码2.2 kb长链非编RNA分子,不编码任何蛋白质。HOTAIR在乳腺癌、胰腺癌、肝细胞癌、胃肠道间质瘤等多种恶性肿瘤中表达显著上调,并与肿瘤的分期、转移及生存等密切相关。目前研究显示,HOTAIR可通过与多梳蛋白抑制复合物2(polycomb repressivecomplex 2,PRC2)共同作用,调控组蛋白H3第27位赖氨酸的三甲基化,从而影响p21 PTEN及WIF1等基因的表达,并通过这些基因调控p53、Wnt及Akt等信号通路,从而在肿瘤的细胞周期、凋亡、血管生成、侵袭及转移等过程中发挥重要生物学功能[6-7]。lincRNA-ANRIL、lincRNA-Xist等目前也已被证实在人体细胞发育及肿瘤发生过程中发挥重要的调节作用[8]。
LINC00261是一利用RNA测序技术发现的在BE组织及BE相关腺癌组织中上调表达的lincRNA,其较正常食管上皮组织上调表达倍数在所发现异常上调表达的32种lncRNA中均最为显著,分别为48.79和181.82倍[3]。在本研究中,我们利用qRT-PCR技术检测了20例正常食管鳞状上皮组织,20例BE组织及20例食管腺癌组织中LINC00261的表达,结果显示在中国人群BE及食管腺癌组织标本中,LINC00261表达较正常食管鳞状上皮组织均显著上调,这一结果提示LINC00261的异常表达可能与BE的发生及发展有关。BE的发生与胃食管反流相关性炎症密切相关。胃食管反流发生时,酸暴露和胆汁引起食管黏膜微环境的改变,其通过对多种细胞与因子的相互作用,引起机体多种生理与病理信号网络的改变,尤其是引起食管干细胞的分化异常,致其向柱状上皮细胞分化,最终导致BE发生[9-11]。我们利用人胚胎干细胞为细胞模型,也初步证实酸暴露及胆酸可诱导LINC00261的表达,进一步提示LINC00261的异常表达参与了BE的发生与发展。
LINC00261定位于染色体20p11.21(22 541 191~22 559 280),利用生物信息学分析的方法,我们发现其恰好位于FOXA2(22 561 643~22 566 093)上游启动子区域。FOXA2是叉头框转录因子家族的一个重要成员,其在哺乳动物胚胎早期发育、器官发生阶段及成体时期体内代谢和内环境稳定等诸多方面发挥重要作用[12-14]。目前的研究表明FOXA2在干细胞向肝细胞、心肌细胞及神经细胞等的分化中起着关键性调节作用[12-14]。lincRNA可通过招募形成染色质修饰复合物等多种方式干扰或沉默邻近基因转录,例如SER3、XIST等[5]。因此我们推测LINC00261可能参与FOXA2表达的负性调控。尾型同源盒转录因子-2(caudal-related homeobox transcription factor-2,CDX2)是影响食管干细胞分化方向的一个关键因素,其表达上调引起食管干细胞转分化为柱状上皮细胞,BE发生[15]。FOXA2是CDX2转录调控的关键调节子,Watts等[16]利用转基因鼠模型证实在胚胎发育过程中FOXA2可预先结合于CDX2启动子+7 kb区域,并招募负性转录调控因子Rfx1(regulatory factor x 1)等以抑制CDX2的转录,且这一机制在多种组织发育过程中均存在。据此,我们推测:在BE的发生、发展过程中,炎性因素可诱导LINC00261异常上调表达,其干扰或沉默FOXA2基因的转录,进而通过调节CDX2等的表达发挥其生物学功能。为了证实这一猜想,我们首先检测了LINC00261慢病毒转染对FOXA2表达的影响,结果显示LINC00261表达水平的上调可显著抑制人胚胎干细胞FOXA2蛋白的表达水平(P < 0.05);进一步,我们探讨了上调FOXA2表达对酸暴露及胆酸诱导下CDX2表达及细胞分化表型等的影响,结果证实FOXA2上调表达可阻断人胚胎干细胞在酸暴露及胆酸诱导下CDX2表达及细胞分化表型的变化。上述这些结果提示FOXA2是LINC00261参与BE发生的重要节点分子。
本实验结果显示LINC00261在BE的发生过程中发挥关键作用,其可能与负性调控FOXA2的基因转录有关。在进一步的实验中,我们将利用Co-IP、CHIP等方法探讨LINC00261负性调控FOXA2表达的具体分子机制,其将为BE发生及针对性预防和治疗提供新的思路。
| [1] | 房殿春, 林三仁, 于中麟, 等. Barrett食管诊治共识(修订版, 2011年6月重庆)[J]. 胃肠病学,2011, 16 (8) : 485 –486. |
| [2] | 张亚飞, 王鹏, 房殿春. Barrett食管相关腺癌的组织病理学诊断[J]. 重庆医学,2011, 40 (10) : 1031 –1033. |
| [3] | Yang X, Song J H, Cheng Y, et al. Long non-coding RNA HNF1A-AS1 regulates proliferation and migration in oesophageal adenocarcinoma cells[J]. Gut,2014, 63 (6) : 881 –890. DOI:10.1136/gutjnl-2013-305266 |
| [4] | Sun Y G, Wang X W, Yang S M, et al. Inhibition of nucleostemin upregulates CDX2 expression in HT29 cells in response to bile acid exposure: implications in the pathogenesis of Barrett's esophagus[J]. J Gastrointest Surg,2009, 13 (8) : 1430 –1439. DOI:10.1007/s11605-009-0899-2 |
| [5] | 朱鹏飞, 张慧媛, 孙文靖, 等. LincRNA的研究进展[J]. 国际遗传学杂志,2012, 35 (1) : 6 –9. |
| [6] | 李雨薇, 王裕民, 张雪莹, 等. 长链非编码RNA HOTAIR在恶性肿瘤中的研究进展[J]. 生物化学与生物物理进展,2015, 42 (3) : 228 –235. |
| [7] | Hajjari M, Salavaty A. HOTAIR: an oncogenic long non-coding RNA in different cancers[J]. Cancer Biol Med,2015, 12 (1) : 1 –9. DOI:10.7497/j.issn.2095-3941.2015.0006 |
| [8] | Dey B K, Mueller A C, Dutta A. Long non-coding RNAs as emerging regulators of differentiation, development, and disease[J]. Transcription,2014, 5 (4) : e944014 . DOI:10.4161/21541272.2014.944014 |
| [9] | Sarosi G, Brown G, Jaiswal K, et al. Bone marrow progenitor cells contribute to esophageal regeneration and metaplasia in a rat model of Barrett's esophagus[J]. Dis Esophagus,2008, 21 (1) : 43 –50. DOI:10.1111/j.1442-2050.2007.00744.x |
| [10] | Nicholson A M, Graham T A, Simpson A, et al. Barrett's metaplasia glands are clonal, contain multiple stem cells and share a common squamous progenitor[J]. Gut,2012, 61 (10) : 1380 –1389. DOI:10.1136/gutjnl-2011-301174 |
| [11] | Doupé D P, Alcolea M P, Roshan A, et al. A single progenitor population switches behavior to maintain and repair esophageal epithelium[J]. Science,2012, 337 (6098) : 1091 –1093. DOI:10.1126/science.1218835 |
| [12] | Arenas E. Foxa2: the rise and fall of dopamine neurons[J]. Cell Stem Cell,2008, 2 (2) : 110 –112. DOI:10.1016/j.stem.2008.01.012 |
| [13] | Kaestner K H. The FoxA factors in organogenesis and differentiation[J]. Curr Opin Genet Dev,2010, 20 (5) : 527 –532. DOI:10.1016/j.gde.2010.06.005 |
| [14] | Zhu H. Forkhead box transcription factors in embryonic heart development and congenital heart disease[J]. Life Sci,2016, 144 : 194 –201. DOI:10.1016/j.lfs.2015.12.001 |
| [15] | Nakagawa H, Whelan K, Lynch J P. Mechanisms of Barrett's oesophagus: intestinal differentiation, stem cells, and tissue models[J]. Best Pract Res Clin Gastroenterol,2015, 29 (1) : 3 –16. DOI:10.1016/j.bpg.2014.11.001 |
| [16] | Watts J A, Zhang C, Klein-Szanto A J, et al. Study of FoxA pioneer factor at silent genes reveals Rfx-repressed enhancer at Cdx2 and a potential indicator of esophageal adenocarcinoma development[J]. PLoS Genet,2011, 7 (9) : e1002277 . DOI:10.1371/journal.pgen.1002277 |



