2. 050011 石家庄,河北医科大学第四医院:消化内科
2. Department of Gastroenterology, the Fourth Affiliated Hospital of Hebei Medical University,Shijiazhuang, Hebei Province, 050011, China
胃癌是严重威胁人类健康的消化系统恶性肿瘤。虽然近年来胃癌的发病率有所下降,但病死率和复发率却无明显改善[1-2]。胃癌病因中遗传因素有较为重要的意义[3-4]。胃癌早期无特异性症状,难以引起患者的重视。待症状明显时多已处于中晚期,许多患者失去了手术根治的机会。因此,采用简便的方法,找到胃癌的易感基因,对胃癌的防治有重要的临床意义。丝氨酸蛋白酶抑制剂B1(serine protease inhibitor,clade B,member 1,Serpin B1)是蛋白酶抑制剂家族成员之一,能通过与多种蛋白酶活性部位不可逆结合,阻止酶原活化、表达、分泌、降解等作用以减少蛋白酶的生成或调节蛋白酶的水解活性,使蛋白酶水解减少,活性减弱,从而维持体内稳定[5-6]。当其发生活性或功能变化时,可能造成肿瘤的发生。有研究表明,Serpin B1对肝癌细胞有调控作用[7],我们前期研究也发现Serpin B1基因与胃癌分化有关[8],但目前关于外周血Serpin B1基因多态性与胃癌之间关系尚不清楚。本研究检测了胃癌患者和健康人群外周血中Serpin B1基因H67Q位点多态性的分布差别以及不同基因型中Serpin B1浓度水平的变化情况,探讨Serpin B1与胃癌的发生、发展之间的联系。
1 材料与方法 1.1 研究对象选取2013年1月至2015年12月河北医科大学第四医院就诊并确诊为胃癌的350例患者作为病例组,均有病理学确诊。患者纳入标准:①有病理学证据确诊为胃癌;②患者均为初诊患者;③入组者未经过放疗、化疗、生物治疗等措施。排除标准:①合并其他恶性肿瘤患者;②复发或手术后患者;③合并严重肝肾、血液系统、免疫系统疾病患者;④经过术前治疗的患者;⑤妊娠期患者;⑥不能配合或不愿配合的患者。其中男性201例,女性149例,年龄(51.7±10.8)岁。选取同期来我院查体的健康人350例为对照组。其中男性203例,女性147例,年龄(51.3±13.3)岁。两组性别、年龄匹配,具有可比性。本研究由医院伦理委员会批准,研究对象均签署知情同意书。
1.2 方法 1.2.1 标本采集所有入选者晨起空腹抽取静脉血6mL,4 mL放入促凝管中,室温静置30 min,3 500 r/min 离心(1 760×g)15 min,分离血清,-20 ℃ 冻存备用;2 mL放入EDTA-K2抗凝管中,充分混匀,-80 ℃ 冻存备用。
1.2.2 血清Serpin B1浓度的检测选用人SERPINB1酶联免疫吸附测定(ELISA)试剂盒(美国 R&D公司,货号:20151113)。使用前室温平衡30 min,严格按照说明书操作。准确性:R≥0.990 0,灵敏度:最低检测浓度<0.5 ng/mL,板内、板间变异系数均<15%,用酶免之星全自动酶标仪在450 nm处测定光密度值[D(450)],检测读数,计算样品浓度。
1.2.3 基因组DNA的提取EDTA-K2抗凝血应用TIANamp Genomic DNA Kit 血液/细胞/组织基因组DNA提取试剂盒(离心柱型,DP304),严格按照试剂盒说明书的规定操作,提取基因组DNA。
1.2.4 扩增目的基因Serpin B1基因H67Q位点引物序列:上游为5′-ACTTTATAGTTTCAAAATAA-3′,下游5′-TTTTAGAATGTGAAGGGCAA-3′。建立由上下游引物、dNTP、模板DNA、Taq DNA聚合酶、MgCl2、10×扩增缓冲液组成的总体积为50 μL的PCR反应体系,先后经过预变性、变性、退火、延伸等实验过程条件下进行PCR 扩增,扩增完成,取反应后体系中5 μL PCR扩增产物,经2%琼脂糖电泳检测确认并与标准(TaKaRa,150 bp)进行比较,判断PCR扩增产物的准确性。
1.2.5 DNA序列分析将扩增的PCR产物纯化,应用超高通量基因组测序系统GS FLX+系统(Roche Applied Science,型号GS FLX+ System)双向测序,得出PCR产物的基因组序列图。应用DNAMAN软件将测定结果与GenBank查询确定的基因序列进行比对,比较两者基因序列的差异。
1.3 统计学处理采用SPSS 13.0统计软件。计量资料以x±s表示,组间比较采用t检验;计数资料以百分率(%)表示,组间比较采用χ2检验;应用Logistic回归分析Serpin B1基因H67Q位点多态性与胃癌之间的关系。检验水准:α=0.05。
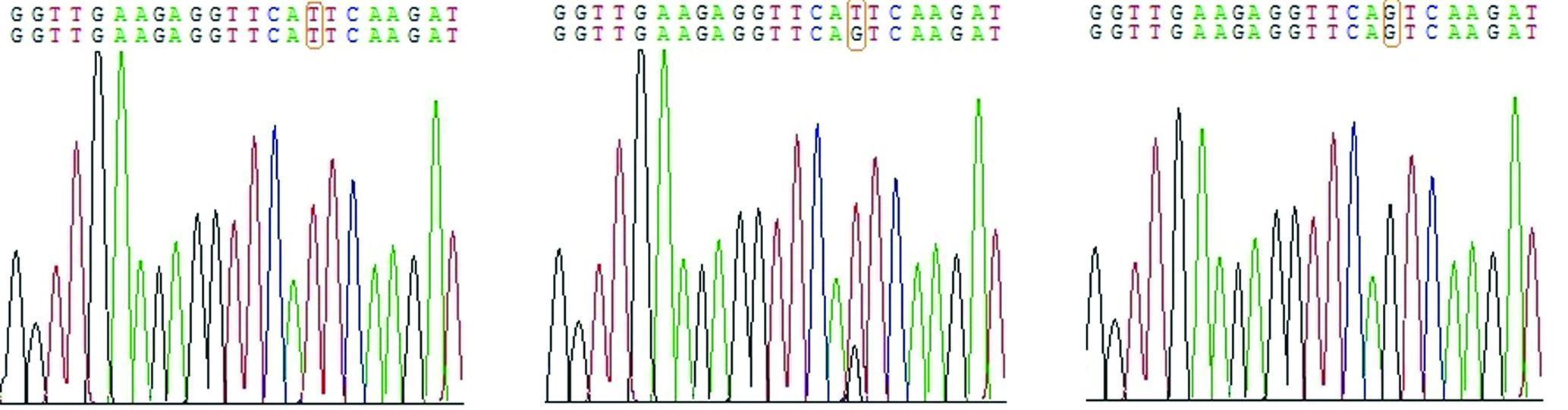
2 结果 2.1 Serpin B1基因H67Q位点直接测序结果PCR产物纯化后双向测序结果显示,Serpin B1基因H67Q位点存在2种等位基因G和T,共有3种基因型:纯合突变型(GG)、杂合突变型(GT)、野生型(TT)。Serpin B1基因H67Q位点发生突变,该突变位于第2外显子,所在区域编码Serpin B1蛋白的RSL环状结构区,第201位碱基由T突变为G,使第67位氨基酸由CAT突变为CAG,即异亮氨酸突变为苯丙氨酸。结果见图 1。
|
| A:TT基因型;B:GT基因型;C:GG基因型 图 1 Serpin B1基因H67Q位点多态性基因序列 |
2.2 Serpin B1基因H67Q位点多态性基因型和等位基因频率分布
病例组与对照组基因型分布比较,差异有统计学意义(χ2=91.95,P<0.01);病例组GG基因型频率、GT基因型频率,均显著高于对照组(χ2=37.41,66.83,P<0.01)。病例组G等位基因频率显著高于对照组(χ2=110.90,P<0.01,表 1)。
| 组别 | n | 基因型 | 等位基因 | |||
| TT | GT | GG | T | G | ||
| 病例组 | 350 | 210(62.0) | 92(26.3)a | 48(13.7)a | 512(73.1) | 188(26.9)a |
| 对照组 | 350 | 319(91.1) | 20(5.7) | 11(3.1) | 658(94.0) | 42(6.0) |
| a:P<0.01,与对照组比较 | ||||||
2.3 不同基因型间Serpin B1浓度水平的比较
病例组中Serpin B1的浓度明显高于对照组(t=145.7,P<0.01)。病例组中,GG基因型Serpin B1的浓度明显高于GT基因型和TT基因型(t=2.846,P<0.01;t=8.895,P<0.01);GT基因型Serpin B1的浓度明显高于TT基因型(t=7.341,P<0.01)。对照组中,GG基因型Serpin B1的浓度明显高于GT基因型和TT基因型(t=36.490,P<0.01;t=43.593,P<0.01);GT基因型Serpin B1的浓度明显高于TT基因型(t=9.630,P<0.01,表 2)。
| 组别 | 例数 | Serpin B1浓度(ng/mL) |
| 病例组 | 350 | 295.3±34.6a |
| GG基因型 | 48 | 333.5±48.2abc |
| GT基因型 | 92 | 312.4±37.8ab |
| TT基因型 | 210 | 279.1±35.6a |
| 对照组 | 350 | 22.7±5.3 |
| GG基因型 | 11 | 67.3±2.7bc |
| GT基因型 | 20 | 28.5±2.9b |
| TT基因型 | 319 | 20.8±3.5 |
| a:P<0.01,与对照组比较;b:P<0.01,与TT基因组比较;c:P<0.01,与GT基因组比较 | ||
2.4 Logistic回归分析Serpin B1基因H67Q位点多态性与胃癌间的关系
以是否患有胃癌(无=0,胃癌=1)为因变量,以年龄(<50岁=0,≥50岁=1)、性别(男=0,女=1)、Serpin B1基因H67Q位点基因型(Tt=0,Gt=1,GG=2)、 等位基因(t=0,G=1)、Serpin B1浓度为自变量,进行分析。结果显示,GG基因型、G等位基因与胃癌关系密切,GG基因型、G等位基因是胃癌的独立危险因素(表 3)。
| 变量 | B | SE | Wald | P | OR | 95%CI |
| 年龄 | 0.374 | 0.389 | 1.246 | 0.213 | 0.853 | 0.437~1.168 |
| 性别 | 0.268 | 0.317 | 2.067 | 0.325 | 0.629 | 0.418~1.023 |
| Serpin B1浓度 | 0.167 | 0.228 | 1.925 | 0.116 | 0.924 | 0.504~1.429 |
| 基因型 | 3.016 | 0.402 | 13.275 | 0.006 | 9.485 | 2.169~44.283 |
| 等位基因 | 0.698 | 0.163 | 2.371 | 0.014 | 5.105 | 1.847~13.360 |
3 讨论
当前胃癌为严重威胁人类生命健康的重要疾病。胃癌的发生与多种因素有关,遗传因素在其中为重要因素[9]。确定与胃癌发生、发展相关的基因意义重大。本课题组前期研究发现Serpin B1基因与胃癌有关[8],但具体情况尚不清楚。其他研究也发现Serpin B1基因与恶性肿瘤有关[7]。为了解Serpin B1蛋白及基因多态性在胃癌患者外周血的表达及意义,本研究检测了外周血中Serpin B1的水平以及Serpin B1基因H67Q位点的多态性。
Serpin B1属于蛋白酶抑制因子家族,广泛存在动植物体内,其主要作用为调节丝氨酸蛋白酶的生物活性。其蛋白结构含有9个α-螺旋和3个β-折叠,并形成RSL环状结构区,用于与靶向酶识别并共价结合,从而改变靶向蛋白酶的活性和功能[10-11]。当Serpin B1出现结构异常或功能异常时,蛋白酶的水解反 应将失去控制,可能引起疾病的发生。本研究结果显示,与对照组相比较,胃癌患者外周血中Serpin B1的水平升高,就证实了Serpin B1可能与胃癌的发生有关。
Serpin B1蛋白由379个氨基酸残基组成,当Serpin B1基因发生突变时,Serpin B1双螺旋结构的空间构象发生变化,Serpin B1蛋白的功能受到影响[12]。本研究中Serpin B1基因H67Q位点位于第2外显子,所在区域编码Serpin B1蛋白的RSL环状结构区,第201位碱基由T突变为G,使第67位氨基酸由CAT突变为CAG,即异亮氨酸突变为苯丙氨酸。该突变可能导致该区域结构异常,无法与蛋白酶识别结合,从而无法发挥其抑制作用。我们检测发现该单核苷酸多态性位点有G、T 2种等位基因,TT、GT、GG 3种基因型。
本研究发现病例组和对照组外周血均存在Serpin B1基因H67Q位点多态性。本研究表明,病例组中GG、GT 2种基因型所占的比例明显高于对照组中的2种基因型所占的比例;病例组中G等位基因的频率 (26.9%)远高于对照组中G等位基因的频率(6.0%)。 因此我们推测Serpin B1基因H67Q位点突变可能与胃癌的发生关系密切,但尚待更为深入的研究予以证实。
本研究进一步把入组者按GG、GT、TT基因型分成3组,比较病例组和对照组中不同基因型之间Serpin B1浓度的变化。结果发现病例组与对照组中GG基因型Serpin B1的浓度明显高于GT基因型和TT基因型者;GT基因型Serpin B1的浓度明显高于TT基因型者。从而证明Serpin B1基因H67Q位点突变影响了外周血中Serpin B1蛋白的水平。结果提示Serpin B1基因H67Q位点发生突变干扰了该基因的正常转录及翻译功能,使蛋白的抑制功能丧失,无法精准地控制细胞内外不断发生的各种各样的水解反应,破坏了机体内部环境的稳定,导致肿瘤发生。
为了解Serpin B1基因H67Q位点多态性与胃癌发生的关系,本研究进行了Logistic回归分析。结果显示GG基因型、G等位基因是胃癌发生的重要危险因素,说明Serpin B1基因H67Q位点突变与胃癌有关,检测外周血Serpin B1基因H67Q位点多态性可能对预测胃癌发生有益。
总之,本研究发现胃癌患者外周血中存在Serpin B1基因H67Q突变,且该突变为胃癌发生的危险因素。因此,检测Serpin B1基因H67Q位点多态性,对早期发现、早期诊断胃癌有益;外周血Serpin B1蛋白的检测也可能作为新的胃癌标志物。但本研究为单中心研究,尚需扩大研究规模并对Serpin B1基因的突变进行深入分析。
| [1] | Li Y, Zhao Q, Fan L Q, et al. Zinc finger protein 139 expression in gastric cancer and its clinical significance[J]. World J Gastroenterol,2014, 20 (48) : 18346 –18353. DOI:10.3748/wjg.v20.i48.18346 |
| [2] | Zhang Z D, Li Y, Fan Q, et al. Annexin A2 is implicated in multi-drug-resistance in gastric cancer through p38MAPK and AKT pathway[J]. Neoplasma,2014, 61 (6) : 627 –637. DOI:10.4149/neo_2014_078 |
| [3] | Zhang M X, Liu K, Wang F G, et al. Association between CYP2E1 polymorphisms and risk of gastric cancer: An updated meta-analysis of 32 case-control studies[J]. Mol Clin Oncol,2016, 4 (6) : 1031 –1038. DOI:10.3892/mco.2016.824 |
| [4] | Nie X, Wang X, Lin Y, et al. SNP rs1059234 in CDKN1A Gene Correlates with Prognosis in Resected Gastric Adenocarcinoma[J]. Clin Lab,2016, 62 (3) : 409 –416. |
| [5] | Farley K, Stolley J M, Zhao P, et al. A serpinB1 regulatory mechanism is essential for restricting neutrophil extracellular trap generation[J]. J Immunol,2012, 189 (9) : 4574 –4581. DOI:10.4049/jimmunol.1201167 |
| [6] | Uchiyama K, Naito Y, Takagi T, et al. Serpin B1 protects colonic epithelial cell via blockage of neutrophil elastase activity and its expression is enhanced in patients with ulcerative colitis[J]. Am J Physiol Gastrointest Liver Physiol,2012, 302 (10) : G1163 –G1170. DOI:10.1152/ajpgi.00292.2011 |
| [7] | Cui X, Liu Y, Wan C, et al. Decreased expression of SERPINB1 correlates with tumor invasion and poor prognosis in hepatocellular carcinoma[J]. J Mol Histol,2014, 45 (1) : 59 –68. DOI:10.1007/s10735-013-9529-0 |
| [8] | Liu Y, Li Y, Tan B B, et al. Technique appraisement of comparative proteomics and screening of differentiation-related protein in gastric carcinoma[J]. Hepatogastroenterology,2013, 60 (123) : 633 –637. DOI:10.5754/hge12794 |
| [9] | Jia Z F, Wang L Z, Cao X Y, et al. CD24 genetic variants contribute to overall survival in patients with gastric cancer[J]. World J Gastroenterol,2016, 22 (7) : 2373 –2382. DOI:10.3748/wjg.v22.i7.2373 |
| [10] | Benarafa C, LeCuyer T E, Baumann M, et al. SerpinB1 protects the mature neutrophil reserve in the bone marrow[J]. J Leukoc Biol,2011, 90 (1) : 21 –29. DOI:10.1189/jlb.0810461 |
| [11] | Baumann M, Pham C T, Benarafa C. SerpinB1 is critical for neutrophil survival through cell-autonomous inhibition of cathepsin G[J]. Blood,2013, 121 (19) : 3900 –3907. DOI:10.1182/blood-2012-09-455022 |
| [12] | El Ouaamari A, Dirice E, Gedeon N, et al. SerpinB1 Promotes Pancreatic β Cell Proliferation[J]. Cell Metab,2016, 23 (1) : 194 –205. DOI:10.1016/j.cmet.2015.12.001 |



