2. 400038 重庆, 第三军医大学军事预防医学院营养与食品卫生学教研室
2. Department of Nutrition and Food Hygiene, College of Military Preventive Medicine, Third Military Medical University, Chongqing, 400038, China
电化学免疫传感器是将电分析化学技术与免疫反应相结合而建立的新型免疫分析技术。为了实现对目标物的准确快速分析,生物分子的固定及电信号的产生和增强至关重要。在生物分子固定化研究中,纳米材料因其具有表面效应、量子尺寸效应、宏观量子隧道效应等特殊物理化学性质而成为生物分子固定化的新型材料 [1-2]。石墨烯(GR)具有高的比表面积(2 630 m-2·g-1)、强导电性(103~104 S·m-1)、高韧性等特点,在电化学免疫传感器的研究中可用于增大电极比表面积和提高电极表面的电子传输能力 [3-4]。同时,金属纳米复合物、石墨烯纳米复合物等复合纳米材料因其具有导电性能强、比表面积大、催化性能高等协同效应而引起广泛关注 [5]。本研究通过对Pt@GR-chi复合膜构建的免疫传感器性能研究及其与PB-GR复合物构建的无试剂型免疫传感器的性能对照,探讨其性质及特性。
1 材料与方法 1.1 材料 1.1.1 主要试剂氯铂酸、氯金酸购于将来实业公司、牛血清白蛋白(BSA)、铁氰化钾、氯化亚铁石墨烯溶液(2 mg/mL)、壳聚糖、氧化铝(粒径;1 μm、0.3 μm、50 nm)、购于天津艾达恒晟科技发展有限公司;无水乙醇、甲胎蛋白(AFP)和AFP抗体(anti-AFP)购于郑州博赛生物技术有限公司;所有试剂均为分析纯;实验用水为超纯水。
1.1.2 主要仪器CHI 6800电化学分析仪(上海舜宇恒平科学仪器有限公司);超声波清洗器(致微仪器有限公司);酸度计;磁力搅拌器78AW-1;电子天平(BSA124S),赛多利斯科学仪器公司;实验采用三电极系统:参比电极为饱和甘汞电极,工作电极为玻碳电极,对电极为铂丝电极。
1.2 方法 1.2.1 纳米金的制备向100 mL沸水中迅速加入1 mL 1% 的氯金酸溶液,搅拌,再加入0.3 mL 10% 柠檬酸钠溶液,继续搅拌30 min,即制得纳米金的分散液,冷却装瓶备用。
1.2.2 Pt@GR-chi纳米复合物首先,将0.02 g壳聚糖(chi)加入100 mL醋酸(1%)中,搅拌,取1.0 mL石墨烯溶液加入5.0 mL 上述壳聚糖溶液,再加入0.25 mL的氯铂酸(1%)和硼氢化钠,2 h后制得Pt@GR-chi纳米复合物。
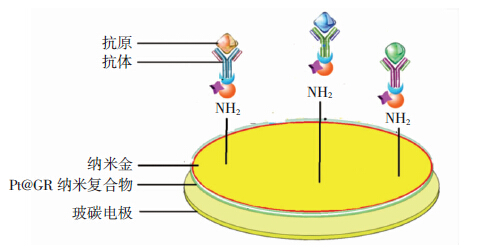
1.2.3 电化学免疫传感器的制备电化学免疫传感器的制备如图 1所示。将玻碳电极分别用1.0 μm、0.3 μm和50 nm的氧化铝粉于麂皮上打磨抛光,使之成镜面,然后无水乙醇和超纯水反复多次超声清洗,室温下自然晾干,然后滴加10 μL Pt@GR-chi纳米复合物溶液于电极表面,晾干后在纳米金溶液中浸泡 30 min,于anti-AFP 4 ℃下反应6 h,BSA封闭,即制得AFP免疫传感器。
|
| 图 1 电化学免疫传感器的制备过程及原理示意图 |
1.2.4 基于PB-GR复合物的免疫传感器制备
将六水合氯化亚铁6.0 mg、铁氰化钾8.0 mg、氯化钾 37 mg 混合于5 mL超纯水溶解,调节pH至1.5。将 2 mL 1 mg/mL GR加入上述溶液中,搅拌24 h,离心洗涤3次,即得到PB-GR复合物,分散在10 mL蒸馏水中。最后将1 mL 1 mg/mL的CS悬浮液加到3 mL 1 mg/mL PB-GR溶液中,搅拌,离心洗涤,再分散于蒸馏水中。将10.0 μL上述溶液滴涂到洁净的玻碳电极表面,在Pt/Au纳米复合物中浸泡6 h,孵育AFP抗体 6 h,用HRP封闭0.5 h,制得传感器,于4 ℃冰箱中保存备用。
1.2.5 测试方法利用循环伏安法(cyclic voltammetry,CV)、示差脉冲伏安法(differential pulse voltammetry,DPV)和三电极系统(参比电极为饱和甘汞电极,工作电极为玻碳电极,对电极为铂丝电极)对电极进行表征,测试底液为 0.5 mmol/L的铁氰化钾溶液(含0.1 mol/L氯化钾)和不同的pH的0.5 mol/L醋酸盐缓冲溶液(含0.1 mol/L氯化钾)及不同pH的磷酸缓冲液。
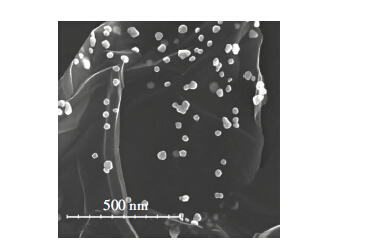
2 结果 2.1 Pt@GR-chi 复合纳米材料的SEM表征本实验采用扫描电子显微镜(SEM)对复合纳米材料进行了表征,结果如图 2所示。从途中可以看到,片状的石墨烯分散在壳聚糖溶液中,铂纳米颗粒较均匀地附着在石墨烯的表面,表明该复合纳米材料得以成功合成。
|
| 图 2 Pt@GR-chi 复合纳米材料的SEM表征图 |
2.2 不同修饰电极的电化学表征
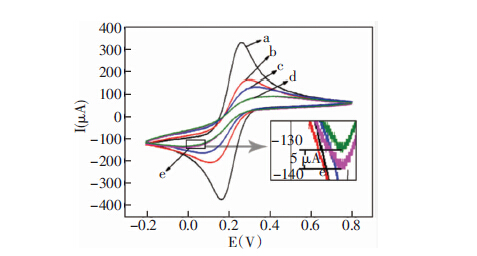
本实验研究运用循环伏安法对免疫传感器的修饰过程进行表征,结果如图 3所示。玻碳电极打磨抛光清洗干净后的循环伏安表征图为a曲线,该曲线出现一对可逆的氧化还原峰,为铁氰化钾的氧化还原峰,峰电位差值为89 mV。滴加10μL的Pt@GR-chi纳米复合物修饰后,由于壳聚糖导电性差,阻碍了电子的传递,氧化还原峰的电位下降(曲线c),沉积一层纳米金后,氧化还原峰有所增加(曲线b),这是由于纳米金有促进电子传输的作用导致的。纳米金可通过共价键和作用固载anti-AFP抗体,由于蛋白分子具有电化学惰性,阻碍电子传输,因此图中(曲线d)电流有明显降低。牛血清白蛋白(BSA)用于封闭电极表面的非特异性吸附位点,导致响应电流的进一步下降(曲线e)。循环伏安表征结果表明,该免疫传感器得以成功构建。
|
| 测试底液为0.5 mmol/L的铁氰化钾溶液(含氯化钾):(a)GCE(b)Au/Pt@GR/GCE(c)Pt@GR/GCE(d)anti-AFP/Au/Pt@GR/GCE(e)BSA封闭 图 3 不同修饰电极的循环伏安法表征 |
2.3 实验条件的优化 2.3.1 测试底液pH的优化
将免疫传感器置于一系列pH (5.0,5.5,6.0,6.5,7.0,7.5)的缓冲溶液中进行电化学表征,实验结果如图 4所示。从图中可以看出,免疫传感器的氧化还原峰电流值随着测试底液的pH增大而减小,pH 6.5~7.0时,响应电流较稳定,继续增大pH反而导致电流的升高。其原因主要是:pH值过高或过低均对生物分子的活性造成影响,同时pH也影响免疫复合物的稳定性,是影响免疫反应平衡的重要因素。基于此,本研究选择pH 6.5为最适pH。

|
| 图 4 pH对免疫传感器的影响 |
2.3.2 孵育时间优化
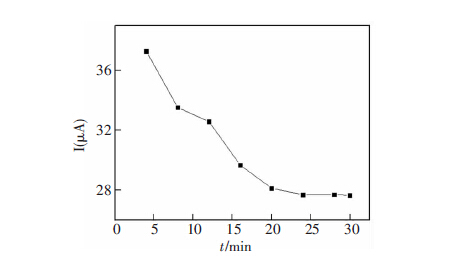
抗原抗体的反应时间直接影响到免疫反应进行程度,通过控制孵育时间这一单一变量研究其对免疫传感器响应的影响。将免疫传感器的孵育时间按一定规律变化,结果如图 5所示。从图中可以看出,随着孵育时间的增加,氧化还原峰电位逐渐降低,说明生成的免疫复合物逐渐增多,到24 min时曲线趋于平台,说明免疫反应达到平衡。因此,本研究选择24 min为孵育时间。
|
| 图 5 孵育时间对响应电流的影响 (AFP 5 ng/mL) |
2.3.3 底物催化对免疫传感器的信号增强作用
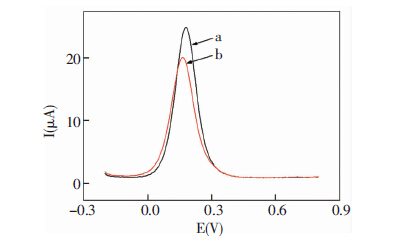
本实验研究了H2O2对免疫传感器响应电流的增强效应。将制备好的电极与10 ng/mL AFP孵育,研究测试底液中H2O2对传感器响应的影响。结果如图 6所示,b为测试底液中无H2O2的表征图,曲线a为在测试底液中加入4 mmol/L H2O2的表征图,可以看到,曲线a的响应电流明显高于曲线b,证明该免疫电极对H2O2的氧化还原有明显的催化作用。
|
| a: 测试底液中有4 mmol/L H2O2; b: 测试底液中H2O2 图 6 免疫传感器底物催化作用的DPV表征图 |
2.4 免疫传感器的性能研究 2.4.1 免疫传感器的响应性能研究
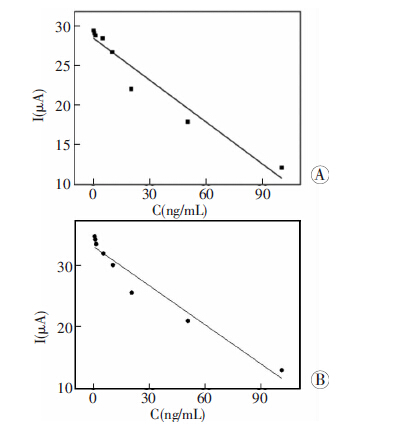
在最佳实验条件下,将该免疫传感器用于不同浓度AFP的检测,研究峰电流和抗原浓度之间的关系。图 7结果表明,在0.1~100.0 ng/mL浓度范围内,随着AFP浓度的增加,响应电流峰逐渐降低。左图为测试底液中未加入H2O2的测试结果,线性回归方程为y=28.668 45 -0.178 23x,检测限为0.04 ng/mL。右图为测试底液中加入4 mmol/L H2O2的测试结果,线性回归方程为y=33.183 38-0.215 08x,检测限为0.026 ng/mL。
|
| A:测试底液中未加入H2O2; B:测试底液中加入4 mmol/L H2O2 图 7 免疫传感器响应电流与AFP的浓度关系图 |
2.4.2 免疫传感器的稳定性、重现性
在最佳实验条件下,将传感器孵育50 ng/mL AFP后,于pH 6.5的测试底液(含4 mmol/L H2O2)中连续扫描100圈,其电流响应下降5.1%。放置30 d后,响应信号下降7.3%,说明该传感器有良好的稳定性。同时制备5支电极用于20 ng/mL的AFP检测,其结果(表 1)的相对标准偏差(RSD)值为 8.1%,说明该传感器重现性良好。
2.4.3 免疫传感器的选择性
本实验同时制备了6支免疫传感器以考察该传感器的选择性,将传感器于20 ng/mL 的HRP、CEA、NT-proBNP、BSA、IgG和 5 ng/mL 的AFP混合溶液孵育30 min,结果见表 2。结果表明,AFP的响应电流(I)与混合溶液的响应电流(I1)之差(△I)为0.008-0.032 μA,表明传感器具有良好的选择性。
2.4.4 回收率的测定
在血清样品中加入5个不同标准浓度的AFP的标准样品溶液,用该免疫传感器进行测定,其结果见表 3。其回收率值在96.4%~102.49%间,说明该传感器具有良好的准确性。
| 加入的标准浓度(ng/mL) | 检出浓度(ng/mL) | 回收率(%) |
| 1 | 0.97 | 97 |
| 5 | 5.12 | 102.4 |
| 10 | 9.85 | 98.5 |
| 20 | 19.28 | 96.4 |
| 25 | 25.21 | 100.84 |
2.4.5 临床应用
使用本研究提出的电化学免疫传感器和ELISA同时检测临床血清标本中AFP的含量,结果如图 8所示,两种检测方法的线性相关性为0.988 72。

|
| 图 8 免疫传感器与ELISA法血清样本检测结果相关性分析 |
2.5 基于PB-GR的免疫传感器研究
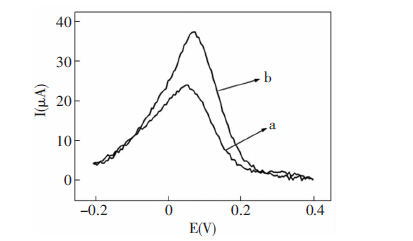
为了研究GR复合物在免疫传感器构建过程中的作用,本研究制备了基于PB-GR的免疫传感器,并对其性能进行了研究。首先考察了免疫传感器对过氧化氢氧化还原的催化作用,结果如图 9所示,从图中可以看到,测试底液中加入过氧化氢后,电信号有明显的上升,说明该传感器对过氧化氢的氧化还原有明显的催化作用。
|
| a: 测试底液中无H2O2; b:测试底液有4 mmol/L H2O2 图 9 免疫传感器酶催化DPV表征图 |
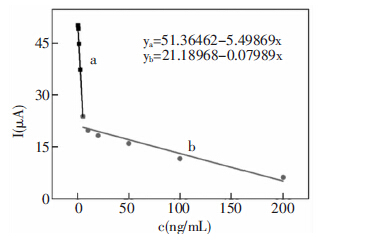
将该免疫传感器与不同浓度的AFP抗原溶液孵育,测定传感器响应电流与AFP浓度(0.1、0.5、1.0、3.0、5.0、10.0、20.0、50.0、100.0、200.0 ng/mL)之间的关系,结果如图 10所示。由图中可以看出,随着AFP浓度增加,传感器上的免疫复合物也越多,使其氧化还原峰电流逐渐减小,抗原浓度在0.1~5.0 ng/mL和5~200 ng/mL范围内与响应值成正比,检测限为0.03 ng/mL。
|
| 图 10 AFP抗原浓度与响应电流之间的关系 |
本实验将100 ng/mL的AFP抗原、100 ng/mL的AFP抗原与干扰物质[100 ng/mL的癌胚抗原(CEA)、25 ng/mL的HRP、0.25%的牛血清白蛋白(BSA)]等体积混合液孵育以考察其选择性。结果显示,免疫传感器在混合样品与相同浓度AFP的标准品的响应电流之差为0.007~0.029 μA。为了考察传感器的重现性,将5只免疫传感器同时与20 ng/mL AFP抗原孵育,测定5只免疫传感器对相同浓度抗原的响应差异。结果显示,5只免疫传感器的响应电流的相对标准偏差为4.8%。同时将免疫传感器与5 ng/mL AFP抗原孵育后4 ℃保存并对该免疫传感器的稳定性开展研究。连续测定100次,电流值下降6.2%。每5天测试一次,连续测试5次,结果表明,响应电流改变0.3%。
3 讨论 3.1 Pt@GR复合纳米材料对过氧化氢的氧化还原具有催化作用由于纳米铂对过氧化氢的氧化还原具有催化作用 [6-7],本研究采用原位合成法制备了Pt@GR复合纳米材料,通过对基于该复合膜的免疫传感器性能研究发现,在测试底液中加入过氧化氢可有效增强电流响应信号(图 6),说明Pt@GR复合纳米材料对过氧化氢的氧化还原具有催化作用。进一步将该免疫传感器分别置于含或不含过氧化氢的两种测试底液中进行测试,对比其灵敏度。结果显示:测试底液中含有过氧化氢的方法可获得更高的检测灵敏度,使检测限更低,亦可证实Pt@GR复合纳米材料对过氧化氢氧化还原的催化作用可有效增强电化学响应信号。
3.2 基于Pt@GR复合纳米材料构建的免疫传感器具有更高的灵敏度为了对Pt@GR复合纳米材料构建的免疫传感器进行性能评价,本实验构建了基于PB-GR复合物的免疫传感器,并对其性能进行了研究。通过对比发现,Pt@GR复合物构建的免疫传感器具有更高的灵敏度。与它研究相比,明显高于李艳 [8]、Yang [9]、Su [10]等研究的灵敏度,加标回收率也令人满意。其原因可能为:①原位合成法合成的Pt@GR纳米复合物的稳定性较直接合成的复合物稳定性高,复合程度大,可获得更强的催化放大信号。②Pt@GR纳米复合物的掺杂大大提高了电极的比表面积。③Pt和GR都具有强的导电性能,Pt@GR的掺杂,有效增强了壳聚糖膜的导电性能,增强了响应信号。④壳聚糖上大量的氨基可共价结合金纳米颗粒,进一步提高生物分子的固载量。
3.3 Pt@GR复合物构建的免疫传感器具有更好的稳定性传感器的制备过程中采用原位合成法制备了 Pt@GR 复合纳米材料。对传感器连续测试100次,其电流响应下降4.8%,低于PB-GR复合物构建的免疫传感器和李艳等 [8]基于多壁碳纳米管-壳聚糖-硫堇构建的传感器,表明基于该复合膜制备的传感器具有更好的稳定性。其原因是壳聚糖具有良好的成膜性,可以将Pt@GR纳米复合物稳定的修饰在电极表面,且原位合成法合成的Pt@GR纳米复合物的稳定性较直接合成的复合物稳定性高,有效增强了免疫传感器的稳定性。
3.4 PB-GR复合物构建无试剂型免疫传感器可有效简化操作流程电信号物质对电信号产生具有关键性作用,在传感器构建过程中,可通过在测试底液中加入电活性物质或将其固载到电极表面来指示电信号的变化。普鲁士蓝(PB)是电化学免疫分析过程中常用的电活性物质,因其对过氧化氢的催化作用有“人工过氧化物酶”之称,可通过对底物的催化作用获得增强的电化学响应信号(图 7),但普鲁士蓝在传感界面上易脱落,会导致免疫传感器的稳定性降低 [11-12],PB-GR复合物构建无试剂型免疫传感器将其PB固定在敏感膜中即可实现检测,无需向待测样品中加入媒介体或其他试剂,可有效简化操作流程,避免其他物质对检测的干扰。
综上,在敏感膜的构建过程中,石墨烯的掺杂可有效提高电子传输效率,结合纳米金属等具有催化活性的物质对底物的催化作用可有效增强响应信号,提高检测的灵敏度。同时,将电活性物质固载在电极表面可简化操作流程,提高分析效率。最后,原位合成法制备的石墨烯复合物具有良好的稳定性,可对提高检测的稳定性奠定基础。较现有方法而言,具有信号稳定、检测快速、低成本、无需标记技术等优点,在免疫分子的高灵敏检测中有广泛的应用前景。
| [1] | Yadav A, Danesh M, Zhong L, et al. Spectral plasmonic effect in the nano-cavity of dye-doped nanosphere-based photonic crystals[J]. Nanotechnology,2016, 27 (16) : 165703 . DOI:10.1088/0957-4484/27/16/165703 |
| [2] | 龚俊华, 郑峻松, 宋明辉, 等. 基于纳米金/多壁碳纳米管-普鲁士蓝-壳聚糖纳米复合物/蛋白A定向固定甲胎蛋白免疫传感器的研究[J]. 第三军医大学学报,2010, 3 (23) : 2478 –2482. |
| [3] | Cheng C K, Lin C H, Wu H C, et al. The Two-Dimensional Nanocomposite of Molybdenum Disulfide and Nitrogen-Doped Graphene Oxide for Efficient Counter Electrode of Dye-Sensitized Solar Cells[J]. Nanoscale Res Lett,2016, 11 (1) : 1 –9. DOI:10.1186/s11671-016-1277-0 |
| [4] | Wang Y, Zhang Y, Yan T, et al. Ultrasensitive electrochemical aptasensor for the detection of thrombin based on dual signal amplification strategy of Au@GS and DNA-CoPd NPs conjugates[J]. Biosens Bioelectron,2016, 80 : 640 –646. DOI:10.1016/j.bios.2016.02.042 |
| [5] | Garg B, Sung C H, Ling Y C. Graphene-based nanomaterials as molecular imaging agents[J]. Wiley Interdiscip Rev Nanomed Nanobiotechnol,2015, 7 (6) : 737 –758. DOI:10.1002/wnan.1342 |
| [6] | Wang L, Tricard S, Yue P, et al. Polypyrrole and graphene quantum dots @ Prussian Blue hybrid film on graphite felt electrodes: Application for amperometric determination of l-cysteine[J]. Biosens Bioelectron,2015, 77 : 1112 –1118. DOI:10.1016/j.bios.2015.10.088 |
| [7] | Hu T, Le Z, Wei W, et al. Enzyme catalytic amplification of miRNA-155 detection with graphene quantum dot-based electrochemical biosensor[J]. Biosens Bioelectron,2015, 77 : 451 –456. DOI:10.1016/j.bios.2015.09.068 |
| [8] | 李艳, 程平, 龚俊华, 等. 基于多壁碳纳米管-壳聚糖-硫堇纳米复合物修饰甲胎蛋白免疫传感器的研究[J]. 第三军医大学学报,2010, 32 (6) : 572 –575. |
| [9] | Yang H, Li Z, Wei X, et al. Detection and discrimination of alpha-fetoprotein with a label-free electrochemical impedance spectroscopy biosensor array based on lectin functionalized carbon nanotubes[J]. Talanta,2013, 111 : 62 –68. DOI:10.1016/j.talanta.2013.01.060 |
| [10] | Su B, Tang J, Chen H, et al. Thionine/nanogold multilayer film for electrochemical immunoassay of alpha-fetoprotein in human serum using biofunctional double-codified gold nanoparticles[J]. Anal Methods,2010, 2 (11) : 1702 –1709. DOI:10.1039/C0AY00468E |
| [11] | Lai G, Zhang H, Yu A, et al. In situ deposition of Prussian blue on mesoporous carbon nanosphere for sensitive electrochemical immunoassay[J]. Biosens Bioelectron,2015, 74 : 660 –665. DOI:10.1016/j.bios.2015.07.026 |
| [12] | Bu F X, Hu M, Zhang W, et al. Three-dimensional hierarchical Prussian blue composed of ultrathin nanosheets: enhanced hetero-catalytic and adsorption properties[J]. Chem Commun,2015, 51 (99) : 17568 –17571. DOI:10.1039/C5CC06281K |



