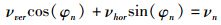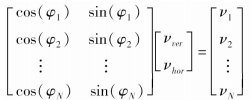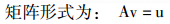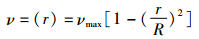目前临床广泛使用的超声血流速度检测方法主要为脉冲多普勒检测和彩色血流成像,但这两种方法局限于血流沿着超声波束方向的一维速度信息,检测结果受超声波束和血流方向之间角度影响。对动脉分叉处、有斑块的血管等伴随复杂血流情况的部位进行成像时,传统超声血流检测方法不能准确测量血流速度[1]。为了克服超声一维血流检测的不足,矢量血流成像(vector flow imaging)方法在近年被广泛研究[2-5],其可适用于上述复杂血流情况,提供成像平面内的二维血流速度信息(包括速度大小和方向),因而有望更准确地对复杂血流进行估计,进一步提供血管壁剪切应力等血流相关量化信息。
基于多普勒(Doppler)技术和散斑跟踪(speckle tracking,ST)的矢量复合算法是两种常用的矢量血流成像方法。其中,基于多普勒的矢量血流成像方法通过沿两个或多个方向进行一维多普勒血流速度测量,得到血流在不同方向上的速度分量,进而重建二维血流速度信息。该方法实现简单,计算量较小,但受到奈奎斯特采样率限制,即最大可测血流速度受到脉冲重复频率的限制。近年来,随着超高速超声成像的发展[6],这一问题被逐渐解决。基于ST的矢量血流成像方法通过在指定区域内追踪超声成像特有的散斑信息来检测血流速度。这种方法通常利用检测目标区域中相邻帧超声数据的二维互相关峰值或绝对误差和最小值等算法来实现,在算法实现过程中要保证较高的超声成像帧频,以提高帧间数据的相关性。本研究利用平面波发射的超高速超声成像技术,运用多普勒和ST方法获得血流速度,分别进行矢量血流成像。通过仿真、仿体及健康志愿者的颈动脉数据,对这两种方法进行比较。
1 方法 1.1 多普勒测量方法利用超声回波频移估计的自相关血流估计方法是目前广泛用于商用超声系统中的通用一维血流速度求解算法。
其中,c为超声传播速度,fprf为超声脉冲重复频率,f0为超声发射中心频率。通过估计同一深度超声信号沿时间方向的自相关Ȓ(1)即可求解沿超声波束方向的一维血流速度。
1.2 ST方法ST方法是通过跟踪超声回波信号特有的散斑信息来实现血流速度的测量。基本方法:在超声图像上选取适当尺寸的数据窗,在下一帧图像的对应位置附近搜索并确定散斑图像的最匹配位置,根据前后两帧之间数据窗与匹配位置的相对位移和时间间隔即可计算出血流速度值。依据此法对整幅超声图像中的数据窗进行最匹配位置的遍历搜索,即可得到整幅图像的血流速度。利用归一化互相关匹配算法(normalized cross correlation)对帧间二维射频数据窗进行二维搜索计算匹配程度[7],通过帧间参考窗与待匹配数据窗间的搜索得到获得最大归一化互相关值的侧向、轴向位移,同时根据数据侧向、轴向采样间距,帧间时间间隔,即可求得二维血流速度的大小和角度。对超声射频信号进行侧向线性插值可提高侧向速度测量精度,对互相关函数进行余弦插值[8]可进一步提高侧向和轴向速度测量精度。
1.3 矢量血流成像算法根据矢量分解原理,当超声发射角度为φn时,对于速度大小为ν、角度为α的血流速度矢量,有:
其中,νn为一维轴向速度分量。基于矢量分解原理和三角函数公式可得,水平和垂直方向血流速度分量νhor、νver可由下式求得:
因此,基于多角度平面波发射可得血流速度矢量ν=(νver,νhor)的矩阵计算公式如下:
二维血流速度矢量的求解即为求解速度矢量的垂直分量νver与水平分量νhor。将由多普勒和散斑跟踪方法测得的多组一维轴向速度分别代入式(4)引入最小二乘法,即可求得未知数νver和νhor,得到优化的具有最小误差平方和的速度矢量结果。
1.4 实验 1.4.1 数据发射与接收采用双模成像序列控制方式,具体成像参数见表 1。在B型超声成像中,采用基于平面波发射的超高速超声成像序列,以10 000 Hz为脉冲重复频率。为提高图像的分辨率与质量,采用平面波复合技术[9],沿着-10°~10°等间隔递增的7个倾斜角度发射平面波,采用多角度复合波束合成获得B型超声图像。在多普勒成像序列中,以脉冲重复频率6 000 Hz交替发射偏转角度分别为-10°与10°的平面波信号(选定平面波倾斜角度时注意在避免较大栅瓣干扰的前提下,获得更大的多角度平面波交叠视场范围)。因此,对应同一角度的实际脉冲重复频率为3 000 Hz,每发射60次做1次速度估计,即每一角度对应的慢时信号(相同采样深度不同次脉冲发射接收到的信号)采样点数为30,线阵全孔径接收获得通道数据。
| 成像类型 | 脉冲中心频率(MHz) | 脉冲长度(周期数) | 慢时信号点数 | 脉冲重复频率(Hz) | 慢时信号获取频率(Hz) | 发射接收通道数 | 阵元间距(mm) | 发射偏转角度(°) |
| 血流图 | 5.0 | 2.5 | 30 | 6 000 | 3 000 | 128 | 0.3 | ±10 |
| B型图像 | 7.5 | 2.0 | - | 10 000 | - | 128 | 0.3 | -10~10 |
1.4.2 仿真设置
应用超声仿真软件FIELD_Ⅱ,设置随机分布散射子模拟固定直管稳流模式,周围组织与血流散射子强度之比为40 dB,每单位面积约分布5/λ2个散射子,λ为对应中心频率的波长。散射子流动速度设定为遵循泊松叶公式的抛物线型血流分布,即:
其中,ν是随直管径向位置r而改变的速度值,νmax为最大速度值,R为直管半径。仿真模拟3个血管深度、血管直径、血管倾斜角度及管内血流速度不尽相同的3个固定直管。3个血管深度分别为2、3.5、5.5 cm,血管直径分别为4、8、12 mm,血管与水平方向之间夹角分别为0°、-5°、5°;管内最大流速分别为100、50、30 cm/s。
1.4.3 仿体及在体实验使用256发射接收通道的Vantage超声采集系统(Verasonics公司,美国)和L10-5线阵探头(嘉瑞公司,中国),对Gammax 1425A标准血流仿体(Gammax公司,美国)进行仿体实验。仿体中,在深度为2 cm处有一个直径5 mm的水平直管,分别设置血流仿体速度最大值是100、50、30 cm/s的恒速层流。利用同一采集系统对健康成人志愿者的颈动脉进行数据采集,成像参数同表 1。
1.5 数据处理和分析进行10次独立的血流仿真及仿体实验,对接收的通道数据,利用动态接收聚焦对每一个像素位置进行汉明窗变迹的波束合成,以降低信号旁瓣。对波束合成后的射频信号进行正交解调,使用二阶回归滤波器作壁滤波[10]以提高血流信号信噪比。以Matlab软件为数据处理平台,分别用多普勒和ST方法对实验数据进行矢量血流成像。结合10次实验中每个像素点的速度矢量测量值,计算水平、垂直速度分量的偏差和标准差,分析测量准确性与稳定性。根据设置速度大小不同,对仿真、仿体数据作ST时,所用数据窗大小分别为0.77 mm×0.89 mm,0.74 mm×1.48 mm(轴向×侧向)。对在体颈动脉数据进行ST时,数据窗大小为0.50 mm×0.89 mm(轴向×侧向)。
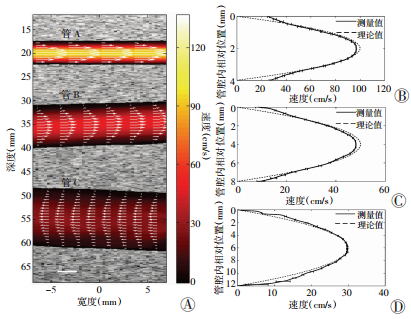
2 结果 2.1 仿真基于多普勒和ST方法的矢量血流成像仿真结果分别见图 1、2,可见两种方法均能获得较好的抛物线型血流分布,所测峰值速度大小均略低于理论峰值。基于多普勒和ST方法,图 1管A内垂直血流速度分量偏差分别为-0.018、-0.017 cm/s,标准差分别为0.33、0.16 cm/s,结合表 2中的评价参数可见,对于仿真所设3个血管,基于多普勒和散斑跟踪方法的矢量血流成像所测得垂直方向、水平方向速度偏差及标准差基本接近。

|
| A:基于多普勒的多血管仿真矢量血流成像图;B~D:分别为管A、B、C的血流速度测量值与真值对比;B:管A,直径4 mm,倾角0°,深度2 cm;C:管B,直径8 mm,倾角-5°,深度3.5 cm;D:管C,直径12 mm,倾角5°,深度5.5 cm 图 1 基于多普勒的多血管仿真矢量血流成像结果 |
|
| A:基于散斑跟踪的多血管仿真矢量血流成像图;B~D:分别为管A、B、C的血流速度测量值与真值对比;B:管A,直径4 mm,倾角0°,深度2 cm;C:管B,直径8 mm,倾角-5°,深度3.5 cm;D:管C,直径12 mm,倾角5°,深度5.5 cm 图 2 基于散斑跟踪的多血管仿真矢量血流成像结果 |
| 仿真血管 | νhor偏差 | νver偏差 | νhor标准差 | νver标准差 | |||||||
| 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | ||||
| 管A | -1.43 | 1.84 | - | - | 1.76 | 0.97 | - | - | |||
| 管B | 3.15 | 4.36 | 2.61 | 1.18 | 1.79 | 1.00 | 3.09 | 2.08 | |||
| 管C | -2.09 | 7.84 | 1.37 | 5.43 | 2.35 | 2.40 | 3.55 | 4.87 | |||
| νhor:水平速度分量,νver:垂直速度分量 | |||||||||||
2.2 仿体实验
利用血流仿体速度最大值是100 cm/s的超声接收数据,基于多普勒和ST方法的矢量血流成像仿体结果见图 3,可见两种方法均能获得较好的抛物线型血流分布,所测峰值速度大小均低于理论峰值,且ST方法峰值较低。结合表 3中方法评价参数可见,使用ST方法比多普勒方法所测垂直方向、水平方向速度偏差及标准差较大,表现为对速度大小的低估。

|
| 图 3 基于多普勒和散斑跟踪的仿体矢量血流成像结果 |
| 最大血流速度(cm/s) | νhor偏差(%) | νver偏差(cm/s) | νhor标准差(%) | νver标准差(cm/s) | |||||||
| 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | 多普勒 | 散斑跟踪 | ||||
| 100 | -5.00 | -5.28 | 0.53 | 1.46 | 5.01 | 5.42 | 1.02 | 0.86 | |||
| 50 | -4.45 | -4.69 | 0.62 | 1.22 | 4.57 | 4.95 | 1.17 | 1.34 | |||
| 30 | -3.76 | -3.94 | 0.48 | 0.93 | 4.53 | 4.68 | 0.98 | 1.27 | |||
| νhor:水平速度分量,νver:垂直速度分量 | |||||||||||
2.3 在体实验
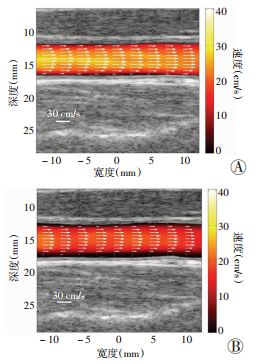
1例健康成人志愿者颈总动脉矢量血流成像结果见图 4,其中彩色编码亮度及箭头长短及方向可见,两种方法所测血流速度方向大体一致,基本平行于血管壁方向,且基于散斑跟踪方法所测血流速度大小较低。
|
| A:多普勒方法;B:散斑跟踪方法 图 4 1例健康成人志愿者颈总动脉矢量血流成像图 |
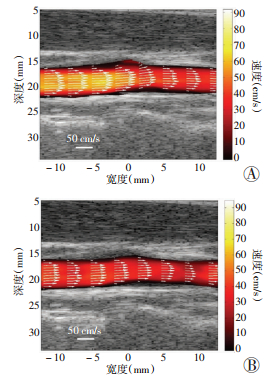
1例健康成人志愿者颈动脉分叉处矢量血流成像结果见图 5、6,可见两种方法所测血流速度方向大体一致,且基于散斑跟踪方法所测血流速度大小较低。
|
| A:多普勒方法;B:散斑跟踪方法 图 5 1例健康成人志愿者颈总动脉与颈内动脉分叉处矢量血流成像图 |

|
| A:多普勒方法;B:散斑跟踪方法 图 6 1例健康成人志愿者颈总动脉与颈外动脉分叉处矢量血流成像图 |
3 讨论
本研究使用的基于多普勒和散斑跟踪的矢量血流成像方法是目前使用较为广泛的两种超声矢量血流成像算法。基于多普勒的矢量血流成像方法具有易于实现、计算量低的优势,利用超高速平面波成像方式可满足奈奎斯特限制,从而测量较高速血流[11]。散斑跟踪方法不受奈奎斯特限制,在保证帧间相关性的帧频条件下即可测得血流速度矢量。本研究通过2个角度平面波发射接收设置,通过多角度轴向速度分量,进一步重建二维血流速度。
由表 2可见,仿真条件下,散斑跟踪方法表现出与多普勒方法相当的测量准确度。提示,在较理想情况下,两种方法都具有较好的矢量血流成像效果。由于综合多个血流分量的最小二乘法的引入,减小了速度估计误差,增强了测量稳定度。因此,相较于只用单一角度接收数据作散斑跟踪具有更好的稳定性。
由表 3中仿体实验结果可见,在非理想仿真情况下,散斑跟踪与多普勒测量方法相比,所测得速度偏差较大,测得峰值速度大小偏低。相似地,在体血流测量结果也表现出同样的趋势,两种方法所测得血流速度方向基本一致,而基于散斑跟踪方法所测得血流速度偏差较大、大小偏低。由于散斑跟踪是一种宽带估计方法,因此所用超声发射脉冲的长度较短、发射能量较低,且平面波发射相较于传统聚焦波发射得到的接收图像质量较差,因此在实际在体应用,尤其是对深度较深的组织成像时,散斑信号信噪比降低,散斑跟踪方法的测量误差较大,这可能是上述结果中这种方法造成血流速度低估的原因之一,这与已有研究[12]结果基本一致。
对于两种超声矢量血流成像算法可增加超声波发射接收角度个数[13]进一步提升测量准确度。此外,由于散斑跟踪方法受检测信号信噪比的影响较大,因此,可考虑加入超声编码激励[14]和使用微泡造影剂增强[15]等方式,提升血流信号的信噪比,进一步提升测量准确度。
综上所述,本研究基于超高速平面波发射方式,对比了多普勒和散斑跟踪方法在矢量血流成像中的血流速度测量准确度。在理想仿真情况下,两种方法能够获得相当测速准确度,仿体和在体实验中,散斑跟踪方法表现出对速度大小的低估,准确度低于多普勒方法。
| [1] | Evans D H, Jensen J A, Nielsen M B. Ultrasonic colour Doppler imaging[J]. Interface Focus,2011, 1 (4) : 490 –502. DOI:10.1098/rsfs.2011.0017 |
| [2] | Pedersen M M, Pihl M J, Haugaard P, et al. Comparison of real-time in vivo spectral and vector velocity estimation[J]. Ultrasound Med Biol,2012, 38 (1) : 145 –151. DOI:10.1016/j.ultrasmedbio.2011.10.003 |
| [3] | Ekroll I K, Swillens A, Segers P, et al. Simultaneous quantification of flow and tissue velocities based on multi-angle plane wave imaging[J]. IEEE Trans Ultrason Ferroelectr Freq Control,2013, 60 (4) : 727 –738. DOI:10.1109/TUFFC.2013.2621 |
| [4] | Fadnes S, Ekroll I K, Nyrnes S A, et al. Robust angle-independent blood velocity estimation based on dual-angle plane wave imaging[J]. IEEE Trans Ultrason Ferroelectr Freq Control,2015, 62 (10) : 1757 –1767. DOI:10.1109/TUFFC.2015.007108 |
| [5] | Jensen J A. Comparison of vector velocity imaging using directional beamforming and transverse oscillation for a convex array transducer[J]. Proceedings of SPIE-The International Society for Optical Engineering,2014, 9040 (15) : 904012 –904012. |
| [6] | 何琼, 罗建文. 超高速超声成像的研究进展[J]. 中国医学影像技术,2014, 30 (8) : 1251 –1255. |
| [7] | Luo J, Konofagou E. A fast normalized cross-correlation calculation method for motion estimation[J]. IEEE Trans Ultrason Ferroelectr Freq Control,2010, 57 (6) : 1347 –1357. DOI:10.1109/TUFFC.2010.1554 |
| [8] | Svilainis L, Lukoseviciute K, Dumbrava V, et al. Subsample interpolation bias error in time of flight estimation by direct correlation in digital domain[J]. Measurement,2013 (10) : 3950 –3958. DOI:10.1016/j.measurement.2013.07.038 |
| [9] | Montaldo G, Tanter M, Bercoff J, et al. Coherent plane-wave compounding for very high frame rate ultrasonography and transient elastography[J]. IEEE Trans Ultrason Ferroelectr Freq Control,2009, 56 (3) : 489 –506. DOI:10.1109/TUFFC.2009.1067 |
| [10] | 王录涛, 肖军, 柴华. 超声血流成像中的壁滤波器设计方法分析与性能比较[J]. 生物医学工程学杂志,2015, 32 (4) : 773 –778. |
| [11] | Dort S, Muth S, Swillens A, et al. Vector flow mapping using plane wave ultrasound imaging[C].2012 IEEE International Ultrasonics Symposium, 2012. DOI: 10.1109/ultsym.2012.0081 |
| [12] | Swillens A, Segers P, Torp H, et al. Two-dimensional blood velocity estimation with ultrasound: speckle tracking versus crossed-beam vector Doppler based on flow simulations in a carotid bifurcation model[J]. IEEE Trans Ultrason Ferroelectr Freq Control,2010, 57 (2) : 327 –339. DOI:10.1109/TUFFC.2010.1413 |
| [13] | Yiu B Y, Lai S S, Yu A C. Vector projectile imaging: time-resolved dynamic visualization of complex flow patterns[J]. Ultrasound Med Biol,2014, 40 (9) : 2295 –2309. DOI:10.1016/j.ultrasmedbio.2014.03.014 |
| [14] | Takahashi H, Hasegawa H, Kanai H. Speckle-enhanced cardiac blood flow imaging with high frame rate ultrasound[J]. 2013 IEEE International Ultrasonics Symposium (IUS),2013 . DOI:10.1109/ultsym.2013.0518 |
| [15] | Leow C H, Bazigou E, Eckersley R J, et al. Flow Velocity Mapping Using Contrast Enhanced High-Frame-Rate Plane Wave Ultrasound and Image Tracking: Methods and Initial in Vitro and in Vivo Evaluation[J]. Ultrasound Med Biol,2015, 41 (11) : 2913 –2925. DOI:10.1016/j.ultrasmedbio.2015.06.012 |