近年学术界发现了一种新型的环境内分泌干扰物,称为金属类雌激素或金属类激素,常见的有镉、锑、钙、钴、铜、镍、铬、铅、汞和锡等[1]。这些金属类雌激素具有类雌激素作用,被发现与雌激素相关疾病如乳腺癌、子宫内膜移位、子宫肌瘤和子宫内膜癌等的发生有密切关系[2]。镉是其中具有代表性的一种。已有研究发现镉可以引起乳腺癌细胞MCF-7细胞ERK和AKT的快速激活,而对MDA-MB-231细胞无作用。甲状腺癌是最常见的内分泌肿瘤之一,而女性发病率明显高于男性[3]。雌激素能通过与细胞内雌激素受体的结合,促进肿瘤的发生[4]。G蛋白偶联受体1(G protein-coupled estrogen receptor,GPER1,曾命名为GPR30)是近年发现的一种新型雌激素膜性受体[5]。并且雌激素能通过GPER1途径促进甲状腺未分化癌细胞FRO的细胞增殖。目前对于镉是如何在甲状腺癌细胞中发挥类雌激素作用少见研究报道。本实验以甲状腺未分化癌FRO细胞为模型,探讨金属镉对甲状腺未分化癌FRO细胞增殖的影响及其作用机制。
1 材料与方法 1.1 主要材料与试剂甲状腺未分化癌FRO细胞株、乳腺癌MCF-7细胞株及MAD-MB-231细胞株由香港中文大学外科实验室提供。Cd(CdCl2)、E2(雌激素)、RPMI1640培养基(不含酚红)、四甲基偶氮唑蓝(MTT)购自美国Sigma公司。GPER1、GPER1拮抗剂(G15)、PI3K-Akt抑制剂(LY294002)和ERK抑制剂(PD98059)购自Calbiochem公司。SDS配胶试剂盒购自碧云天生物技术有限公司。β-actin抗体、p-Akt抗体、t-Akt抗体购自Santa Cruz公司。GPER1抗体购自Abcam公司。p-ERK1/2抗体、t-ERK1/2抗体购自Cell signaling公司,限制性内切酶购自TaKaRa公司,Lipofectamine2000购自Invitrogen公司。GPER-siRNA序列由上海生工生物工程有限公司合成。
1.2 方法 1.2.1 细胞培养用RPMI1640培养基(含10%FBS、100 U/mL青霉素和100 μg/mL链霉素),于37 ℃, 5% CO2饱和湿度孵箱中常规贴壁传代培养FRO细胞,取对数生长期的细胞进行后续实验。
1.2.2 MTT法取对数生长期的细胞,经胰酶消化后制成单细胞悬液,以5×103/孔接种于96孔培养板,待细胞完全贴壁后,用无血清、无酚红培养液培养48 h,使细胞同步化,分别用0.25、0.50、0.75、1.00 mmol/L CdCl2处理48 h,每孔加入5 mg/mL的MTT 20 μL,37 ℃孵育4 h,吸去培养液,每孔加入DMSO 150 μL,振荡10 min,待紫色结晶完全溶解后,测定D(490)值,重复3次,计算细胞增殖率。
1.2.3 GPER-siRNA的构建和转染根据GenBank中人GPER mRNA(NM 001039966)全长序列,设计siRNA序列,命名为GPER-siRNA(+),并同时设计阴性对照序列,命名为GPER1-siRNA(-)。将siRNA的单链退火,与pGenesil-1质粒连接,转化DH5α感受态细胞,挑取单菌落提取质粒,用Lipofectamine2000转染,48 h后用CdCl2处理细胞15 min,提取蛋白进行Western blot检测。
1.2.4 免疫印记根据不同实验要求,0.5 mmol/L CdCl2处理FRO细胞不同时间(0、5、10、15、30 min)。将GPER-siRNA(+)、GPER-siRNA(-)质粒转染FRO细胞48 h。CdCl2作用于分别加入G15、PD98059、LY294002以及转染GPER-siRNA的FRO细胞15 min。分别处理FRO细胞后,取总蛋白50 μg进行10%聚丙烯酰胺凝胶电泳(SDS-PAGE)。湿转法将蛋白转移到PVDF膜上,5%的脱脂奶粉封闭1 h,加入一抗,4 ℃过夜。TBST洗膜后加二抗,常温孵育1 h,TBST洗膜后,用ECL发光法显色, Bio-Rad凝胶成像系统采集图像。
1.3 统计学方法计量资料数据以x±s表示,应用SPSS 17.0统计软件进行单因素方差分析,以P < 0. 05为差异有统计学意义。
2 结果 2.1 GPER1在MCF-7、MDA-MB-231、FRO细胞中的表达GPER1在MCF-7、FRO细胞中表达明显高于MDA-MB-231细胞(图 1),MDA-MB-231细胞可作为阴性对照组。

|
| 1:MCF-7;2:FRO;3:MDA-MB-231 图 1 GPER1在MCF-7、FRO、MDA-MB-231中的表达 |
2.2 CdCl2对MCF-7、MDA-MB-231、FRO细胞的影响
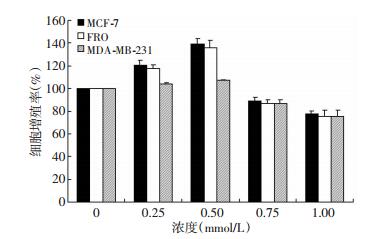
0、0.25、0.50、0.75、1.00 mmol/L CdCl2分别处理人甲状腺未分化癌FRO细胞、乳腺癌MCF-7和MDA-MB-231细胞48 h,MTT法测细胞增殖率(图 2),结果表明低浓度CdCl2对MCF-1、FRO细胞有促进作用(P < 0.05),但对MDA-MB-231细胞作用不显著。高浓度CdCl2对细胞均有抑制作用。
|
| 图 2 不同浓度CdCl2处理MCF-7、FRO、MDA-MB-231细胞对细胞增殖率的影响 |
2.3 CdCl2促进ERK1/2和Akt磷酸化
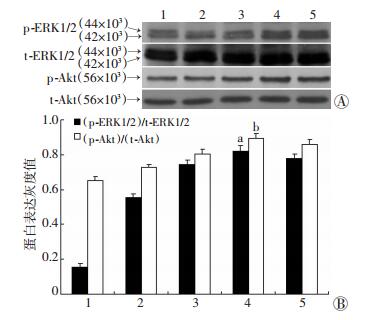
0.5 mmol/L CdCl2处理人甲状腺未分化癌FRO细胞0、5、10、15、30 min,Western blot法检测ERK1/2和Akt的磷酸化水平发现(图 3),随着CdCl2处理FRO细胞时间的增加,ERK1/2和Akt的磷酸化水平逐渐增高,在15 min时ERK1/2、Akt的磷酸化水平达到峰值,随后降低。表明CdCl2在短时间内可促进FRO细胞Akt和ERK1/2磷酸化水平增高。
|
| 1: 0 min; 2: 5 min; 3: 10 min; 4: 15 min; 5: 30 min;A: Western blot检测;B:半定量分析a:P < 0.05, 与0 min时(p-ERK1/2)/(t-ERK1/2)值比较; b:P < 0.05, 与0 min时(p-Akt)/(t-Akt)值比较 图 3 Western blot检测CdCl2处理不同时间对FRO细胞ERK1/2和Akt蛋白磷酸化水平的影响 |
2.4 GPER1抑制剂G15抑制CdCl2引起的ERK1/2、Akt磷酸化
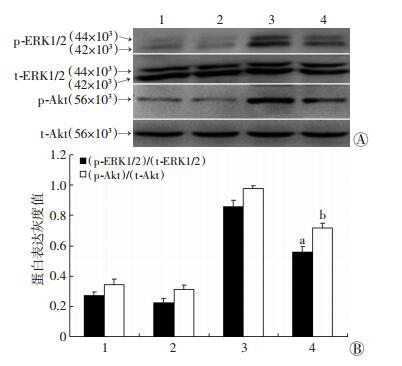
用GPER1抑制剂G15处理FRO细胞,ERK1/2、Akt磷酸化水平显著降低(P < 0.05,图 4)。
|
| 1:对照组;2:G15;3:CdCl2; 4:G15+CdCl2;A: Western blot检测;B:半定量分析a:P < 0.05, 与CdCl2处理组(p-ERK1/2)/(t-ERK1/2)值比较;b:P < 0.05, 与CdCl2处理组(p-Akt)/(t-Akt)值比较 图 4 Western blot检测G15对FRO细胞ERK1/2和Akt蛋白磷酸化水平的影响 |
2.5 GPER-siRNA干扰抑制CdCl2引起的ERK1/2、Akt磷酸化
将GPER-siRNA(+)、GPER-siRNA(-)质粒转染FRO细胞48 h,Western blot检测ERK1/2、Akt的磷酸化水平。CdCl2组、CdCl2+GPER-siRNA(+)组中p-ERK1/2、t-ERK1/2蛋白表达灰度值分别为0.715±0.023、0.248±0.034,p-Akt、t-Akt蛋白表达灰度值分别为0.911±0.033、0.658±0.038。表明GPER-siRNA干扰后,ERK1/2与Akt的磷酸化水平明显降低(P < 0.05,图 5)。

|
| 1:对照组;2:CdCl2;3:CdCl2+GPER-siRNA(-);4:CdCl2+ GPER-siRNA(+);A: Western blot检测;B:半定量分析a:P < 0.05, 与CdCl2组(p-ERK1/2)/(t-ERK1/2)值比较;b:P < 0.05, 与CdCl2组(p-Akt)/(t-Akt)值比较 图 5 Western blot检测GPER-siRNA干扰对FRO细胞ERK1/2和Akt蛋白磷酸化水平的影响 |
2.6 ERK、AKT和GPER1的抑制剂及GPER-siRNA干扰对CdCl2诱导的FRO细胞增殖的影响
G15、PD98059、LY294002、GPER-siRNA均可抑制CdCl2诱导的FRO细胞增殖,增殖率由处理前的(140.67±2.47)%分别降至(110.96±2.62)%、(118.26±4.07)%、(121.98±2.65)%、(108.98±3.65)%,表明CdCl2通过GPER1激活ERK1/2、Akt通路,促进FRO细胞增殖。
3 讨论镉是一种重要的环境和工业毒物。研究发现镉与乳腺癌、卵巢癌、子宫内膜癌等雌激素相关癌症的发生有密切关系,离体实验与体内实验均有研究显示镉具有类雌激素作用[6]。Brama等[7]研究发现:镉能通过刺激Akt、ERK1/2和PDGFRα激酶促进乳腺癌细胞增殖。甲状腺癌是一种与雌激素相关的内分泌系统肿瘤。研究[8]表明,雌激素通过GPER1促进甲状腺未分化癌FRO细胞Akt、ERK1/2的磷酸化水平增高,诱导FRO细胞增殖。镉是通过怎么的途径促进甲状腺癌未分化癌FRO细胞的增殖目前尚少见研究。
本研究首先以FRO、MCF-7及MDA-MB-231细胞为研究对象,检测3种细胞中GPERI的表达,结果表明GPER1在FRO、MCF-7细胞中表达量较高,在MDA-MB-231中表达量相对较少。这与研究[9]结果一致。用不同浓度的CdCl2处理3种细胞,48 h后测细胞增殖率,表明低浓度CdCl2促进FRO、MCF-7细胞增殖,对MDA-MB-231细胞无显著影响,高浓度对细胞均有抑制作用。高浓度镉对细胞抑制作用可能与镉引起的DNA氧化损伤和修复抑制有关[10]。研究[9]表明雌激素能够通过GPER1-ERK/AKT信号通路促进甲状腺癌FRO细胞增殖,那么镉在FRO细胞中是否有相似的信号通路?本研究用0.5 mmol/L CdCl2处理FRO细胞不同时间,发现CdCl2可促进ERK、AKT磷酸化,且15 min时磷酸化水平最高。用GPER1抑制剂G15处理FRO细胞,ERK/AKT磷酸化水平显著降低。证明CdCl2刺激GPER1介导的ERK/AKT的磷酸化作用。将GPER-siRNA转染至FRO细胞中干扰GPER1的表达,结果显示ERK/AKT的磷酸化水平显著降低,进一步证明CdCl2刺激GPER1介导的ERK/AKT的磷酸化作用。
为进一步证明金属镉通过GPER1-ERK/AKT信号通路促进甲状腺未分化癌FRO细胞增殖,分别用GPER1抑制剂G15、ERK1/2抑制剂PD98059和PI3K-Akt抑制剂LY294002及GPER-siRNA处理FRO细胞,MTT法测细胞增殖率,结果表明G15、PD98059、LY294002和GPER-siRNA均可抑制镉诱导的FRO细胞增殖。
综上所述,金属镉通过GPER1,促进人甲状腺未分化癌FRO细胞ERK1/2、Akt的磷酸化水平增高,诱导FRO细胞增殖。但金属隔是如何通过GPER1-ERK/AKT途径在细胞核中发挥作用从来促进细胞增殖本实验尚未涉及,这也是下一步的研究方向。镉的雌激素样作用需要引起高度关注,应特别加强对镉的雌激素样毒性及其机制的研究,以便采取更合理有效的预防措施,减少癌症的发生。
| [1] | Byrne C, Divekar S D, Storchan G B, et al. Metals and breast cancer[J]. J Mammary Gland Biol Neoplasia,2013, 18 (1) : 63 –73. DOI:10.1007/s10911-013-9273-9 |
| [2] | Silva N, Peiris-John R, Wickremasinghe R, et al. Cadmium a metalloestrogen: are we convinced?[J]. J Appl Toxicol,2012, 32 (5) : 318 –332. DOI:10.1002/jat.1771 |
| [3] | Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012[J]. CA Cancer J Clin,2012, 62 (1) : 10 –29. DOI:10.3322/caac.20138 |
| [4] | Revankar C M, Cimino D F, Sklar LA, et al. A transmembrane intracellular estrogen receptor mediates rapid cell signaling[J]. Science,2005, 307 (5715) : 1625 –1630. DOI:10.1126/science.1106943 |
| [5] | Vivacqua A, Bonofiglio D, Albanito L, et al. 17beta-estradiol, genistein, and 4-hydroxytamoxifen induce the proliferation of thyroid cancer cells through the g protein-coupled receptor GPR30[J]. Mol Pharmacol,2006, 70 (4) : 1414 –1423. DOI:10.1124/mol.106.026344 |
| [6] | 李煌元, 吴思英, 张文昌, 等. 镉的雌性性腺生殖毒性研究现状[J]. 中国公共卫生,2002, 18 (3) : 379 –381. |
| [7] | Brama M, Gnessi L, Basciani S, et al. Cadmium induces mito-genic signaling in breast cancer cell by an ER-alpha-dependent mechanism[J]. Mol Cell Endocrinol,2007, 264 (1/2) : 102 –108. |
| [8] | 吴婷婷, 龙方懿, 刘智敏, 等. G蛋白偶联受体在雌激素诱导人甲状腺未分化癌FRO细胞增殖中的作用及其机制[J]. 第三军医大学学报,2011, 33 (2) : 164 –168. DOI:10.16016/j.1000-5404.2011.02.027 |
| [9] | Liu Z, Yu X, Shaikh Z A. Rapid activation of ERK1/2 and AKT in human breast cancer cells by cadmium[J]. Toxicol Appl Pharmacol,2008, 228 (3) : 286 –294. DOI:10.1016/j.taap.2007.12.017 |
| [10] | Schwerdtle T, Ebert F, Thuy C, et al. Genotoxicity of soluble and particulate cadmium compounds: impact on oxidative DNA damage and nucleotide excision repair[J]. Chem Res Toxicol,2010, 23 (2) : 432 –442. DOI:10.1021/tx900444w |



