肺癌是世界上最常见的一种恶性肿瘤,严重威胁着人类的生命和健康[1]。最新研究结果显示,我国肺癌的发生率和死亡率均居肿瘤首位[2]。近年来,随着生物技术的发展和相关研究的不断深入,分子靶向治疗作为一种新兴的肿瘤治疗方式已逐渐成为一个研究热点,为肺癌的治疗提供了一种有效的手段[3]。
哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)是PI3K/Akt/mTOR经典信号通路下游的一个重要激酶。它可通过形成mTORC1/2两种复合物(mTOR complex,mTORC)从而参与细胞生长、周期、凋亡等多种生物学活动的调节。在许多肿瘤中都存在mTOR信号通路的过度活化[4]。Torin2作为一种新的二代mTOR抑制剂,对多种肿瘤细胞的生长和转移均有抑制作用,如甲状腺癌、肝癌、卵巢癌等[5-7],但关于Torin2对肺癌细胞生物学行为的影响尚不清楚。本研究旨在观察Torin2对人非小细胞肺癌A549细胞系生长和迁移的影响,并对其作用机制进行初步探讨,为Torin2用于治疗非小细胞肺癌提供一定的科学依据。
1 材料与方法 1.1 材料与试剂人非小细胞肺癌A549细胞购自美国ATCC公司;DMEM高糖培养基购自美国Gibco公司;CCK-8试剂盒购自日本同仁化学公司;FITC AnnexinⅤ凋亡检测试剂盒购自美国BD公司;细胞小室24 孔Millicell 购自Millipore公司;BCA蛋白定量试剂盒购自上海碧云天公司;鼠抗人β-actin、Cyclin D1、兔抗人4EBP1、P-4EBP1、Akt、P-Akt473、Cleaved Caspase 9抗体均购自美国Cell Signal Technology公司;山羊抗鼠和山羊抗兔IgG购自中杉金桥公司;Torin2购自美国Sigma公司。
1.2 方法 1.2.1 A549细胞培养A549细胞接种于无菌培养皿中,加入适量DMEM高糖培养基(含10%胎牛血清),在37 ℃、5%CO2及饱和湿度的培养箱中进行孵育培养。
1.2.2 CCK-8检测Torin2对A549细胞增殖的影响实验分空白对照组、阴性对照组和加药组,取对数生长期的A549细胞经胰酶消化后接种于96孔板中,每孔100 μL(细胞数约5 000个/孔)。细胞贴壁后加药组采用倍比稀释法分别加入终浓度为0、50、100、200、400、800 nmol/L的Torin2,每个浓度设3个复孔,每孔终体积为200 μL。孵箱培养48 h后弃去96孔板的培养基,每孔加入90 μL DMEM高糖培养基和10 μL CCK-8,再取3 个没有接种细胞的孔加入相同量的培养基和CCK-8 作为空白对照,放细胞培养箱孵育2 h后,用酶标仪于450 nm光波处测各孔光密度值D(450)。以阴性对照组细胞存活率记100%,按公式计算加药组细胞存活分数=实验组D(450)值/对照组D(450)值×100%。相同条件下实验重复3次。
1.2.3 流式细胞仪检测Torin2对A549细胞凋亡的影响A549细胞经胰酶消化后铺6孔板,每孔2 mL 培养基,细胞数约1×106个/孔。细胞贴壁后分别加入终浓度为0、200、400 nmol/L的Torin2,细胞培养箱孵育48 h后收集细胞,依次加入5 μL PE Annexin V和5 μL 7-AAD,轻轻混匀后室温避光孵育15 min。 1 h后进行流式细胞仪检测。相同条件下实验重复3次。
1.2.4 流式细胞仪检测Torin2对A549细胞周期的影响取对数生长期的A549细胞,经胰酶消化后铺6孔板,每孔体积2 mL(细胞数约2×106个/孔),贴壁后分别加入终浓度为0、200、400 nmol/L的Torin2,处理48 h后经胰酶消化收集细胞,加入预冷的75%乙醇4 ℃固定过夜,离心收集细胞,PBS清洗,加RNaseA(终浓度1 μg/mL),37 ℃水浴消化30 min。加PI 至终浓度50 μg/mL,冰浴避光染色30 min。尼龙网过滤,流式细胞仪检测,488 nm 激发光激发检测。相同条件下实验重复3次。
1.2.5 Transwell实验检测Torin2对A549细胞迁移的影响A549细胞经胰酶消化后铺6孔板,每孔2 mL培养基,细胞数约1×106个/孔。细胞贴壁后分别加入终浓度为0、200、400 nmol/L的Torin2,细胞培养箱孵育48 h后收集细胞,各组细胞以5×104/孔铺种于Transwell 小室内,上层以400 μL无血清DMEM 培养基孵育,下层加入1 mL含10%FBS 的DMEM培养基。继续培养24 h后取出Transwell小室,棉签刮除小室内面存留的细胞,用4%多聚甲醛固定,0.1%结晶紫染色。倒置显微镜下任选5 个视野观察照相。相同条件下实验重复3次。
1.2.6 Western blot检测Torin2对相关蛋白表达的影响分别收集终浓度为0、200、400 nmol/L的Torin2处理48 h的A549细胞,预冷的PBS清洗后加入RIPA裂解液和蛋白酶抑制剂,冰浴20 min。离心,收集上清液,采用BCA法测定蛋白含量。各组取等量总蛋白加上样缓冲液,煮沸变性5 min,进行SDS-PAGE电泳。然后转移到硝酸纤维素膜上,10% 脱脂奶粉封闭1 h,将对应分子量条带剪下后分别用一抗β-actin、Cyclin D1、4EBP1、p-4EBP1、Akt、p-Akt473、Cleaved Caspase 9在4 ℃孵育过夜后,加相应二抗孵育1 h,膜上滴加化学发光剂在暗室进行曝光显影。
1.3 统计学分析数据以x±s表示,采用Origin 8.0软件作图,SPSS 18.0统计软件进行数据分析,组间比较采用两独立样本t检验,P<0.05为差异有统计学意义。
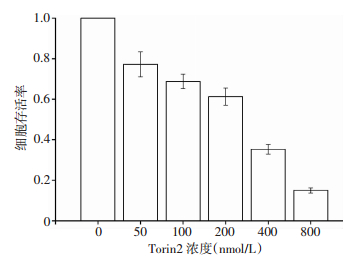
2 结果 2.1 Torin2抑制了A549细胞的增殖Torin2(0、50、100、200、400、800 nmol/L)处理A549细胞48 h,CCK-8结果表明随着Torin2浓度增加,A549细胞的增殖活性呈现明显剂量依赖性降低(图 1),采用Probit回归分析得药物半数抑制浓度IC50 =214.96 nmol/L。
|
| 图 1 不同浓度Torin2对A549细胞增殖的影响 |
2.2 Torin2促进了A549细胞的凋亡
A549细胞经Torin2处理后,对照组、200 nmol/L和400 nmol/L药物组的凋亡率分别为(4.51±1.32)%、(9.56±2.34)%和(16.40± 3.57)%,药物作用组凋亡率均较对照组显著增高(P<0.05,图 2),提示Torin2可促进A549细胞的凋亡。

|
| A:对照组;B:200 nmol/L药物组;C:400 nmol/L药物组 图 2 流式细胞仪检测Toin2对A549细胞凋亡的影响 |
2.3 Torin2可引起A549细胞周期G1/S期阻滞
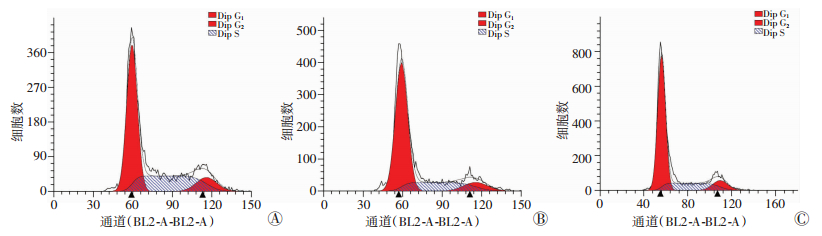
A549细胞经Torin2处理后,对照组、200 nmol/L和400 nmol/L药物组G1期细胞比例分别为(58.15±1.71)%、(69.64±1.10)%和(69.27±0.70)%,S期细胞分别为(33.06±2.29)%、(20.79±1.88)%和 (22.62±1.23)%,加药组与对照组细胞相比,细胞周期中G1期细胞比例增高,S期细胞比例减少(P<0.05,图 3),表明Torin2可诱导A549细胞阻滞在G1/S期。
|
| A:对照组;B:200 nmol/L药物组;C:400 nmol/L药物组 图 3 流式细胞仪检测Toin2对A549细胞周期的影响 |
2.4 Torin2抑制了A549细胞的迁移
Transwell实验检测对照组和Torin2药物组(200 nmol/L 和400 nmol/L)A549细胞的迁移能力,观察各组200倍视野下穿过的细胞个数。结果显示药物组(200 nmol/L和400 nmol/L)穿过的细胞数[分别为(107.2±18.9)、(13.4±3.0)]显著少于对照组[(190.2±14.2),P<0.05,图 4],表明Torin2可显著抑制A549细胞的迁移能力。

|
| A:对照组;B:200 nmol/L药物组;C:400 nmol/L药物组 图 4 Transwell实验检测Toin2对A549细胞迁移的影响(结晶紫 ×200) |
2.5 Torin2影响了PI3K/Akt/mTOR信号通路及相关蛋白的表达
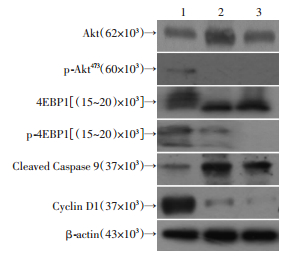
与细胞凋亡和周期结果一致,A549细胞经Torin2处理后,尽管总Akt和4EBP1的表达水平有升高,但p-Akt473、p-4EBP1以及Cyclin D1蛋白表达明显降低,Cleaved Caspase 9蛋白酶切片段表达显著增加(图 5)。由于mTORC1和mTORC2的直接作用底物分别为p-4EBP1和p-Akt473,此结果也说明了Torin2抑制了PI3K/Akt/mTOR信号通路的活性以及Cyclin D1周期蛋白的表达。
|
| 1: 对照组; 2: 200 nmol/L药物组; 3: 400 nmol/L药物组 图 5 Western blot检测Torin2对A549细胞相关蛋白表达的影响 |
3 讨论
PI3K/Akt/mTOR信号通路是体内蛋白质合成的主要信号通路之一,广泛参与了多种生物学活性的调控,如细胞增殖、凋亡、转录、翻译、细胞周期、自噬等。PI3K/Akt/mTOR通路异常活化是许多肿瘤重要的致瘤机制之一,包括乳腺癌、卵巢癌、前列腺癌、胰腺癌等[8-11]。因此,PI3K/Akt/mTOR信号通路将有可能成为治疗肺癌的一个有效的靶点,其中mTORC1抑制剂依维莫司在肾透明细胞癌和神经内分泌肿瘤的临床治疗中已有应用[12-13]。
本实验发现Torin2对人非小细胞肺癌A549细胞的增殖具有抑制作用,且有明显的剂量依赖效应。同时,Torin2可促进A549细胞凋亡,使细胞周期阻滞在G1/S期,并下调p-Akt473、p-4EBP1和Cyclin D1周期蛋白表达,诱导凋亡蛋白Cleaved Casepase 9上调。持续高度活化的mTORC1可通过调控4EBP1的磷酸化,影响真核细胞翻译起始因子(elF4E)的活性,从而诱导抗凋亡蛋白Mcl-1的表达。该调控方式是Akt/mTOR通路过度活化的致瘤和维持肿瘤细胞生长的重要机制[14]。与该研究一致,Torin2可诱导非小细胞肺癌A549细胞凋亡并同时显著下调P-4EBP1水平,推测在A549细胞中Torin2通过诱导类似凋亡机制介导其抗增殖活性[15]。
另一方面,Akt和4EBP1分别为mTORC1和mTORC2的直接作用底物,它们表达水平的下降间接说明了Torin2同时抑制了mTORC1和mTORC2这两种复合物的形成,而雷帕霉素等传统的mTOR抑制剂只能抑制mTORC1复合物,且可能会激活mTOR/P70S6K/IRS-1负反馈环,导致Akt活性增强,引起肿瘤细胞对mTOR抑制剂产生耐药[4]。因此,二代的mTOR抑制剂如Torin2等可能会有更好的抗肿瘤效果。
Akt蛋白及其活性是介导肿瘤细胞增殖和存活的重要蛋白。我们在Torin2处理的A549细胞中发现p-Akt473蛋白表达水平较对照组显著降低,但总Akt蛋白表达却升高。事实上,抑制Akt/mTOR通路导致受其抑制的下游基因活化即负反馈机制的释放是肿瘤细胞对药物适应性生长的普遍现象,也是重要的耐药机制。在HER2扩增乳腺癌细胞系BT474和PTEN缺失的前列腺癌细胞系LNCaP中抑制Akt或PI3KCβ可诱导HER3、IGF-1R、IRS1等蛋白表达上调并再次活化Akt[16-17]。另外,亦有上调Akt蛋白表达的报道[18]。卵巢癌细胞OV2008用雷帕霉素、Torin1以及PI3K/mTOR抑制剂BEZ235处理后均可上调AKT蛋白表达,其中的机制尚待进一步探讨。本研究中Akt磷酸化水平持续被抑制,与Torin2促进凋亡一致,但Torin2抑制mTOR导致的负反馈释放机制尚需系统研究。
此外,PIK3CA激酶区激活突变、肿瘤抑制基因TSC2截短突变以及mTOR自身激活突变等均可导致mTOR生长依赖性进而对mTOR抑制剂敏感[19-20]。在乳腺癌和黑色素瘤等其他靶向药物继发耐药的细胞模型中,对mTOR再次活化的抑制是重要的抗耐药机制[21-22]。但本研究只使用了一种细胞株,且没有将非小细胞肺癌特定基因或特定突变与Torin2敏感性进行相关研究,如A549细胞存在RAS激活突变,RAS基因可以通过影响PI3K、MAPK和STAT这3条信号通路从而调控细胞的生长和增殖。另外,在Torin2诱导凋亡的具体机制中也没有深入探讨。尽管如此,本实验结果表明了Torin2对A549细胞增殖具有明显抑制作用,其机制可能与抑制了PI3K/Akt/mTOR信号通路的活性以及Cyclin D1周期蛋白的表达密切相关,为以后开展Torin2的动物实验奠定了理论和实验基础,也为将来Torin2用于治疗非小细胞肺癌提供一定的科学依据。
| [1] | Takenaka T, Yamazaki K, Miura N, et al. The Prognostic Impact of Tumor Volume in Patients with Clinical Stage IA Non-small Cell Lung Cancer[J]. J Thorac Oncol,2016, 11 (7) : 1074 –1080. DOI:10.1016/j.jtho.2016.02.005 |
| [2] | Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin,2016, 66 (2) : 115 –132. DOI:10.3322/caac.21338 |
| [3] | Sheng M, Zhao Y, Wang F, et al. Targeted drugs for unselected patients with advanced non-small-cell lung cancer: a network meta-analysis[J]. J Thorac Dis,2016, 8 (1) : 98 –115. DOI:10.3978/j.issn.2072-1439.2016.01.28 |
| [4] | Brotelle T, Bay J O. PI3K-AKT-mTOR pathway: Description, therapeutic development, resistance, predictive/prognostic biomarkers and therapeutic applications for cancer[J]. Bull Cancer,2016, 103 (1) : 18 –29. DOI:10.1016/j.bulcan.2015.09.011 |
| [5] | Hussain A R, Al-Romaizan M, Ahmed M, et al. Dual Targeting of mTOR Activity with Torin2 Potentiates Anticancer Effects of Cisplatin in Epithelial Ovarian Cancer[J]. Mol Med,2015, 21 : 466 –478. DOI:10.2119/molmed.2014.00238 |
| [6] | Sadowski S M, Boufraqech M, Zhang L, et al. Torin2 targets dysregulated pathways in anaplastic thyroid cancer and inhibits tumor growth and metastasis[J]. Oncotarget,2015, 6 (20) : 18038 –18049. DOI:10.18632/oncotarget.3833 |
| [7] | Wang C, Wang X, Su Z, et al. The novel mTOR inhibitor Torin-2 induces autophagy and downregulates the expression of UHRF1 to suppress hepatocarcinoma cell growth[J]. Oncol Rep,2015, 34 (4) : 1708 –1716. DOI:10.3892/or.2015.4146 |
| [8] | Ye Y, Tang X, Sun Z, et al. Upregulated WDR26 serves as a scaffold to coordinate PI3K/AKT pathway-driven breast cancer cell growth, migration, and invasion[J]. Oncotarget,2016, 7 (14) : 17854 –17869. DOI:10.18632/oncotarget.7439 |
| [9] | Cai J, Xu L, Tang H, et al. The role of the PTEN/PI3K/Akt pathway on prognosis in epithelial ovarian cancer: a meta-analysis[J]. Oncologist,2014, 19 (5) : 528 –535. DOI:10.1634/theoncologist.2013-0333 |
| [10] | Chen J, O’Donoghue A, Deng Y F, et al. The effect of lycopene on the PI3K/Akt signalling pathway in prostate cancer[J]. Anticancer Agents Med Chem,2014, 14 (6) : 800 –805. DOI:10.2174/1871520614666140521121317 |
| [11] | Khan K H, Yap T A, Yan L, et al. Targeting the PI3K-AKT-mTOR signaling network in cancer[J]. Chin J Cancer,2013, 32 (5) : 253 –265. DOI:10.5732/cjc.013.10057 |
| [12] | Rizzo M, Carteni G, Pappagallo G, et al. The ORCHIDEE study: gathering new evidence on the use of everolimus in clinical practice[J]. Tumori,2014, 100 (6) : e290 –e292. DOI:10.1700/1778.19300 |
| [13] | Poh A. Expanding Therapy for Neuroendocrine Tumors[J]. Cancer Discov,2016, 6 (3) : 221 –222. DOI:10.1158/2159-8290.CD-NB2016-010 |
| [14] | Hsieh A C, Costa M, Zollo O, et al. Genetic dissection of the oncogenic mTOR pathway reveals druggable addiction to translational control via 4EBP-eIF4E[J]. Cancer Cell,2010, 17 (3) : 249 –261. DOI:10.1016/j.ccr.2010.01.021 |
| [15] | Faber A C, Coffee E M, Costa C, et al. mTOR inhibition specifically sensitizes colorectal cancers with KRAS or BRAF mutations to BCL-2/BCL-XL inhibition by suppressing MCL-1[J]. Cancer Discov,2014, 4 (1) : 42 –52. DOI:10.1158/2159-8290.CD-13-0315 |
| [16] | Chandarlapaty S, Sawai A, Scaltriti M, et al. AKT inhibition relieves feedback suppression of receptor tyrosine kinase expression and activity[J]. Cancer Cell,2011, 19 (1) : 58 –71. DOI:10.1016/j.ccr.2010.10.031 |
| [17] | Schwartz S, Wongvipat J, Trigwell C B, et al. Feedback suppression of PI3Kalpha signaling in PTEN-mutated tumors is relieved by selective inhibition of PI3Kbeta[J]. Cancer Cell,2015, 27 (1) : 109 –122. DOI:10.1016/j.ccell.2014.11.008 |
| [18] | Muranen T, Selfors L M, Worster D T, et al. Inhibition of PI3K/mTOR leads to adaptive resistance in matrix-attached cancer cells[J]. Cancer Cell,2012, 21 (2) : 227 –239. DOI:10.1016/j.ccr.2011.12.024 |
| [19] | Wagle N, Grabiner B C, Van-Allen E M, et al. Activating mTOR mutations in a patient with an extraordinary response on a phase Ⅰ trial of everolimus and pazopanib[J]. Cancer Discov,2014, 4 (5) : 546 –553. DOI:10.1158/2159-8290.CD-13-0353 |
| [20] | Wagle N, Grabiner B C, Van-Allen E M, et al. Response and acquired resistance to everolimus in anaplastic thyroid cancer[J]. N Engl J Med,2014, 371 (15) : 1426 –1433. DOI:10.1056/NEJMoa1403352 |
| [21] | Elkabets M, Vora S, Juric D, et al. mTORC1 inhibition is required for sensitivity to PI3K p110alpha inhibitors in PIK3CA-mutant breast cancer[J]. Sci Transl Med,2013, 5 (196) : 196ra99 . DOI:10.1126/scitranslmed.3005747 |
| [22] | Corcoran R B, Rothenberg S M, Hata A N, et al. TORC1 suppression predicts responsiveness to RAF and MEK inhibition in BRAF-mutant melanoma[J]. Sci Transl Med,2013, 5 (196) : 196ra98 . DOI:10.1126/scitranslmed.3005753 |



