2. 610083 成都,成都军区总医院:病理科 ;
3. 610083 成都,成都军区总医院:中医科
2. Department of Pathology, General Hospital of Chengdu Military Command, Chengdu, Sichuan Province, 610083, China ;
3. Department of Traditional Chinese Medicine, General Hospital of Chengdu Military Command, Chengdu, Sichuan Province, 610083, China
高温高湿环境下机体排热困难,体温升高,可引起机体不适并产生一系列的生理应激反应,包括呼吸频率及肺通气量增加、心率加快、消化功能抑制等,严重时可引发机体免疫功能、水电解质平衡、神经内分泌、血流动力学、能量代谢等系统和器官功能改变[1]。热习服(heat acclimatization,HA)作为一种有效和有益的训练,能够增强机体热适应和耐受能力,对热损伤有一定的保护作用[2-3]。现有大量高温高湿环境下热损伤的研究主要集中在热应激和热休克,热习服的研究则更多关注于热适应和热保护效应,对热习服过程中高温高湿可能引起机体生理病理改变的相关研究较少。凋亡是机体细胞程序性死亡的重要方式,在某种因素刺激下,凋亡相关基因和蛋白可诱导细胞产生相应的凋亡改变[4-5]。本研究采用人工模拟高温高湿环境,观察热习服过程中高温高湿对肺脏细胞凋亡及Bax、Bcl-2、Cyt-C等凋亡相关因子的影响,探讨高温高湿习服过程中可能的损伤作用和机制,为热习服时器官功能保护提供实验依据。
1 材料与方法 1.1 材料 1.1.1 实验动物20只3~4月龄清洁级健康雄性Sprague-Dawley(SD)大鼠[成都达硕生物科技有限公司提供,实验动物许可证号:scxk(川)2008-24],体质量(180±10)g,饲养于清洁环境。
1.1.2 仪器及试剂RXZ-1000A-zl多段编程人工气候箱(中国宁波江南仪器厂),Sorvell ST16R台式冷冻离心机,Excelsior ES自动组织脱水机,HistoStar组织包埋机,Finesse E+石蜡切片机,Leica DM3000显微镜,KIA-T10组织匀浆器,Thermo Multiskan GO全波长酶标仪,Promega GloMaxTM 20/20发光检测仪,SANYO MDF-U53V -80 ℃低温冰箱等。武汉博士德(BOSTER)生物工程有限公司细胞凋亡检测试剂盒、碧云天生物素复染液、武汉伊莱瑞特(Elabscience)生物科技有限公司Bax、Bcl-2、Cyt-C酶联免疫检测试剂盒,ATP-Na标准品(Sigma)、荧光素酶(中科院上海植物生理研究所)、北京索莱宝(Solarbio)科技有限公司BCA蛋白浓度测定试剂盒。
1.2 方法 1.2.1 动物模型制作大鼠按随机数字表法分为高温高湿环境组和常温常湿对照组,每组10只动物。参照文献[6]的方法,采用人工气候箱模拟高温高湿环境条件,设置温度为35 ℃、相对湿度90%~95%,实验组动物每天置于箱内10 h,连续处理30 d。对照组饲养于清洁环境,环境条件:22~26 ℃,相对湿度40%~60%。动物模型制作完成后,乙醚麻醉,取肺组织标本保存于-80 ℃待测。另取肺脏组织以10%甲醛固定,石蜡切片,光镜下观察HE染色病理改变,TUNEL观察细胞凋亡情况。
1.2.2 指标检测 1.2.2.1 原位缺口末端标记法(TUNEL)测定肺组织细胞凋亡取肺组织石蜡切片,依照试剂说明书分别经消化、标记、封闭,加入抗体,DAB显色,苏木精复染等步骤,封片,以细胞核有棕黄色颗粒者为阳性细胞,观察并计数5个高倍视野(×400)下凋亡细胞数,凋亡指数(apoptosis index,AI)=凋亡细胞数/5个高倍视野检测到的细胞总数×100%,实验同时以PBS代替抗体制作阴性对照片。
1.2.2.2 ATP含量检测称取肺组织约200 mg,以2 mL 0.4 mol/L的HCLO4匀浆去蛋白,荧光素酶法检测组织ATP含量。
1.2.2.3 Bax、Bcl-2、Cyt-C含量检测称取肺组织约100 mg以1 mL生理盐水制成组织匀浆,4 ℃条件下3 000 r/min离心10 min,取上清液以12 000 r/min离心15 min,弃沉淀,上清液即为去除线粒体的胞质提取液,采用ELISA检测Bax、Bcl-2、Cyt-C含量,严格按说明书操作,酶标仪测定450 nm波长下光密度值,依标准曲线计算样品中含量。BCA测定组织匀浆蛋白含量。
1.3 统计学分析采用SPSS 13.0统计软件。实验结果以x±s表示。采用Levene’s检验分析实验组与对照组方差齐性。各变量两组方差均齐同,采用成组t检验比较两组差异。
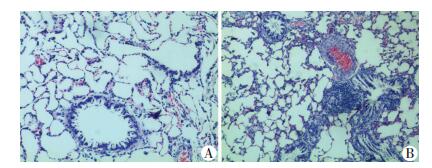
2 结果 2.1 常规病理切片光镜下观察常温常湿对照组肺泡腔清晰,肺泡隔结构正常(图 1A)。高温高湿环境组肺泡隔增宽、水肿,毛细血管增生、扩张充血;血管及支气管周围淋巴细胞浸润(图 1B)。
|
| A:对照组;B:实验组 图 1 两组大鼠肺脏组织病理学变化(HE ×40) |
2.2 肺组织细胞凋亡检测
常温常湿对照组少见细胞核呈棕黄色或棕褐色的阳染颗粒,高温高湿环境组阳染颗粒增多,主要为支气管上皮细胞和肺泡上皮细胞(图 2A、B),凋亡指数为(20.79±7.65),显著高于对照组[(3.81±1.90),t=8.339,P < 0.01]。

|
| A:对照组;B:实验组 图 2 两组肺组织细胞凋亡情况(TUNEL ×400) |
2.3 肺组织细胞胞质中Bax、Bcl-2、Cyt-C和ATP含量变化
与常温常湿对照组比较,高温高湿环境组大鼠肺组织细胞胞质中Bax含量升高了53.07%(P < 0.001),Bcl-2升高11.23%,但与对照组比较差异无统计学意义(P=0.081),Bax/Bcl-2升高30.18%(P=0.021),Cyt-C升高了85.36%(P < 0.001),ATP含量降至对照组的69.30%(P=0.002,表 1)。
| 组别 | Bax(pg/mg) | Bcl-2(pg/mg) | Bax/Bcl-2 | Cyt-C(pg/mg) | ATP(μmol/g) |
| 常温常湿对照组 | 48.489±9.851 | 45.973±6.200 | 1.130±0.349 | 10.347±2.876 | 2.723±0.358 |
| 高温高湿环境组 | 74.222±8.798 | 51.136±6.289 | 1.471±0.248 | 19.179±3.946 | 1.887±0.636 |
| t值 | 6.161 | 1.849 | 2.519 | 5.719 | 3.622 |
| P值 | < 0.001 | 0.081 | 0.021 | < 0.001 | 0.002 |
3 讨论
环境温度达到或超过35 ℃,相对湿度超过80%即属于高温高湿环境[7]。而连续21~30 d的反复适应性训练可获得细胞和系统对热负荷的习服[8-9]。有研究表明[10],经过热习服训练的个体,体温升高幅度低、升速较慢,皮质醇浓度相对较低,受热时安静,可耐受外界较高的环境温度,机体没有出现明显的应激反应;但由于反复的受热,热习服动物比热应激动物更易出现电解质紊乱、低血糖等表现。本研究采用人工气候箱模拟高温高湿环境,结果表明,每天处于35 ℃,相对湿度90%环境10 h,持续30 d,大鼠肺脏细胞凋亡指数显著增加,表明热习服过程中,长期反复的热刺激可导致组织细胞产生明显的凋亡改变。
线粒体是维持细胞生命活动的能量基地,90%以上ATP来自于线粒体的氧化磷酸化。Cyt-C是线粒体呼吸链中传递电子的载体,正常情况下存在于线粒体内膜和外膜之间的腔隙内。大量研究表明,线粒体凋亡途径是细胞凋亡的主要途径之一[11-12],在此途径中,Bax受凋亡信号刺激位移到线粒体外膜,形成线粒体内部通向胞质的同源或异源二聚体蛋白孔道,促使线粒体内Cyt-C向胞质释放,激活并启动半胱氨酸蛋白酶(Caspases)级联反应,引发凋亡[13]。Bax是促细胞凋亡因子,Bcl-2是抑细胞凋亡因子,正常情况下Bax与Bcl-2的表达量处于相对稳态,二者发挥着相互拮抗的作用,作用结果取决于Bax或Bcl-2蛋白的表达量,以及Bax/Bcl-2的比率,Bax/Bcl-2升高促进凋亡,反之则抑制凋亡[14]。本研究为避免线粒体所含成分对检测结果的影响,制备了去线粒体细胞提取液,实验结果显示,高温高湿环境组大鼠肺组织细胞Bax含量显著升高(P < 0.001),Bax/Bcl-2较常温常湿对照组升高了30.18%(P=0.021),胞质中Cyt-C较对照组升高了85.36%(P < 0.001),而ATP含量降至对照组的69.30%(P=0.002)。表明高温高湿环境下,机体可能通过Bax/Bcl-2途径促使Cyt-C从线粒体内释放到细胞质,导致细胞凋亡[15-17],同时线粒体呼吸链电子传递受损,氧化磷酸化失偶联,使ATP合成障碍,能量代谢失衡,细胞生命活动受到抑制。
本研究实验对象为大鼠,汗腺不发达,呼吸蒸发是其散热的主要形式,而高温高湿环境可使蒸发量相对减少,刺激呼吸频率增加,过度通气不仅没有起到散热作用,还可能加重肺脏组织细胞的功能、结构变化。总之,高温高湿环境可造成机体器官功能的影响和损害,习服训练能提高对极端环境的适应性,减轻应激损害程度。但习服过程中高温高湿的反复刺激,使细胞发生凋亡改变,同时伴有能量供应不足等损伤因素,亦可导致机体产生蓄积性损伤效应。
| [1] | Liu Z F, Li B L, Tong H S, et al. Pathological changes in the lung and brain of mice during heat stress and cooling treatment[J]. World J Emerg Med,2011, 2 (1) : 50 –53. DOI:10.5847/wjem.j.1920-8642.2011.01.009 |
| [2] | 易均凤. 热习服及其交叉耐受的研究进展[J]. 热带医学杂志,2015, 15 (2) : 276 –279. |
| [3] | Kaldur T, Kals J, Oopik V, et al. Effects of heat acclimation on changes in oxidative stress and inflammation caused by endurance capacity test in the heat[J]. Oxid Med Cell Longev,2014, 2014 : 107137 . DOI:10.1155/2014/107137 |
| [4] | Wlodkowic D, Telford W, Skommer J, et al. Apoptosis and beyond: cytometry in studies of programmed cell death[J]. Methods Cell Biol,2011, 103 : 55 –98. DOI:10.1016/B978-0-12-385493-3.00004-8 |
| [5] | 马晓东, 李扬, 梁永平. 高温高湿环境对大鼠创伤性脑水肿的影响[J]. 军医进修学院学报,2012, 33 (1) : 66 –70. |
| [6] | 李昆, 郭鑫, 杨芸, 等. 高湿环境对大鼠肝脏异柠檬酸脱氢酶及α-酮戊二酸脱氢酶的影响[J]. 第三军医大学学报,2013, 35 (23) : 2595 –2596. DOI:10.16016/j.1000-5404.2013.23.004 |
| [7] | 朱童, 詹剑华. 高温环境热应激研究进展[J]. 职业与健康,2010, 26 (9) : 1061 –1063. |
| [8] | Sawka M N, Leon L R, Montain S J, et al. Integrated physiological mechanisms of exercise performance, adaptation, and maladaptation to heat stress[J]. Compr Physiol,2011, 1 (4) : 1883 –1928. DOI:10.1002/cphy.c100082 |
| [9] | 王涛, 王静, 王尚, 等. 热习服兔实验模型的建立及其病理生理特征[J]. 中国应用生理学杂志,2013, 29 (5) : 473 –476. DOI:10.13459/j.cnki.cjap.2013.05.002 |
| [10] | 朱国标, 栗群英, 李继红, 等. 热习服和热应激生物学效应差别的实验研究[J]. 西南国防医药,1999, 9 (4) : 204 –207. |
| [11] | Bender C E, Fitzgerald P, Tait S W, et al. Mitochondrial pathway of apoptosis is ancestral in metazoans[J]. Proc Natl Acad Sci U S A,2012, 109 (13) : 4904 –4909. DOI:10.1073/pnas.1120680109 |
| [12] | Stoyanoff T R, Todaro J S, Aguirre M V, et al. Amelioration of lipopolysaccharide-induced acute kidney injury by erythropoietin: involvement of mitochondria-regulated apoptosis[J]. Toxicology,2014, 318 : 13 –21. DOI:10.1016/j.tox.2014.01.011 |
| [13] | Ola M S, Nawaz M, Ahsan H. Role of Bcl-2 family proteins and caspases in the regulation of apoptosis[J]. Mol Cell Biochem,2011, 351 (1/2) : 41 –58. DOI:10.1007/s11010-010-0709-x |
| [14] | Huttemann M, Pecina P, Rainbolt M, et al. The multiple functions of cytochrome c and their regulation in life and death decisions of the mammalian cell: From respiration to apoptosis[J]. Mitochondrion,2011, 11 (3) : 369 –381. DOI:10.1016/j.mito.2011.01.010 |
| [15] | Landes T, Martinou J C. Mitochondrial outer membrane permeabilization during apoptosis: the role of mitochondrial fission[J]. Biochim Biophys Acta,2011, 1813 (4) : 540 –545. DOI:10.1016/j.bbamcr.2011.01.021 |
| [16] | Lofrumento D D, La-Piana G, Abbrescia D I, et al. Valinomycin induced energy-dependent mitochondrial swelling, cytochrome c release, cytosolic NADH/cytochrome c oxidation and apoptosis[J]. Apoptosis,2011, 16 (10) : 1004 –1013. DOI:10.1007/s10495-011-0628-7 |
| [17] | Chang Z, Xing J, Yu X. Curcumin induces osteosarcoma MG63 cells apoptosis via ROS/Cyto-C/Caspase-3 pathway[J]. Tumour Biol,2014, 35 (1) : 753 –758. DOI:10.1007/s13277-013-1102-7 |



