2. 121001 辽宁 锦州,辽宁医学院:放射科 ;
3. 121001 辽宁 锦州,辽宁医学院:护理学院
2. Department of Radiology, the First Affiliated Hospital of Liaoning Medical College, Liaoning Medical College, Jinzhou, Liaoning Province, 121001, China ;
3. College of Nursing, Liaoning Medical College, Jinzhou, Liaoning Province, 121001, China
血管性痴呆(vascular dementia, VD)是脑血管病引起的脑损害所致的痴呆,是继阿尔茨海默病之后的第二大常见痴呆,具有较高的病死率和致残率。目前其发病机制仍不十分清楚。有研究表明,认知障碍的发生与额叶、顶叶、丘脑的功能改变有关[1-2]。然而,目前据此制定的治疗方案对VD的早期预防效果仍不理想。近年来大量研究发现小脑病变可引起小脑认知情感障碍[3],我们前期观察VD大鼠小脑顶核形态学变化及活化型Caspase-3、PARP-1的表达时发现VD大鼠顶核神经元细胞数较假手术组减少,证实了VD大鼠小脑顶核发生了损伤[4]。也有研究发现电刺激小脑顶核可明显改善VD患者的认知功能[5],而我们前期研究也证实电刺激小脑顶核可明显改善VD大鼠的抑郁状态[6]。因此,我们推测血管性痴呆的发生与小脑的功能改变有关。为此,本研究采用氢质子磁共振波谱(1H-MR spectroscopy,1H-MRS)技术检测VD患者的小脑物质代谢的改变,并探讨其与认知损害间的关系。
1 资料与方法 1.1 分组及入组标准 1.1.1 卒中组收集2013年10月至2015年12月辽宁医学院第一附属医院神经内科符合纳入和排除标准的住院患者40例。查体神志清楚,均为右利手,既往无神经系统及精神系统疾病,否认家族遗传病史。
纳入标准:①近3个月内患有脑卒中,且符合中国急性缺血性脑卒中诊治指南(2014)中的脑梗死的诊断要点,并经头MRI证实;②经头MRI证实为单侧基底节脑梗死;③年龄45~65岁;④发病前社会适应能力良好,发病后能配合进行认知功能测试。排除标准:①短暂性脑缺血发作及各种脑出血;②有颅内肿瘤、脑积水、蛛网膜下腔出血、动静脉畸形、癫痫、脑部手术病史者;③甲状腺功能低下、维生素B12或叶酸缺乏以及梅毒患者等;④有脑炎、脑外伤等病史;⑤患有某些干扰认知功能评价的疾病,如嗜酒、某些精神性药物滥用者;⑥严重的心肝肾功能障碍者;⑦有MRI检查禁忌者;⑧额颞叶、丘脑、小脑梗死。
1.1.2 对照组选择与卒中组患者年龄、性别、教育程度相匹配的志愿者20名,均为右利手,既往无神经系统及精神系统疾病,否认家族遗传病史。该20名志愿者来源于2013年10月至2015年12月到辽宁医学院第一附属医院神经内科就诊的非脑血管病患者。
研究经辽宁医学院附属第一医院伦理委员会通过,所有患者签署知情同意书。
1.2 方法 1.2.1 1H-MRS检查方法使用3.0T超导磁共振(德国西门子),以T1WI序列行MRI常规扫描排除脑部病变,并为1H-MRS定位,本研究采用三轴(X轴、Y轴、Z轴)定位,感兴趣区定位于小脑深部核团。定位后选择感兴趣区VOI 16×16,体素大小为1 cm×1 cm×1.5 cm,避开颅骨、气腔、脂肪及脑脊液等结构,并使用饱和带以避免周围组织对检查结果的影响。
采用MRS头颅专用线圈,利用3D-CSI序列对受试者进行单体素1H-MRS扫描(TR=1 700 ms,TE=135 ms),扫描完成后使用随机LEONORDA程序进行基线、相位校正。观察的代谢指标:乙酰天门冬氨酸盐(N-acetyl aspartate,NAA)、胆碱(choline complex,Cho)、肌酸(creatine,Cr)等,并计算NAA/Cr、Cho/Cr的比值以及进行相对定量分析。所有扫描由同一经验丰富的放射科医师操作,并将所有图像录于光盘,在同一时间测量。
1.2.2 认知功能的评估所有受试者均由同一名受专业训练的神经科医生进行蒙特利尔量表(Montreal cognitive assessment,MoCA)及简易的精神状态量表(mini-mental state examination,MMSE)评分,根据评分将卒中组分为2个亚组:MoCA评分≥25分和MoCA评分 < 25分,且MMSE评分17分 < 文盲组 < 20分、20分 < 小学组 < 25分、中学及以上组 > 22分为卒中后非痴呆组;MoCA评分 < 25分,MMSE评分文盲组≤17分、17分 < 小学组≤20分、20分 < 中学及以上组≤22分为卒中后痴呆组(VD组)。对各组的一般情况(包括年龄、性别、受教育年限)进行比较分析。
1.2.3 小脑各物质代谢产物变化与MoCA评分之间的相关性分析对VD组、卒中后非痴呆组患者MoCA评分与1H-MRS测得的各代谢产物的相关性进行分析。
1.3 统计学方法利用SPSS 17.0统计软件,计量资料采用x±s的形式表示,多组间均数比较采用方差分析,组间多重比较采用LSD法,计数资料间比较采用χ2检验,相关性分析采用Pearson线性相关性分析。以P < 0.05认为差异有统计学意义。
2 结果 2.1 认知功能和一般情况评估对照组MoCA评分均≥25分,各组的认知功能评分和一般情况见表 1。VD组、卒中后非痴呆组、对照组比较,性别、年龄、受教育年限等一般资料比较差异均无统计学意义(P > 0.05),具有可比性。MoCA评分间差异具有统计学意义(P < 0.05)。
| 组别 | 例数 | 性别(男/女) | 年龄(岁) | 受教育年限(年) | MoCA评分 |
| 对照组 | 20 | 10/10 | 54.95±4.83 | 7.20±2.02 | 27.85±1.84 |
| 卒中组 | |||||
| VD组 | 22 | 10/12 | 54.82±6.25 | 8.68±2.15 | 18.36±1.97 |
| 卒中后非痴呆组 | 18 | 9/9 | 53.89±5.68 | 8.28±2.91 | 24.89±1.78 |
| P值 | > 0.05 | > 0.05 | > 0.05 | < 0.05 | |
2.2 1H-MRS检测小脑物质代谢
对3组各代谢物质进行自身对照比较,卒中后非痴呆组病灶同侧与对侧、对照组左右侧小脑半球NAA/Cr及Cho/Cr比值差异均无统计学意义(P>0.05);VD组病灶对侧及同侧NAA/Cr、Cho/Cr比值差异有统计学意义(P < 0.05,表 2)。与卒中后非痴呆组病灶对侧小脑及对照组左侧小脑比较,VD组患者病灶对侧NAA/Cr比值降低(z=-0.120,P=0.002;z=-0.138,P=0.03),Cho/Cr比值升高(z=0.10,P=0.011;z=0.114,P=0.017,图 1)。
| 组别 | 例数 | NAA/Cr | Cho/Cr | |||
| 病灶对侧 | 病灶同侧 | 病灶对侧 | 病灶同侧 | |||
| 对照组 | 20 | 0.963±0.089b | 0.971±0.084 | 0.770±0.150b | 0.786±0.166 | |
| 卒中组 | ||||||
| VD组 | 22 | 0.879±0.121a | 1.019±0.089 | 0.952±0.991a | 0.847±0.152 | |
| 卒中后非痴呆组 | 18 | 0.998±0.118b | 0.973±0.108 | 0.851±0.145b | 0.829±0.174 | |
| 对照组病灶对侧对应为左侧,病灶同侧对应为右侧 a:P < 0.05,与病灶同侧比较;b:P < 0.05,与VD组比较 | ||||||
|
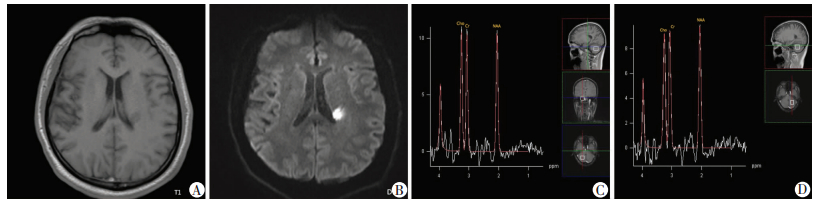
| A、B:分别为MRI平扫T1WI、DWI;C、D:分别为1H-MRS病变对侧和病变同侧 图 1 VD组患者MRI平扫及双侧小脑半球1H-MRS检测 |
2.3 卒中患者代谢物质比值与MoCA评分间的相关性
VD组病灶对侧1H-MRS检测的代谢物质与MoCA评分间具有相关性,且MoCA与NAA/Cr比值呈正相关(r=0.590,P=0.004),与Cho/Cr比值呈负相关(r=-0.569,P=0.006)。卒中后非痴呆组病灶对侧NAA/Cr、Cho/Cr与MoCA评分间无相关性(P > 0.05)。
3 讨论本研究应用1H-MRS技术来观察卒中后患者小脑物质代谢的变化,并探讨其物质变化与认知损伤之间的关系。1H-MRS是用来观察活体细胞物质代谢的无创性检测方法,可检测到的代谢物质包括NAA、Cho和Cr等。本研究将NAA/Cr、Cho/Cr作为观察指标,NAA/Cr比值的降低被理解为神经细胞的丢失或功能异常,Cho/Cr比值增高反映细胞繁殖旺盛[7-8]。
本研究发现,VD组患者的病灶对侧小脑NAA/Cr、Cho/Cr比值与病变同侧存在差异,且NAA/Cr比值较病变同侧降低,Cho/Cr比值较病变同侧增高,且均具有统计学意义。而非痴呆组和对照组代谢物质比值自身双侧对比,均无统计学差异。这提示VD患者病灶对侧小脑存在一定程度的神经功能异常和神经细胞或胶质细胞的改变,造成了NAA/Cr值的降低和Cho/Cr值的增高。有关VD患者病变对侧小脑代谢物质发生改变的机制目前尚不清楚。目前有学说认为这可能与“交叉性小脑功能联系不全(crossed cerebellar diaschisis,CCD)”有关。CCD是指一侧大脑半球的损伤,如下丘脑、基底节、海马等区域的损伤,均可通过该部位与小脑之间的突触联系(如“额叶-脑桥-小脑”环路)引起对侧远隔部位的小脑代谢及血流量的减低,从而引起小脑物质代谢的改变[9-10]。同时,本研究对VD组NAA/Cr值与MoCA评分进行相关性分析,结果显示两者呈显著正相关。因此,我们推测卒中病灶对侧小脑神经元功能异常甚至神经元的丧失可能参与了VD的发生,而NAA/Cr值有可能在临床上作为一种客观定量指标用来对VD患者进行筛查及风险评估。
本研究主要选择小脑深部核团作为感兴趣区,VD组病灶对侧小脑深部核团NAA/Cr比值较病灶同侧、卒中后非痴呆组及对照组明显降低,Cho/Cr比值较病灶同侧、卒中后非痴呆组及对照组明显增高,且均有统计学意义(P < 0.05)。因此,可以推测VD患者病灶对侧小脑深部核团的物质代谢发生了改变,这种改变预示着深部核团细胞的功能异常甚至凋亡,并伴有胶质细胞的增生。同时,我们将其与MoCA评分进行相关性分析,结果显示NAA/Cr与MoCA呈正相关,Cho/Cr与MoCA呈负相关,说明小脑深部核团的这种物质代谢的改变与认知损伤相关。采用小脑顶核电刺激治疗不同程度血管性认知障碍,随后观察其疗效证实了电刺激小脑顶核显著改善了VD患者的认知功能[11-12]。我们的前期工作亦表明,血管性痴呆的大鼠小脑顶核的细胞形态学发生了变化,均与本研究的结果相符,但各个核团与VD的发生及核团间的联系仍不明确,仍需进一步研究。
解剖学将小脑分为古小脑、旧小脑、新小脑。新小脑又称大脑小脑,位于小脑外侧部,很多研究表明其与大脑皮层之间存在广泛的纤维联系(如大脑-脑桥-小脑投射[13]),与大脑共同参与认知及情感功能的调控[14]。我们前期在观察卒中后抑郁大鼠小脑蒲肯野细胞形态学改变及神经元凋亡情况中发现,一侧大脑半球的缺血可引起对侧小脑蒲肯野细胞的损伤,且小脑的这种改变与PSD的发生有关[15]。故在解剖学上进一步说明了小脑参与了VD的发生。
本研究尽管也选择了各区小脑皮层作为感兴趣区,然而,由于此感兴趣区选于小脑皮层,易受脑脊液干扰,未能得到有效数据,尚需大样本实验进一步研究。由于本研究MoCA及MMSE量表评分具有一定的主观性且样本量偏小,尚需要进一步扩大样本量的研究。
本研究从神经生化的水平上定量探讨了VD患者小脑内物质代谢的变化及其与认知损害之间的相关性,初步证实小脑的代谢异常参与了血管性痴呆的发生。本研究为血管性痴呆发病机制的深入研究提供了新的思路,为其早期预防提供了新线索。
| [1] | 刘忠玲, 李华. 事件相关电位P300和蒙特利尔认知评估量表对不同部位脑卒中患者早期认知功能的评估价值研究[J]. 中国全科医学,2013, 16 (7B) : 2338 –2342. DOI:10.3969/j.issn.1007-9572.2013.20.008 |
| [2] | 董艳红, 贾彩云, 陈慧芳, 等. 磁共振波谱与弥散张量成像联合评价皮质下血管性认知功能障碍左丘脑损害[J]. 中国神经精神疾病杂志,2014, 40 (3) : 143 –148. DOI:10.3936/j.issn.1002-0152.2014.03.004 |
| [3] | Alexander M P, Gillingham S, Schweizer T, et al. Cognitive impairments due to focal cerebellar injuries in adults[J]. Cortex,2012, 48 (8) : 980 –990. DOI:10.1016/j.cortex.2011.03.012 |
| [4] | 夏海苗, 隋汝波, 张磊, 等. 血管性痴呆大鼠小脑顶核形态学变化及活化型Caspase-3、PARP-1的表达[J]. 山东大学学报:医学版,2014, 52 (8) : 34 –38. DOI:10.040/j.issn.1671-7554.0.2014.104 |
| [5] | 陈松盛, 何娅, 袁平花. 电刺激小脑顶核对血管性痴呆认知功能及血液流变学的影响[J]. 陕西医学杂志,2013, 42 (6) : 731 –732. DOI:10.3969/j.issn.1000-7377.2013.06.043 |
| [6] | 李宝强, 隋汝波, 张磊, 等. 小脑顶核电刺激干预在卒中后抑郁大鼠细胞因子发病机制中的作用[J]. 解放军医学院学报,2013, 34 (5) : 502 –505. DOI:10.3969/j.issn.2095-5227.2013.05.025 |
| [7] | Morana G, Piccardo A, Puntoni M, et al. Diagnostic and prognostic value of 18F-DOPA PET and 1H-MRS spectroscopy in pediatric supratentorial infiltrative gliomas: a comparative study[J]. Neuro Oncol,2015, 17 (12) : 1637 –1647. DOI:10.1093/neuonc/nov099 |
| [8] | 谭子虎, 兰汉超, 杨琼, 等. 非痴呆型血管性认知功能障碍的磁共振波谱分析特点[J]. 临床神经病学杂志,2013, 26 (5) : 325 –328. |
| [9] | Komaba Y, Mishina M, Utsumi K, et al. Crossed cerebellar diaschisis in patients with cortical infarction: logistic regression analysis to control for confounding effects[J]. Stroke,2004, 35 (2) : 472 –476. DOI:10.1161/01.STR.0000109771.56160.F5 |
| [10] | Massaro A M. Teaching NeuroImages: Crossed cerebellar diaschisis in hemispheric status epilepticus[J]. Neurology,2012, 79 (20) : e182 . DOI:10.1212/WNL.0b013e318274de51 |
| [11] | 韩颖, 李来有, 史欣, 等. 电刺激小脑顶核治疗不同程度血管性认知障碍的疗效研究[J]. 中国全科医学,2012, 15 (5C) : 1677 –1680. DOI:10.3969/j.issn.1007-9572.2012.15.006 |
| [12] | Sui R, Zhang L. Cerebellar dysfunction may play an important role in vascular dementia[J]. Medical Hypotheses,2012, 78 (1) : 162 –165. DOI:10.1016/j.mehy.2011.10.017 |
| [13] | Fitzpatrick L E, Crowe S F. Cognitive and Emotional Deficits in Chronic Alcoholics: a Role for the Cerebellum?[J]. Cerebellum,2013, 12 (4) : 520 –533. DOI:10.1007/s12311-013-0461-3 |
| [14] | Villanueva R. The cerebellum and neuropsychiatric disorders[J]. Psychiatry Res,2012, 198 (3) : 527 –532. DOI:10.1016/j.psychres.2012.02.023 |
| [15] | 刘丹丹, 隋汝波, 张磊, 等. 卒中后抑郁大鼠小脑浦肯野细胞形态学改变及神经元凋亡情况研究[J]. 中国全科医学,2014, 17 (15) : 1744 –1748. DOI:10.3969/j.issn.1007-9572.2014.15.014 |



