对人类视觉功能或眼部疾病进行研究时经常需要借助动物实验作为基础和准备[1]。眼科动物实验首先需要评价动物的视功能,人类可以通过视敏度等主观视觉反应来获得定性或定量的数据,但实验动物只能通过辅助的检查客观评估视功能。视觉电生理具有客观、定量、无创等优势,是视功能检查的重要组成部分,应用广泛[2]。非灵长类动物与人类眼球形态和结构方面的差异较大,不能很好地用于指导人类手术和实验[3]。灵长类动物,如猕猴,进化史与人类相近,整个视觉系统的结构和功能与人类非常相似,作为眼科实验动物模型被广泛应用[4]。本研究比较了人与猕猴视网膜电图及视觉诱发电位的异同,为进一步将猕猴作为眼科实验动物提供数据支持。
1 材料与方法 1.1 实验对象猕猴两雄一雌共3只(6眼),3~4岁龄(相当于人类15~20岁),来源于重庆硕斯灵长类动物研究有限公司猕猴养殖基地,合格证号: SCXR(渝) 2008-0001,眼前节及眼底检查无明显异常。选取健康成年人8例(16眼),年龄15~23岁,眼前节及眼底无明显异常,最佳矫正视力>1.0。该研究经项目合作单位香港大学医学院伦理委员会批准。所有人均在了解该检查措施的风险后签署知情同意书。
1.2 眼底照相及光学相干断层扫描猕猴禁食禁饮6 h,舒眠宁(主要成分为氯胺酮,南京农业大学小动物疾病研究室)0.2 mL/kg臀部肌肉注射麻醉,眼部滴入美多丽(复方托吡卡胺滴眼液,参天制药株式会社,日本)充分散瞳后倍诺喜(盐酸奥布卡因滴眼液,参天制药株式会社,日本)眼球表面麻醉,调整猕猴眼球位置与镜头至合适距离,以视盘定位,运用眼底照相机(Kowanonmyd a-D 5MEGA,日本)行眼底照相。照相完成后运用OCT机器(HEID-ELBERG EGINEERING,德国)行OCT扫描,扫描方式为3D-Scan。
1.3 视觉电生理检测本研究视觉电生理检测项目为:闪光视网膜电图(FERG),闪光视觉诱发电位(FVEP),图形视网膜电图(PERG),图形视觉诱发电位(PVEP)。所有检测参数均参照国际电生理协会(ISCEV)最新标准设置[5]。检测仪器为(RETI-scan,ROLAND CONSULT,德国),麻醉方式同前,70%酒精消毒需要接电极部位。
记录电极置于枕骨粗隆上2~3 cm,参考电极置于前额正中,接地电极置于耳垂,非测试眼遮盖,用儿童用开睑器开睑,先右后左眼的顺序记录PVEP。
参考电极接于双眼的外眦部,接地电极接于前额正中,用小儿开睑器张开双眼睑,用倍诺喜双眼表面麻醉后滴加亮视(羟甲基纤维素钠,艾尔建制药公司,爱尔兰)于角膜接触电极后放入双眼,与角膜完全接触,记录PERG。
FVEP电极位置与PVEP相同,将猕猴固定于刺激器前方,单眼记录。
记录完FVEP后用美多丽散瞳,并在暗室环境下暗适应30 min,按顺序记录暗适应0.01 ERG,暗适应3.0 ERG,暗适应Ops,明适应10 min后,记录明适应3.0 ERG,明适应30 Hz震荡电位。
人类视网膜电图及视觉诱发电位检测过程、电极放置部位及刺激参数与猕猴相同。两者所用电极略有不同:检测ERG的记录电极为环状角膜电极(Roland Consult,德国),参考电极及接地电极为针状电极(猕猴)或银-氯化银圆盘状表面电极(人)。VEP电极为针状电极(猕猴)或银-氯化银圆盘状表面电极(人),各电极自身阻抗均小于5 kΩ。
1.4 统计学分析将所有电生理数据导出,运用Igor软件行图像处理,SPSS 13.0行统计学分析,各参数用 ±s表示,猕猴与人的比较采用独立样本t检验。P<0.05为差异有统计学意义。
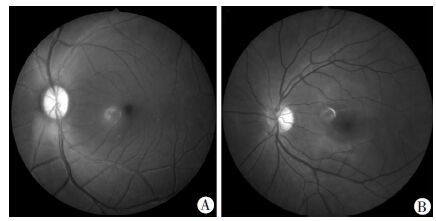
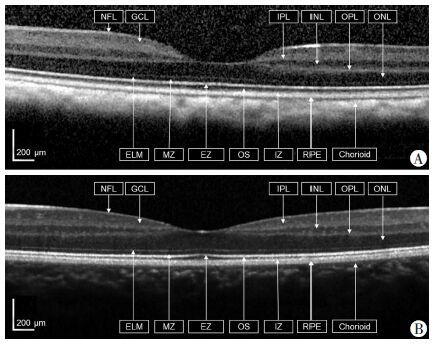
2 结果 2.1 猕猴眼底照相及光学相干断层扫描检测本研究所选择猕猴眼部无明显异常,通过检查可见猕猴眼底结构与人类相似:视盘边界清楚,血管从视盘发出后主要分为4支,血管走行相似,动静脉比约为2 ∶3,黄斑区毛细血管均较密集,有形态完整呈不规则状的血管拱环,黄斑中央凹反光可见(图 1)。通过光学相干断层扫描(OCT)检查可见猕猴视网膜各层次的显微结构与人类相近:可见明显的黄斑中央凹,节细胞层、内核层、外核层、椭圆体带等结构相同,清晰可辨,未见明显的异常高低荧光(图 2)。
|
| A:猕猴眼底观;B:人眼底观 图 1 猕猴和人眼底照相观察 |
|
| A:猕猴OCT扫描结果;B:人OCT扫描结果;NFL:神经纤维层;GCL:节细胞层;IPL;内丛状层:INL:内核层;OPL:外丛状层;ONL:外核层;ELM:外界膜;MZ:肌样带;EZ:椭圆体带;OS:光感受器外节;IZ:交错带:RPE:色素上皮层;Chorioid:脉络膜 图 2 猕猴和人光学相干断层扫描图形比较 |
2.2 FERG
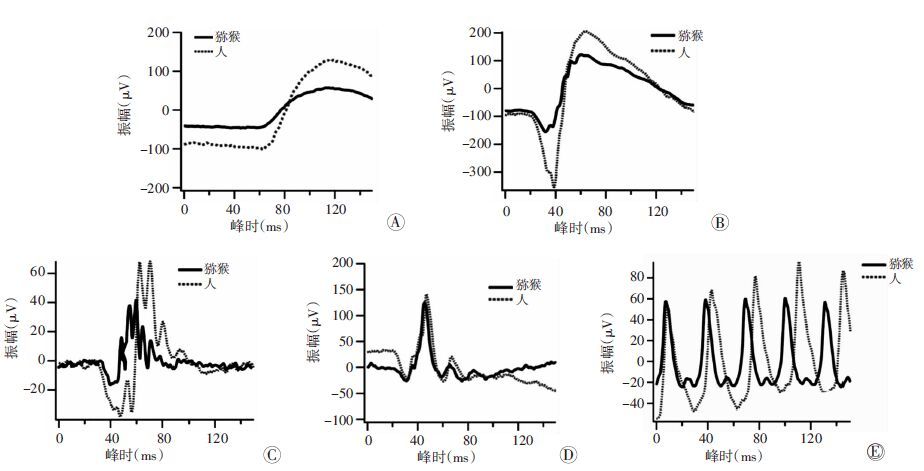
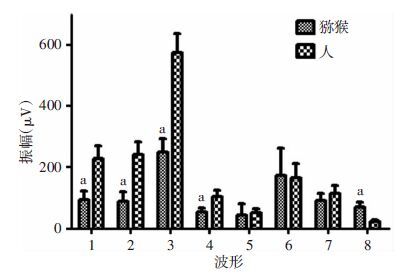
暗适应0.01ERG视杆细胞反应波形表现为不明显的a波及缓慢上升的b波,b波峰时猕猴与人相比明显较短(P<0.05),b波振幅猕猴与人相比明显较低(P<0.05)。暗适应3.0ERG最大混合反应波形由负向a波及正向b波组成,a波峰时猕猴与人相比明显较短(P<0.05),a波振幅猕猴与人相比明显较低(P<0.05),b波峰时猕猴与人相比明显较短(P<0.05),b波振幅猕猴与人相比明显较低(P<0.05)。猕猴与人类暗适应Ops波形相似,OS2波振幅猕猴与人相比明显较低(P<0.05)。猕猴与人明适应3.0ERG的a波,b波峰时和振幅,明适应30 Hz震荡电位振幅差异没有统计学意义(图 3~5)。
|
| A:暗适应0.01ERG检测波形;B:暗适应3.0ERG检测波形;C:暗适应Ops检测波形;D:明适应3.0ERG检测波形;E:明适应30 Hz flicker检测波形 图 3 猕猴与人FERG波形比较 |
|
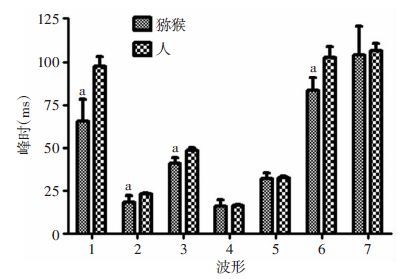
| 1:暗适应0.01ERG b波;2:暗适应3.0ERG a波;3: 暗适应3.0ERG b波;4:明适应3.0ERG a波;5:明适应3.0ERG b波;6:FVEP P2波;7:PVEP P100波 a:P<0.05,与人比较 图 4 猕猴与人视网膜电图及视觉诱发电位各波形的峰时对比 |
|
| 1:暗适应0.01ERG b波;2:暗适应3.0ERG a波;3:暗适应 3.0ERG b波;4:暗适应Ops OS2波;5:明适应3.0ERG a波; 6:明适应3.0ERG b波;7:明适应30 Hz P1波;8:FVEP P2波 a:P<0.05,与人比较 图 5 猕猴与人FERG、FVEP各波形振幅对比 |
2.3 FVEP
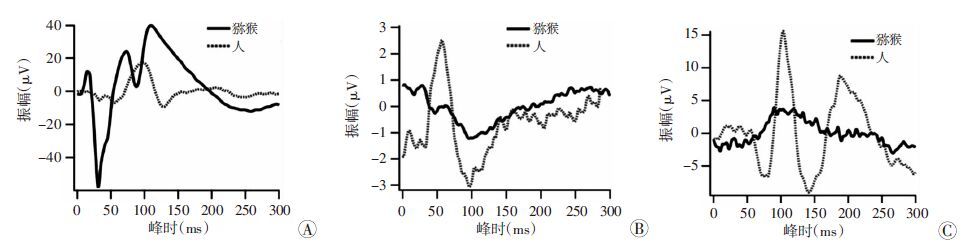
FVEP波形猕猴表现为1个负向的a波及向上的b波,P2波峰时猕猴与人相比明显较短(P<0.05),P2波振幅猕猴与人相比明显较高(P<0.05,图 4、5、6A)。
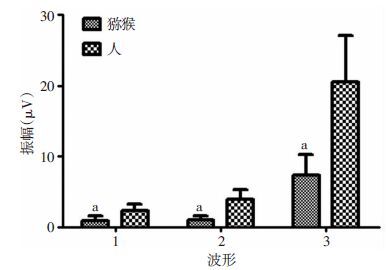
2.4 PERGPERG波形表现为明显的P50及N95,猕猴P50波振幅猕猴与人相比明显较低(P<0.05),N95振幅猕猴与人相比明显较低(P<0.05,图 4、6B、7)。
|
| A:FVEP检测波形;B:PERG检测波形;C:PVEP检测波形< 图 6 猕猴与人FVEP、PERG、PVEP波形比较 |
|
| 1:PERG P50波;2:PERG N95波;3:PVEP P100波 a:P<0.05,与人比较 图 7 猕猴与人PERG、PVEP各波形振幅对比(猕猴n=6,人n=16, ±s) |
2.5 PVEP
PVEP波形人表现为明显的N75,P100,N135波,而猕猴P100波较明显,P100波峰时猕猴与人差异无 统计学意义,P100波振幅猕猴与人相比较低(P<0.05,图 4、6C、7)。
3 讨论视觉电生理是阐明视觉系统各级神经元的生物电产生机理,研究如何验证和测定这些生物电的科学,为非侵袭性的检查方法,能够反复多次测量,客观的定量评价实验动物从视网膜到视皮质整个视觉传递通路的功能状态,能够反映视觉系统细微的功能下降,从而发现早期的组织损伤。正因为有以上优点,视觉电生理在视功能评价方面得到了广泛的应用[6]。
本研究FERG结果与同样使用氯胺酮为麻醉药品的Lei[7]及冷云霞[8]研究团队结果一致。以往的研究发现猕猴与人的眼部结构,视网膜血管走行、分级以及黄斑区血管拱环等有良好的相似性[9],视锥与视杆细胞的比例均为20 ∶1左右[10],但视网膜的大小猕猴略小于人。明适应3.0ERG的b波峰时和振幅、明适应30 Hz震荡电位振幅人与猕猴差异无统计学意义,说明猕猴视锥细胞功能与人类相似。暗适应0.01ERG反映全视网膜功能,猕猴峰时较短,振幅较低可能与视网膜的大小有关;暗适应3.0ERG、OPs振幅较低,说明猕猴的视杆细胞及内层细胞功能可能要弱于人类;另 外值得注意的是对于人Ops记录带宽为7.5~300 Hz,经过频谱分析猕猴主波范围在这范围之内,但300~500 Hz之间也有少量的波形出现。
FVEP是一种亮度反应,只能作为 确定受检者有无对光反应的检查,不能定量诊断,不要求受检者高度的合作,不需要矫正视力,即使受检者闭眼接受光刺激也能记录到VEP,可用于不能很好合作的受检者的检查[11],有研究表明睡眠时人的VEP增大,清醒或注意力集中时电位降低[12],本研究中猕猴FVEP的P2峰时短于人类,P2振幅大于人类。受检的猕猴处于麻醉睡眠状态,而人类是在清醒状态下做的检测,该结果说明麻醉状态下猕猴FVEP电反应强于人类。
闪光刺激视觉电生理是一种对亮度的反应,而图像刺激视觉电生理是一种亮度和图像结合的反应,需要受试者的配合,需要正常的感光系统,还需要正常的视觉中枢对图像特殊加工和处理[11]。明适应FERG测得数据猕猴与人类差异无统计学意义,说明两者视锥功能相似。但PERG反映黄斑区功能的P50波猕猴与人相比为低,且差异具有统计学意义,说明存在其他一些原因使得图形刺激猕猴所得视网膜电图及视觉诱发电位的波形振幅偏低。猕猴在麻醉状态下测试PERG及PVEP幅值较低可能原因为:①猕猴处于麻醉状态,本研究所用麻醉药物为舒眠宁,其主要成分为氯胺酮,肌肉注射后能迅速达到麻醉、镇痛效果[13],有研究发现其能够引起视觉电生理振幅的降低[14]。②麻醉状态下虽然运用开睑器,使视轴尽量正对图形显示器,但不能像人类受试者一样主动调整注视点至显示器上,可能引起注视点的轻度偏移,从而使得振幅降低。③虽然有研究表明称猕猴眼角膜、晶体等屈光介质的厚度、直径等参数与人类相同或非常接近[15],但也有研究表明笼养30月龄猕猴自发性近视发生率 可达86.7%,屈光度最高可达-3.3D[16]。本研究中所使用猕猴可能因为使用麻醉药物,存在固视不良及屈光不正等原因使测出的PERG及PVEP幅值较人低。
综上所述,猕猴与人类眼底及视网膜各层次结构相似,但本研究发现猕猴FERG明适应刺激条件下与人类峰时和振幅相似,暗适应刺激条件下视网膜电图猕猴峰时比人短,振幅比人低。FVEP的振幅高于正常人。PERG、PVEP电反应振幅低于人类。可见两者的检测结果有同有异,不能将人类的各检测项目的参考值范围直接应用于猕猴,有必要建立猕猴的正常数据库。同时本实验研究动物数量偏少,但验证了国内外使用同样麻醉药品的实验结果,提示以猕猴作为眼科实验动物时,ERG及VEP是可选用的视功能评价指标,应根据需要选择检测项目,并增大样本量建立正确的参考值范围。
| [1] | Alberts B. Model organisms and human health[J]. Science,2010, 330 (6012) : 1724 . DOI:10.1126/science.1201826 |
| [2] | 刘俊, 徐海伟, 李世迎, 等. 可见光诱导广西巴马小型猪视网膜变性的实验研究[J]. 第三军医大学学报,2013, 35 (24) : 2614 –2618. DOI:10.16016/j.1000-5404.2013.24.008 |
| [3] | Vaegan. Animal models of clinical electrophysiology of vision[J]. Doc Ophthalmol,2002, 104 (1) : 1 –3. |
| [4] | Qin Y, Tan X, Zhang Y, et al. A new nonhuman primate model of severe dry eye[J]. Cornea,2014, 33 (5) : 510 –517. DOI:10.1097/ICO.0000000000000085 |
| [5] | McCulloch D L, Marmor M F, Brigell M G, et al. ISCEV Standard for full-field clinical electroretinography (2015 update)[J]. Doc Ophthalmol,2015, 130 (1) : 1 –12. DOI:10.1007/s10633-014-9473-7 |
| [6] | 李世迎, 王刚. 重视临床视觉电生理检查的规范应用[J]. 第三军医大学学报,2015, 37 (12) : 1174 –1177. DOI:10.16016/j.1000-5404.201412110 |
| [7] | Lei B. The ERG of guinea pig (Cavisporcellus): comparison with Ⅰ-type monkey and E-type rat[J]. Doc Ophthalmol,2003, 106 (3) : 243 –249. |
| [8] | 冷云霞, 饶志波, 匡丽晖, 等. 正常恒河猴闪光视网膜电图特点的研究[J]. 国际眼科杂志,2012, 12 (7) : 1263 –1265. DOI:10.3969/j.issn.1672-5123.2012.07.12 |
| [9] | 孔祥梅, 孙兴怀, 俞道义, 等. 正常猕猴与人视网膜血管的比较[J]. 中国实验动物学报,2008, 16 (1) : 27 –30. DOI:10.3969/j.issn.1005-4847.2008.01.007 |
| [10] | Wikler K C, Williams R W, Rakic P. Photoreceptor mosaic: number and distribution of rods and cones in the rhesus monkey retina[J]. J Comp Neurol,1990, 297 (4) : 499 –508. DOI:10.1002/cne.902970404 |
| [11] | Nehamkin S, Windom M, Syed T U. Visual evoked potentials[J]. Am J ElectroneurodiagnosticTechnol,2008, 48 (4) : 233 –248. |
| [12] | 李海生, 潘家普. 视觉电生理的原理与实践[M]. 上海: 科学普及出版社, 2002 : 198 . |
| [13] | Flecknell P A. Injectable anaesthetics[M]. Philadelphia: WB Saunders, 1994 : 129 -156. |
| [14] | Lalonde M R, Chauhan B C, Tremblay F. Retinal ganglion cell activity from the multifocal electroretinogram in pig: optic nerve section, anaesthesia and intravitrealtetrodotoxin[J]. J Physiol,2006, 570 (Pt 2) : 325 –338. DOI:10.1113/jphysiol.2005.098046 |
| [15] | 黄秀榕, 祁明信, 李志雄, 等. 猕猴眼屈光间质及实用参数研究[J]. 福建中医学院学报,1997, 7 (2) : 15 –17. DOI:10.13261/j.cnki.jfutcm.000455 |
| [16] | 陈胜, 胡艳红, 冯春燕, 等. 笼养青幼年猕猴自发性近视的研究[J]. 中国医药导报,2015, 12 (36) : 17 –20. |



