Wu Depei,E-mail: wudepei@medmail.com.cn
近年来,随着新药的开发和新治疗方案的应用,靶向治疗以及免疫治疗的进展,急性淋巴细胞白血病(acute lymphocytic leukemia,ALL)的治疗缓解率和长期生存率明显提高,然而,仍然有15%~20%的成人ALL不能通过诱导化疗获得完全缓解(complete remission,CR),部分患者通过大剂量强化疗获得缓解后短期内即出现复发,再诱导化疗无效[1-2]。这类难治复发的ALL患者长期存活率低,预后极差,异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)是目前这类患者争取长期生存的唯一有效手段。一般情况下,移植的疗效与移植前肿瘤负荷相关,移植前高肿瘤负荷状态与移植后较高的复发率相关[3-6]。然而难治复发性ALL由于疾病本身的限制,部分患者即使采用挽救性化疗也难以达到CR,此外多次化疗也使得患者器官毒性累积,增加移植相关死亡的风险,部分患者甚至难以耐受预处理,失去移植机会[5-6]。临床上经常会面临这样的问题:针对这部分ALL患者应该是立即行挽救性移植,还是经过挽救性化疗达到缓解后再行移植?至今为止,难治复发ALL患者二种不同移植前状态对移植预后的影响尚不明确,为此,本研究回顾性分析我中心52例未缓解(non-remission,NR) 状态和≥CR2状态下行allo-HSCT的难治复发性ALL患者的临床资料,以探讨难治复发ALL患者移植前缓解状态对移植预后的影响,现报告如下。
1 资料与方法 1.1 病例资料收集我研究所2012年1月至2015年6月非CR1状态下行allo-HSCT的ALL患者52例,其中男性35例,女性17例,中位年龄22.5(5~51)岁。所有病例均根据细胞形态学、免疫学、细胞遗传学和分子生物学分型诊断,其中B细胞ALL 46例,T细胞ALL 6例,Ph+ALL 16例,Ph-ALL 36例;合并髓外浸润者5例;经2疗程及以上化疗未完全缓解者2例,初次缓解后6个月内出现复发者36例,6个月到1年内复发者6例,1年以上复发者7例,allo-HSCT后复发者1例;单次复发者40例,多次复发者9例。≥CR2状态下移植者33例,NR状态下移植者19例,移植时骨髓中原始和幼稚细胞中位水平为14.5%(6%~83%)。
1.2 预处理方案及移植方式所有患者均采取清髓性预处理方案。其中采用改良马利兰+环磷酰胺(Bu/Cy)者38例,全身放疗+环磷酰胺(TBI+Cy)者14例。供者类型为HLA全相合的同胞供者7例,HLA半相合的血缘供者35例(来源于父亲15例,母亲10例,同胞6例,子代4例),HLA相合的非血缘供者10例(10/10全相合7例,9/10相合3例)。干细胞来源于骨髓9例,外周血18例,骨髓联合外周血25例。
1.3 移植物抗宿主病预防HLA相合同胞供者移植采用环孢素(CsA)联合短程甲氨蝶呤(MTX)预防移植物抗宿主病(graft versus host disease,GVHD),非亲缘供者移植及单倍体移植在此基础上加用霉酚酸酯(MMF)和抗胸腺细胞球蛋白(ATG)。具体剂量为:CsA 2~3 mg/(kg·d),预处理期间开始静脉输注,待患者肠道功能恢复后改为口服,并监测血药浓度,如无GVHD,移植后3个月逐渐减停。MTX 15 mg/m2,回输后第1天,MTX 10 mg/m2,回输后第3、6、11天,静脉注射。MMF 1.0 g/d,预处理期间开始口服,移植后28 d减停。 ATG 2.5 mg/(kg·d) ×4 d(预处理第-5~-2天)。
1.4 其他并发症的预防为预防巨细胞病毒(cytomegalovirus,CMV)感染,自预处理起,接受更昔洛韦10 mg/(kg·d)×8 d,随后给予阿昔洛韦,至30 d后过渡为口服;为预防肝静脉闭塞病(veno-occlusive disease,VOD),从预处理开始至移植后30 d,肝素100 U/(kg·d)持续静脉滴注,脂质体前列腺素El 0.03 μg/(kg·h),熊去氧胆酸600~900 mg/d口服。
1.5 观察指标观察移植后造血重建时间、GVHD发生率及严重程度,其它移植相关并发症,监测移植后1、2、3、6个月和1、2年的骨髓形态、微小残留病灶(minimal residual disease,MRD)和供体嵌合率(STR)情况,对复发和生存情况等进行评价。移植相关死亡(transplantation related mortality,TRM)定义为移植后100 d内因移植相关并发症死亡。造血重建的标准:连续3 d中性粒细胞(ANC)≥0.5×109/L,脱离血小板输注后连续3 d血小板(PLT)计数≥20×109/L。
1.6 统计学方法采用SPSS 17.0统计软件进行分析。以χ2检验及Mann Whitney检验分别比较分类数据和数值数据的基线值,以Kaplan-Meier法计算总生存率(overall survival,OS)及无白血病生存率(leukemia-free survival,LFS)。P<0.05定义为差异有统计学意义。
2 结果 2.1 患者特征表 1显示了52例在非CR1状态下行allo-HSCT的难治复发的ALL患者临床特征及移植情况。NR组与≥CR2组患者在年龄、性别、疾病类型、染色体预后分层、预处理方案、移植类型、HLA相合与否方面差异均无统计学意义。
2.2 植入情况除1例NR移植患者早期死亡,其余51例均获得造血重建。NR和≥CR2患者的ANC和PLT重建的中位时间分别为12 (11~22) d和12(11~21) d (P=0.976),14(10~40) d 和16 (10~46) d (P=0.476),达到完全供者嵌合(≥95%)中位时间分别为21 (13~35) d和25 (14~41) d(P=0.477),两组差异无统计学意义。
2.3 GVHD的发生NR和≥CR2患者aGVHD的发生率为52.6%和57.6%(P=0.730),其中Ⅰ~Ⅱ度为42.1%和33.3%(P=0.527),Ⅲ~Ⅳ度为10.5%和24.3%(P=0.399),1例CR2患者因Ⅳ度aGVHD死亡,其余均经治疗得到控制。可评估的14例NR和27例≥CR2患者中,cGVHD的发生率为41.6%和57.9%(P=0.660),主要为局限型cGVHD。
2.4 其它移植相关并发症100 d内移植相关死亡率11.5%(6例),分别为肺部感染3例,Ⅳ度aGVHD、VOD、出血各1例,其中≥CR2与NR患者TRM分别为12.1%(4例)和10.5%(2例),差异无统计学意义(P=1.000)。其他移植相关并发症以1~2度消化道黏膜炎、2~3度感染以及出血性膀胱炎多见,两组患者并发症的发生率无明显差异,且均经治疗后痊愈。
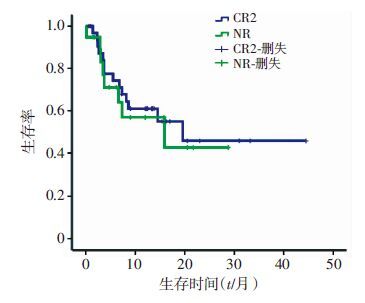
2.5 生存情况除去3例失访和1例早期死亡患者,中位随访时间12(1.8~44.5)个月,26例患者均无白血病生存。预计2年OS为45.3%,预计2年LFS为45.9%。NR与≥CR2患者的预计2年OS和LFS分别为42.6%、45.7%(P=0.740)和46.3%、46.2%(P=0.998)(图 1、2)。达到完全嵌合的51例患者中有13例出现复发,其中仅血液学复发者10例,仅髓外复发者2例,血液学合并髓外复发者1例,1例血液学复发患者经干扰素联合供者淋巴细胞输注治疗存活至今,余患者均死亡。复发的中位时间为4(1.6~15.7)个月,累积复发率为39.1%。NR组患者累积复发率高于CR组(47% vs 34.3%,P=0.425),但差异无统计学意义。
| 组别 | n(男/女) | 中位数年龄(范围) | 疾病类型 | 费城染色体 | 染色体预后分层 | 预处理方案 | HLA | 移植方式 | 干细胞来源 | ||||||||||
| B-ALL | T-ALL | Ph+ | Ph- | 低危 | 中危 | 高危 | BUCY | TBI+CY | 相合 | 不相合 | 无关 | 同胞 | 单倍体 | 骨髓 | 外周血 | 骨髓+外周血 | |||
| NR组 | 19(11/8) | 32(9~51) | 18 | 1 | 6 | 13 | 1 | 14 | 4 | 15 | 4 | 3 | 16 | 2 | 1 | 16 | 4 | 2 | 13 |
| ≥CR2组 | 33(24/9) | 23(5~44) | 28 | 5 | 10 | 23 | 1 | 21 | 11 | 23 | 10 | 11 | 22 | 8 | 6 | 19 | 5 | 16 | 12 |
| P | 0.272 | 0.157 | 0.533 | 0.924 | 0.609 | 0.469 | 0.209 | 0.159 | 0.013 | ||||||||||
|
| 图 1 难治复发ALL患者allo-HSCT前≥CR2与NR状态对2年OS的影响 |

|
| 图 2 难治复发ALL患者allo-HSCT前≥CR2与NR状态对2年LFS的影响 |
2.6 危险因素分析
单因素分析可能影响这52例难治复发ALL患者移植预后的因素,结果显示,移植后发生cGVHD的患者2年OS和LFS显著延长(P=0.011和P=0.025),亲缘供者移植较无关供者移植预后良好(OS:P=0.033;LFS:P=0.031),骨髓移植较外周血细胞移植预后良好(OS:P=0.025;LFS:P=0.029),而患者年龄、性别、疾病类型、初治时染色体危险分层、移植前缓解状态、预处理方案、HLA是否相合、是否发生重度aGVHD均不是OS、LFS的影响因素。对其中49例移植前曾出现复发的患者进行单因素分析,结果显示,初次缓解后6个月内出现复发的患者2年OS明显缩短(P=0.017),复发后2个月内进行移植的患者2年OS显著延长(P=0.051)。对其中19例NR状态下移植患者预后影响因素单因素分析显示,移植前骨髓中原幼细胞数<20%患者与原幼细胞数≥20%患者的OS和LFS相比,差异无统计学意义(P=0.060和P=0.061)。多因素分析结果显示,只有移植后发生cGVHD是影响OS和LFS的独立预后因素,即移植后发生cGVHD患者较移植后未发生cGVHD患者的OS和LFS明显延长,而移植前疾病缓解状态、供体来源、移植物来源等均与预后无关。
3 讨论以往多数学者认为[4-8],白血病患者行allo-HSCT应在获得缓解后进行,然而难治复发性ALL往往存在白血病细胞原发或者继发耐药,部分患者即使采用挽救性化疗后仍不能获得缓解,而且多次化疗将导致器官累积毒性增加,机会性感染的发生率增高,甚至使部分患者失去移植机会。因此,难治复发ALL患者可否在NR状态下实施挽救性移植是一个值得探讨的问题。
本研究就19例NR和33例CR2以上状态下行allo-HSCT的难治复发性ALL进行回顾性分析,发现NR患者2年LFS达到46.3%,与CR患者接近(P=0.998),提示对于无法通过诱导化疗获得CR的难治复发性ALL患者,在NR状态下进行移植是可行的。本研究中难治复发ALL患者的2年OS和LFS均比早期病例明显提高[9-10],考虑可能与早期减停免疫抑制剂,干扰素抢先治疗诱发移植物抗白血病效应(GVL)有关。本研究对移植后30~60 d无GVHD表现的高危患者,以每周10%~20%的比例逐渐撤减免疫抑制剂,若半年内无GVHD表现,予干扰素300万U皮下注射,部分患者联合预防性或治疗性供体淋巴细胞输注以诱导GVL效应。结果显示NR与≥CR2患者的cGVHD的发生率均高于50%,同时单因素和多因素分析的结果均表明发生cGVHD的患者OS和LFS相对延长,说明GVHD尤其是cGVHD的存在是维持GVL效应和维持患者持续缓解的重要因素,这和大多数研究证实GVL和GVHD密切相关以及发生cGVHD的患者非复发死亡率明显降低的结果是一致的[11]。
对于难治复发白血病患者,复发是目前影响移植预后的主要因素,达34%~58%[10]。本研究中患者复发死亡占总体死亡的54.5%(12/22),2年累积复发率为39.1%。NR状态下移植患者累积复发率高于CR组(47% vs 34.3%,P=0.425),但差异无统计学意义。同样提示对难治复发ALL患者在NR状态下行HSCT是可行的,降低复发率是提高移植预后的关键。另外,难治复发的白血病患者往往在移植前接受过多次或大剂量化疗,器官毒性累积,一般情况较差,移植相关死亡率高[6]。本研究中NR组和≥CR2组患者TRM分别为10.5%和12.1%,明显低于国际血液和骨髓研究组(CIBMTR)报道的39%[10]。移植相关死亡的主要原因为感染和严重的GVHD,说明仍需积极加强支持治疗、防治感染、促进免疫重建,并进一步寻求最大程度增强GVL效应同时减少GVHD的方法。
有研究表明,复发至移植间隔的时间与疗效相关[12],诱导缓解后过多的巩固治疗不仅增加移植相关死亡的发生,还会使患者面临随时复发的风险,错过移植的最佳时机。我们对本研究中移植前出现复发患者进行分析,发现诱导达缓解后短期(6个月以内)复发患者OS明显缩短(P=0.043),复发后2个月内进行移植患者OS可显著延长(P=0.051),对其中19例NR状态下移植患者预后影响因素分析显示,移植前骨髓中原幼细胞数<20%患者的OS和LFS高于移植前骨髓原幼细胞数≥20%的患者(83.3% vs 19.3%,P=0.060和83.3% vs 20.6%,P=0.061),若进一步扩增病例数可能会达到统计学差异。同时单因素分析发现,亲缘供者较无关供者预后较好,外周血来源干细胞较骨髓来源干细胞预后差,但多因素分析却发现供者类型及移植物来源不是独立的预后因素,考虑其可能原因为回输外周血来源干细胞的多为非亲缘移植,而非亲缘供者没有亲缘供者供给及时,患者普遍较晚接受移植,这更印证了早期移植对复发患者的优势。
综上所述,allo-HSCT挽救性治疗难治复发ALL,移植前NR患者与诱导达到缓解(≥CR2)患者相比,复发率、移植相关死亡率及OS和LFS差异均无统计学意义,复发至移植的时间、移植前肿瘤负荷及移植后能否维持GVL效应才是影响患者生存的主要因素。因此,对难治复发性ALL患者可以在NR状态下实施挽救性allo-HSCT,移植前不必过分追求完全缓解,而是应积极寻找合适供体尽早移植,并通过积极撤停免疫抑制剂和过继免疫治疗诱导产生cGVHD,以期获得长期生存。
| [1] | Tavernier E, Boiron J M, Huguet F, et al. Outcome of treatment after first relapse in adults with acute lymphoblastic leukemia initially treated by the LALA-94 trial[J]. Leukemia,2007, 21 (9) : 1907 –1914. DOI:10.1038/sj.leu.2404824 |
| [2] | 于亚平. 成人急性淋巴细胞白血病治疗进展[J]. 现代肿瘤医学,2009, 17 (12) : 2444 –2448. DOI:10.3969/j.issn.1672-4992.2009.12.076 |
| [3] | Blum W, Bolwell B J, Phillips G, et al. High disease burden is associated with poor outcomes for patients with acute myeloid leukemia not in remission who undergo unrelated donor cell transplantation[J]. Biol Blood Marrow Transplant,2006, 12 (1) : 61 –67. DOI:10.1016/j.bbmt.2005.06.004 |
| [4] | Ciceri F, Labopin M, Aversa F, et al. A survey of fully haploidentical hematopoietic stem cell transplantation in adults with high-risk acute leukemia: a risk factor analysis of outcomes for patients in remission at transplantation[J]. Blood,2008, 112 (9) : 3574 –3581. DOI:10.1182/blood-2008-02-140095 |
| [5] | 黄晓军. 难治/复发白血病的造血干细胞移植[J]. 中华医学杂志,2006, 86 (32) : 2240 –2242. DOI:10.3760/j:issn:0376-2491.2006.32.003 |
| [6] | Horan J T, Logan B R, Agovi-Johnson M A, et al. Reducing the risk for transplantation-related mortality after allogeneic hematopoietic cell transplantation: how much progress has been made?[J]. J Clin Oncol,2011, 29 (7) : 805 –813. DOI:10.1200/jco.2010.32.5001 |
| [7] | 李桥川, 章忠明, 刘练金, 等. 异基因外周血造血干细胞移植治疗急性淋巴细胞白血病95例疗效分析[J]. 中华器官移植杂志,2015, 36 (2) : 82 –86. DOI:10.3760/cma.j.issn.0254-1785.2015.02.005 |
| [8] | Burke M J, Verneris M R, Le-Rademacher J, et al. Transplant Outcomes for Children with T Cell Acute Lymphoblastic Leukemia in Second Remission: A Report from the Center for International Blood and Marrow Transplant Research[J]. Biol Blood Marrow Transplant,2015, 21 (12) : 2154 –2159. DOI:10.1016/j.bbmt.2015.08.023 |
| [9] | Biggs J C, Horowitz M M, Gale R P, et al. Bone marrow transplants may cure patients with acute leukemia never achieving remission with chemotherapy[J]. Blood,1992, 80 (4) : 1090 –1093. |
| [10] | Duval M, Klein J P, He W, et al. Hematopoietic stem-cell transplantation for acute leukemia in relapse or primary induction failure[J]. J Clin Oncol,2010, 28 (23) : 3730 –3738. DOI:10.1200/JCO.2010.28.8852 |
| [11] | Arai S, Arora M, Wang T, et al. Increasing incidence of chronic graft-versus-host disease in allogeneic transplantation: a report from the Center for International Blood and Marrow Transplant Research[J]. Biol Blood Marrow Transplant,2015, 21 (2) : 266 –274. DOI:10.1016/j.bbmt.2014.10.021 |
| [12] | 唐举贤, 朱康儿, 张涛, 等. 异基因造血干细胞移植治疗未缓解白血病的临床研究[J]. 中华血液学杂志,2013, 34 (3) : 267 –268. DOI:10.3760/cma.j.issn.0253-2727.2013.03.021 |



