2. 300350 天津,华博特生物科技有限公司
2. HUABOTE Biotechnological Inc., Tianjin, 300350, China
结直肠癌是一类严重危害生命健康的常见恶性肿瘤,其发病率逐年递增[1]。癌胚抗原(carcinoembryonic antigen,CEA)等肿瘤血清标志物检测的普及,为结直肠癌的诊断提供了帮助。然而临床实践证实,单独检测血清CEA无法满足结直肠癌早期诊断的要求[2]。因此,寻找新的肿瘤标志物一直是肿瘤研究领域的热点。脱嘌呤脱嘧啶核酸内切酶1(apurinic/apyrimidinic endonuclease 1,APE1),又被称为氧化还原因子1(redox factor 1,Ref-1),广泛存在于机体各组织器官。它作为碱基切除修复(base excision repair,BER)途径中的关键限速酶,一方面参与多种生理及病理条件下的DNA损伤修复;另一方面也参与包括P53、NF-κB、AP-1等多种关键转录因子的氧化还原调控[3-4]。基于本课题组前期的研究,我们首先提出并证实肿瘤患者外周血中存在APE1蛋白和APE1自身抗体(APE1 autoantibodies,APE1-AAbs)。2011年,Katsumata等[5]报道了在红斑狼疮患者的血清中存在APE1-AAbs。随后,Dai等[6]又发现了在非小细胞肺癌患者血清中APE1-AAbs水平较正常人群升高,并且与组织中APE1表达及化疗药物有效性密切相关。然而目前关于血清APE1-AAbs应用于肿瘤诊断仍鲜有报道,其临床意义还需要进一步验证。因此,本研究通过检测结直肠癌患者血清中APE1-AAbs水平,联合经典血清标志物CEA、糖类抗原19-9(carbohydrate antigen19-9,CA199)以及糖类抗原242(carbohydrate antigen242,CA242)进行分析,探讨其在结直肠癌诊断中的价值。
1 材料与方法 1.1 研究对象收集2010年1月至2012年12月在第三军医大学大坪医院肿瘤中心诊治的结直肠癌患者血清150人 份。患者情况:男性91例,女性59例,中位年龄64.5岁 (24~90岁),均经组织病理学证实并未经任何治疗。排除严重感染、创伤、自身免疫疾病、其他恶性肿瘤病史等。另收集相关临床资料,包括年龄、性别、吸烟、饮酒、临床TNM分期等。同期收集的健康体检人群血清170人份作为对照组,其中男性110例,女性60例,中位年龄60岁(29~87岁)。
1.2 血清采集及血清APE1-AAbs检测所有受试者清晨空腹静脉采血,室温静置30 min 后,3 000 r/min离心10 min,分离血清,-80 ℃冰箱保存,实验前剔除溶血标本。实验采用APE1-AAbs半定量试剂盒(由本实验室与天津华博特生物科技有限公司共同研发)检测,其中所需APE1蛋白按照Wilson实验室方法纯化[7]。实验前1 d将待测血清标本置于4 ℃冰箱缓融。检测前将标本与试剂平衡至室温(20~28 ℃)。具体检测方法:①用样本稀释液将待测样本按照1 ∶5 000稀释;②将100 μL标准品和稀释后的样品分别加到对应的微孔底部,振荡混匀,盖板后于37 ℃恒温箱中孵育60 min;③弃去孔内液体,每孔加入250 μL清洗液洗板,共4次,最后1次将微孔板控干水分;④每孔加入酶结合物(标记辣根过氧化物酶的抗人IgG抗体)100 μL,振荡混匀,盖板后于37 ℃孵育30 min;⑤再次洗板,同步骤3;⑥每孔加入TMB底物100 μL显色后避光孵育15 min;⑦每孔加入50 μL 2 mol/L 硫酸进行终止,在波长450 nm(参比波长620 nm)条件下测定各孔光密度值[D(450)]。使用Origin 9.0软件计算血清APE1-AAbs水平。
1.3 血清CEA、CA199、CA242浓度的检测采用C-12肿瘤诊断用蛋白芯片试剂盒(浙江湖州数康生物科技有限公司)进行检测。CEA的正常参考范围 <5 ng/mL,CA199的正常参考范围 <35 U/mL,CA242的正常参考范围 <20 U/mL。高于正常参考值判定为阳性或升高。联合检测时,其中只要有1项为阳性,该样本即被判定为阳性。
1.4 统计学分析采用SPSS 22.0统计软件进行统计学处理。临床基线资料的比较采用χ2检验,血清APE1-AAbs水平的比较采用非参数检验。绘制受试者工作特征曲线 (receiver operative characteristic curve,ROC)并计算曲 线下面积(area under curve,AUC)和约登系数(Youden’s index,灵敏度+特异性-1)判定血清APE1-AAbs作为检验指标在结直肠癌早期诊断中的合理性及其截断值(cut-off值),Youden’s index最大时对应的血清APE1-AAbs水平即为其cut-off值,本研究中将血清APE1-AAbs水平高于此cut-off 值定义为阳性。运用Logistic回归和ROC曲线分析血清APE1-AAbs和CEA、CA199及CA242的联合检测价值。P <0.05为差异有统计学意义。
2 结果 2.1 血清APE1-AAbs在结直肠癌患者和健康对照人群中的差异150例结直肠癌患者与170例健康对照人群,其年龄、性别、吸烟、饮酒、肿瘤家族史差异无统计学意义(P>0.05,表 1)。病例组的中位血清APE1-AAbs水平为2.697(1.175~9.608),对照组为1.920(0.800~5.586),病例组的血清APE1-AAbs水平显著高于对照组(P <0.001)。
| 因素 | 病例组 | 对照组 | P值 |
| 年龄(岁) | |||
| <60 | 53(35.33) | 76(44.71) | 0.088 |
| ≥60 | 97(64.67) | 94(55.29) | |
| 性别 | |||
| 男 | 91(60.67) | 110(64.71) | 0.456 |
| 女 | 59(39.33) | 60(35.29) | |
| 吸烟史 | |||
| 有 | 45(30.00) | 41(24.12) | 0.236 |
| 无 | 105(70.00) | 129(75.88) | |
| 饮酒史 | |||
| 有 | 29(19.33) | 26(15.29) | 0.339 |
| 无 | 121(80.67) | 144(84.71) | |
| 肿瘤家族史 | |||
| 有 | 23(15.33) | 21(12.35) | 0.440 |
| 无 | 127(84.67) | 149(87.65) |
2.2 根据ROC曲线评价血清APE1-AAbs在结直肠癌中的诊断价值
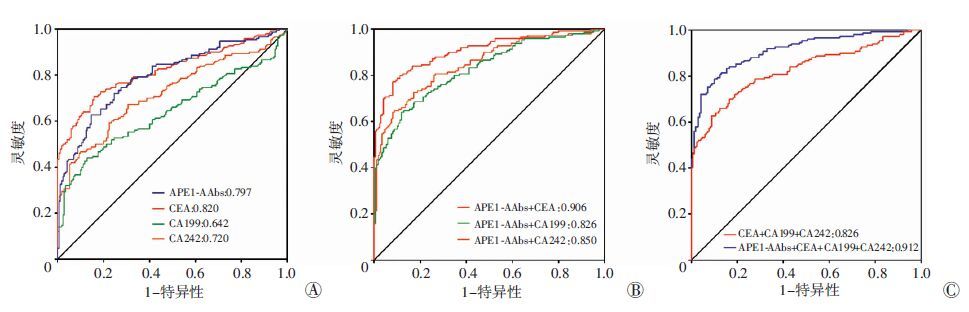
分别绘制血清APE1-AAbs、CEA、CA199及CA242的ROC曲线,CEA的AUC最大,为0.820(95%CI=0.772~0.868),其次是APE1-AAbs,AUC为0.797 (95%CI=0.747~0.846),其cut-off值为2.457。在 此水平下,APE1-AAbs诊断结直肠癌的灵敏度为62.67%,特异性为85.29%(图 1A)。利用Logistic回归模型,分别联合血清APE1-AAbs和CEA、CA199及CA242,利用预测概率绘制ROC曲线,联合后的AUC较单一指标升高,其中APE1-AAbs与CEA联合后,AUC最大,为0.906(95%CI=0.872~0.939),见图 1B。APE1-AAbs与CEA、CA199及CA242四者联合分析,其AUC较后三者联合升高,达到0.912(95%CI=0.880~0.944),诊断效能明显提高(图 1C)。
|
| A:APE1-AAbs、CEA、CA199、CA242的ROC曲线;B:APE1-AAbs与CEA、 CA199、CA242分别联合的ROC曲线;C:CEA+CA199+CA242与APE1-AAbs+CEA+ CA199+CA242的ROC曲线 图 1 结直肠癌患者血清APE1-AAbs与CEA、CA199及CA242的ROC曲线 |
2.3 血清APE1-AAbs水平与其临床因素的关系
病例组中血清APE1-AAbs水平与肿瘤TNM分期关系密切,表现为Ⅲ+Ⅳ期患者的血清APE1-AAbs水平显著高于Ⅰ+Ⅱ期患者(P=0.001);但是,Ⅲ+Ⅳ期与Ⅰ+Ⅱ期患者中血清APE1-AAbs水平阳性患者所占比例差异并无统计学意义。与性别、年龄、吸烟、饮酒等因素无相关性(表 2)。
| 临床因素 | n | APE1-AAbs水平(中位数) | P值 | 阳性例数(%) | P值 |
| 年龄(岁) | |||||
| <60 | 53 | 2.851 | 0.712 | 34(64.15) | 0.781 |
| ≥60 | 97 | 2.664 | 60(61.86) | ||
| 性别 | |||||
| 男 | 91 | 2.553 | 0.151 | 54(59.34) | 0.296 |
| 女 | 59 | 2.778 | 40(67.80) | ||
| 吸烟史 | |||||
| 有 | 45 | 2.851 | 0.769 | 28(62.22) | 0.941 |
| 无 | 105 | 2.664 | 66(62.86) | ||
| 饮酒史 | |||||
| 有 | 29 | 2.479 | 0.562 | 16(55.17) | 0.353 |
| 无 | 121 | 2.730 | 78(64.46) | ||
| TNM分期 | |||||
| Ⅰ+Ⅱ | 68 | 2.513 | 0.001 | 39(57.35) | 0.220 |
| Ⅲ+Ⅳ | 82 | 3.207 | 55(67.07) |
2.4 APE1-AAbs、CEA、CA199及CA242对结直肠癌诊断效能的比较
APE1-AAbs在结直肠癌诊断中灵敏度最高,其次是CEA和CA242,而CA199最低。在诊断特异性方面,CA242、CEA、CA199、APE1-AAbs依次降低,而APE1-AAbs和CEA达到相同的诊断准确度。APE1- AAbs分别联合CEA、CA199和CA242,虽然联合诊断特异性有所降低,但灵敏度和准确度均有所提高(表 3)。
| 检测指标 | 灵敏度 | 特异性 | 准确度 |
| APE1-AAbs | 62.67 | 85.29 | 74.69 |
| CEA | 47.33 | 98.82 | 74.69 |
| CA199 | 18.67 | 97.65 | 60.63 |
| CA242 | 24.00 | 99.41 | 64.06 |
| APE1-AAbs+CEA | 82.00 | 84.12 | 83.13 |
| APE1-AAbs+CA199 | 68.67 | 82.94 | 76.25 |
| APE1-AAbs+CA242 | 72.67 | 84.71 | 79.06 |
2.5 多因素Logistic回归分析病例组血清APE1-AAbs水平
利用多因素Logistic回归分析,纳入年龄、性别、吸烟史、饮酒史、家族史,结果表明,APE1-AAbs和CEA是结直肠癌发病的危险因素,APE1-AAbs的OR值为4.291,OR值的95%CI为2.671~6.895,P <0.001。这提示APE1-AAbs升高人群患结直肠癌的风险是未升高人群的4.291倍。
3 讨论DNA损伤修复相关蛋白或其抗体在肿瘤诊断及预后评估等方面具有巨大潜力[8-9]。APE1作为DNA损伤修复相关蛋白的一种,已经被证实在非小细胞肺癌、肝癌、结直肠癌、卵巢癌、骨肉瘤等多种肿瘤组织中的表达模式与相应正常组织明显不同,主要体现在表达强度增高和胞质异位表达,且这些改变与肿瘤的发生、放化疗抵抗以及不良预后等密切相关[3, 10-13]。因此认为APE1是多种恶性肿瘤稳定的组织标志物。理论上,APE1表达模式的改变可能刺激机体产生APE1-AAbs,因此血清APE1-AAbs水平的改变可能间接反映肿瘤的发展及演变。本课题组前期研究已经证实了肿瘤患者外周血中APE1蛋白的存在,及其可作为抗原刺激机体产生自身抗体。Dai等[6]证实了非小细胞肺癌患者血清APE1-AAbs水平较正常人群显著升高,且与组织和外周血中的APE1表达有相关性,推测其原因可能是癌变组织内APE1呈现过量和胞质异位表达,随着肿瘤细胞快速增殖,凋亡或坏死的肿瘤细胞裂解后释放胞内蛋白,从而激活了免疫系统产生了APE1-AAbs。本研究检测了150例结直肠癌患者和170例健康对照人群血清中APE1-AAbs水平,发现结直肠癌患者血清中的APE1-AAbs水平显著高于正常对照人群(P <0.001),与Dai等[6]在非小细胞肺癌中的发现一致。Ⅲ+Ⅳ期结直肠患者的APE1-AAbs水平显著高于Ⅰ+Ⅱ期患者,这可能与晚期患者肿瘤负荷较大,癌变组织中的APE1蛋白较高,从而引起机体产生更强的免疫应答有关。APE1-AAbs水平越高可能能够提示分期越晚,预后也有可能越差。
目前临床上用于结直肠癌诊断的肿瘤标志物其灵敏度和准确度尚达不到早期诊断的要求[14]。因此,合理选择肿瘤标志物联合检测,对于提高肿瘤诊断的灵敏度和准确性尤为重要。本研究利用ROC曲线对血清APE1-AAbs诊断结直肠癌的灵敏度和特异度进行了分析,通过计算Youden’s index,得到血清APE1-AAbs诊断结直肠癌的最佳筛查阳性界值,结果显示血清APE1-AAbs诊断结直肠癌有较高的灵敏度,可达到62.67%,提示血清APE1-AAbs可以作为结直肠癌早期筛查指标。进而运用Logistic回归模型和ROC曲线联合分析血清APE1-AAbs和CEA、CA199及CA242,发现联合后的AUC、灵敏度均较单一指标升高,说明APE1-AAbs和现有的肿瘤标志物联合检测可以提高结直肠癌的诊断效能。
我们进一步采用CEA、CA199、CA242的临床正常参考范围,分别计算三者单独以及与APE1-AAbs联合后的灵敏度、特异性以及准确度,结果发现三者中灵敏度从高到低依次为CEA、CA242、CA199,特异性从高到低依次为CA242、CEA、CA199,此结果与仲召阳等[15]的报道基本相同。而三者分别与APE1-AAbs联合后分析,灵敏度和准确度均显著升高,表明检测血清APE1-AAbs对结直肠癌有一定的辅助诊断价值,联合检测可以显著提高结直肠癌的检出率。但是,联合后特异性有所降低,提示还需要更大样本量的验证,进一步确定APE1-AAbs的最佳参考值范围,从而更好地发挥其临床价值。
| [1] | 陈万青, 郑荣寿, 张思维, 等. 2012年中国恶性肿瘤发病和死亡分析[J]. 中国肿瘤,2016, 25 (1) : 1 –8. DOI:10.11735/j.issn.1004-0242.2016.01.A001 |
| [2] | De-Maio G, Rengucci C, Zoli W, et al. Circulating and stool nucleic acid analysis for colorectal cancer diagnosis[J]. World J Gastroenterol,2014, 20 (4) : 957 –967. DOI:10.3748/wjg.v20.i4.957 |
| [3] | Li M, Wilson D M 3rd. Human apurinic/apyrimidinic endonuclease 1[J]. Antioxid Redox Signal,2014, 20 (4) : 678 –707. DOI:10.1089/ars.2013.5492 |
| [4] | Kelley M R, Georgiadis M M, Fishel M L. APE1/Ref-1 role in redox signaling: translational applications of targeting the redox function of the DNA repair/redox protein APE1/Ref-1[J]. Cur Mol Pharmacol,2012, 5 (1) : 36 –53. |
| [5] | Katsumata Y, Kawaguchi Y, Baba S, et al. Identification of three new autoantibodies associated with systemic lupus erythematosus using two proteomic approaches[J]. Mol Cell Proteomics,2011, 10 (6) : M110.005330 . DOI:10.1074/mcp.M110.005330 |
| [6] | Dai N, Cao X J, Li M X, et al. Serum APE1 autoantibodies: a novel potential tumor marker and predictor of chemotherapeutic efficacy in non-small cell lung cancer[J]. PLoS One,2013, 8 (3) : e58001 . DOI:10.1371/journal.pone.0058001 |
| [7] | Erzberger J P, Barsky D, Scharer O D, et al. Elements in abasic site recognition by the major human and Escherichia coli apurinic/apyrimidinic endonucleases[J]. Nucleic Acids Res,1998, 26 (11) : 2771 –2778. |
| [8] | Ochiai H, Ohishi T, Osumi K, et al. Reevaluation of serum p53 antibody as a tumor marker in colorectal cancer patients[J]. Surg Today,2012, 42 (2) : 164 –168. DOI:10.1007/s00595-011-0044-1 |
| [9] | Li Z, Qing Y, Guan W, et al. Predictive value of APE1, BRCA1, ERCC1 and TUBB3 expression in patients with advanced non-small cell lung cancer (NSCLC) receiving first-line platinum-paclitaxel chemotherapy[J]. Cancer Chemother Pharmacol,2014, 74 (4) : 777 –786. DOI:10.1007/s00280-014-2562-1 |
| [10] | Al-Attar A, Gossage L, Fareed K R, et al. Human apurinic/apyrimidinic endonuclease (APE1) is a prognostic factor in ovarian, gastro-oesophageal and pancreatico-biliary cancers[J]. Br J Cancer,2010, 102 (4) : 704 –709. DOI:10.1038/sj.bjc.6605541 |
| [11] | Wang D, Xiang D B, Yang X Q, et al. APE1 overexpression is associated with cisplatin resistance in non-small cell lung cancer and targeted inhibition of APE1 enhances the activity of cisplatin in A549 cells[J]. Lung Cancer,2009, 66 (3) : 298 –304. DOI:10.1016/j.lungcan.2009.02.019 |
| [12] | 何乐, 刘勇, 张诗珩, 等. APE1免疫组化表达与恶性肿瘤相关性的Meta分析[J]. 重庆医学,2015, 44 (26) : 3664 –3668. DOI:10.3969/j.issn.1671-8348.2015.26.021 |
| [13] | Tell G, Fantini D, Quadrifoglio F. Understanding different functions of mammalian AP endonuclease (APE1) as a promising tool for cancer treatment[J]. Cell Mol Life Sci,2010, 67 (21) : 3589 –3608. DOI:10.1007/s00018-010-0486-4 |
| [14] | Fung K Y, Nice E, Priebe I, et al. Colorectal cancer biomarkers: to be or not to be? Cautionary tales from a road well travelled[J]. World J Gastroenterol,2014, 20 (4) : 888 –898. DOI:10.3748/wjg.v20.i4.888 |
| [15] | 仲召阳, 王东, 李增鹏, 等. 多肿瘤标志物蛋白质芯片检测系统对结直肠癌诊断的临床意义[J]. 重庆医学,2007, 36 (23) : 2406 –2408. DOI:10.3969/j.issn.1671-8348.2007.23.026 |



