中枢神经系统是急性白血病髓外浸润最常见的部位,虽然在患者初诊时中枢神经系统白血病(central nervous system leukemia,CNSL)发生率较低(5%)[1],但由于血脑屏障的存在,白血病患者往往需要在常规化疗过程中进行预防性鞘注,来减低CNSL发生或复发风险。CNSL可以发生于急性白血病患者治疗过程的任何时期,以缓解期为主;任何类型白血病均可发生,以急性淋巴细胞白血病居高。现指南推荐对于全部急性淋巴细胞白血病患者在诱导缓解及巩固强化期均需要进行预防性鞘注,急性髓系白血病特别是初诊白细胞超过100×109/L、伴髓外病变、M4/M5、伴t(8;21)或inv(16)等亦需要进行预防性鞘内注射[2-3]。对于在化疗过程中出现CNSL患者的缓解后最佳治疗方案,现仍无定论。造血干细胞移植是减少急性白血病复发风险的最有效治疗手段,非血缘脐血因获取简便,免疫原性低,移植可耐受HLA1-2/6位点不合,术后移植物抗宿主病(graft-versus-host disease,GVHD)发生率低等优点而得到广泛应用。然而非血缘脐血移植对既往伴CNSL急性白血病患者的疗效,目前国内对此类研究报道甚少。现对15例行单份非血缘脐血移植(single-unit umbilical cord blood transplantation,sUCBT)治疗伴CNSL的急性白血病患者疗效进行了回顾性分析,并报告如下。
1 资料与方法 1.1 病例资料收集我科2009年7月至2014年9月行sUCBT的既往伴CNSL的急性白血病患者15例临床资料,男性10例,女性5例。中位年龄15(6~37)岁,中位体质量45(23~100)kg。其中急性单核细胞白血病2例,急性未分化型白血病1例,急性淋巴细胞白血病12例。所有患者移植前经鞘注治疗中枢神经系统白血病达完全缓解状态,3例移植时骨髓未完全缓解。CNSL诊断标准:所有患者均进行腰椎穿刺,取脑脊液行常规、生化、细胞学检查,诊断符合文献[4]标准。
1.2 单份非血缘脐血移植 1.2.1 脐血配型及输注脐血与受者HLA低分辨4/6个位点相合4例,5/6个位点相合8例,6/6个位点相合3例;供受者ABO血型全相合7例,主要不合4例,次要不合3例,主次均不合1例。回输总有核细胞数(TNC)中位数为3.62(1.98~6.76)×107/kg(受者体质量),其中CD34+细胞中位数为2.46(0.79~3.38)×105/kg。
1.2.2 预处理方案全部采用强化清髓预处理方案,其中全身照射(total body irradiation,TBI)+阿糖胞苷(Ara-C)+环磷酰胺(CY)方案[5]9例[TBI 3 Gy 每天2次,第-7~-6天;Ara-C 2.0 g/m2 每12 h 1次,第-5~-4天;CY 60 mg/kg 每天1次,第-3~-2天]; 氟达拉滨(Flu)+白消安(Bu)+CY方案3例[Flu 30 mg/m2,每天1次,第-8~-5天;Bu 0.8 mg/kg,每6 h 1次,第-7~-4天;CY 60 mg/kg 每天1次,第-3~-2天],Ara-C+Bu+CY方案3例[Ara-C 2.0 g/m2 每12 h 1次,第-9~-8天;Bu 0.8 mg/kg,每6 h 1次,第-7~-4天;CY 60 mg/kg 每天1次,第-3~-2天,重组人粒细胞集落刺激因子(G-CSF)5 μg/(kg·d),Ara-C前开始应用至Ara-C结束]。所有患者预处理用药前1 d加用卡莫司汀(BCNU)250 mg/m2。
1.2.3 GVHD预防全部采用环孢素(cyclosporine A,CsA)联合短程霉酚酸酯(mycophenolate mofetil,MMF)方案[5]。
1.2.4 支持对症治疗从预处理开始至移植后30 d予以小剂量100 U/(kg·d)肝素钠和0.3 μg/(kg·h) 前列腺素E1预防肝静脉闭塞症;积极碱化、水化、强迫利尿,以及于CY应用时及应用后给予美司钠预防出血性膀胱炎;移植第1~35天予以阿昔洛韦(10 mg/kg)预防单纯疱疹病毒感染;口服氟康唑或伏立康唑预防真菌感染;粒细胞恢复后口服复方磺胺甲噁唑预防卡氏肺囊虫。移植第6天开始静脉应用 G-CSF,至白细胞总数恢复正常后停用。移植 中维持患者HGB≥60 g/L,PLT≥ 20×109/L,所有输注的血制品采用X-ray辐照。巨细胞病毒(cytomegalovirus,CMV)的监测和抢先治疗:移植后检测外周血标本CMV-DNA拷贝数,当CMV-DNA≥103拷贝数/mL时,改用更昔洛韦治疗;发生植入前综合征(pre-engraftment syndrome,PES)、Ⅱ度或以上GVHD时加用甲基泼尼松龙(MP)治疗。
1.2.5 移植后CNSL的诊断和治疗患者移植后不常规复查脑脊液,当出现头痛、恶心、呕吐等症状怀疑CNSL时,予以头颅MRI及腰椎穿刺脑脊液检查,对于明确诊断CNSL患者予以每周2次MTX+Ara-C+ DXM三联鞘注,至脑脊液中未见异常细胞后每2~4周 进行巩固治疗,同时合并头颅照射,总剂量为18 Gy。
1.2.6 疗效评定中性粒细胞植入时间为移植后连续3 d外周血中性粒细胞(ANC)绝对值≥0.5×109/L的第1天;血小板植入时间为停止外源血小板输注7 d后PLT≥20×109/L的第1天;GVHD的诊断和分级采用西雅图标准[6];移植后患者原发病复发:外周血重新出现白血病细胞或骨髓原始细胞>5%(除外其他原因如骨髓恢复期等)或髓外出现白血病细胞浸润或分子生物学复发或细胞遗传学复发。移植第7、14、21天采集外周血标本及第30天骨髓标本行短串联重复序列(STR-PCR)检测供受者嵌合体变化。定期监测血常规、生化指标、骨髓细胞学、微小残留病、发病时阳性融合基因情况、STR及免疫功能等。
1.3 统计学方法采用SPSS 19.0进行统计分析。预计生存率采用Kaplan-Meier法;中性粒细胞植入率、血小板植入率、急性GVHD发生率、慢性GVHD发生率及复发率采用含竞争风险的累积发生率统计,应用R软件3.1.3计算[7]。
2 结果 2.1 造血重建14/15例患者获得造血重建,ANC及血小板植入的中位时间分别为19(13~27)d和41(20~85)d。42 d 中性粒细胞累积植入率为93.33%(95%CI: 91.58%~95.09%),120 d血小板累积植入率为73.33% (95%CI:70.28%~76.38%)。
2.2 移植相关并发症80%(12/15)患者出现PES,加用MP治疗后症状控制;1例患者移植第9天出现抽搐、血尿、全身瘀斑伴CSA浓度高,考虑存在血栓性微血管病(TMA),予以立即停用CsA,但随后患者出现多脏器功能衰竭,于移植第15天死亡;5例患者在粒缺期出现血流感染,1例血培养为草绿色链球菌,3例大肠杆菌(ESBL+),1例溶血性葡萄球菌,经抗感染治疗后控制;10例患者移植后出现CMV病毒血症,加用更昔洛韦抗病毒,输注丙种球蛋白后病毒转阴;2例患者出现出血性膀胱炎,经积极碱化水化强制利尿后膀胱炎症状消失;无HVOD及移植后淋巴细胞增殖性疾病(PTLD)的发生。可评估的14例患者中,3例患者出现Ⅱ~Ⅳ度急性GVHD,其中2例经MP及巴利昔单抗治疗后控制,1例患者于治疗过程中同时合并肝脏Ⅳ度GVHD,于移植后141 d死亡,100 d Ⅱ~Ⅳ度急性GVHD累积发 生率为20.00%(95%CI:17.74%~22.26%),Ⅲ~Ⅳ度急性GVHD的累积发生率为13.33%(图 1A);3例患者出现局限型皮肤慢性GVHD,应用小剂量甲氨蝶呤(MTX)和MP后症状控制,720 d慢性GVHD累积发生率为20.00%(95%CI:17.59%~22.41%,图 1B)。

|
| 图 1 CNSL急性白血病患者sUCBT术后重度aGVHD(A)及2年cGVHD发生率(B)比较 |
2.3 移植后疾病状态及生存情况
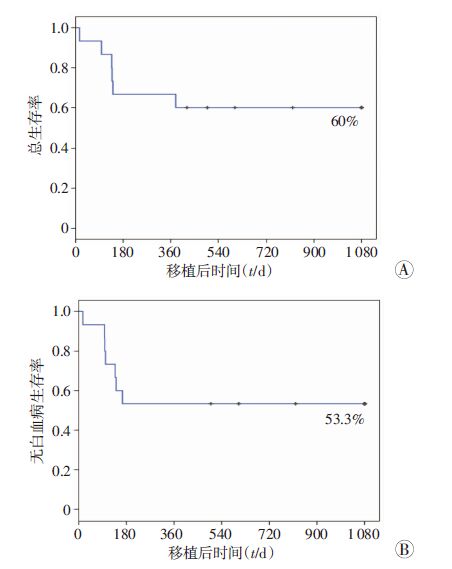
所有患者随访至2015年10月31日,中位随访时间为43.2(14.1~76.5)个月。死亡4例,死亡原因为植入前多脏器功能衰竭(1例),重度急性GVHD(1例)及原发病复发(2例);复发3例,其中2例于移植后3个月余骨髓复发,仅1例患者于移植后5个月余出现CNSL复发,经鞘内注射及头颅放疗,脑脊液恢复正常。2年累积复发率为20.00%(95%CI:17.70%~22.30%),预计3年总OS及LFS分别为60.0%和53.3%。见图 2。
|
| 图 2 CNSL急性白血病患者sUCBT术后3年总生存率(A)及无白血病生存率(B)比较 |
3 讨论
造血干细胞移植是治疗急性白血病的最有效手段,患者移植后可长期维持缓解状态。随着移植技术的不断提高,移植相关死亡率有所下降,但术后复发仍是患者移植后死亡的主要原因,特别对于急性淋巴细胞白血病患者,中枢神经系统是最常见的髓外复发部位[8]。移植前有CNSL病史患者移植术后复发率明显高于无CNSL病史患者。Aldoss等[9]回顾性研究显示,87例行allo-HSCT的伴有CNSL的急淋CR期患者,其2年累积复发率为34%,2年无病生存率及总生存率分别为38%和44%,均明显劣于移植同期无CNSL患者。本研究应用强化清髓不含ATG的sUCBT技术体系治疗15例伴CNSL的急性白血病患者,移植后仅1例患者出现中枢神经系统复发,后经鞘内注射及头颅放疗,脑脊液恢复正常,且骨髓持续处于完全缓解状态,与本中心同期移植患者总体复发率相近(20.00% vs 15.25%),总OS无统计学差异(60.0% vs 64.8%),可见该sUCBT技术体系可消除既往CNSL病史对患者远期生存的影响,具有较好的疗效。
传统清髓方案TBI/CY(TBI,10~12 Gy;CY,120 mg/kg)和BU/CY是脐血移植的经典方案[10],我中心采用强化清髓预处理方案,在传统方案基础上加用大剂量Ara-C或Flu,彻底破坏患者自身免疫系统,获得良好干细胞植入同时最大限度清除受者体内的肿瘤细胞。Ara-C通过形成活性代谢物(阿糖胞苷三磷酸盐)被肿瘤细胞摄取,且大剂量较普通剂量能更长时间与肿瘤细胞接触[11],甚至在脑脊液中长时间维持治疗浓度,从而彻底清除脑脊液存留的白血病细胞。Arai等[12]通过队列研究比较脐血移植行大剂量Ara-C/TBI/CY和TBI/CY预处理方案治疗髓系白血病患者的临床疗效,发现增加大剂量Ara-C组患者其复发率(包括髓外复发)明显低于TBI/CY组,同时未增加移植相关死亡。另外,我中心在预处理中加用G-CSF可提高白血病细胞对阿糖胞苷的敏感性[13]。同时,所有患者预处理方案中均加入BCNU,该药已证实能有效通过血脑屏障,在脑脊液中达到较高浓度,从而有效降低移植术后中枢神经系统的复发。
除外预处理方案中使用放疗或易于透过血脑屏障药物外,我中心15例患者中80%患者接受HLA低分辨(1~2)/6位点不相合脐血移植,且预防GVHD方案均未使用ATG,故移植后强大的移植物抗白血病(GVL)作用可能是控制术后CNSL复发的另一重要因素。现已有多篇文献证实移植后中枢神经系统中供者来源的T淋巴细胞具有强大的GVL作用,Maude等[14]通过对接受CART治疗患者脑脊液的监测,可以观察到效应T细胞能迁移至脑脊液中,持续发挥抗白血病效应。因脐血中T淋巴细胞免疫原性低,虽本技术体系预防GVHD的方案未使用ATG,移植后重度GVHD的发生率并未增加(13.33%),低于国外相关报道,如Barker等[15]对1 061例单份脐血移植患者回顾性分析,其Ⅲ~Ⅳ度aGVHD累积发生率为26%;Chantepie等[16]回顾性分析63例接受骨髓移植的伴CNSL急淋患者,其重度GVHD发生率为20.7%。同时本组患者中无重症感染发生,虽巨细胞病毒血症发生率不低,但应用更昔洛韦抢先治疗后均能使病毒转阴,无巨细胞病毒病的发生,无1例患者出现PTLD。 另外,本组15例患者移植后PES的发生率高(12/15),PES是HSCT术后,特别是脐血移植(cord blood transplantation,CBT)术后,患者在中性粒细胞植入前出现的免疫反应,该反应目前病因学不明。日本虎之门医院提出供者的T细胞很有可能参与PES的免疫反应,他们采用流式细胞仪对接受非血缘CBT患者外周血进行供受者嵌合状态的检测发现,CBT后1周嵌合体中供者CD3+T细胞>90%的患者PES的发生率明显高于≤90%的患者(84% vs 47%,P=0.017),同时发现naïve T细胞向记忆T细胞的转化加速,CBT后2周发生PES患者的供者CD4+和CD8+的naïve T细胞和记忆T细胞的表达明显高于未发生PES的患者,认为早期即转为供者为主的嵌合体,并从naïve T细胞到记忆T细胞的增殖可能来解释PES的发生机制[17];目前多篇文献证实PES与GVHD发生有相关性,Park等[18]研究显示,发生PES患者其aGVHD发生率明显高于无PES患者,但不增加移植相关死亡率,而既往研究表明移植术后GVHD具有显著的GVL效应,能够明显改善患者无病生存率及减低术后复发[19],因此推测PES亦具有GVL效应。
本中心采用sUCBT治疗伴CNSL的急性白血病患者,初步结果显示疗效较好,可改善移植前伴有中枢神经系统累及患者的远期预后,考虑可能与强化清髓预处理方案、不含ATG的预防GVHD方案技术体系有关,且CBT后特有的PES进一步发挥GVL效应。但本研究为回顾性分析,病例数较少,故需大样本、多中心前瞻性研究进一步验证结果。
| [1] | Lazarus H M, Richards S M, Chopra R, et al. Central nervous system involvement in adult acute lymphoblastic leukemia at diagnosis: results from the international ALL trial MRC UKALL XII/ECOG E2993[J]. Blood,2006, 108 (2) : 465 –472. DOI:10.1182/blood-2005-11-4666 |
| [2] | Alvarnas J C, Brown P A, Aoun P, et al. Acute lymphoblastic leukemia, version 2[J]. J Natl Compr Canc Netw,2015, 13 (10) : 1240 –1279. |
| [3] | O’Donnell M R, Abboud C N, Altman J, et al. Acute myeloid leukemia[J]. J Natl Compr Canc Netw,2012, 10 (8) : 984 –1021. |
| [4] | O’Donnell M R, Appelbaum F R, Baer M R, et al. Acute myeloid leukemia clinical practice guidelines in oncology[J]. J Natl Compr Canc Netw,2006, 4 (1) : 16 –36. |
| [5] | 刘会兰, 孙自敏, 耿良权, 等. 非血缘脐血移植治疗成人恶性血液病患者的临床研究[J]. 中华血液学杂志,2010, 31 (8) : 519 –522. DOI:10.3760/cma.j.issn.0253-2727.2010.08.005 |
| [6] | Przepiorka D, Weisdorf D, Martin P, et al. 1994 Consensus Conference on Acute GVHD Grading[J]. Bone Marrow Transplant,1995, 15 (6) : 825 –828. |
| [7] | Scrucca L, Santucci A, Aversa F. Competing risk analysis using R: an easy guide for clinicians[J]. Bone Marrow Transplant,2007, 40 (4) : 381 –387. DOI:10.1038/sj.bmt.1705727 |
| [8] | Poon L M, Hamdi A, Saliba R, et al. Outcomes of adults with acute lymphoblastic leukemia relapsing after allogeneic hematopoietic stem cell transplantation[J]. Biol Blood Marrow Transplant,2013, 19 (7) : 1059 –1064. DOI:10.1016/j.bbmt.2013.04.014 |
| [9] | Aldoss I, Al-Malki M M, Stiller T, et al. Implications and Management of Central Nervous System Involvement before Allogeneic Hematopoietic Cell Transplantation in Acute Lymphoblastic Leukemia[J]. Biol Blood Marrow Transplant,2016, 22 (3) : 575 –578. DOI:10.1016/j.bbmt.2015.10.016 |
| [10] | Ballen K K, Gluckman E, Broxmeyer H E. Umbilical cord blood transplantation: the first 25 years and beyond[J]. Blood,2013, 122 (4) : 491 –498. DOI:10.1182/blood-2013-02-453175 |
| [11] | Reese N D, Schiller G J. High-dose cytarabine (HD araC) in the treatment of leukemias: a review[J]. Curr Hematol Malig Rep,2013, 8 (2) : 141 –148. DOI:10.1007/s11899-013-0156-3 |
| [12] | Arai Y, Takeda J, Aoki K, et al. Efficiency of high-dose cytarabine added to CY/TBI in cord blood transplantation for myeloid malignancy[J]. Blood,2015, 126 (3) : 415 –422. DOI:10.1182/blood-2015-04-642652 |
| [13] | Lowenberg B, van-Putten W, Theobald M, et al. Effect of priming with granulocyte colony-stimulating factor on the outcome of chemotherapy for acute myeloid leukemia[J]. N Engl J Med,2003, 349 (8) : 743 –752. DOI:10.1056/NEJMoa025406 |
| [14] | Maude S L, Frey N, Shaw P A, et al. Chimeric antigen receptor T cells for sustained remissions in leukemia[J]. N Engl J Med,2014, 371 (16) : 1507 –1517. DOI:10.1056/NEJMoa1407222 |
| [15] | Barker J N, Scaradavou A, Stevens C E. Combined effect of total nucleated cell dose and HLA match on transplantation outcome in 1061 cord blood recipients with hematologic malignancies[J]. Blood,2010, 115 (9) : 1843 –1849. DOI:10.1182/blood-2009-07-231068 |
| [16] | Chantepie S P, Mohty M, Tabrizi R, et al. Treatment of adult ALL with central nervous system involvement at diagnosis using autologous and allogeneic transplantation: a study from the Société Française de Greffe de Moelle et de Thérapie Cellulaire[J]. Bone Marrow Transplant,2012, 48 (5) : 684 –690. DOI:10.1038/bmt.2012.213 |
| [17] | Matsuno N, Yamamoto H, Watanabe N, et al. Rapid T-cell chimerism switch and memory T-cell expansion are associated with pre-engraftment immune reaction early after cord blood transplantation[J]. Br J Haematol,2013, 160 (2) : 255 –258. DOI:10.1111/bjh.12097 |
| [18] | Park M, Lee S H, Lee Y H, et al. Pre-engraftment syndrome after unrelated cord blood transplantation: a predictor of engraftment and acute graft-versus-host disease[J]. Biol Blood Marrow Transplant,2013, 19 (4) : 640 –646. DOI:10.1016/j.bbmt.2013.01.014 |
| [19] | Narimatsu H, Miyakoshi S, Yamaguchi T, et al. Chronic graft-versus-host disease following umbilical cord blood transplantation: retrospective survey involving 1072 patients in Japan[J]. Blood,2008, 112 (6) : 2579 –2582. DOI:10.1182/blood-2007-11-118893 |



