脂肪甘油三酯脂肪酶(adipose trigtyceride lipase,ATGL)是甘油三酯(triglyceride,TG)水解过程中发挥起始作用的关键酶。自2004年被报道以来,其越来越多的功能不断被发现:它参与脂肪动员、能量代谢、慢性炎症、肥胖及2型糖尿病等多种生理病理过程[1, 2, 3]。2006年Haemmerle等[4]在小鼠中发现Atgl基因缺失会导致脂肪向心脏、肝脏、肾脏及睾丸等多种器官聚集。之后关于ATGL与心脏、肝脏之间联系不断有新的发现[5, 6, 7, 8, 9],而ATGL在肾脏中的作用却仍不清楚。作为重要的代谢器官,肾脏与多种代谢性疾病如肥胖、1型糖尿病、2型糖尿病均密切相关。因此,研究Atgl与肾脏之间的关系显得尤为重要。我们利用Atgl基因敲除小鼠,通过检测其尿白蛋白肌酐比(urinary albumin /creatinine ratio,ACR)、HE染色观察肾脏结构改变、油红O染色观察脂肪在肾脏中的分布、透射电镜观察肾脏超微病理改变初步探讨了Atgl基因缺失对肾脏结构和功能的影响,从而为研究Atgl与肾脏之间的关系提供了新的思路。
1 材料与方法 1.1 实验动物Atgl基因敲除小鼠(Atgl-/-鼠)及野生型小鼠(Atgl+/+鼠)均由Atgl+/-鼠经过近亲交配繁殖产生。(Atgl+/-鼠购买自美国杰克逊实验室,货号019003,遗传背景为C57BL/6)为保证实验结果的一致性,所有实验小鼠为雄性,8~10周龄,体质量约20 g。所有小鼠在SPF条件下饲养并给予正常饮食。
1.2 方法 1.2.1 尿白蛋白、肌酐检测收集各组小鼠随机尿,ELISA法检测尿白蛋白及尿肌酐浓度(试剂盒购自碧云天生物技术公司)。
1.2.2 组织学观察小鼠常规麻醉后,用PBS经心脏灌流充分,迅速分离肾脏,左侧肾脏置于4%多聚甲醛中固定48 h,常规脱水、透明、浸蜡、包埋制作石蜡切片。HE染色观察肾脏结构改变。每个组织随机选取6个视野观察。
1.2.3 油红O染色分离肾脏后,右侧肾脏沿冠状面分成两部分,一部分用于制作冰冻切片油红O染色。另一部分用于电镜标本制作。油红O染色步骤:①油红O稀释液配置:油红饱和液6 mL加蒸馏水4 mL 混匀后过滤使用。②制作的冰冻切片充分洗涤,油红O稀释液避光染色10 min。③60%乙醇镜下分化,水洗。④苏木精复染核,水洗后70%甘油封片。2h内显微镜下观察拍照。
1.2.4 透射电镜标本制作及观察将标本用手术刀切成1 mm×1 mm×1 mm大小固定于2.5%戊二醛中4 ℃过夜,1%锇酸室温固定 2 h,丙酮脱水,树脂包埋,LKB-I 型切片机制作超薄切片(60 nm),枸橼酸铅染色,透射电镜下观察。
1.2.5 肾脏组织TG检测肾脏组织经匀浆后离心取上清,送西南医院检验科检测TG含量。
1.3 统计学分析计量资料以x±s表示,采用SPSS 13.0统计软件,两组间比较采用Kruskal-Wallis检验或t检验。
2 结果 2.1 Atgl基因敲除导致小鼠尿ACR显著增加与对照组相比,Atgl-/-鼠尿ACR升高了约10倍(P<0.05),而尿肌酐浓度在两组间差异无统计学意义(P>0.05,表 1)。肌酐的改变反映终末期肾病,而ACR是反映肾功能的早期指标。这些结果提示Atgl基因敲除小鼠肾脏功能可能处于早期受损阶段。
| 组别 | n | 尿白蛋白浓度(μg/L) | 尿肌酐浓度(μmol/L) | 尿白蛋白肌酐比 (g/mol) |
| Atgl+/+ 组 | 8 | 9 650.00±2 389.86 | 32.60±9.16 | 329.76±175.61 |
| Atgl-/-组 | 8 | 129 362.50±21 097.19a | 36.65±13.73 | 4 219.04±2 331.76a |
| a: P<0.05,与Atgl+/+组比较 | ||||
图 1显示两种小鼠肾脏大体比较。Atgl+/+小鼠约0.9 cm×0.5 cm大小,色泽鲜红;而Atgl-/-小鼠较Atgl+/+小鼠明显缩小,约0.8 cm×0.45 cm大小,且颜色泛白,提示可能存在较多脂肪。HE染色提示,与对照组相比,实验组肾小管出现明显肿胀,肿胀的肾小管对肾小囊的挤压使得肾小囊体积明显缩小,肾皮质弥漫性存在大量空泡状结构;油红O染色进一步显示这些空泡状结构为脂滴,大量脂滴累及Atgl-/-小鼠肾小球及肾小管,其中以肾小管受累最严重(图 2)。肾脏TG定量提示Atgl-/-小鼠每毫克肾脏组织中TG含量较Atgl+/+小鼠高出10倍以上(39.89±5.14)μg vs (2.18±0.58) μg。
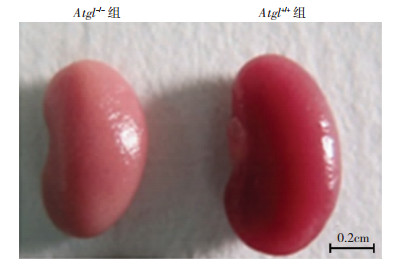 |
| 图 1 两组小鼠肾脏大体观 |
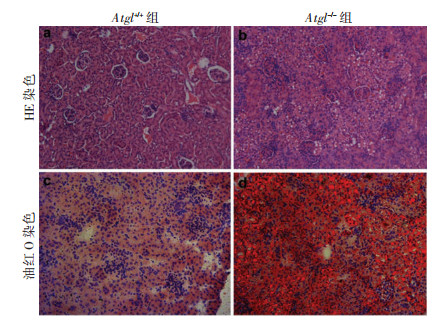 |
| 图 2 光镜下观察两组小鼠肾脏组织病理变化 (×200) |
肾脏透射电镜检测结果显示,在对照组中,肾小球滤过屏障结构完整,足细胞足突形态正常(图 3A),各细胞中均未见脂滴存在,肾小管细胞内线粒体丰富,形态结构正常(图 3C),微绒毛形态正常;在实验组中,足细胞足突出现大量融合(图 3B),肾小球滤过屏障结构受损。大量脂滴堆积于足细胞及肾小管细胞中(图 3B、D),肾小管细胞线粒体棘突可见不同程度消失(图 3D),微绒毛不同程度脱落、萎缩,提示肾小管细胞功能失调,重吸收障碍。
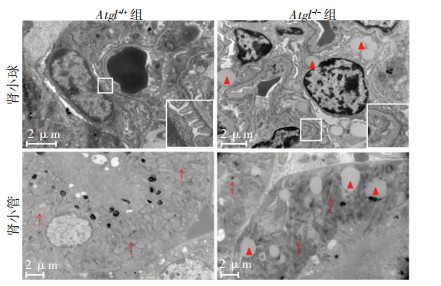 |
| ▲:示脂滴;↑:示线粒体;小框为足细胞足突;大框为小框的放大观察 图 3 透射电镜观察两组小鼠肾小球、肾小管超微结构变化 |
脂肪代谢紊乱导致过多的脂肪酸及甘油三酯聚集于非脂肪细胞包括心肌细胞、骨骼肌细胞、肝细胞等可对靶器官和细胞造成严重损伤,这种过程被称作脂毒性作用[10],但其中的分子机制还并不太清楚。文献[11, 12]报道,线粒体损伤诱导的活性氧(ROS)增加在这个过程中扮演重要作用。线粒体作为细胞的能量中心,也承担着清除多余ROS的功能[13]。线粒体功能失调可导致细胞及组织ROS活性增加,ROS可通过激活下游信号分子诱导细胞失能或死亡[14, 15]。
ATGL作为脂肪分解反应第一步的关键酶,在脂肪分解代谢中发挥至关重要作用。研究发现,Atgl基因敲除可产生明显的异位脂质沉积,大量脂质沉积在心脏、肝脏、肾脏、睾丸等组织中[4]。尽管如此,却并没有关于Atgl基因敲除导致肾脏结构功能损伤的报道。本研究发现Atgl基因敲除小鼠中,脂滴大量堆积在肾小球足细胞及肾小管细胞中,通过对足细胞足突的融合及微绒毛的损伤对肾脏滤过屏障功能及重吸收功能产生重要影响。但其中的机制却并不清楚。作为脂毒性作用的重要靶点,线粒体,在电镜下Atgl基因敲除小鼠足细胞及肾小管细胞中均有不同程度的损伤,主要表现在线粒体肿胀和内嵴不同程度的消失,提示线粒体损伤。当然,在Atgl基因敲除小鼠中,脂毒性通过线粒体介导的足细胞及肾小管细胞死亡方式及分子机制,还需更进一步研究。
脂毒性与代谢相关肾病密切相关,但其中的机制仍然不清楚,其中很大一个原因就是缺少相关的动物模型。而Atgl-/-鼠显然具有一些优势:首先,成熟的Atgl-/-鼠具有稳定的蛋白尿和肾小球滤过屏障受损,可以很好模拟糖尿病肾病的早期病理改变;其次,大量的TG聚集在肾脏,提示Atgl-/-鼠具有明显的脂毒性。当然,这其中也存在某些问题:如,Atgl-/-鼠寿命有限,为12~16周,不足以坚持到出现晚期肾病就因心功能衰竭而死亡;其次,在电镜下很难找到典型的凋亡或自噬的证据,无法为细胞死亡方式提供依据。这些问题需要后续不断深入研究。
总之,本研究发现在Atgl基因敲除小鼠中,脂滴大量堆积在足细胞及肾小管细胞对肾脏滤过屏障及重吸收产生重大损伤,为研究脂毒性与肾脏相关疾病奠定了基础。
| [1] | Zimmermann R, StraussJG, Haemmerle G, et al. Fat mobilization in adipose tissue is promoted by adipose triglyceride lipase[J]. Science, 2004, 306(5700): 1383-1386. DOI: 10.1126/science. 1100747 |
| [2] | Schreiber R, Hofer P, Taschler U, et al. Hypophagia and metabolic adaptations in mice with defective ATGL-mediated lipolysis cause resistance to HFD-induced obesity[J]. Proc Natl Acad SciUS A, 2015, 112(45): 13850-13855. DOI: 10.1073/pnas.1516004112 |
| [3] | WangPP, SheMH, HePP, et al. Piromelatine decreases triglyceride accumulation in insulin resistant 3T3-L1 adipocytes: role of ATGL and HSL[J]. Biochimie, 2013, 95(8): 1650-1654. DOI: 10.1016/j.biochi.2013.05.005. |
| [4] | Haemmerle G, Lass A, Zimmermann R, et al. Defective lipolysis and altered energy metabolism in mice lacking adipose triglyceride lipase[J]. Science, 2006, 312(5774): 734-737. DOI: 10.1126/ science.1123965 |
| [5] | Jha P, Claudel T, Baghdasaryan A, et al. Role of adipose triglyceride lipase (PNPLA2) in protection from hepatic inflammation in mouse models of steatohepatitis and endotoxemia[J]. Hepatology, 2014, 59(3): 858-869. DOI: 10.1002/hep.26732 |
| [6] | Gao H, FengXJ, LiZM, et al. Downregulation of adipose triglyceride lipase promotes cardiomyocyte hypertrophy by triggering the accumulation of ceramides[J]. Arch Biochem Biophys, 2015, 565: 76-88.DOI:10.1016/j.abb.2014.11.009 |
| [7] | DiopSB, Bisharat-Kernizan J, BirseRT, et al. PGC-1/Spargel counteracts high-fat-diet-induced obesity and cardiac lipotoxicity downstream of TOR and brummer ATGL lipase[J]. Cell Rep, 2015, 10(9): 1572-1584. DOI: 10.1016/j.celrep. 2015.02.022 |
| [8] | OngKT, MashekMT, DavidsonNO, et al. Hepatic ATGL mediates PPAR-alpha signaling and fatty acid channeling through an L-FABP independent mechanism[J].JLipid Res, 2014, 55(5): 808-815.DOI: 10.1194/jlr.M039867 |
| [9] | Taschler U, Schreiber R, Chitraju C, et al. Adipose triglyceride lipase is involved in the mobilization of triglyceride and retinoid stores of hepatic stellate cells[J]. Biochim Biophys Acta, 2015, 1851(7): 937-945.DOI: 10.1016/j.bbalip.2015.02.017 |
| [10] | WeinbergJM. Lipotoxicity[J]. Kidney Int, 2006, 70(9): 1560-1566.DOI: 10.1038/sj.ki.5001834 |
| [11] | Dong X, Bi L, He S, et al. FFAs-ROS-ERK/P38 pathway playsakey role in adipocyte lipotoxicity on osteoblasts in co-culture[J]. Biochimie, 2014, 101: 123-131. DOI: 10.1016/ j.biochi.2014. 01.002 |
| [12] | Gehrmann W, Wurdemann W, Plotz T, et al. Antagonism Between Saturated and Unsaturated Fatty Acids in ROS Mediated Lipotoxicity in Rat Insulin-Producing Cells[J]. Cell Physiol Biochem, 2015, 36(3): 852-865. DOI: 10.1159/000430261 |
| [13] | ZorovDB, Juhaszova M, SollottSJ. Mitochondrial reactive oxygen species (ROS) and ROS-induced ROS release[J]. Physiol Rev, 2014, 94(3): 909-950.DOI: 10.1152/physrev.00026.2013 |
| [14] | BrownDI, GriendlingKK. Regulation of signal transduction by reactive oxygen species in the cardiovascular system[J]. Circ Res, 2015, 116(3): 531-549. DOI: 10.1161/CIRCRESAHA.116.303584 |
| [15] | Zhang Y, Han L, Qi W, et al. Eicosapentaenoic acid (EPA) induced apoptosis in HepG2 cells through ROS-Ca(2+)-JNK mitochondrial pathways[J]. Biochem Biophys Res Commun, 2015, 456(4): 926-932.DOI: 10.1016/j.bbrc.2014.12.036 |



