肝细胞性肝癌(hepatocellular carcinoma,HCC)是全球发病率及病死率较高的恶性肿瘤之一。我国是肝癌的高发地区,肝癌在我国恶性肿瘤致死率中亦处于较高位置。HCC最常见的转移途径:以门静脉癌栓的形式发生肝内转移,手术切除是目前公认最主要的治疗方法,切除方式可分为:解剖性肝切除与非解剖性肝切除。理论上解剖性肝切除能更多地切除肝内微转移病灶,进而减少肿瘤复发[1]。然而开腹情况下关于两者优劣尚无定论[1, 2, 3, 4, 5, 6]。解剖性肝段切除通常要求在肝断面显露肝静脉、肝蒂等重要的管道结构,对手术技巧提出了更高要求,开腹手术时常采用肝段染色[7]、3D虚拟导航系统[8]等技术辅助实现解剖性肝段切除。而腹腔镜下不易行预切除肝段染色,对肝切除界线则由术者结合术中超声及肝表面解剖标志来判断。关于腹腔镜解剖性肝切除术时有报道,但多限于左外叶以及左、右半肝等大范围的解剖性肝切除[9, 10, 11],解剖性肝段切除治疗HCC则鲜有报道。本研究回顾性分析2011年1月至2014年4月第三军医大学西南医院肝胆外科采用腹腔镜解剖性肝段切除治疗的29例HCC患者临床资料,旨在探讨以肝段为本的腹腔镜解剖性肝切除治疗HCC的疗效。
1 资料与方法 1.1 一般资料本组HCC患者29例,其中男性22例,女性7例;年龄28~69岁,平均49.51岁。 乙肝标志物检查提示: HBsAg阳性者25例,AFP (401.16±1139.56 )μg/L。 肝脏储备功能评估参考ICG R15值及剩余肝脏体积测算。根据上腹部增强CT结合肝脏Couinaud分段法各肿瘤中心均位于预切除肝段内。术前CT检查结果显示:肿瘤直径﹥5 cm者2例,≦5 cm者27例。肝功能按照Child.Pugh分级:A级26例,B级3例(表 1)。
| 临床特征 | 数值 |
| 年龄(岁) | 49.52(28~69) |
| 性别 男/女 | 22/7 |
| HBsAg(+)[例(%)] | 25(86.21) |
| 肝硬化[例(%)] | 23(79.31) |
| Child-Pugh 分级 | |
| A | 26 |
| B | 3 |
| ICGR 15(%) | 14.43±2.44 |
| AFP( μg/L) | 401.16±1139.56 |
| PLT(109个/L) | 147.34±51.89 |
| AST (U/L) | 45.76±36.79 |
| ALT(U/L) | 40.31±32.52 |
| Abl( μg/L) | 41.43±5.62 |
| TBIL(μmol/L) | 17±7.37 |
| PT(s) | 11.7±0.86 |
| 肿瘤中心位置 | |
| Ⅰ/Ⅱ/Ⅲ/Ⅳa/Ⅳb/V/Ⅵ/Ⅶ/Ⅷ(例) | 3/2/3/3/1/6/7/2/2 |
| 肿瘤直径 >5 cm者/≤5 cm者(例) | 2/27 |
| HBsAg(+) :肝炎表面抗原,乙型,阳性 | |
纳入标准:(1)全身情况良好,能耐受肝切除术。(2)术前临床诊断为肝细胞性肝癌。(3) 肿瘤局限于单个肝段且无邻近器官组织侵犯及远处转移。(4)肝功能Child-Pugh分级为A级或B级,无严重肝硬化、门静脉高压症及活动性肝炎者。(5)ICG R15<15%,肝硬化患者:剩余肝脏体积/标准肝脏体积>40%、无肝硬化患者:剩余肝脏体/标准肝脏体积>30%。(6)术中探查肿瘤无破裂,无血性腹腔积液。(7)术前未行RFA、TACE等治疗。(8)既往上腹部手术史不作为绝对禁忌证。
排除标准:(1) 肿瘤累及肝段数目>1。(2)肿瘤侵犯肝门或合并门静脉、肝静脉、下腔静脉及胆管癌栓。(3)术中探查上腹部严重粘连,腹腔镜手术器械无法置人或无法建立CO2气腹者。(4)术中发现肝肿瘤破裂出血或已累及肝周组织。(5)术后病理检查为胆管细胞性、混合细胞性肝癌或其他性质的肿瘤。
1.3 手术方法采用气管插管,吸入、静脉复合全身麻醉。仰卧、头高脚底位,病变位于右肝者以滚筒垫高右侧腰背部,术中根据需要将手术床向左或右倾斜10°~15°。建立CO2气腹,控制腹内压12~14 mmHg(1 mmHg=0.133 kPa)。Trocar分布原则是围绕病变肝段呈扇形分布,30°腹腔镜孔位于扇形边缘的中点,一般采用4孔法或5孔法。经Winslow孔预置自行设计的腔镜下第一肝门入肝血流阻断装置(专利号:ZL 200920127107.7)。根据术中探查情况结合术前影像资料、ICG R15值及剩余肝脏体积测算结果综合评估解剖性肝切除安全性、可行性,满足解剖性肝切除条件方可实施手术。
术中超声检查确定病变部位、肝内重要管道结构的走向及其与病变肝段的毗邻关系并可协助布置戳卡孔位置。行肝Ⅵ、Ⅶ、Ⅷ段切除者需要充分游离右半肝,将右半肝向左前上翻转,此处需使用右肝后叶暴露装置(专利号ZL200920127106.2),行Ⅶ、Ⅷ段切除者需沿肝右后叶与下腔静脉之间间隙由下向上解剖出肝短静脉,用连发钛夹夹闭后离断,游离至肝右静脉根部,解剖出肝右静脉,用血管吊带悬吊。使用术中超声(GE Co,Inc,USA)定位肿瘤位置,在肝外解剖出预切除肝段的Glisson蒂行区域性入肝血流阻断,在此操作过程中常需借助肝蒂剥离装置(金手指),若区域性入肝血流阻断不能有效控制肝实质离断过程中出血需加行第一肝门入肝血流阻断。用超声刀离断肝实质,所遇管道用生物夹或者钛夹夹闭后离断,肝蒂或者肝静脉用腹腔镜下直线切割闭合器离断,肝断面用双击电凝止血,必要时以Prolene线缝合止血。如术中出现腹腔镜下难以控制的大出血,即时中转开腹。切除肿瘤后装入标本袋,经腹上区操作孔扩大切口或耻骨联合上横切口取出,用游标卡尺测量肿瘤直径、肿瘤切缘长度。反复冲洗、仔细检查肝断面,确认无出血及胆汁漏,彻底清洗腹腔,放置腹腔引流管后结束手术。
1.4 随访术后采用电话或门诊随访,所有患者术后行腹部彩色多普勒超声、肝功能、AFP检查。有乙型病毒性肝炎史患者加行乙型病毒性肝炎血清标志物和HBV定量检测。疑有肿瘤复发患者,行增强CT、超声造影检查或特异性磁共振明确诊断。复查时间为术后第1年每3个月1次,第2年每4个月1次,以后每6个月1次,随访截止日期为2015年4月1日。
1.5 统计学分析使用软件SPSS 20.0 (SPSS,Inc,Chicago,US)进行统计学分析。计数资料用χ2检验或Fisher确切概率法。计量资料用x±s表示,采用t检验或者Wilcoxon秩和检验,采用Kaplan-Meier法绘制生存曲线,生存率比较采用Log-rank检验。
2 结果 2.1 围手术期结果29例患者中3例中转开腹 (1例因肝中静脉损伤、2例因肝实质深部出血腔镜下止血困难),26例成功施行腹腔镜解剖性肝段切除术(表 2)。1例Ⅶ段切除患者术后出现反应性胸腔积液;1例Ⅳ段切除患者术后出现肝断面积液,1例Ⅴ段切除患者术后出现轻度胆漏,以上患者经积极对症治疗后均好转出院,围手术期无死亡病例。 将本研究病例按切除部位分为左前下段组(AL组: 19例)与后上段组(PS组:10例)(表 3),将本研究病例按切除部位分为前外段组(AL组:19例)与后上段组(PS组:10例)(表 1),对比提示两组手术时间[(207.05±48.79)vs (245.10±77.31) min,P=0.035]、术中失血量[(382.63±384.10) vs (457.33± 388.18) mL,P=0.015]、肝门阻断率(5.26% vs 33.33%,P=0.041)、肝门阻断时间[(27.03± 23.08) vs (32.63±24.52)min,P=0.028]、术后住院时间[(8.11±2.45) vs (9.90±3.57)d,P=0.038] 差异有统计学意义,而围手术期输血率(0% vs 3.4%,P=0.215)、中转开腹率(5.3% vs 20.0%,P=0.267)、术后开始进食时间[(1.74±0.65) vs (1.60±0.84)d,P=0.206]、切缘[(2.21±0.65) vs (2.09±0.77)cm,P=0.561]、并发症发生率(10.5% vs 10.0%,P=1.000)。
| 临床特征 | 数值 |
| 手术时间(min) | 220.17±61.56 |
| 术中失血量(mL) | 311.72±127.70 |
| 围手术期输血率(%) | 3.44 |
| 中转开腹率(%) | 10.34 |
| 肝门阻断时间(min) | 28.24±21.08 |
| 肝门阻断例数[ 例(%)] | 5(17.24) |
| 切缘(cm) | 2.11±0.87 |
| 肿瘤直径(cm) | 3.66±1.14 |
| 术后开始进食时间 (d) | 1.69±0.71 |
| 术后住院时间 (d) | 8.11±2.45 |
| 并发症发生率(%) | 10.34 |
| 术后病理(高分化/中分化/低分化)(n) | 6/20/3 |
组别 | 手术时间 (min) | 术中失血 量(mL) | 围手术期 输血率 (%) | 中转开 腹率 (%) | 肝门阻 断时间 (min) | 肝门阻 断例数 [例(%)] | 切缘 (cm) | 肿瘤大 小(cm) | 术后开始 进食时间 (d) | 术后住院 时间 (d) | 并发症 发生率 (%) |
| AL组(19) | 207.05±48.79 | 382.63±384.10 | 0 | 5.34 | 27.03±23.08 | 2(5.34) | 2.21±0.65 | 3.49±1.18 | 1.74±0.65 | 8.11±2.45 | 10.53 |
| PS组(10) | 245.10±77.31 | 457.33±388.18 | 10 | 20 | 29.63±24.52 | 3(33.33) | 2.09±0.77 | 3.98±1.07 | 1.60±0.84 | 9.90±3.57 | 10 |
| P值 | 0.035 | 0.015 | 0.215 | 0.267 | 0.028 | 0.041 | 0.561 | 0.554 | 0.206 | 0.038 | 1 |
29例患者均获得随访,随访时间为12~48个月,中位随访时间为26个月。截止随访终点有7例复发,3例在术后1年内复发、4例在1年以后复发,其中3例再次行腹腔镜根治性切除术、2例行开腹根治性切除术、2例因发生肝内转移行射频消融术后半年死亡,以上再手术病例其中3例再次复发后无法行根治性切除,行射频消融术后带瘤生存直至死亡。术后1、3年总体生存率分别为92.8 %、81.7%,术后1、3年无瘤生存率分别为 89.5%、71.7 %(图 1)。AL组与PS组比较,两组1、3年总体生存率(89.5% vs 90.0%;P=0.947)、(79.6 % vs 75.0%;P=0.796),无瘤生存率(87.8% vs 82.6%;P=0.894)、(70.8% vs 73.2%;P=0.908),差异无统计学意义(图 2、3)。
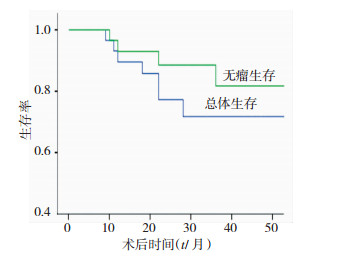 |
| 图 1 HCC患者3年总体与无瘤生存曲线分析 |
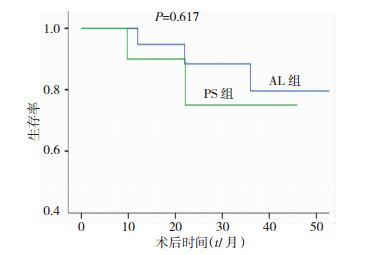 |
| 图 2 不同切除部位组HCC患者总体生存曲线分析 |
 |
| 图 3 不同切除部位组HCC患者无瘤生存曲线分析 |
肝癌在我国属于发病率较高的恶性肿瘤,严重威胁着国人生命健康,手术切除疗效确切。1982年Bismuth等[12]首次报道了以肝段切除治疗肝脏疾病,并称其为“segmentectomy”,文献[13]报道了超声引导下美蓝染色标定肝段的解剖性肝切除技术方法。学术界关于开腹情况下解剖性与非解剖性肝切除术对肝细胞癌疗效尚无定论,然而更多学者把优势倾向于解剖性肝切除术[1, 2, 5, 6]。解剖性肝段切除通常要求肝断面显露肝静脉、肝蒂等重要的管道结构,开腹手术时常采用肝段染[7]、3D虚拟导航系统[8]等技术辅助实现解剖性肝段切除。然而与开腹解剖性肝段切除术不同,腹腔镜下不易甚至无法对预切除肝段进行染色,术中肝实质离断平面则由术者根据术前影像学资料结合术中超声以及肝表面解剖标志加以判断,技术要求更高、难度更大。文献[14]报道中推荐位于Ⅱ~Ⅵ段病灶行腹腔镜肝切除,关于腹腔镜下解剖性肝切除术治疗HCC国内亦有报道[9, 10, 11],但多限于左肝解剖性肝段切除而较少涉及后上段解剖性肝切除。文献[15]报道了肝脏Ⅰ~Ⅷ段系列解剖性肝切除技术,初步证实了腹腔镜解剖性肝切除术运用于所有肝段的可行性,但着重技术层面的讨论未对手术的近远期疗效作评估。本研究所搜集病例涉及所有肝段,其中亦包括肝Ⅰ、Ⅶ、Ⅷ段等难度较大的解剖性肝段切除。
3.1 解剖性肝段切除术疗效将本研究结果与文献报道的基本资料相近的腹腔镜肝切除结果进行对比,同时期Tranchart等[15]报道的术中平均失血量为364 mL,本研究311.72 mL的术中失血量则更低。Alkhalili等[16]进行的大样本腹腔镜 肝癌切除术荟萃分析提示围手术期输血率 0%~19.2%,而本研究中仅有1例患者需术中输血,围手术期输血率3.44%。本研究病例均行腹腔镜解剖性肝段切除术,手术步骤较普通肝切除术更为复杂,因而手术时间比该荟萃分析及Soubrane等[17]报道的手术时间长。与Soubrane等[17]报道相比,本研究10.3%的术后并发症发生率相对较低。综合Alkhalili等[16]分析结果与Soubrane等[17]报道数据,其中术后1、3年总体生存率分别为90.3%、60%~89%,与本研究结果相近。然而较其术后1、3年无瘤生存率85.2%、55.9%,本研究术后早期无瘤生存率则具有明显优势。研究结果表明:对部分选择性HCC病例采用腹腔镜解剖性肝段切除术治疗安全、可行,尚有术中出血量少、围手术期输血率低、术后并发症发生率低等优势,术后1、3年无瘤生存率优于文献报道的腹腔镜非解剖性肝切除病例。
针对以上结果,结合文献[1, 2, 5, 6, 18]我们分析原因如下:(1)出血少、输血率低:Couinaud将肝脏划分为8个功能区域,相邻肝段之间界面缺乏大的血管和胆管,断肝过程中手术器械通过的肝实质可认为是“乏管道区域”,从而减少了对血管、胆管的损伤,进而可减少术中失血及输血,而术中大量失血及围手术期输血是肿瘤复发的危险因素。此为本研究术后1、3年无瘤生存率较文献报道结果更佳的一方面原因;(2)术后并发症发生率低:由于沿肝段间的解剖标记和平面进行断肝操作,降低了对大血管和胆管的损伤概率、更完整地保存了预留肝段血供、肝静脉回流以及胆汁引流,从而减少了术后发生残肝缺血、瘀血、胆漏、坏死和肝断面大量渗出的可能性,进而减少了术后并发症。而本研究病例发生肝断面积液与胆漏各1例均经保守治疗好转,无严重并发症发生;(3)远期效果更佳:肝癌最常见的转移途径是以微门静脉癌栓的形式发生肝内转移,这种播散形式可由主体瘤的卫星灶发展成为同肝区转移灶,进而播散整个半肝或对侧肝,而早期卫星灶和主体瘤多位于同一肝段,以肝段为本的解剖性肝切除能在尽可能减少肝衰的前提下切除更多同一肝段内的微转移灶,从而降低术后复发率,此为本研究无瘤生存率更佳的主要原因。
3.2 左前下段与后上段肝切除对比与左前下段相比,后上段肝切除难度更大,本研究将29例病例按切除部位分为左前下段组(AL组)与后上段组(PS组),对比提示:PS组手术时间、 肝门阻断时间、术后住院时间较AL组长,术中失血量较AL组 大、肝门阻断率更高,差异有统计学意义。而两者在围手术期输血率、中转开腹率、术后开始进食时间、切缘、并发症发生率对比中差异均无统计学意义。而引起的上述差异我们分析原因如下:(1) PS组的肝切除需要充分显露肝脏,该过程涉及对肝短静脉与肝右静脉的处理,较AL组以上操作则在瘤体暴露方面延长了手术时间。(2)与AL组相比,PS组在离断肝实质过程中因更靠近肝静脉主干可能会处理更多由肝静脉损伤引发的出血,且其中多有难处理的出血。 (3)PS组肝切除操作空间更靠近膈肌,如此则增加了术后反应性胸腔积液、肺不张的发生风险,以上结果与文献[19]报道结果一致。两组1、3年总体生存率(89.5% vs 90.0%;P=0.947)、(79.6 % vs 75.0%;P=0.796),无瘤生存率(87.8% vs 82.6%;P=0.894)、(70.8% vs 73.2%;P=0.908),差异均无统计学意义。因而本研究亦初步证实腹腔镜解剖性肝段切除术治疗后上段肝癌同样安全、可行,并与笔者所在中心既往报道结果相近[20]。
综上,与腹腔镜非解剖性肝段切除术相比,在选择性病例中采用腹腔镜解剖性肝段切除术治疗肝细胞癌安全、可行,具有术中出血少、围手术期输血率低、术后并发症发生率低等近期优势,且可获得更佳的远期效果,初步证实腹腔镜解剖性肝段切除术不仅适用于左前下段肝癌的治疗,亦可运用于手术难度和风险较大的后上段肝癌的外科治疗。然而限于病例数偏少,尚需大样本前瞻性随机对照试验为本研究观点提供更高级别循证医学证据。
| [1] | 刘允怡, 余俊豪. 肝段为本的肝切除手术[J]. 中华普通外科杂志, 2003, 18(2): 123-125. |
| [2] | Eguchi S, Kanematsu T, Arii S, et al. Comparison of the outcomes between an anatomical subsegmentectomy and a non-anatomical minor hepatectomy for single hepatocellular carcinomas based on a Japanese nationwide survey[J]. Surgery, 2008,143(4): 469-475. DOI: 10.1016/j.surg.2007.12.003 |
| [3] | Tomimaru Y, Eguchi H, Marubashi S, et al. Equivalent outcomes after anatomical and non-anatomical resection of small hepatocellular carcinoma in patients with preserved liver function[J]. Dig Dis Sci, 2012, 57(7): 1942-1948. DOI: 10.1007/s10620-012-2114-7 |
| [4] | Okamura Y, Ito T, Sugiura T, et al. Anatomic versus nonanatomic hepatectomy for a solitary hepatocellular carcinoma: a case-controlled study with propensity score matching[J]. J Gastrointest Surg, 2014, 18(11): 1994-2002. DOI: 10.1007/s11605-014-2646-6 |
| [5] | Hasegawa K, Kokudo N, Imamura H, et al. Prognostic impact of anatomic resection for hepatocellular carcinoma[J]. Ann Surg, 2005, 242(2): 252-259. |
| [6] | Eltawil K M, Kidd M, Giovinazzo F, et al. Differentiating the impact of anatomic and non-anatomic liver resection on early recurrence in patients with Hepatocellular Carcinoma[J]. World J Surg Oncol, 2010, 8: 43. DOI: 10.1186/1477-7819-8-43 |
| [7] | Makuuchi M, Hasegawa H, Yamazaki S. Ultrasonically guided subsegmentectomy[J]. Surg Gynecol Obstet, 1985, 161(4): 346-350. |
| [8] | Aoki T, Murakami M, Koizumi T, et al. Three-Dimensional Virtual Endoscopy for Laparoscopic and Thoracoscopic Liver Resection[J]. J Am Coll Surg, 2015, 221(2): e21-e26. DOI: 10.1016/j.jamcollsurg.2015.04.012 |
| [9] | 王恺, 徐智, 黄明文, 等. 腹腔镜解剖性肝切除术治疗肝癌16例[J]. 世界华人消化杂志, 2010, 18(20): 2163-2165. |
| [10] | 赵国栋, 胡明根, 刘荣. 模式化腹腔镜肝左外叶切除术: 附71例临床应用报道[J]. 南方医科大学学报, 2011, 31(4): 737-740. |
| [11] | 陈焕伟, 王峰杰, 邓斐文, 等. 腹腔镜解剖性肝切除治疗肝细胞癌: 附30例报告[J]. 中华腔镜外科杂志: 电子版, 2015, 8(2): 128-131. DOI: 10.3877/cma.J.issn.1674-6899.2015.02.011 |
| [12] | Bismuth H, Houssin D, Castaing D. Major and minor segmentectomies “réglées” in liver surgery[J]. World J Surg, 1982, 6(1): 10-24. |
| [13] | Buell J F, Cherqui D, Geller D A, et al. The international position on laparoscopic liver surgery: The Louisville Statement, 2008[J]. Ann Surg, 2009, 250(5): 825-830. |
| [14] | Ishizawa T, Gumbs A A, Kokudo N, et al. Laparoscopic segmentectomy of the liver: from segment I to Ⅷ[J]. Ann Surg, 2012, 256(6): 959-964. DOI: 10.1097/SLA.0b013e31825ffed3 |
| [15] | Tranchart H, Diop P S, Lainas P, et al. Laparoscopic major hepatectomy can be safely performed with colorectal surgery for synchronous colorectal liver metastasis[J]. HPB (Oxford), 2011, 13(1): 46-50. DOI: 10.1111/j.1477-2574.2010.00238.x |
| [16] | Alkhalili E, Berber E. Laparoscopic liver resection for malignancy: a review of the literature[J]. World J Gastroenterol, 2014, 20(37): 13599-13606. DOI: 10.3748/wjg.v20.i37.13599 |
| [17] | Soubrane O, Goumard C, Laurent A, et al. Laparoscopic resection of hepatocellular carcinoma: a French survey in 351 patients[J]. HPB (Oxford), 2014, 16(4): 357-365. DOI: 10.1111/hpb.12142 |
| [18] | 余钒, 郑树国, 李建伟, 等. Glisson蒂横断式腹腔镜解剖性肝切除术的临床疗效[J]. 中华消化外科杂志, 2015, 14(4): 305-309. DOI:10.3760/cma.j.issn.1673-9752.2015.04.010. |
| [19] | Nguyen K T, Gamblin T C, Geller D A. World review of laparoscopic liver resection-2,804 patients[J]. Ann Surg, 2009, 250(5): 831-841. DOI: 10.1097/SLA.0b013e3181b0c4df |
| [20] | Xiang L, Xiao L, Li J, et al. Safety and feasibility of laparoscopic hepatectomy for hepatocellular carcinoma in the posterosuperior liver segments[J]. World J Surg, 2015, 39(5): 1202-1209. DOI: 10.1007/s00268-015-2946-3 |



