Yu Zheng, E-mail: yuzheng196094@163.com
乳腺癌是一种异质性疾病,不同患者具有不同的组织学亚型和分子亚型,并有不同的临床表现、治疗反应和预后[1]。新辅助化疗目前作为乳腺癌术前全身治疗的标准方案,呈现出较好的临床效果,但激素受体(ER、PR)阳性的乳腺癌患者或者不能耐受化疗的患者很难通过新辅助化疗达到病理学完全缓解[2],并且细胞毒性药物具有较强的毒副作用,导致患者在接受手术时往往处于低免疫状态,甚至不能耐受手术治疗。可否通过内分泌治疗等相对低毒性的方式来达到术前对恶性肿瘤的降期治疗尚不清楚。目前新辅助内分泌治疗报道相对较少,缺乏大宗的前瞻性临床试验来明确新辅助内分泌治疗的有效性和安全性,不能有效指导临床合理应用。尽管如此,在有限的报道中仍然显示新辅助内分泌治疗对于绝经后的激素依赖性乳腺癌患者有较好的疗效和安全性[2, 3, 4],对于不适用或拒绝化疗的激素受体阳性乳腺癌患者采用新辅助内分泌治疗[5],我们也看到了令人乐观的结果。
在乳腺癌的内分泌治疗中,雌激素受体阻滞剂和AIs最为常用。对于绝经后激素依赖性乳腺癌患者的术后内分泌治疗,AIs的疗效更为显著[6]。目前临床广泛使用第三代AIs,包括非类固醇类如阿那曲唑、来曲唑,以及类固醇类如依西美坦。然而在术前的新辅助内分泌治疗中AIs的优势并没有被证实[3]。化疗联合内分泌治疗或联合两种内分泌治疗药物的新辅助治疗方案也被提出,但其优势并没有被证实[3, 7]。
本研究旨在分析使用AIs的新辅助内分泌治疗和新辅助化疗的疗效和安全性差异,并且比较AIs和雌激素受体阻滞剂应用于新辅助内分泌治疗中的疗效差异。为临床合理地将AIs用于新辅助内分泌治疗提供理论依据。
1 资料与方法 1.1 纳入文献 1.1.1 研究类型随机对照试验,无论是否采用盲法。排除动物实验及体外试验。
1.1.2 研究对象纳入标准:①纳入病例均为绝经后乳腺癌患者;②实验组激素受体均为阳性,且未出现远处转移;③均为术前的新辅助治疗,之前未做任何治疗;④原始数据提供危险差(risk difference RD)及95%可信区间(95%CI)或者可以转化为RD值及95%CI;⑤治疗效果评价均为术前的短期评价,评价方式均采用影像学评价,评价指标包括:完全缓解率、部分缓解率、总有效率、疾病稳定率、总获益率、疾病进展率,且各指标的定义相同。
1.1.3 干预措施实验组采用AIs,包括来曲唑、阿那曲唑或者依西美坦,对照组采用三苯氧胺(他莫昔芬)或化疗。
1.1.4 结局指标参照WHO疗效评价标准,评价价值比较统一。①完全缓解(CR):肿瘤完全消失并持续至少4周;②部分缓解(PR):肿瘤缩小50%以上并持续至少4周,且无新发病灶出现;③总有效率:CR+PR;④疾病稳定(SD):肿瘤缩小50%以下,或增大25%以内,持续至少4周且无新发病灶;⑤总获益率:CR+PR+SD;⑥疾病进展(PD):肿瘤增大25%以上或者出现新发病灶。
1.2 文献检索计算机检索Cochrane 图书馆、PubMed、中国期刊全文数据库(CNKI)及中国生物医学文献数据库(CBMdisc),截止时间为2015年10月,英文检索词包括:breast cancer,aromatase inhibitors,letrozole,tamoxifen,neoadjuvant end ocrine therapy,neoadjuvant chemotherapy。 中文检索词包括:乳腺癌、芳香化酶抑制剂、来曲唑、阿那曲唑、他莫昔芬、依西美坦、三苯氧胺、新辅助内分泌治疗、新辅助化疗。
1.3 文献筛选、质量评价与数据提取文献筛选由2名研究者独立进行,阅读题目和摘要,排除明显不符合纳入标准的文献后,通读全文并分析是否符合全部纳入标准。依据Cochrane 系统评价手册5.0.0版关于RCT 的质量评价标准进行质量评价。用自拟的资料提取表提取数据,内容包括:①试验的一般情况:研究者、病例数、干预措施、2组患者的基线情况、年龄范围、结局指标、治疗方式;②研究质量:随机方法、分配隐藏、盲法、失访/退出情况。2名研究者独立进行质量评价和数据提取之后相互核对,若有异议于第三方讨论解决。
1.4 统计学分析采用Cochrane 协作网提供的RevMan 5.0 软件。首先对纳入的研究进行异质性检验,若纳入研究的异质性较小(P>0.05,I2 < 50%),采用固定效应模型进行meta分析;若纳入研究的异质性较大(P≤ 0.05,I2≥50%),则应考察异质性的来源并去除异质性;若异质性不能去除,而纳入的研究具有临床同质性,则应用随机效应模型进行Meta 分析;若纳入研究间的临床异质性较大而不能合并,则采用描述性分析。本研究资料为计数资料,使用相对危险度(RR)作为统计量,并计算其95%CI。通过漏斗图对发表性偏倚进行分析,保证Meta分析的可靠性。
2 结果 2.1 检索结果和质量评价 2.1.1 检索结果和文献特征根据检索策略共检索出相关文献162篇,阅读题目及摘要后排除重复文献40篇,排除综述类文献32篇,不符合纳入标准的文献77篇,最终纳入文献9篇,共纳入病例1 512例。其中6篇为英文文献,3篇为中文文献(表 1)。
| 研究 | 病例数(治疗组/对照组) | 干预措施 | 疗程 (月) | 年龄(岁) | 基线相似性 | 结局指标 | 治疗方式 | |
| 治疗组 | 对照组 | |||||||
| 王永霞等 [ 8] | 25/25 | 来曲唑2.5 mg/d | 他莫昔芬20 mg/d | 3 | 54~79 | 是 | ①②④⑥ | 术前 |
| 李荣萍等 [ 9] | 55/55 | 来曲唑2.5 mg/d | 他莫昔芬20 mg/d | 3 | 58~72 | 是 | ①②③④ | 术前 |
| 芦珊等 [ 10] | 29/29 | 来曲唑2.5 mg/d | 他莫昔芬20 mg/d | 3 | 60~76 | 是 | ①②③④ | 术前 |
| Smith等 [ 11] | 113/108 | 阿那曲唑1 mg/d | 他莫昔芬20 mg/d | 3 | 50~90 | 是 | ①②④⑥ | 术前 |
| Alba等 [ 12] | 48/47 | 来曲唑2.5 mg/d | 化疗⑦ | 4~6 | 不详 | 是 | ①②④⑥ | 术前 |
| Luigi等 [ 13] | 163/151 | 阿那曲唑1 mg/d | 他莫昔芬20 mg/d | 3 | 44~96 | 是 | ③ | 术前 |
| Semiglazov等 [ 14] | 121/118 | 阿那曲唑/依西美坦 | 化疗⑧ | 3 | 55~80 | 是 | ①②③④ | 术前 |
| Eiermann等 [ 15] | 154/170 | 来曲唑2.5 mg/d | 他莫昔芬20 mg/d | 4 | 55~80 | 是 | ①②④⑥ | 术前 |
| Mohammadianpanah等 [ 16] | 50/51 | 来曲唑2.5 mg/d+化疗⑨ | 化疗⑨ | 2~5 | 47~83 | 是 | ①②④⑥ | 术前 |
| ①完全缓解;②部分缓解;③总有效率;④疾病稳定;⑤总获益率;⑥疾病进展率;⑦多柔比星+多西他赛+环磷酰胺;⑧多柔比星+紫杉醇;⑨氟尿嘧啶+多柔比星+环磷酰胺 | ||||||||
本研究纳入9篇RCT中,质量评价A 级6篇,B 级3 篇(表 2)。
纳入研究6个,其中有4个研究病例组使用来曲唑,有2个研究病例组使用阿那曲唑。6个研究中,病例组539人,对照组538人,①总有效率的Meta分析:经异质性检验,各研究间具有同质性(P=0.46,I2=0),采用固定效应模型合并统 计量,结果显示2组间差异有统计学意义[RR为1.52,95%CI(129,178),P < 0.01],可以认为AIs在总有效率上优于他莫昔芬(图 1)。②完全缓解率的Meta分析:有5个研究提供了完全缓解率的对比,经异质性检验,各研究间差异无统计学意义(P=0.23,I2=28%),采用固定效应模型合并统计量,结果显示2组间差异有统计学意义[RR为3.69,95%CI(1.85,3.36),P < 0.01],可以认为AIs在完全缓解率上优于他莫昔芬(图 2)。
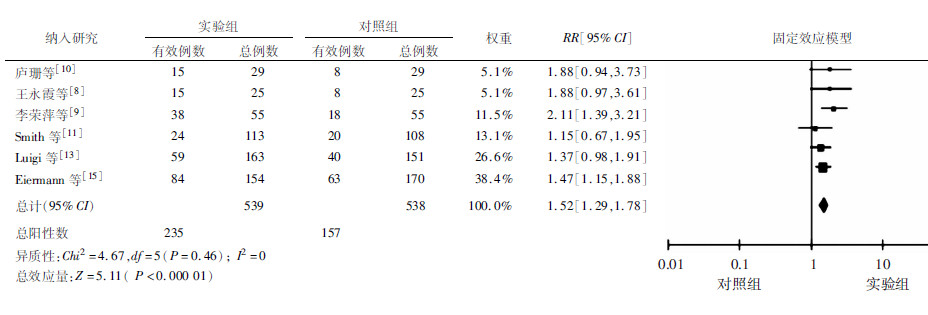 |
| 图 1 AIs和他莫昔芬总有效率(CR+PR)比较的Meta分析 |
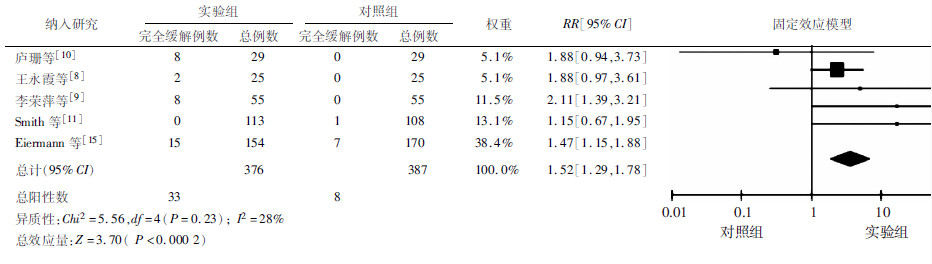 |
| 图 2 AIs和他莫昔芬完全缓解率(CR)比较的Meta分析 |
入2个研究[12, 14],病例组169人,对照组165人。①总有效率的Meta分析:经异质性检验,各研究间差异无统计学意义(P=0.11,I2=26%),纳入的2个研究具有同质性,采用固定效应模型合并统计量,结果显示2组间差异无统计学意义[RR为0.93,95%CI(0.79,1.10),P=0.40]。故尚不能认为使用AIs的新辅助内分泌治疗同新辅助化疗在总有效率上存在差异。②完全缓解率的Meta分析:经异质性检验,各研究间差异无统计学意义(P=0.38,I2=0%),纳入的2个研究具有同质性,采用固定效应模型合并统计量,结果显示2组间差异无统计学意义[RR为0.81,95%CI(0.42,1.56),P=0.53]。故尚不能认为使用AIs的新辅助内分泌治疗同新辅助化疗在完全缓解率上存在差异。
2.2.3 新辅助化疗联合内分泌治疗与仅使用新辅助化疗仅有1篇研究比较新辅助化疗联合内分泌治疗同仅使用新辅助化疗之间的疗效差异[16],故未进行Meta分析。该研究纳入患者101人(50/51),结果显示联合新辅助治疗同单独新辅助化疗其总有效率的差异没有统计学意义[OR=1.48,95%CI(0.58,3.77)]。但若只包括ER(+)的患者,那么总有效率的差异就有统计学意义[OR=7.5,95%CI(1.48,37.91)],其完全缓解率的差异也有统计学意义[OR=4.09,95%CI(1.0,16.72)],联合治疗组的完全缓解率和总有效率均高于单一治疗组。该研究结果表明将内分泌治疗加入新辅助化疗中没有增加毒性反应。
2.2.4 毒副作用AIs和他莫昔芬的毒副反应发生率都较低,症状也较轻。潮热、乏力、白带增多在他莫昔芬组更常见,各个研究报道2组间的差异没有统计学意义。头痛、恶心在AIs组中更常见,同样也没有统计学意义[8, 9, 10, 11, 13, 15]。有1篇研究详细比较了细胞毒性药物和AIs的毒副反应[14],AIs常见的不良反应包括潮热(23%)、乏力(15%)、阴道出血(7%)、关节痛(7%)等,而细胞毒性药物常见的不良反应包括白细胞减少(43%)、神经病变(30%)、乏力(8%)、口腔炎(7%)、腹泻(7%)、脱发(79%)、心脏毒性(7%)等,相比之下,AIs具有更轻的毒副症状和更低的毒副反应发生率。
2.2.5 发表性偏倚分析应用Revman5.3软件制作的AIs同他莫昔芬总有效率比较的漏斗图进行分析,各研究基本沿中线呈对称分布,呈倒置的漏斗状,说明纳入的研究发表性偏倚较小,符合本文文献纳入的要求。
3 讨论新辅助治疗可以在手术治疗之前缩小实体肿瘤的大小,这不仅可以达到降期治疗的目的,也可以在治疗过程中观察疾病对于治疗的反应,这个优势可以让医师在得知患者总生存期和无病生存期的获益之前,就能判断短期的治疗效果。新辅助化疗作为术前新辅助治疗的常规方案已得到国际公认,然而新辅助内分泌治疗的应用价值却尚未达成共识。对于绝经前的激素依赖性乳腺癌患者,内分泌治疗方案通常是以三苯氧胺(他莫昔芬)为代表的雌激素受体阻滞剂,而对于绝经后妇女,内分泌治疗方案可选择雌激素受体阻滞剂或者AIs,既往研究已证实术后采用AIs行内分泌治疗其无病生存期和总生存期均优于采用雌激素受体阻滞剂治疗[6],但在术前对于肿瘤的降期治疗,二者的差异却并不明确。
本Meta分析研究的群体局限在绝经后的激素依赖性乳腺癌患者,这部分人群以老年女性居多,通常对于化疗的耐受性较差,尤其是术前的新辅助化疗,常常因为化疗引起的低免疫状态或肝肾功能、心功能损伤而丧失手术机会,如果能通过相对低毒性的内分泌治疗方案达到同样的降期治疗目的将大大缓解患者的痛苦并提高治疗的效率。相对于其他治疗方式,新辅助内分泌治疗的研究并不多,本Meta分析通过严格的文献筛选纳入9个符合要求的随机对照研究,其中6个研究比较AIs和他莫昔芬在新辅助内分泌治疗中的疗效差异,Meta分析结果显示AIs治疗组和他莫昔芬治疗组在总有效率和完全缓解率上有明显差异,AIs治疗组能获得更好的治疗效果,完全缓解率也更高(尽管2组都比较低),两类药物的毒副作用是不同的,但都在可控范围内,药物相关性死亡都罕见。
本Meta分析纳入了2个比较新辅助内分泌治疗和新辅助化疗之间疗效差异的随机对照研究。Meta分析结果没有显示出二者在总有效率和完全缓解率上存在显著差异,但在2个临床随机试验中呈现出化疗更有优势,如果要明确这种优势需要大型的临床随机对照试验。因此,认为新辅助内分泌治疗在效果上和新辅助化疗相当可能并不安全,后者仍应该视为对合适患者的标准选择。而对于化疗耐受性较差的绝经后激素依赖性乳腺癌患者,使用AIs的新辅助内分泌治疗可以作为一种合适的选择。相对于细胞毒性药物,内分泌治疗药物毒副作用明显偏低,潮热、恶心、乏力、头痛、白带增多、皮疹和瘙痒等是常见的不良反应,均不会造成患者生活质量的明显下降。
对于术后将内分泌治疗和化疗同期进行的治疗方案也曾被研究过,然而并没有显示出在无病生存期和总生存期上有明显的优势[17],有研究指出:在肿瘤细胞分化的G0期,内分泌治疗药物会抑制化疗药物的敏感性[18],一些临床研究数据显示化疗和内分泌治疗结合有更大的毒副作用[19],对于术前将二者联合应用的研究较少。本Meta分析纳入了一个将二者联合用于新辅助治疗方面的随机对照研究,结果显示联合治疗在短期疗效上显现出优势,并且没有增加毒副作用。若要证实这种优势还需要更多的实验室和临床研究。
本Meta分析的局限性:①纳入的文献样本量均较低,统计学强度有限;②没有对保乳率、两类内分泌药物联用的治疗方案进行研究,也没有研究ER和PR阳性、ER或PR阳性这两种分子类型对于新辅助内分泌治疗的疗效差异,以及ER强阳性和ER弱阳性对于新辅助内分泌治疗的敏感性差异。因此,我们将在这些方面做进一步的研究。
综上所述,对于绝经后的激素依赖性乳腺癌患者,AIs在总有效率和完全缓解率上都显示出优于雌激素受体阻滞剂的疗效,并且显示出和化疗疗效相当的水平,提示可以作为绝经后激素依赖性乳腺癌患者新辅助治疗的一个安全有效的方案,值得更深入研究,有待于大规模、高质量的研究进一步评价。
| [1] | Goldhirsch A, Winer E P, Coates A S, et al. Personalizing the treatment of women with early breast cancer: highlights of the St Gallen International Expert Consensus on the primary therapy of early breast cancer 2013. Ann Oncol, 2013, 24(9): 2206-2223. DOI: 10.1093/annonc/mdt303 |
| [2] | Mathew J, Asgeirsson K S, Jackson L R, et al. Neoadjuvant endocrine treatment in primary breast cancer: review of literature . Breast, 2009, 18(6): 339-344. DOI: 10.1016/j.breast.2009.09.012 |
| [3] | Chia Y H, Ellis M J, Ma C X. Neoadjuvant endocrine therapy in primary breast cancer: indications and use as a research tool. Br J Cancer, 2010, 103(6): 759-764. DOI: 10.1038/sj.bjc.6605845 |
| [4] | Dixon J M, Anderson T J, Miller W R. Neoadjuvant endocrine therapy of breast cancer: a surgical perspective. Eur J Cancer, 2002, 38(17): 2214-2221. DOI: 10.1016/S0959-8049(02)00265-4 |
| [5] | 张彦武, 常庆龙, 贾国丛.NCT不敏感的局部晚期乳腺癌的新辅助内分泌治疗疗效分析.中国普通外科杂志, 2010, 19(5): 569-571. |
| [6] | Howell A, Cuzick J, Baum M, et al.Rseults of the ATAC(Arimidex, Tamoxifen, Alone or in Combination)trial after completion of 5 years’adjuvant treatment for breast cancer.Lancet, 2005, 365(9453): 60-62. DOI: 10.1016/S0140-6736(04)17666-6 |
| [7] | Makris A, Powles T J, Ashley S E, et al. A reduction in the requirements for mastectomy in a randomized trial of neoadjuvant chemoendocrine therapy in primary breast cancer. Ann Oncol, 1998, 9(11): 1179-1184. |
| [8] | 王永霞, 张爱玲, 张蓉, 等. 来曲唑与他莫西芬在绝经后乳腺癌新辅助内分泌治疗中的应用. 南方医科大学学报, 2008, 28(4): 667-668. |
| [9] | 李荣萍, 任佳, 吕文静, 等. 来曲唑在绝经后乳腺癌新辅助内分泌治疗中的应用. 山东医药, 2009, 49 (32): 67-69. |
| [10] | 芦珊, 周玮. 来曲唑在老年乳腺癌新辅助内分泌治疗中的疗效观察. 实用癌症杂志, 2012, 27(6): 632-634, 637. |
| [11] | Smith I E, Dowsett M, Ebbs S R, et al. Neoadjuvant Treatment of Postmenopausal Breast Cancer With Anastrozole, Tamoxifen, or Both in Combination: The Immediate Preoperative Anastrozole, Tamoxifen, or Combined With Tamoxifen (IMPACT) Multicenter Double-Blind Randomized Trial. J Clin Oncol, 2005, 23(22): 5108-5116. DOI: 10.1200/JCO.2005.04.005 |
| [12] | Alba E, Calvo L, Albanell J, et al. Chemotherapy (CT) and hormonotherapy (HT) as neoadjuvant treatment in luminal breast cancer patients: results from the GEICAM/2006-03, a multicenter, randomized, phase-II study. Ann Oncol, 2012, 23(12): 3069-3074. DOI: 10.1093/annonc/mds132 |
| [13] | Luigi C, Buzdar A, Noguchi S, et al. Comparison of Anastrozole versus Tamoxifen as Preoperative Therapy in Postmenopausal Women with Hormone Receptor-Positive Breast Cancer: the Pre-Operative “Arimidex” Compared to Tamoxifen (PROACT) trial. Cancer, 2006, 106(10): 2095-2103. DOI: 10.1002/cncr.21872 |
| [14] | Semiglazov V F, Semiglazov V V, Dashyan G A, et al. Phase 2 randomized trial of primary endocrine therapy versus chemotherapy in postmenopausal patients with estrogen receptorpositive breast cancer. Cancer, 2007, 110(2): 244-254. DOI: 10.1002/cncr.22789 |
| [15] | Eiermann W, Paepke S, Appfelstaedt J, et al. Preoperative treatment of postmenopausal breast cancer patients with letrozole: a randomized double-blind multicenter study. Ann Oncol, 2001, 12(11): 1527-1532. |
| [16] | Mohammadianpanah M, Ashouri Y, Hoseini S, et al. The efficacy and safety of neoadjuvant chemotherapy +/- letrozole in postmenopausal women with locally advanced breast cancer: a randomized phase Ⅲ clinical trial. Breast Cancer Res Treat, 2012, 132(3): 853-861. DOI: 10.1007/s10549-011-1814-6 |
| [17] | Albain K S, Green S J, Ravdin P M, et al. Adjuvant chemohormonal therapy for primary breast cancer should be sequential instead of concurrent: initial results from intergroup trial 0100(SWOG-8824). Proc Am Soc Clin Oncol, 2002, 2(1): 37-39. |
| [18] | Hug V, Thames H, Clark J. Chemotherapy and hormonal therapy in combination. J Clin Oncol, 1988, 6(1): 173-177. |
| [19] | Bear H D, Anderson S, Smith R E, et al. Sequential preoperative or postoperative docetaxel added to preoperative doxorubicin plus cyclophosphamide for operable breast cancer: National Surgical Adjuvant Breast and Bowel Project Protocol B-27. J Clin Oncol, 2006, 24(13): 2019-2027. DOI: 10.1200/JCO.2005. 04.1665 |



