2. 401147 重庆,重庆医科大学附属口腔医院:口腔疾病与生物医学重庆市重点实验室 ;
3. 401147 重庆,重庆医科大学附属口腔医院:重庆市高校市级口腔生物医学工程重点实验室
2. Affiliated Stomatology Hospital of Chongqing Medical University, Chongqing, 401147, China Chongqing Key Laboratory for Oral Diseases and Biomedical Sciences ;
3. Affiliated Stomatology Hospital of Chongqing Medical University, Chongqing, 401147, China Chongqing Key Laboratory of Oral Biomedical Engineering of Higher Education
Lin Juhong, Tel: 86-23-88860090, E-mail:juhonglin@sina.com
髓室底穿孔是牙髓病治疗中可能出现的并发症,也是牙科治疗难点之一。不适当的开髓、根管预备、桩腔预备、牙齿病理性吸收、龋坏等是造成穿孔的主要因素。若穿孔不能及时修复,细菌侵入使牙周组织发生炎症反应,进一步会导致牙槽骨的吸收破坏,最终引起牙齿缺失。髓室底穿孔的修复治疗,选择适宜的修复材料是非常重要的。一种具有良好的生物相容性,严密的封闭性,对组织无毒、无刺激,能促进组织再生能力形成的修复材料是髓室底穿孔治疗的关键。
近年来,无机三氧化聚合物(mineral trioxide aggregate,MTA)凭借其良好的生物学性能在临床上应用于髓室底穿孔的修复治疗,且效果显著[1-2]。有研究[3-4]表明,波特兰水门汀(Portland cement, PC)与MTA有着相似的生物学性能,且价格低廉,不易使牙体变色,有望成为MTA的替代材料应用于临床。因此,本研究通过体外实验比较PC与MTA修复磨牙髓室底穿孔的封闭性能与牙体形态恢复情况,为PC进一步应用于临床提供一定实验依据。
1 材料与方法 1.1 主要材料与设备PC(安徽阿尔博波特兰安庆有限公司),MTA(ProRoot MTA,Dentsply,美国),全自动研究级体视荧光显微镜(Carl Zeiss,德国),SEM(FEI公司,荷兰),硬组织切割系统(VertriebsGmH,德国),生化分析仪(Roche, 美国)。
1.2 样本选择选取重庆医科大学附属口腔医院颌面外科新鲜拔除的上下颌恒磨牙共53颗。清洁牙体表面后浸泡在4℃含0.2%叠氮钠的生理盐水中备用。样本选择标准:髓底完整且牙根分叉明显,无裂纹,无龋,无牙体吸收,根分叉处的牙本质厚度为2.5~2.8 mm;排除标准:融合根,因治疗或其他原因髓底破坏者[5]。
1.3 样本处理及分组用高速涡轮机将收集的离体牙常规开髓,揭髓室顶,按烤瓷冠牙体预备标准, 降低牙冠2 mm,清理髓腔,用游标卡尺测量离体牙髓室底厚度,得到53颗离体牙(髓底牙本质厚度为2.5~2.8 mm)。对离体牙进行编号,按随机数字表法分为2个实验组(PC、MTA组,n=24)和1个对照组(n=5)。实验组离体牙,采用4号球钻在髓室底中心制备穿孔,直径为2 mm,金刚砂车针修整穿孔,要求洞壁光滑,向冠方展10°;PC组:采用PC直接修复髓室底穿孔样本;MTA组:采用MTA直接修复髓室底穿孔样本。两个实验组修复材料均按照厂家说明以1 g材料与0.3 mL蒸馏水的比例混合调拌成黏稠状送入穿孔区,垂直加压器轻轻加压。对照组离体牙只开髓不制备髓室底穿孔模型。
所有样本牙的根分叉处放一蒸馏水湿润的小棉球,模拟根分叉处湿润环境。于37℃、100%湿度的恒温箱中储存7 d后取出,进行形态学观察和微渗漏实验。
1.4 形态学观察 1.4.1 体视显微镜观察体视显微镜下观察修复后根分叉形态,并按下列标准进行优劣等级评价:修复体平齐穿孔处根分叉表面、或超/欠距离<0.5 mm视为形态恢复良好,否则应视为较差形态修复[6]。
1.4.2 扫描电子显微镜观察按随机数字表法分别从PC、MTA组中各取12个样本用硬组织切割系统纵向切开,每个样本得到两个纵剖面,干燥后真空喷金。扫描电子显微镜观察黏结界面形态,并检测每个纵剖面两侧材料与牙体组织结合界面的微间隙宽度,记录每个结合界面的最大值,重复3次,取平均值[7-8]。
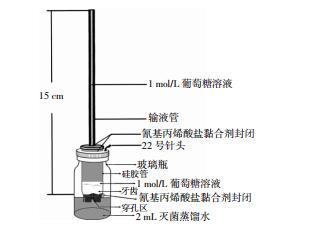
1.5 葡萄糖定量法检测微渗漏每个实验组剩余12个样本及对照组5个样本分别置入如图 1装置中[9-10],37℃饱和湿度的环境中,于第1、2、4、7、10、15、21天在玻璃瓶内取10μL样品,用生化分析仪测量其中的葡萄糖浓度,同时补足玻璃瓶内含0.2%叠氮钠的灭菌蒸馏水至2 mL。
|
| 图 1 葡萄糖微渗漏测试模型 |
1.6 统计学分析
使用SPSS 17.0统计软件进行数据分析。因数据变量为非正态分布,采用秩和检验(Kruskal-Wallis法)进行比较,显著性标准α=0.05。
2 结果 2.1 形态学观察结果如图 2所示,体视显微镜观察下两实验组所有样本均达到了良好标准的形态恢复,完整的恢复了穿孔区根分叉表面。

|
| A:PC组;B:MTA组 图 2 PC、MTA组髓室底穿孔修复后体视显微镜下根分叉形态观察(×10) |
2.2 SEM下观察修复后的接触面
图 3所示,SEM下PC和MTA与牙体组织之间均可观察到不连续的微小间隙。在SEM下检测到PC与牙体组织间隙宽度为(7.363±2.159)μm,MTA与牙体组织间隙宽度为(8.693±3.551)μm,两者间隙宽度无统计学差异(P=0.248)。

|
| A:PC组;B:MTA组 图 3 PC、MTA髓室底穿孔修复后SEM观察 |
2.3 微渗漏观察结果
阴性对照组在观察周期内均未检测到葡萄糖渗漏,说明微渗漏测试模型的封闭性是可信的。PC、MTA组在不同时间点的葡萄糖渗漏量见表 1。PC组、MTA组从第1天开始均有样本检测出少量的葡萄糖渗漏,虽然从各时间点渗漏量的变化趋势看PC组的微渗漏量要小于MTA组,但2组的葡萄糖渗漏量在所有观察时间点均无统计学差异(P>0.05)。
| 组别 | 1 d | 2 d | 4 d | 7 d | 10 d | 15 d | 21 d |
| PC组 | 1.070±0.648 | 2.193±0.877 | 3.729±1.087 | 5.928±1.286 | 8.896±1.192 | 12.143±1.722 | 16.698±2.359 |
| MTA组 | 1.018±0.353 | 2.142±0.573 | 3.844±0.783 | 6.977±1.433 | 10.227±1.942 | 14.303±2.379 | 19.306±3.135 |
3 讨论
髓腔穿孔修复治疗的预后与穿孔的位置,穿孔的大小,邻近牙周状况以及修复材料的选择有关。而其治疗失败最主要原因是由于穿孔区不能有效的、及时的封闭,以及修复材料生物相容性不佳,从而导致牙周组织感染。因此,材料的封闭性和生物活学是治疗成败的关键因素[11-12]。
MTA凭借其良好的理化性能及生物活学作为髓腔穿孔修复材料,疗效是肯定的,但是由于其价格比较昂贵,难以在临床上广泛应用[1-2]。有研究发现PC与MTA成分相似,并且PC价格十分便宜[3]。Shahi等[13]观察5个时间点(7、15、30、60、90 d)MTA与PC对大鼠皮下组织反应,结果表明,两者具有相似的组织相容性。王燕等[14-15]在体外抑菌实验中显示PC对白色念珠菌及大肠杆菌有一定抑制生长能力, 以及PC作为根尖屏障材料的封闭性与MTA相当,并且明显优于玻璃离子水门汀和银汞合金。Ahmed等[16]系统性评估在SEM下观察PC类材料对细胞生物活性、形态学影响,结果发现PC有良好的细胞相容性,可作为MTA替代材料进一步研究。
目前,国内外关于微渗漏的研究方法主要有染料渗透法,流体输送法,蛋白渗透法,细菌渗漏法,同位素示踪法,葡萄糖定量检测法等[11]。每种检测方法都有一定的优点和不足,目前尚无统一的测试标准。本实验采用葡萄糖氧化酶-蒽酮法用葡萄糖作为示踪物检测微渗漏, 通过直接检测漏出的葡萄糖的浓度对微渗漏进行定量测定, 检测方法灵敏、准确,在不破坏试件的情况下可以重复测试,且动态监测,评估时间与微渗漏之间的关系[9]。本实验结果表明:两实验组在观察的各个时间点均检测出微渗漏的存在,并且随着时间的延长,两组的葡萄糖渗出量均有所增加,虽然在观察时期内,PC组的渗漏量总体趋势小于MTA组,但两者在各观察时间点内的葡萄糖渗出量均无统计学差异(P>0.05)。De-Deus等[5]利用液体输送法对比MTA和PC修复磨牙髓室底穿孔的研究表明,两者封闭能力相当,与本实验结果一致。而Shahi等[17]采用蛋白渗透法比较PC与MTA作为底穿修补材料的封闭性研究,结果显示PC的封闭性明显优于MTA。造成实验结果有差异可能是由于检测微渗漏实验方法的不同以及材料地域的差异等所造成的。
扫描电镜下PC组和MTA组的纵切图片中均可观察到材料与牙体组织之间微间隙的存在,这可能是由于材料是人工调拌后送入穿孔区,而水粉比例、调拌时间会存在一定的误差,另外逐层加压过程中可能受力不均,不能紧密压实材料。微间隙的存在导致材料不能完全封闭穿孔,引起微渗漏的发生。本实验中,在SEM下对间隙宽度检测分析表明PC、MTA与牙体组织的间隙大小无明显差异(P>0.05)。同样,Bidar等[8]利用SEM形态学观察MTA与PC作为根尖倒充填材料的边缘封闭情况,结果表明材料与牙本质壁之间也存在微间隙,且间隙宽度无统计学差异(P>0.05)。而Torabinejad等[18]研究表明MTA的边缘封闭能力优于银汞合金、intermediaterestorative material和Super-EBA。
口腔科材料的更新与发展一直是口腔领域的研究热点。然而至今尚没有一种修复方法或生物材料能完全消除微渗漏。本实验探讨PC修复髓室底穿孔的体外效果,通过和MTA对比,结果发现:PC与MTA修复髓室底穿孔在封闭性和外形恢复方面无显著差异,提示PC可以考虑作为MTA替代材料进一步研究,但本研究的结果并不能完全代表临床情况, 要进一步结合临床研究进行综合考虑。
| [1] | Pace R, Giuliani V, Pagavino G. Mineral trioxide aggregate as repair material for furcal perforation: case series[J]. J Endod,2008, 34 (9) : 1130 –1133. DOI:10.1016/j.joen.2008.05.019 |
| [2] | Parirokh M, Torabinejad M. Mineral trioxide aggregate: a comprehensive literature review--Part III: Clinical applications, drawbacks, and mechanism of action[J]. J Endod,2010, 36 (3) : 400 –413. DOI: 10.1016/j.joen.2009.09.009 |
| [3] | Asgary S, Parirokh M, Eghbal M J, et al. A comparative study of white mineral trioxide aggregate and white Portland cements using X-ray microanalysis[J]. Aust Endod J,2004, 30 (3) : 89 –92. |
| [4] | Keskin C, Demiryurek E O, Ozyurek T. Color stabilities of calcium silicate-based materials in contact with different irrigation solutions[J]. J Endod,2015, 41 (3) : 409 –411. DOI:10.1016/j.joen.2014.11.013 |
| [5] | De-Deus G, Reis C, Brandao C, et al. The ability of Portland cement, MTA, and MTA Bio to prevent through-and-through fluid movement in repaired furcal perforations[J]. J Endod,2007, 33 (11) : 1374 –1377. DOI:10.1016/j.joen.2007.07.024 |
| [6] | 谢俊, 尹仕海, 肖俐娟, 等. 树脂嵌体修复磨牙髓室底穿孔的形态学及微渗漏研究[J]. 华西口腔医学杂志,2009, 27 (2) : 160 –163. |
| [7] | 王密, 尹世海, 王奇, 等. IRoot BP修复磨牙髓室底穿孔的研究[J]. 华西口腔医学杂志,2013, 31 (3) : 257 –266. DOI:10.7518/hxkq.2013.03.010 |
| [8] | Bidar M, Moradi S, Jafarzadeh H, et al. Comparative SEM study of the marginal adaptation of white and grey MTA and Portland cement[J]. Aust Endod J,2007, 33 (1) : 2 –6. |
| [9] | Xu Q, Fan M W, Fan B, et al. A new quantitative method using glucose for analysis of endodontic leakage[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2005, 99 (1) : 107 –111. DOI:10.1016/j.tripleo.2004.06.006 |
| [10] | Zou L, Liu J, Yin S, et al. In vitro evaluation of the sealing ability of MTA used for the repair of furcation perforations with and without the use of an internal matrix[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod,2008, 105 (6) : e61 –e65. DOI:10.1016/j.tripleo.2008.01.038 |
| [11] | Torabinejad M, Parirokh M. Mineral trioxide aggregate: a comprehensive literature review--part II: leakage and biocompatibility investigations[J]. J Endod,2010, 36 (2) : 190 –202. DOI:10.1016/j.joen.2009.09.010 |
| [12] | Silva M J, Caliari M V, Sobrinho A P, et al. An in vivo experimental model to assess furcal lesions as a result of perforation[J]. Int Endod J,2009, 42 (10) : 922 –929. DOI:10.1111/j.1365-2591.2009.01595.x |
| [13] | Shahi S, Rahimi S, Yavari H R, et al. Effect of mineral trioxide aggregates and Portland cements on inflammatory cells[J]. J Endod,2010, 36 (5) : 899 –903. DOI:10.1016/j.joen.2010.01.001 |
| [14] | 王燕, 林居红, 张红梅, 等. 波特兰水门汀对3种微生物的体外生长抑制实验研究[J]. 重庆医科大学学报,2013, 38 (7) : 801 –804. DOI:10.11699/cyxb20130733 |
| [15] | 王燕, 林居红, 罗俊, 等. Portland Cement用于根尖屏障材料的封闭性研究[J]. 第三军医大学学报,2012, 34 (3) : 223 –225. DOI:10.16016/j.1000-5404.2012.03.022 |
| [16] | Ahmed H M, Luddin N, Kannan T P, et al. Cell attachment properties of Portland cement-based endodontic materials: biological and methodological considerations[J]. J Endod,2014, 40 (10) : 1517 –1523. DOI:10.1016/j.joen.2014.06.013 |
| [17] | Shahi S, Rahimi S, Hasan M, et al. Sealing ability of mineral trioxide aggregate and Portland cement for furcal perforation repair: a protein leakage study[J]. J Oral Sci,2009, 51 (4) : 601 –606. DOI:10.1016/j.joen.2014.06.013 |
| [18] | Torabinejad M, Smith P W, Kettering J D, et al. Comparative investigation of marginal adaptation of mineral trioxide aggregate and other commonly used root-end filling materials[J]. J Endod,1995, 21 (6) : 295 –299. |



