2. 400042 重庆,第三军医大学大坪医院野战外科研究所放射科
2. Department of Radiology, Institute of Surgery Research, Daping Hospital, Third Military Medical University, Chongqing, 400042, China
抗中性粒细胞胞浆抗体(antineutrophil cytoplasmic autoantibody,ANCA)相关性系统性血管炎(ANCA-associated systemic vasculitides,AASV)是以血管发生坏死性炎症为特征的一类自身免疫性疾病,其最新的临床分型包括显微镜下多血管炎(microscopic polyangiitis,MPA)、肉芽肿性多血管炎(韦格纳氏肉芽肿)、嗜酸性肉芽肿性多血管炎(变应性肉芽肿性血管炎)和局限性肾脏血管炎[1-2]。ANCA呈胞浆型(cANCA)和核周型(pANCA),cANCA对应的抗原是蛋白酶3(proteinase 3,PR3),pANCA对应的抗原是髓过氧化物酶(myeloperoxidase MPO),cANCA和PR3阳性多见于肉芽肿性多血管炎(韦格纳肉芽肿),而pANCA和MPO阳性多见于MPA[1]。MPA是我国的主要发病类型,临床表现大多为肾组织和肺部损伤,肺脏受累除有咳嗽咯痰外,咯血为最突出的首发表现[2]。大部分患者起病缓慢,表现咯血量小,而部分患者肺泡毛细血管广泛渗出和出血,患者则表现为来势凶险的大咯血,若不采取积极抢救措施可导致患者窒息或低氧血症休克死亡,而早期诊断并给予及时正规的治疗可以使患者的预后得到明确的改善[3]。目前临床尚无有效的手段及时预测MPA患者是否会发生咯血,而CT为无创检查,快速,可重复性好。因此,本研究回顾性分析MPA患者在咯血前的胸部CT表现,探讨咯血前的胸部CT影像学是否对早期预测咯血有一定帮助,从而指导临床治疗与改善预后。
1 资料与方法 1.1 一般资料收集2013年1月至2015年9月四川省资阳市第一 人民医院确诊的原发性MAP患者资料。纳入标准:①年 龄18~85岁;②符合Chapel Hill会议(Chapel Hill Consensus Criteria,CHCC)关于显微镜下型多血管炎的 诊断标准,即患者有多系统损害的临床表现,血P-ANCA、 MPO阳性和/或血管壁有炎症和纤维素样坏死。排除标准:①合并肺结核、肺癌导致咯血;②丙基硫氧嘧啶等药物服用史;③长期绿脓杆菌感染和狼疮性肾炎等结缔组织疾病导致的ANCA阳性。共纳入30例MPA患者,根据初次住院是否有咯血分为2组:咯血组11例,其中男性9例,女性2例,年龄27~74(65.4±27.8)岁;非咯血组19例,其中男性7例,女性12例,年龄34~85(71.2±18.7)岁。分析咯血组在咯血前的胸部CT影像学特点,并与非咯血组进行对比分析。
1.2 实验室检查、CT检查设备及扫描方法间接免疫荧光法检测血pANCA,特异性酶联免疫吸附法(ELISA)检测血髓过氧化物酶(MPO)。其余实验室检查均按常规操作。患者均使用64排128层螺旋CT(美国GE Optima CT660),螺距0.984 ∶1,层厚5 mm,行常规扫描,扫描范围覆盖肺尖至膈肌水平。扫描条件:120 kV,100~110 mA,患者仰卧位,吸气后屏气扫描。
1.3 图像分析由2位不同的放射科医师分别独立盲法阅片,如果意见不一致则由第3位放射科医师读片,最终以取得一致意见为准。
1.4 统计学分析利用SPSS 16.0统计学软件分析数据,因样本量小于40,故两组样本间率的比较采用Fisher 精确概率法检验,以P<0.05为差异有统计学意义。
2 结果 2.1 MPA患者胸部CT影像表现本组30例患者均有不同程度的胸部CT异常表现。纤维条索影25例(83.3%),胸腔积液20例(66.7%),肺大泡15例(50.0%),网格影14例(46.7%),磨玻璃影和斑片影均为13例(43.3%),纵隔淋巴结肿大11例(36.7%),支气管扩张9例(30.0%),实变影8例(26.7%),小叶间隔增厚7例(23.3%),结节影2例(6.7%)均为非咯血组患者,空洞1例(3.3%)为咯血组患者。两组患者的网格影、磨玻璃影、斑片影和实变影病变既可见于双肺,也可以见于单侧肺部,但以中下肺最常见,咯血组病灶分布更广泛,表现为双肺多叶多段的病变。斑片影表现为高密度影,边缘模糊,网格影周边可见淡片状渗出液。非咯血组患者无空洞发现。11例尿少、血肌酐升高需要血液净化的患者均存在不同程度的胸腔积液。两组患者具体胸部CT影像表现见图 1,咯血组在咯血前的斑片影、实变影、磨玻璃样改变和网格影较非咯血组患者明显增多。对两组上述胸部CT表现结果进行统计学分析,差异均具有统计学意义(P<0.05,表 1),而且咯血组病灶分布更广泛。两组患者的其他病变比较差异无统计学意义(P>0.05,表 1)。
|
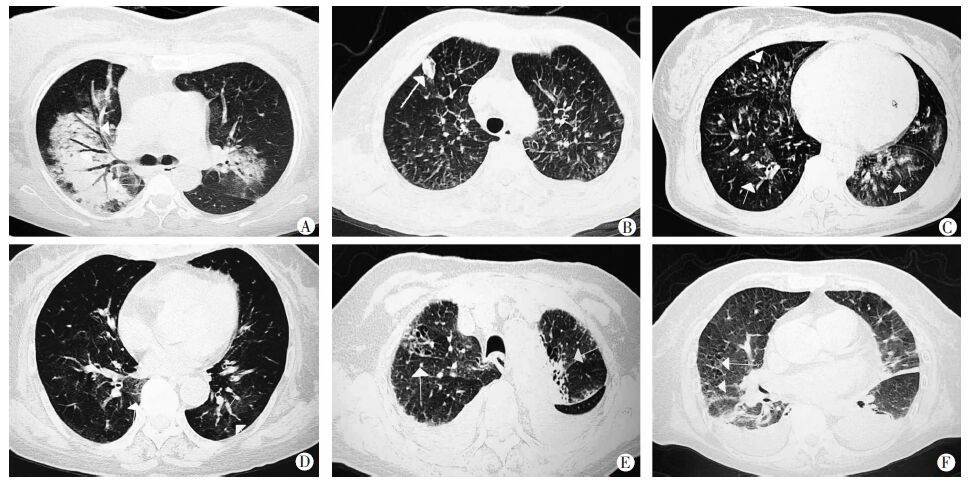
| A:咯血组右肺下叶大片实变影内可见含气支气管影;B:非咯血组右上肺局限性实变影;C:咯血组双肺磨玻璃影;D:非咯血组左肺下叶后基底段,右肺下叶内基底段磨玻璃影;E:咯血组双肺上叶网格影和斑片影;F:非咯血组散在网格影;白色箭头示病变部位 图 1 两组显微镜下多血管炎患者肺部CT表现 |
| CT表现 | 咯血组(n=11) | 非咯血组(n=19) | P值 |
| 斑片影 | 8 | 5 | 0.023 |
| 实变影 | 7 | 1 | 0.001 |
| 磨玻璃影 | 9 | 4 | 0.002 |
| 网格影 | 9 | 5 | 0.007 |
| 纤维条索影 | 10 | 15 | 0.626 |
| 胸腔积液 | 9 | 11 | 0.246 |
| 肺大泡 | 6 | 9 | 0.990 |
| 纵隔淋巴结增大 | 4 | 7 | 0.990 |
| 支气管扩张 | 4 | 5 | 0.687 |
| 空洞 | 1 | 0 | 0.058 |
| 小叶间隔增厚 | 5 | 2 | 0.068 |
| 结节影 | 0 | 2 | 0.520 |
2.2 胸部CT影像改变距离咯血的时间
咯血组患者在初次胸部CT影像学异常表现发现后2~14 d均出现不同程度的咯血,4例表现为痰中带血,7例患者咯血量达50 mL/d以上,肺血管受累程度越重者,其咯血量也越多。其中2例老年男性和1例老年女性患者在病变之初表现为单叶单段的局限性斑片影和条索影,但在病变发展过程及合并肺部感染后,即出现发热、咳嗽咯痰和心累气紧加重,复查胸部CT出现较为广泛的多叶多段的斑片影、实变影、网格影、磨玻璃影和小叶间隔增厚表现(图 1A、C、E),并分别在胸部影像学病变加重1、5、6 d后出现不同程度的咯血和呼吸衰竭,后经抢救无效死亡。提示MPA患者应结合临床资料和胸部影像学改变及时判断咯血可能并 给予及时治疗。非咯血组患者胸部影像学虽然有不同程度的改变,但病变较局限,在随访期间均无咯血表现。
2.3 临床和实验室资料收集30例MPA患者咯血前临床资料,发现发热6例,胸痛7例,咳嗽咯痰23例,心累气紧23例,15例患者双肺可闻及湿啰音。患者肾损害均表现为血尿、蛋白尿和 血肌酐升高,血P-ANCA和MPO均呈阳性。血白细胞 升高17例[(15.31±4.32)×109/L],贫血25例(81.10± 25.21)g/L,血沉增快26例(49.40±11.34)mm/h,C反应蛋白升高22例(12.30±4.58)mg/dL。结果显示咯血组患者胸痛、心累气紧、咳嗽咯痰和炎症指标较非咯血组有统计学差异(P<0.05,表 2)。
| 临床指标 | 咯血组(n=11) | 非咯血组(n=19) | P值 |
| 发热 | 4 | 2 | 0.110 |
| 胸痛 | 5 | 2 | 0.043 |
| 心累气紧 | 11 | 12 | 0.025 |
| 咳嗽咯痰 | 11 | 12 | 0.025 |
| 血白细胞高 | 9 | 8 | 0.040 |
| sCRP高 | 11 | 11 | 0.013 |
| 贫血 | 11 | 14 | 0.082 |
| 血沉高 | 11 | 15 | 0.141 |
| 死亡 | 7 | 0 | 0.001 |
2.4 入组患者的治疗和转归
患者在初次发病住院期间均给予糖皮质激素加环磷酰胺静脉冲击治疗,但咯血组有7例患者在咯血前进行了大剂量甲泼尼龙琥珀酸钠治疗,非咯血组患者无大剂量甲泼尼龙琥珀酸钠治疗。咯血组和非咯血组分别有8例和3例患者在病变之初进行了普通血液透析治疗。患者初次住院3个月后的随访结果:咯血组11例患者中有7例死亡,1例进入维持性血液透析;非咯血组19例患者随访期间均无死亡,其中2例进入维持性血液透析。
3 讨论15%~45%的ANCA相关性血管炎患者以肺损害起病,且病程中肺损害也会加重[1]。该病与遗传、环境、感染、药物等因素有关[4-7]。MPA患者一旦肺脏受累就容易出现肺咯血而危及生命,而早期诊断并给予及时正规治疗会使患者的预后得到明确的改善[3],但目前临床无有效手段预测咯血的出现。本研究回顾性分析提示MPA患者肺部广泛的斑片影、实变影、磨玻璃影和网格影结合胸痛、咳嗽咯痰、心累气紧以及炎症指标升高提示可能要出现咯血。虽然上述表现无疾病诊断的特异性,但在MPA患者预示可能要出现咯血。本组患者在初次发病入院之初均给予糖皮质激素加环磷酰胺静脉冲击治疗,但咯血组4例没有死亡的患者均进行了大剂量糖皮质激素治疗,非咯血组19例患者随访期间均无死亡。上述转归结果提示MPA出现咯血的患者预后很差。由于不能及时早期发现肺咯血,部分患者没有及时给予大剂量糖皮质激素,同时因为经济条件限制,本研究入选患者未能进行血浆置换治疗,这也是本组咯血患者死亡率较高的原因。有研究表明,咯血患者如果能早期及时给予糖皮质激素、细胞毒药物及血浆置换治疗可改善预后[8]。因此,早期预测肺咯血对指导临床治疗和改善预后至关重要。
MPA肺损害的主要影像表现为磨玻璃影、实变影及网格状影,相应的病理基础为肺泡出血、间质慢性炎症、血管炎或纤维化,其次为由于淋巴细胞浸润及轻度纤维化所致支气管血管束增厚,以及单发或多发的结节、空洞性病变[9]。本研究咯血组患者较非咯血组患者肺斑片影、实变影、磨玻璃影和网格影明显增加,且病变更广泛,表现为病变既可见于双肺,也可以见于单侧肺部的多叶多段,但以双中下肺最常见,斑片影表现为高密度影,边缘模糊,网格影周边可见淡片状渗出液。咯血组部分患者在咯血前表现为局限性斑片影和条索影,但在病变发展过程或合并肺部感染后,即容易出现多叶多段的斑片影、实变影、网格影和磨玻璃样等改变;咯血组患者在初次胸部CT影像学异常表现发现后均出现不同程度的咯血,提示肺部多叶多段的斑片影、肺实变、磨玻璃样改变和网格影有可能出现后续的咯血。因此,临床应当注意感染的预防、治疗以及胸部CT的动态随访,以减少咯血的发作改善预后。非咯血组患者无空洞表现,但和咯血组相比差异无统计学意义,其临床意义需要进一步增加样本量分析。
胸部影像学的改变与其肾脏病理改变有一定关系。本组30例患者中有7例行肾穿刺病理检查,其中4例非咯血组患者肾脏病理表现为免疫荧光阴性的新月体肾炎,胸部CT表现为局限性斑片影、纤维条索影,合并肺大泡、单侧胸膜增厚各1例,合并支气管扩张和单个结节影各1例。咯血组3例患者肾脏病理均表现为血管纤维素样坏死和新月体肾炎,相应的CT影像为弥漫磨玻璃影、局限性实变影并伴有胸腔积液,提示咯血组患者胸部CT影像表现和肾脏病理损伤更为严重。
MPA肺脏受累临床表现有发热、咳嗽、咯血、呼吸困难等,而胸片显示多样化,临床如果不结合MPO和P-ANCA的阳性极易误诊为其他疾病。当MPA的胸部CT表现为大片实变影、散在斑片影时要和肺部感染性病变鉴别,而肺部感染是诱发和加重MPA病变的重要病因,因此两种病变的表现可同时存在,抗感染治疗无好转时要想到MPA所致损伤。由于MPA患者较韦格纳肉芽肿患者肺内肉芽肿改变少见[10],所以本组MPA入选患者发生空洞、结节影的患者较少。MPA肺部网格影要与结缔组织性疾病引起的纤维化鉴别,目前研究认为肺纤维化或肺间质病变在ANCA血管炎患者比较常见[11-16],其肺纤维化的机制可能与特发性含铁血黄素沉着症类似的反复发生的肺泡出血有关[14],另外血管炎活跃期中性粒细胞脱颗粒,大量释放活性氧自由基,引起血管损伤导致的间质纤维化也是肺纤维化的重要发生机制[17]。
总之,本研究基于临床表现、实验室资料和胸部CT的统计结果分析提示MPA患者肺部广泛的斑片影、实变影、磨玻璃影和网格影CT影像表现结合胸痛、咳嗽咯痰、心累气紧以及炎症指标升高提示可能出现咯血,对临床医师早期诊断和治疗咯血有一定的意义。但由于本研究为单中心的回顾性研究,入选病例数较少,随访时间较短,其临床意义及实用性有待将来大规模、多中心的随机临床对照研究进一步证实。
| [1] | 唐莎, 张静波. ANCA相关性血管炎的免疫发病机制新进展[J]. 免疫学杂志,2013, 29 (7) : 628 –631. DOI:10.13431/j.cnki.immunol.j.20130135 |
| [2] | Lally L, Spiera R. Current landscape of antineutrophil cytoplasmic antibody-associated vasculitis: classification, diagnosis, and treatment[J]. Rheum Dis Clin North Am,2015, 41 (1) : 1 –19. DOI:10.1016/j.rdc.2014.09.003 |
| [3] | Kallenberg C G. Key advances in the clinical approach to ANCA-associated vasculitis[J]. Nat Rev Rheumatol,2014, 10 (8) : 484 –493. DOI:10.1038/nrrheum.2014.104 |
| [4] | Zhou X J, Cheng F J, Lv J C, et al. Higher DEFB4 genomic copy number in SLE and ANCA-associated small vasculitis[J]. Rheumatology (Oxford),2012, 51 (6) : 992 –995. DOI:10.1093/rheumatology/ker419 |
| [5] | Gatenby P A. Anti-neutrophil cytoplasmic antibody-associated systemic vasculitis: nature or nurture?[J]. Intern Med J,2012, 42 (4) : 351 –359. DOI:10.1111/j.1445-5994.2011.02705.x |
| [6] | Csernok E, Lamprecht P, Gross W L. Clinical and immunological features of drug-induced and infection-induced proteinase 3-antineutrophil cytoplasmic antibodies and myeloperoxidase-antineutrophil cytoplasmic antibodies and vasculitis[J]. Curr Opin Rheumatol,2010, 22 (1) : 43 –48. DOI:10.1097/BOR.0b013e3283323538 |
| [7] | Laudien M, Gadola S D, Podschun R, et al. Nasal carriage of Staphylococcus aureus and endonasal activity in Wegener's granulomatosis as compared to rheumatoid arthritis and chronic Rhinosinusitis with nasal polyps[J]. Clin Exp Rheumatol,2010, 28 (1 Sippl 57) : 51 –55. |
| [8] | 陈旻. KDIGO指南解读:血管炎肾损伤治疗[J]. 中国实用内科杂志,2012, 32 (12) : 932 –934. |
| [9] | Collins C E, Quismorio F P Jr. Pulmonary involvement in microscopic polyangiitis[J]. Curr Opin Pulm Med,2005, 11 (5) : 447 –451. DOI:10.1097/01.mcp.0000170520.63874.fb |
| [10] | Mueller A, Holl-Ulrich K, Lamprecht P, et al. Germinal centre-like structures in Wegener’s granuloma: the morphological basis for autoimmunity?[J]. Rheumatology (Oxford),2008, 47 (8) : 1111 –1113. DOI:10.1093/rheumatology/ken202 |
| [11] | Eschun G M, Mink S N, Sharma S. Pulmonary interstitial fibrosis as a presenting manifestation in perinuclear antineutrophilic cytoplasmic antibody microscopic polyangiitis[J]. Chest,2003, 123 (1) : 297 –301. DOI:10.1378/chest.123.1.297 |
| [12] | Tzelepis G E, Kokosi M, Tzioufas A, et al. Prevalence and outcome of pulmonary fibrosis in microscopic polyangiitis[J]. Eur Respir J,2010, 36 (1) : 116 –121. DOI:10.1183/09031936.00110109 |
| [13] | Arulkumaran N, Periselneris N, Gaskin G, et al. Interstitial lung disease and ANCA-associated vasculitis: a retrospective observational cohort study[J]. Rheumatology (Oxford),2011, 50 (11) : 2035 –2043. DOI:10.1093/rheumatology/ker236 |
| [14] | Homma S, Matsushita H, Nakata K. Pulmonary fibrosis in myeloperoxidase antineutrophil cytoplasmic antibody- associated vasculitides[J]. Respirology,2004, 9 (2) : 190 –196. DOI:10.1111/j.1440-1843.2004.00581.x |
| [15] | Yamada H. ANCA: associated lung fibrosis[J]. Semin Respir Crit Care Med,2011, 32 (3) : 322 –327. DOI:10.1055/s-0031-1279828 |
| [16] | Birnbaum J, Danoff S, Askin F B, et al. Microscopic polyangiitis presenting as a “pulmonary-muscle” syndrome: is subclinical alveolar hemorrhage the mechanism of pulmonary fibrosis?[J]. Arthritis Rheum,2007, 56 (6) : 2065 –2071. DOI:10.1002/art.22633 |
| [17] | Pankhurst T, Savage C O. Pathogenic role of anti-neutrophil cytoplasmic antibodies in vasculitis[J]. Curr Opin Pharmacol,2006, 6 (2) : 190 –196. DOI:10.1016/j.coph.2005.10.009 |



