2. 400020 重庆,重庆市人口和计划生育科学技术研究院
2. Chongqing Institute of Science and Technology in Population and Family Planning, Chongqing, 400020, China
男性精子质量在过去的几十年里呈现下降的趋势,病因学调查发现空气污染是导致精子质量下降的主要原因之一[1]。研究发现汽车尾气环境的持续暴露与人精子质量的下降相关[2]。目前相关机制研究众多,包括氧化应激[3]、雌激素样作用[4]、化学性损伤致生殖毒性[5],但这些研究成果未能有效地延伸于临床。在尾气染毒的模型研究中缺乏对尾气暴露模拟装置稳定性的讨论,导致病因学的进一步机制研究不能形成完整可靠的数据链。本研究构建并评估模拟尾气暴露环境的条件,制作汽车尾气暴露动物模型,明确汽车尾气暴露对雄鼠生精功能的损伤情况,尝试探讨汽车尾气暴露对雄性小鼠生精功能损伤可能的机制。
1 材料与方法 1.1 实验动物及分组雄性SPF级C57BL/6小鼠(第三军医大学实验动物中心提供)20只,8~10周龄,体质量20~24 g,进行适应性饲养1周,按随机数字表法分成对照组及暴露组,每组各10只。
1.2 主要实验设备与试剂自制玻璃缸,汽油发电机(伊藤动力,型号YT2000TM,上海伊眷实业有限责任公司),93号汽油(中国石油公司),石蜡切片机RM2245型(德国Leica公司),血气分析仪(美国NOVA Biomedical公司),PM2.5检测仪(8533型,美国TSI公司),空气循环系统(风扇型号L602,深圳齐心集团股份有限公司),希玛氧气检测仪AR8100(东莞万创电子制品有限公司),SO2检测仪(深圳吉顺安有限公司),计算机辅助精子分析系统(CASA,广州友林有限公司),一氧化氮、总抗氧化能力检测试剂盒(碧云天公司),Ham’s F-12培养液(美国Hyclone公司),戊巴比妥钠(美国Sigma公司)。
1.3 方法 1.3.1 构建汽车尾气持续暴露条件将通过汽油发电机怠速状态下排出的气体经连接管通入自制玻璃缸(2 m×1.5 m×0.8 m)装置内,根据药理Up and Down法[6]设计尾气染毒方案(暴露组),每次通入尾气30 s(尾气 ∶新鲜空气=1 ∶10)暴露1 h,每日重复3次,暴露40 d,监测尾气暴露开始和结束的氧含量,二氧化硫含量以及PM2.5含量。汽车尾气持续暴露3次后检测2组小鼠血气分析情况,用肝素预先湿润处理过的一次性注射器插入心脏取动脉血,快速将针头用橡皮塞密封后迅速进行血气分析。
1.3.2 实验动物的处理与标本收集小鼠染毒40 d后,腹腔注射0.1%戊巴比妥钠(0.01 mL/g)麻醉小鼠,活体取出睾丸和附睾,剔除脂肪组织并用滤纸滤干,称质量并记录睾丸、附睾组织质量,计算脏器系数:脏器系数=脏器质量(g)/体质量(g)×1 000‰。右侧睾丸固定液固定,石蜡包埋作病理组织切片,左侧睾丸在冰上立即进行匀浆。右心室取血后立即分离血浆。
1.3.3 小鼠生精功能检测摘取双侧附睾尾转入装有500 μL、37 ℃的Ham’s F-12培养液的培养皿中,在立体显微镜下使用眼科剪使附睾内精子充分游离,孵育5 min,制成精子悬液。接着,取4 μL精子悬液滴入微孔板中,用计算机辅助精子分析系统分析精子密度、精子活动力(快速前向运动、慢速前向运动、非前向运动、极慢或不动精子)及精子运动参数:曲线速度(VCL)、直线速度(VSL)、平均速度(VAP),线性指数(LIN)、直线指数(STR)、振动指数(WOB)。
1.3.4 血浆及生精组织氧化水平检测取右心室血,在4 ℃、2 000 r/min离心8 min分离血浆检测。取适量睾丸组织冰上匀浆后即在4 ℃、12 000×g离心5 min,移取上清液,BCA法测蛋白浓度后进行检测。血浆及睾丸组织均按试剂盒操作说明进行T-AOC和NO检测。 1.4 统计学分析
采用SPSS 13.0软件分析,数据以x±s表示,用独立样本t检验进行2组间均数比较。
2 结果 2.1 尾气暴露环境的安全稳定性评估通过对自制尾气持续暴露装置内成分检测发现,从暴露开始到暴露结束装置内氧含量、二氧化硫含量、PM2.5含量恒定。安全性评价发现,在持续3次尾气暴露后,暴露组小鼠进行血气分析发现均未发生缺氧,与对照组比较差异无统计学意义(P>0.05,表 1、2)。
| (n=10, x±s) | |||
| 时间点 | 氧 (%) | 二氧化硫 (μg/m3) | PM2.5 (μg/m3) |
| 暴露开始 | 20.43±0.01 | 372.00±31.00 | 789.20±20.68 |
| 暴露结束 | 20.42±0.02 | 358.86±15.98 | 777.20±14.60 |
| 参见《中华人民共和国环境空气质量标准GB3095-2012》环境空气污染二级值:二氧化硫含量大于每小时平均500 μg/m3,PM2.5含量大于每24小时300 μg/m3。 | |||
| (n=10, x±s) | |||
| 组别 | PO2(kPa) | PCO2(kPa) | pH |
| 对照组 | 12.71±0.48 | 5.31±0.07 | 7.35±0.02 |
| 暴露组 | 12.49±0.33 | 5.35±0.08 | 7.34±0.03 |
尾气持续暴露40 d后,暴露组与对照组的体质量、睾丸脏器系数、附睾脏器系数比较,差异无统计学意义(P>0.05,表 3)。
| (n=10, x±s) | |||
| 组别 | 体质量(g) | 睾丸脏器 系数(‰) | 附睾脏器 系数(‰) |
| 对照组 | 27.30±1.37 | 7.45±0.43 | 2.64±0.18 |
| 暴露组 | 26.43±0.99 | 7.26±0.26 | 2.61±0.21 |
病理观察显示:尾气持续暴露后,对照组睾丸组织内生精细胞排列紧密、整齐,暴露组睾丸组织生精细胞排列稀疏且生精层明显减少,同时出现空泡样改变,管腔内精子减少(图 1)。尾气持续暴露后发现,与对照组相比,暴露组的精子数量及活力参数明显下降(P<0.05,P<0.01,表 4)。
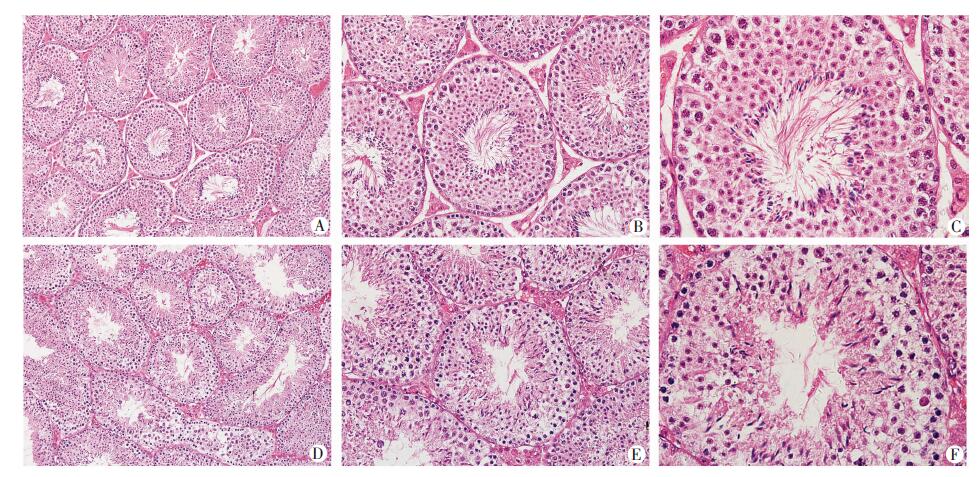 |
| A~C:分别为对照组放大100、200、400倍;D~F:分别为暴露组放大100、200、400倍图 1 HE染色观察2组小鼠的睾丸组织病理学改变 |
| (n=10, x±s) | ||
| 参数 | 对照组 | 暴露组 |
| 精子密度(×106) | 91.03±18.36 | 66.11±14.25b |
| 快速前向运动(a级,%) | 22.78±1.51 | 16.95±1.66b |
| 慢速前向运动(b级,%) | 31.27±1.90 | 23.22±2.84b |
| 非前向运动(c级,%) | 26.91±1.90 | 29.88±2.79a |
| 极慢或不动(d级,%) | 19.04±4.07 | 29.94±3.66b |
| 曲线速度(VCL,μm/s) | 40.67±5.04 | 28.50±3.95b |
| 直线速度(VSL,μm/s) | 13.22±1.42 | 7.71±0.78b |
| 平均速度(VAP,μm/s) | 16.05±1.96 | 13.68±1.96a |
| 线性指数(LIN,%) | 32.90±5.04 | 27.70±6.05 |
| 直线指数(STR,%) | 71.39±14.80 | 57.53±11.80a |
| 振动指数(WOB,%) | 42.17±3.93 | 40.42±5.60 |
| a:P<0.05,b:P<0.01,与对照组比较 | ||
尾气持续暴露后,与对照组比较,暴露组的血浆及生精组织T-AOC水平明显下降,血浆及生精组织NO水平明显升高(P<0.05,P<0.01,表 5)。
| (n=10, x±s) | ||||
| 组别 | 血浆T-AOC (mmol/L) | 睾丸T-AOC (mmol/g) | 血浆NO (μmol/L) | 睾丸NO (μmol/g) |
| 对照组 | 0.41±0.16 | 1.05±0.12 | 1.15±0.17 | 2.97±0.35 |
| 暴露组 | 0.26±0.09a | 0.76±0.11b | 1.33±0.12a | 5.25±0.34b |
| a:P<0.05,b:P<0.01,与对照组比较 | ||||
近年人口学研究发现,男性精子质量的下降严重影响了人类生育的质量[7]。流行病学调查研究发现环境的污染特别是空气质量的污染与男性精子的质量密切相关[8],但其具体机制未能诠释。国内外相关机制研究发现,汽车尾气中的有害物质严重影响了动物模型的生育。既往通过现场暴露[9]﹑尾气吸入暴露[10]﹑尾气成分染毒[11]构建的模型,缺乏对尾气暴露条件的安全稳定性、尾气成分复杂性以及自然人生存的尾气污染环境真实性的模拟。本研究严格应用大气污染的环境评估指标,全程实施安全稳定监测,具体采用相对密闭的实验空间、搅拌气流、持续多点位监测,保证了稳定的高浓度尾气环境。每次暴露开始到暴露结束装置内氧含量、二氧化硫含量、PM2.5含量基本符合自然人生存的尾气导致的空气污染的恒定水平环境,且暴露前后未发生改变。通过借鉴药理学Up and Down法测定合理通气时间和尾气与空气的合理比例,并对暴露组和对照组进行血气分析显示小鼠未处于缺氧状态,排除缺氧性损伤的影响,提供了安全稳定的实验条件。
对持续尾气暴露40 d的小鼠生精功能的评估发现,暴露组体质量、睾丸和附睾的脏器系数与对照组比较,差异无统计学意义(P>0.05)。分析原因可能与尾气暴露的时长相关,在此暴露时间内睾丸附睾形态上没有明显的损伤表现,而在睾丸组织病理方面,生精组织存在明显损伤性变化。主要表现为睾丸组织生精细胞排列稀疏且生精层明显减少、空泡样改变、管腔内精子减少,这与国内有关研究结果一致[12, 13]。对精子数量和质量的评价发现,持续的尾气暴露后精子数量和活力下降。以上的研究结果证实本实验模拟尾气持续暴露的方案是在组织和细胞层面发生,进而发挥影响小鼠生精功能的作用。
已有的睾丸生精功能损伤的研究,通过尾气暴露模型发现其机制包括基因、分子、组织三个水平,涉及氧化组织损伤、内分泌功能紊乱、精子发育异常等[14]。研究还发现,NO水平的升高,总抗氧化能力下降后会造成氧化损伤,从而影响生育力[15]。本研究对暴露组及对照组小鼠血浆和生精组织中的氧化水平检测发现,暴露组血浆及生精组织中的抗氧化T-AOC水平明显下降,同时氧化物质NO水平明显升高,提示在汽车尾气持续短期暴露状态下,模型鼠中氧化应激能力存在明显变化;持续尾气的短期暴露对组织和细胞的水平的改变与氧化水平的改变的一致性,可能提示氧化水平与生精功能下调存在相关性[16]。
既往研究表明,NO是从L-精氨酸氧化生成L-瓜氨酸的一种氧自由基,NO的合成是由一氧化氮合酶(NOS)的合成量决定[17]。NO在生精功能中起到双重作用。在生理条件下,NO对精子生成和精子活动力都起着至关重要的作用。低浓度的NO增加精子活动力[18],而高浓度的NO对精子活动力起着抑制作用[19]。本研究对氧化应激对生精功能的机制进行了初步探讨。通过本研究结果可以进一步实验探讨NO与NOS之间的相关通路是否对生精功能产生影响。在众多通路中,与NO相关的P38MAPK信号通路参与了生殖细胞的许多发育阶段,包括精子发生、生殖细胞周期、生殖细胞凋亡[20],这为汽车尾气暴露损伤生精功能的机制研究提供重要线索。
本研究制作了模拟尾气污染条件下尾气暴露对生精功能损伤的模型,完善了从模拟尾气污染环境到生精功能损伤评价指标和方法。本研究对在此建模条件下造成的生精功能损伤的评估尚属初步的探讨,仍有待深入的实验研究,如不同浓度、不同时间的尾气持续性暴露对生精功能损伤的系统性评估指标的建立,以及损伤类型和程度的确定等问题。
| [1] | Hammoud A, Carrell D T, Gibson M, et al. Decreased sperm motility is associated with air pollution in Salt Lake City. Fertil Steril, 2010, 93(6): 1875-1879. |
| [2] | 徐菲菲, 马大骅, 丁之德. 空气污染物对哺乳动物生殖和胚胎发育的影响. 国际生殖健康/计划生育杂志, 2015, 34(3): 229-233, 247. |
| [3] | 董建云, 王治, 董小梅, 等. 1, 2, 3, 4-二环氧丁烷对雄性小鼠生殖细胞损伤的研究. 第三军医大学学报, 2015, 37(9): 881-885. |
| [4] | Li X, Li H, Jia L, et al. Oestrogen action and male fertility: experimental and clinical finding. Cell Mol Life Sci, 2015, 72(20): 3915-3930. |
| [5] | 汤召兵, 苟欣, 王明, 等. 美洛昔康对铝过负荷致雄鼠生殖损害的保护作用. 第三军医大学学报, 2011, 33(13): 1362-1365. |
| [6] | 张方舟, 王益, 颜文君, 等. 上下法与传统急性毒性法测定薄荷油LD50的试验研究. 河南科技大学学报: 医学版, 2012, 30(4): 268-270. |
| [7] | Sharma R, Biedenharn K R, Fedor J M, et al. Lifestyle factors and reproductive health: taking control of your fertility. Reprod Biol Endocrinol, 2013, 11: 66. |
| [8] | Fathi-Najafi T, Latifnejad-Roudsari R, Namvar F, et al. Air pollution and quality of sperm: a meta-analysis. Iran Red Crescent Med J, 2015, 17(4): e26930. |
| [9] | 孙娜, 郑铃, 王征桦, 等. 大气交通污染物对雄性小鼠生殖系统影响. 中国公共卫生, 2010, 26(8): 1045-1047. |
| [10] | Huang J Y, Liao J W, Liu Y C, et al. Motorcycle exhaust induces reproductive toxicity and testicular interleukin-6 in male rats. Toxicol Sci, 2008, 103(1): 137-148. |
| [11] | Kisin E R, Yanamala N, Farcas M T, et al. Abnormalities in the male reproductive system after exposure to diesel and biodiesel blend. Environ Mol Mutagen, 2015, 56(2): 265-276. |
| [12] | 王征桦, 郑铃, 孙娜, 等.城市地面交通现场暴露对雄性小鼠的生殖毒性. 环境与职业医学, 2012, 29(10): 632-634, 637. |
| [13] | 陈秋生, 洪新如, 宋岩峰, 等. 柴油机尾气颗粒物对小鼠精子质量的影响. 中华男科学杂志, 2009, 23(3): 22-25. |
| [14] | 王忠尧, 唐爱发, 蔡志明. 汽车尾气对男性生殖功能的影响. 中华男科学杂志, 2009, 23(4): 66-68, 72. |
| [15] | Yousefniapasha Y, Jorsaraei G, Gholinezhadchari M, et al. Nitric oxide levels and total antioxidant capacity in the seminal plasma of infertile smoking men. Cell J, 2015, 17(1): 129-136. |
| [16] | 刘冰, 马栋, 毛鹏飞, 等. 氧化应激损伤在男性不育症中的影响. 中华男科学杂志, 2014, 20(10): 927-931. |
| [17] | Balercia G, Moretti S, Vignini A, et al. Role of nitric oxide concentrations on human sperm motility. J Androl, 2004, 25(2): 245-249. |
| [18] | Herrero M B, de-Lamirande E, Gagnon C. Tyrosine nitration in human spermatozoa: a physiological function of peroxynitrite, the reaction product of nitric oxide and superoxide. Mol Hum Reprod, 2001, 7(10): 913-921. |
| [19] | Badade Z G, More K M, Narshetty J G, et al. Human seminal oxidative stress: correlation with antioxidants and sperm quality parameters. Ann Biol Res, 2011, 2(5): 351-359. |
| [20] | Almog T, Naor Z. Mitogen activated protein kinases (MAPKs) as regulators of spermatogenesis and spermatozoa functions. Mol Cell Endocrinol, 2008, 28(1/2): 39-44. |



