2. 400014 重庆,儿童发育疾病研究教育部重点实验室 ;
3. 400014 重庆,儿科学重庆市重点实验室 ;
4. 400014 重庆,重庆市儿童发育重大疾病诊治与预防国际科技合作基地
2. Key Laboratory of Child Development and Disorders of Ministry of Education, Chongqing, 400014, China ;
3. Chongqing Key laboratory of Pediatrics, Chongqing, 400014, China ;
4. Chongqing International Science and Technology Cooperation Center for Child Development and Disorders, Chongqing Medical University, Chongqing, 400014, China
原发性膀胱输尿管反流(vesicoureteral reflux,VUR)是一种常见的先天性尿路异常,其导致尿液从膀胱反流至输尿管以及肾脏,是尿路感染(urinary tract infection,UTI)、肾脏瘢痕的高危因素。目前对VUR的处理措施有众多争议[1-4],但保护肾脏功能,防止进展为肾盂肾炎仍是其治疗的主要目标。
婴儿不同等级的膀胱输尿管反流和儿童轻中度反流很早便采用了预防性抗菌药物[5]。但有试验表明抗生素的使用对于膀胱输尿管反流,尤其是低等级的反流并无益处,另外一些研究[6-9]表明抗生素能够防止肾脏进一步的损害,然而大部分实验设计并不完善,其研究的局限性限制了研究结论的临床应用[10-11]。近年来,国内外的专业机构及部门针对预防性使用抗生素对于保护儿童肾脏、预防肾脏瘢痕及新发肾盂肾炎是否有效建立了多组随机对照模型[6-9, 12-15]。但不同等级的原发性输尿管反流患儿如何选择CAP仍然缺乏对应的系统性分析和评价。
本研究通过检索预防性使用抗生素治疗VUR的相关RCT文献,整理数据后进行Meta分析,对预防性使用抗生素治疗VUR的疗效性进行系统性的评价,为VUR的防治提供循证学证据,希望为临床工作提供依据。
1 资料与方法 1.1 纳入标准纳入同时满足下列所有标准的文献:① 研究对象为确诊为原发性膀胱输尿管反流的患儿,每天服用抗生 素,持续时间至少2个月,有比较预防性使用抗生素以及安慰剂/不治疗预防复发性尿路感染等方面疗效;② 随机对照试验(RCT),准随机对照试验,随机双盲法,发表形式及语种均不受限制;③ 干预方式为预防性使用抗生素,但不在给药方式、给药剂量以及用药疗程等方面予以区分,对照组给予安慰剂或支持治疗;④ 各试验组均未使用会影响本研究结局指标的任何干扰措施。
1.2 排除标准排除符合以下任意一条标准的研究:① 术前预防性应用抗生素的患者;② 非随机对照试验(病例对照试验、历史性对照试验甚至未设置对照的);③ 随机化方法使用不正确;④ 无此次Meta分析制定出需予以观察的主要、次要结局指标的。
1.3 文献检索策略本研究主要通过检索电子期刊全文数据库以获得相关原始文献,包括Cochrane图书馆临床对照试验数据库、PubMed、EMBASE、Ovid、Springer,以及中国期刊全文数据库、维普中文科技期刊数据库、万方数据库和中国生物医学文献光盘数据库等,检索2014年1月前 发表的相关随机对照试验。英语数据库检索词:Vesico-Ureteral Reflux,Vesico Ureteral Reflux,VesicoureteralReflux,VesicoureteralReflux,Antibiotic Premedication和 Antibiotic Prophylaxis。中文检索词:输尿管反流,VUR,抗生素,CAP,尿路感染,UTI。
1.4 文献质量评价方法 1.4.1 纳入和排除文献筛选、资料提取与质量评价由两人按照纳入和排除标准独立完成文献筛选、资料提取和文献质量评价,如遇分歧则由第三方决定,若数据缺失则联系原始研究作者获得。
1.4.2 资料提取① 一般信息;② 纳入研究对象的一般情况;③ 干预措施;④ 需要予以观察的主要、次要结局指标。
1.4.3 临床试验质量评价本研究评价纳入RCT所用到的是Cochrane协作网推荐的国际Jadad记分法,且为两名评价者各自独立完成,当两名评价者存在有意见不一致时,可以商讨或咨询第3人予以解决。具体评价方法如下:① 选择偏倚(如何实施分配隐藏);② 实施偏倚(如何对干预方法的实施者采取盲法);③ 失访偏倚(如何减少随机化后的排除或失访);④ 测量偏倚(如何实施对结局评价的盲法)。评价为A级的需同时达到以上所列四条标准要求,表明该研究存在各种偏倚可能性是最低;评价为B级的仅在上述四条标准中的任何一条或多条只为部分满足(或文献未提及),则此试验存在偏倚的可能性为中等;评价为C级的是在上述4条标准中任意一条或者多条完全不满足,则存在偏倚的可能性最大。
1.5 统计学方法采用RevMan 5.1软件完成此次Meta分析。首先采用χ2检验进行异质性检验,显著水平设定为α=0.10,当P≥0. 10,I2<50%,各项研究间具有统计学方面的同质性,可以采用固定效应模型进行分析;当P<0.10,I2>50%,各项研究间具有统计学方面的异质性,则需分析其异质性产生的来源,若不能用临床异质性和方法学异质性等来解释说明时,则需采用随机效应模型进行分析。若遇到Meta分析无法进行的部分,则可以采用描述性分析的方法。采用Stata进行Bgger检验、egger检验进行发表偏倚的分析。计数资料用危险比/率比(RR)及其95%CI表示,计量资料用加权均数差(WMD)及其95%CI表示。
2 结果 2.1 筛选结果截至2015年5月,初步检索总共获得相关文献82篇,阅读文题及其提要之后8篇文献被进一步选入,通过进一步仔细阅读全文、分析其研究方法,按照制定的纳入及排除标准,最后确定了8项 随机对照试验被纳入。8项RCT中共纳入预防性抗生素组828例,对照组811例被纳入。
2.2 纳入文献质量评价8项研究均为随机对照试验,并具体描述了随机化方法,均采取双盲法,均采取分配隐藏的方案,并对于失访及退出说明原因及合理解释。8项RCT都描述了预防性使用抗生素组和对照组纳入对象的一些相关基本信息情况,其基本信息情况间差异无统计学意义,具有可比性;且8篇文献质量均评价为A级(表 1)。
| 文献 | n | 干预方式(例) | 结局指标 | 质量评价(分) | |||||
| 治疗组 | 对照组 | 随机序列的产生 | 随机化隐藏 | 盲法 | 退出与失访 | 评价 | |||
| Hari P12015[6] | 93 | 47 | 46 | 尿路感染发生率 | 2 | 2 | 2 | 1 | 7 |
| RIVUR Trial Investigators2014[7] | 602 | 301 | 301 | 尿路感染发生率,肾脏瘢痕 | 2 | 2 | 2 | 1 | 7 |
| Brandstrm P12011[13] | 137 | 69 | 68 | 尿路感染发生率,肾脏瘢痕 | 2 | 2 | 1 | 1 | 6 |
| Craig JC12009[8] | 243 | 122 | 121 | 尿路感染发生率 | 2 | 2 | 2 | 1 | 7 |
| Montini G12008[12] | 128 | 82 | 46 | 尿路感染发生率,肾脏瘢痕 | 2 | 2 | 1 | 1 | 6 |
| Pennesi M12008[9] | 100 | 50 | 50 | 尿路感染发生率 | 2 | 2 | 1 | 1 | 6 |
| Roussey-Kesler G12008[14] | 223 | 102 | 121 | 尿路感染发生率 | 2 | 2 | 2 | 1 | 6 |
| Garin EH12006[15] | 113 | 55 | 58 | 尿路感染发生率 | 2 | 2 | 1 | 1 | 6 |
2.3 Meta分析结果 2.3.1 两组复发尿路感染发生率比较
对所有纳入的8项RCT数据整合,患者总人数为1 639例,8项RCT都有关于预防性使用抗生素组与对照组复发性尿路感染的报道,各项研究间的同质性较好,可以采用固定效应模型进行分析。在服用抗生素一组,复发性尿路感染或者肾盂肾炎的风险是13.94%(115 ∶825),在对照组,复发性尿路感染或者肾盂肾炎的风险是19.96%(162 ∶811)。通过Meta分析结果显示,RR= 0.69,95%CI:0.56~0.86,P<0.05,此结果提示使用预防性使用抗生素可降低复发性尿路感染率(图 1)。

|
| 图 1 CAP组与对照组患儿UTI/肾盂肾炎复发率的对比 |
我们发现,纳入Hari等[6]以及2005年Garin等[15]这两篇文献的系统评价中,整体I2=67%,RR=0.69[0.56,0.86] P<0.05,异质性较大,而排除两篇 文献进一步分析后得出I2=45%,同质性较好,且RR= 0.60[0.48,0.76],P<0.05。进一步分析后考虑相对其他6篇文章,该两篇文章中选取患儿年龄跨度过大(前者1~12岁,后者1~18岁),试验过程中抗生素的更换及复合使用都有可能是产生偏倚的原因。而对于入选Meta分析的研究分析,根据漏斗图以及Stata 13.0进行的Bgger检验得Pr>|z|=0.266,egger检验中Pr>|z|=0.066,考虑可能不存在发表偏倚。
2.3.2 两组不同程度的输尿管反流复发尿路感染发生率比较亚组分析在GradeⅠ~Ⅱ的患儿中,异质性检验各项研究间的同质性较好,进行Bgger检验得Pr>|z|=1.000,egger检验中Pr>|z|=0.164,考虑可能不存在发表偏倚,可以采用固定效应模型进行分析。抗生素组中复发性尿路感染或者肾盂肾炎的风险是6.87%(28 ∶407);对照组中复发性尿路感染或者肾盂肾炎的风险是12.5%(51 ∶408)。通过Meta分析结果显示,RR=0.57,95%CI:0.37~0.87,P<0.05,此结果提示对于Ⅰ~Ⅱ级反流的患儿,使用预防性使用抗生素可降低复发性尿路感染率(图 3)。
在Grade Ⅲ~Ⅳ的患儿中,异质性检验各项研究间的同质性较好,进行Bgger检验得Pr>|z|=0.536,egger检验中Pr>|z|=0.245,考虑可能不存在发表偏 倚,可以采用固定效应模型进行分析。抗生素组中复发性尿路感染或者肾盂肾炎的风险为20.67%(87 ∶421); 对照组中复发性尿路感染或者肾盂肾炎的风险是27.54%(111 ∶403)。通过Meta分析结果显示,RR=0.76,95%CI:0.59~0.96,P<0.05,此结果提示对于Ⅲ~Ⅳ级的输尿管反流,预防性使用抗生素可降低复发性尿路感染率(图 2)。

|
| 图 2 不同等级的输尿管反流在CAP组与对照组中UTI/肾盂肾炎的复发率比较 |
2.3.3 不同干预下的原发性输尿管反流新肾脏瘢痕发生率比较亚组分析
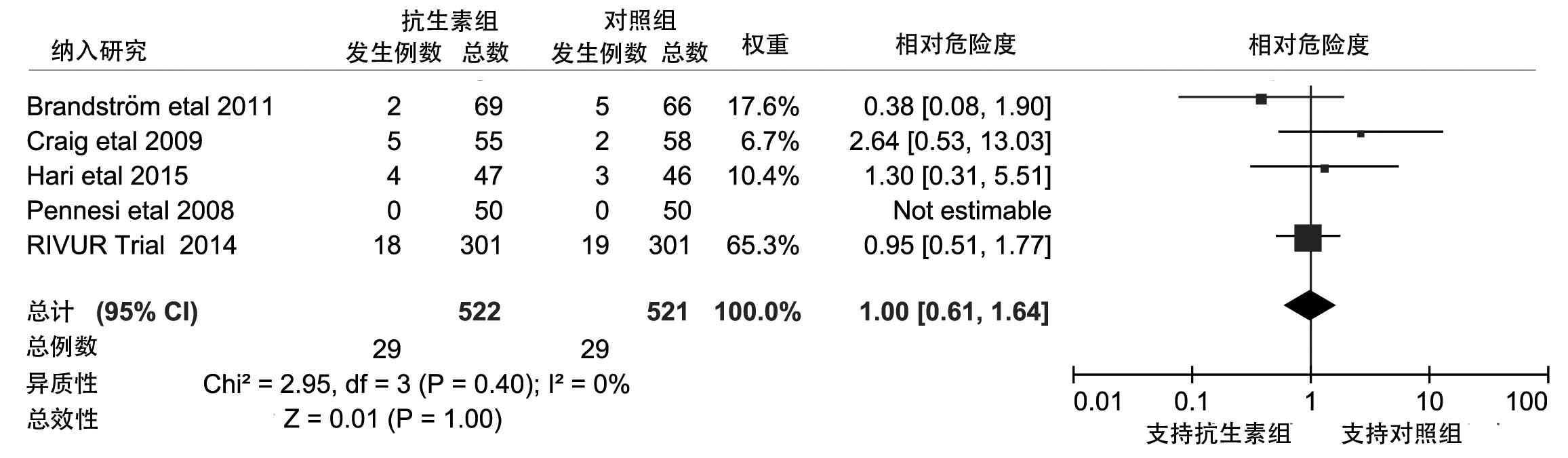
在原发性输尿管反流的患儿中,7篇RCT均进行了99m锝-DMSA(Dimerca-pto-Succinic二巯基丁二酸)的检查,以观察肾脏损伤的情况。其中5篇对于不同干预因素下UVR和UVR患者人数进行了详细叙述,异质性检验P>0.05,I2=0%,各项研究间的同质性较好,进行Bgger检验得Pr>|z|= 0.308,egger检验中Pr>|z|=0.613,考虑可能不存在发表偏倚,可以采用固定效应模型进行分析。抗生素组中新瘢痕的风险是5.56%(29 ∶522);对照组中新瘢痕出现的风险是5.57%(29 ∶521)。通过Meta分析结果显示,RR=1,95%CI:0.61~1.64,P>0.05,此结果提示对于原发性输尿管反流的患儿,使用预防性使用抗生素对肾脏瘢痕出现的影响无意义(图 3)。
|
| 图 3 预防性抗生素组与对照组患儿肾脏新瘢痕出现率的比较 |
3 讨论
尿路感染的防治是困扰VUR治疗的一个重要因素[16],尽管CAP对于VUR防治的有效性仍缺乏高质量的证据支持,但预防性抗生素的使用早已被临床广泛应用[17]。欧洲泌尿外科协会(European Association of Urology,EAU)最新的指南指出[18],预防性抗生素的使用等保守治疗就是为了防止发热性尿路感染,尿路感染一旦被控制,也就不会对肾脏继续造成伤害。为了验证预防性使用抗生素的有效性,出现了大批试验设计,但最初实验设计并不完善,其中大部分是非随机对照实验,少部分的随机对照实验得出的结论也引起了很大争议。因此,目前无论是对于抗生素是否有效,还是对于哪种 程度的输尿管反流有效,不同学者持有不同的观点[10, 15, 19]。
欧洲泌尿外科学会认为纵然有很多学者怀疑CAP的有效性,尤其是对于Ⅰ~Ⅱ级的原发性膀胱输尿管反流,面对很多验证CAP对Ⅲ~Ⅳ反流的有效性实验,临床医师所能做的就是选择合适的反流患儿使用抗生素。
回顾性分析所检索到的所有关于预防性抗生素使用的RCT,最早的是2006年Garin等[15]的研究。VUR患儿被随机分配,接受或不接受抗生素预防,每3个月监测1次,一直持续1年,监测指标包括尿常规、肾脏超声扫描和排泄性尿路造影。研究结果发现,VUR的反流程度对复发性尿路感染率、肾盂肾炎的发生率差异无统计学意义。整个研究设计存在诸多不足之处:① 从其年龄分布来讲,Garin 整个试验中的患儿年龄跨度较大,相对2008 Roussey-Kesler等[14]选择的1个月到3岁的患儿,后者年龄更集中,不同年龄段肾脏、输尿管发育情况所带来的偏差可能就更小。② 纳入的标准也并 非严格按照原发性输尿管反流的诊断,大量不存在反流患儿的纳入为后期分析增加了难度。③ 其中对于抗生素使用的更换也可能导致结果的分析需要更全面评估。
Pennesi等[9]及Montini等[12]2008年所报道的研究仍然存在这几个问题,缺乏安慰剂对照、纳入的患者筛选到最后比例过少,期间也使用了复方新诺明、复合阿莫西林克拉维酸或多种抗生素同期给药。2009年的Craig[8]试验中患儿年龄跨度大,接受的药物除了复 方磺胺甲恶唑亦有甲氧苄啶等,但其不同于前面试验在于有安慰剂对照,观察指标同样为UTI,随访持续12个 月后发现在抗生素组,尿路感染的绝对风险降低了6个百分点,证实了低剂量的抗生素使用可减少易感儿童尿路感染发生率。
2011年瑞典科学家Brandstrm[13]指出,他们将年龄在1~2岁的VUR Ⅲ级或Ⅳ级的患者随机分为预防性抗生素治疗组(女性86例,男性49例),内镜下注射组或监督组,进行了长达2年的随访后发现在女孩中,预防性使用抗生素和内镜下注射能减少UTI复发率和新的肾损伤率。而治疗效果对于男孩没有并没有太大差异。
众多随机对照实验当中,样本量最大的为RIVUR[7](Randomized Intervention for Children with Vesicoureteral Reflux ),这是一个跨越了多个中心的随机对照试验,其结果指出预防性使用抗生素能减少UTI的复发率,对于肾脏瘢痕未见明显作用。同样多个中心的研究导致抗生素的服用具有不确定性,并且样本量中的男女比例严重失衡,对于亚组的分析影响不可忽视。de-Bessa等[20]在对前面RCTs总结分析中也提出类似的评估。
本文纳入的文章当中,最新的是Hari等[6]的研究。该机构以UTI和肾脏瘢痕为监测指标,对一批 1~12岁的患儿进行了预防性使用抗生素与安慰剂的随机对照实验,发现对于Ⅰ~Ⅳ级的原发性输尿管反流,预防性使用抗生素会增加复发性UTI的风险。我们发现,纳入Hari等[6]以及2005年Garin等[15]这两篇文献的系统评价中,整体I2=67%,RR=0.69(0.56,0.86),P<0.05,而排除两篇文献进一步分析后得出I2=45%,同质性较好,且RR=0.60(0.48,0.76) ,P<0.05。进一步分析考虑相对其他6篇文章,该两篇文章中选取患儿年龄跨度过大(前者1~12岁,后者1~18岁),试验过程中抗生素的更换及复合使用都有可能是产生偏倚的原因。而对于入选Meta分析的研究分析,根据漏斗图以及数据的Bgger检验和egger检验的结果,考虑可能不存在发表偏倚。
虽然此次研究中纳入的随机对照试验患儿普遍年龄跨度较大、大部分RCT对照组为单纯的空白对照,缺乏安慰剂对照、试验组抗生素并不单一,但结合以上的研究结果,我们分析得出对于原发性输尿管反流的患儿,无论反流等级,预防性使用抗生素对于预防复发性UTI是有效的。
抗生素使用对肾脏瘢痕发生发展的影响也是争论的热点,从无症状到肾脏瘢痕形成和严重的肾实质疾病、终末期疾病,如何有效介入很重要[21],大部分学者仍支持CAP对肾脏瘢痕并不会带来影响,我们严格筛选了8篇文献,其中给出肾脏瘢痕相关数据的文章有7篇,7篇中分别给出UVR和非UVR瘢痕前后变化的有5篇,纳入后分析得出结果提示对于原发性输尿管反流的患儿,使用预防性使用抗生素对肾脏瘢痕出现的影响无意义。但该亚组的分析仍存在参考文献数不足等缺陷。
因此,仍需要设计更加严密的大规模多中心的随机对照试验来判断预防性使用抗生素对于减少原发性输尿管反流的患儿发热性UTI以及肾脏瘢痕作用,并对其临床使用的疗效进一步明确。本文纳入的RCT中出现耐药性尿路感染的复发也让我们不得不警惕抗生素使用带来的副作用,从而更好指导临床工作。
| [1] | Fanos V, Cataldi L. Antibiotics or surgery for vesicoureteric reflux in children[J]. Lancet,2004, 364 (9446) : 1720 –1722. DOI:10.1016/S0140-6736(04)17359-5 |
| [2] | Sargent M A. What is the normal prevalence of vesicoureteral reflux?[J]. Pediatr Radiol,2000, 30 (9) : 587 –593. |
| [3] | Skoog S J, Peters C A, Arant B S Jr, et al. Pediatric Vesicoureteral Reflux Guidelines Panel Summary Report: Clinical Practice Guidelines for Screening Siblings of Children With Vesicoureteral Reflux and Neonates/Infants With Prenatal Hydronephrosis[J]. J Urol,2010, 184 (3) : 1145 –1151. DOI:10.1016/j.juro.2010.05.066 |
| [4] | Pirker M E, Colhoun E, Puri P. Renal scarring in familial vesicoureteral reflux: is prevention possible?[J]. J Urol,2006, 176 (4 Pt 2) : 1842 –1846. DOI:10.1016/j.juro.2006.04.089 |
| [5] | Downs S M. Technical report: urinary tract infections in febrile infants and young children. The Urinary Tract Subcommittee of the American Academy of Pediatrics Committee on Quality Improvement[J]. Pediatrics,1999, 103 (4) : e54 . |
| [6] | Hari P, Hari S, Sinha A, et al. Antibiotic prophylaxis in the management of vesicoureteric reflux: a randomized double-blind placebo-controlled trial[J]. Pediatr Nephrol,2015, 30 (3) : 479 –486. DOI:10.1007/s00467-014-2943-z |
| [7] | Hoberman A, Chesney R W, RIVUR Trial Investigators. Antimicrobial prophylaxis for children with vesicoureteral reflux[J]. N Engl J Med,2014, 371 (11) : 1072 –1073. DOI:10.1056/NEJMc1408559 |
| [8] | Craig J C, Simpson J M, Williams G J, et al. Antibiotic prophylaxis and recurrent urinary tract infection in children[J]. N Engl J Med,2009, 361 (18) : 1748 –1759. DOI:10.1056/NEJMoa0902295 |
| [9] | Pennesi M, Travan L, Peratoner L, et al. Is antibiotic prophylaxis in children with vesicoureteral reflux effective in preventing pyelonephritis and renal scars? A randomized, controlled trial[J]. Pediatrics,2008, 121 (6) : e1489 –e1494. DOI:10.1542/peds.2007-2652 |
| [10] | Subcommittee on Urinary Tract Infection, Steering Committee on Quality Improvement and Management, Roberts K B. Urinary tract infection: clinical practice guideline for the diagnosis and management of the initial UTI in febrile infants and children 2 to 24 months[J]. Pediatrics,2011, 128 (3) : 595 –610. DOI:10.1542/peds.2011-1330 |
| [11] | Mattoo T K. Evidence for and against urinary prophylaxis in vesicoureteral reflux[J]. Pediatr Nephrol,2010, 25 (12) : 2379 –2382. DOI:10.1007/s00467-010-1632-9 |
| [12] | Montini G, Rigon L, Zucchetta P, et al. Prophylaxis after first febrile urinary tract infection in children? A multicenter, randomized, controlled, noninferiority trial[J]. Pediatrics,2008, 122 (5) : 1064 –1071. DOI:10.1542/peds.2007-3770 |
| [13] | Brandstrm P, Esbjrner E, Herthelius M, et al. The Swedish reflux trial in children: III. Urinary tract infection pattern[J]. J Urol,2010, 184 (1) : 286 –291. DOI:10.1016/j.juro.2010.01.061 |
| [14] | Roussey-Kesler G, Gadjos V, Idres N, et al. Antibiotic prophylaxis for the prevention of recurrent urinary tract infection in children with low grade vesicoureteral reflux: results from a prospective randomized study[J]. J Urol,2008, 179 (2) : 674 –679. DOI:10.1016/j.juro.2007.09.090 |
| [15] | Garin E H, Olavarria F, Garcia-Nieto V, et al. Clinical significance of primary vesicoureteral reflux and urinary antibiotic prophylaxis after acute pyelonephritis: a multicenter, randomized, controlled study[J]. Pediatrics,2006, 117 (3) : 626 –632. DOI:10.1542/peds.2005-1362 |
| [16] | Hannula A, Venhola M, Perhomaa M, et al. Imaging the urinary tract in children with urinary tract infection[J]. Acta Paediatr,2011, 100 (12) : e253 –e259. DOI:10.1111/j.1651-2227.2011.02391.x |
| [17] | Elder J S, Peters C A, Arant B S Jr, et al. Pediatric Vesicoureteral Reflux Guidelines Panel summary report on the management of primary vesicoureteral reflux in children[J]. J Urol,1997, 157 (5) : 1846 –1851. |
| [18] | Springer A, Subramaniam R. Re: Serdar Tekgul, Hubertus Riedmiller, Piet Hoebeke, et al. EAU guidelines on vesicoureteral reflux in children. Eur Urol 2012;62;534-42[J]. Eur Urol,2012, 62 (6) : e101 . DOI:10.1016/j.eururo.2012.08.021 |
| [19] | Wan J, Skoog S J, Hulbert W C, et al. Section on Urology response to new Guidelines for the diagnosis and management of UTI[J]. Pediatrics,2012, 129 (4) : e1051 –e1053. DOI:10.1542/peds.2011-3615 |
| [20] | de-Bessa J Jr, de-Carvalho-Mrad F C, Mendes E F, et al. Antibiotic prophylaxis for prevention of febrile urinary tract infections in children with vesicoureteral reflux: a meta-analysis of randomized, controlled trials comparing dilated to nondilated vesicoureteral reflux[J]. J Urol,2015, 193 (5 Suppl) : 1772 –1777. DOI:10.1016/j.juro.2014.10.092 |



