2. 400016 重庆,重庆医科大学附属第一医院:重庆市分子肿瘤及表观遗传学重点实验室;
3. 400016 重庆,重庆医科大学附属第一医院:核医学&肿瘤学实验室
2. Chongqing Key Laboratory of Molecular Oncology and Epigenetics,the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China;
3. Laboratory Radiology & Oncology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China
目前肺腺癌已替代鳞癌成为最普遍的非小细胞肺癌(NSCLC)类型,以铂类为主的联合辅助化疗方案仍然是局部晚期NSCLC的标准治疗策略,但由于原发或继发耐药以及多药耐药的出现使仅有不到50%的NSCLC患者能够从一线化疗方案中获益,其绝对5年生存率仅为5.3%[1, 2]。
ABCG2又称乳腺癌耐药蛋白(BCRP),是ATP依赖的多药耐药蛋白家族的新成员,具有药物外排泵的作用,能介导肿瘤细胞对多种化疗药物的抵抗[3]。研究发现在NSCLC患者及相应细胞系中ABCG2的高表达状态与SP表型和化疗耐药有关,且在一定程度上影响患者的预后,高表达ABCG2的患者对一线铂类化疗方案反应率低,总生存期(OS)和无进展生存期(PFS)均缩短[4]。因此特异性的靶向ABCG2,下调其表达有望逆转其介导的多药耐药。本研究拟通过噬菌体展示肽库技术构建全人源肺腺癌噬菌体单链抗体库,以A549细胞和ABCG2抗原联合筛选出ABCG2特异性肺腺癌单链抗体,最终实现靶向ABCG2+肺癌干样细胞和化疗增敏作用。
1 材料与方法 1.1 材料 1.1.1 组织标本10例肺腺癌患者癌旁淋巴结来 源于重庆医科大学附属第一医院胸心外科2014年3-7月的手术患者,均知情同意,病检证实为癌转移淋巴结。
1.1.2 噬菌体展示系统、细胞株及其他试剂噬菌粒载体pCANTAB5E、菌株TG1、HB2151、辅助噬菌体M13KO7均为本实验室保存。限制性内切酶 SfiⅠ和NotⅠ 购自NEB公司;逆转录试剂盒为大连宝生物 (TaKaRa)公司产品;TRIzol试剂为Invitrogen公司产品;PCR相关试剂为Promega公司产品;质粒提取试剂盒、DNA琼脂糖凝胶回收试剂盒购自天根公司;人肺癌细胞系A549,正常支气管上皮细胞HBE16,鼻咽癌细胞系CNE2和乳腺癌细胞系MDA-MB231均由本实验室保存。HRP标记的抗M13单抗、兔抗E-tag多抗、 鼠抗ABCG2单抗和ABCG2纯化抗原分别购自Abcam公司和Abnova公司;HRP-羊抗兔及羊抗鼠二抗购自Cell Signaling Technology公司;胰蛋白酶、胎牛血清、PRMI1640购自Gibco公司;其他相关试剂均为国产分析纯。
1.1.3 PCR引物设计及合成参考文献[5],引物 设计包括6条VH,5条Vκ和6条Vλ上下游序列,1条 可重叠的互补Linker序列和相应的合成scFv的上下游序列,所有PCR和SOE-PCR引物均委托华大基因公司合成。
1.2 方法 1.2.1 总RNA的提取、VH、VL基因的扩增TRIzol 法提取癌转移淋巴结总RNA,1% 琼脂糖凝胶电泳鉴定其完整性。逆转录合成cDNA,PCR扩增全部VH和VL基因片段。PCR条件:95 ℃ 5 min;94 ℃ 40 s,55 ℃ 40 s,72 ℃ 1 min,共30个循环;72 ℃ 10 min。产物经1% 琼脂糖凝胶电泳鉴定,胶回收试剂盒回收VH和VL片段。
1.2.2 ScFv基因的合成以VH和VL为模板继续PCR,分别在其上下游加上Linker序列。将等摩尔量的VH-Linker-和Linker+-VL片段经SOE-PCR拼接成scFv片段。反应条件:95 ℃ 5 min;94 ℃ 40 s,58 ℃ 40 s,72 ℃ 60 s,共5个循环;补加合成scFv的上下游各1 μL后,继续PCR,95 ℃ 5 min;94 ℃ 40 s,55 ℃ 40 s,72 ℃ 60 s,共25个循环;72 ℃ 10 min。1% 琼脂糖凝胶电泳检测并切胶回收scFv片段。
1.2.3 ScFv初级抗体库的制备ScFv片段经 SfiⅠ和NotⅠ双酶切后连接到噬菌体表达载体,连接产物电转化至感受态E.coli TG1,铺SOBAG平板,行质粒PCR和双酶切鉴定,阳性克隆进一步测序验证。转化后菌液涂SOBAG平板,2-YT培养基洗下菌苔,稀释菌液至A600约为0.3,加入辅助噬菌体M13KO7超感染1 h,离心,2-YTAK 培养基重悬菌体,振摇12 h后收集上清加入1/5体积PEG/NaCl溶液冰浴1 h,离心,2-YT培养基重悬菌体,再次离心,上清即为含scFv的初级抗体库,0.45 μm滤器过滤,4 ℃保存备用。
1.2.4 单链抗体scFv的筛选富集初级抗体库液先用正常支气管上皮细胞HBE16进行1轮负性筛选,再以人肺腺癌A549细胞进行3轮“吸附-洗脱-扩增”的全细胞筛选,最后用ABCG2抗原进行3轮固相筛选。ABCG2抗原(2 μg/mL)包被免疫管,4 ℃过夜,加入1% BSA/PBS于37 ℃孵育2 h,弃封闭液,加入经A549细胞筛选后的抗体库液继续孵育2 h,0.1% PBST洗3遍后加入500 μL洗脱液(0.1 mol/L甘氨酸-HCl,pH 2.2)充分混匀,30 μL中和液(1 mol/L Tris,pH 7.4)终止反应。洗脱下来的噬菌体加入3 mL对数生长期的TG1菌液,37 ℃慢摇2 h,添加氨苄青霉素和葡萄糖至终浓度分别为100 μg/mL 和1%,3×1010 pfu的M13KO7超感染1.5 h,离心,菌体重悬于10 mL 2YT-AK液,37 ℃振摇过夜。次日菌液离心,上清中加入1/5体积PEG/NaCl冰浴1 h,离心,2 mL 2-YT液重悬菌体,离心取上清,获得第1轮靶抗原筛选后的噬菌体抗体,共进行3轮。对每轮筛选后的抗体进行滴度测定。
1.2.5 单链抗体scFv的诱导表达及特性鉴定筛选后的抗体库液涂布SOBAG平板,随机挑取平板上的单菌落,37 ℃摇菌过夜,加入M13KO7感染,2YT-AK培养基30 ℃摇床过夜,离心,上清即为噬菌体单链抗体。ABCG2抗原(2 μg/mL)包被96孔板,以制备的单链抗体为一抗,HRP/anti-M13为二抗行ELISA检测,筛选阳性的scFv。将鉴定呈阳性的scFv感染E.coli HB2151,涂布SOBAG平板。次日挑取单克隆,加入终浓度为1 mmol/L的IPTG诱导培养,收集菌液,离心,菌体重悬于2 mL HEPES提取缓冲液,超声碎菌,离心,上清即为可溶性scFv; 菌沉淀用1×TES缓冲液重悬后加入1/5×TES缓冲液涡旋振荡,冰浴30 min,4 ℃离心,上清即含周质中的scFv,-80 ℃保存备用。
1.2.5.1 单链抗体scFv的可溶性表达及对A549细胞ABCG2蛋白表达的影响ScFv纯化后经SDS-PAGE电泳检测,同时以抗E-tag抗体为一抗(1 ∶3 000)行Western blot鉴定其表达和分子量大小。A549细胞经scFv处理48 h后,提取细胞总蛋白,以抗ABCG2抗体为一抗(1 ∶3 000)行Western blot检测ABCG2蛋白表达变化情况,ECL化学发,Fusion Fx Vilber Lourmat凝胶成像系统进行成像,Image J 软件进行图像分析、灰度值计算,本实验重复3次。
1.2.5.2 单链抗体scFv的特异性鉴定肺腺癌A549细胞、乳腺癌MDA-MB231细胞和鼻咽癌CNE2细胞分别接种于96孔板(1×104/孔),贴壁后4%多聚甲醛固定30 min,1% BSA/PBS于37 ℃封闭1 h。以纯化scFv(100 μL/孔)为一抗,HRP-anti E-tag抗体为二抗,行Elisa检测,TMB避光显色,2N H2SO4终止反应,酶标仪测450 nm波长处光密度值[D(450)];对于免疫细胞化学(ICC)法,最后以DAB避光显色20 min,倒置显微镜观察拍照。
1.2.5.3 单链抗体scFv对A549细胞的顺铂增敏作用A549细胞接种于96孔板(5×103 /孔),不同剂量的scFv(0 ~20 μg)处理48 h后,再加入不同浓度的顺铂,37 ℃ 孵箱继续培养,24 h后每孔加入10 μL CCK8试剂,37 ℃避光反应2 h,酶标仪检测450 nm处光密度值[D(450)]。GraphPad Prime 5.0分析软件计算各组的IC50 值并比较。实验重复至少3次。
1.3 统计学分析采用SPSS19.0统计软件分析,数据以x± s 表示,计量资料分析采用t检验:计数资料用χ2检验,P<0.05为差异有统计学意义。
2 结果 2.1 VH、VL和scFv片段的扩增TRIzol法提总RNA,凝胶电泳可见28 S和18 S两条带,A260/A280比值为1.98,表明RNA提取无降解且纯度较好,可用于后续实验。PCR产物VH、VL、VH-Linker-、Linker+-VL和SOE-PCR产物scFv经电泳分析,可见VH、VL、VH-Linker-及Linker+-VL大小分别为360 bp、340 bp、410 bp、390 bp,scFv在750 bp处有特异性条带,大小与预期相符(图 1)。
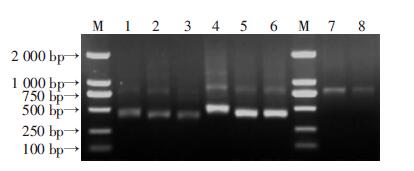 |
| M:DNA 标准;1~3:VH(360 bp)、Vκ(340 bp)和Vλ(340 bp)片段;4~6:VH-Linker-(410 bp)和Linker+-Vκ/Vλ(390 bp)片段;7~8:scFv片段(750 bp)图 1 PCR产物琼脂糖凝胶电泳分析 |
随机挑选初级抗体库的16个克隆行质粒PCR鉴定,结果均扩增出大小750 bp的片段,插入率达100% (图 2)。阳性质粒双酶切(SfiⅠ、NotⅠ)鉴定,分别得到大小为4 522 bp的pCANTAB5E载体片段和750 bp的scFv基因片段(图 3)。进一步送测序鉴定,序列比对结果与整码的scFv编码序列一致性可达99%。
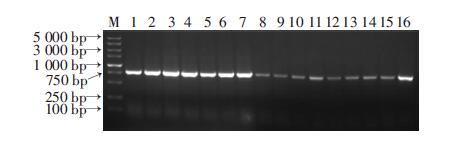 |
| M:DNA标准;1~16: 随机挑选初级抗体库16个克隆图 2 质粒PCR鉴定 |
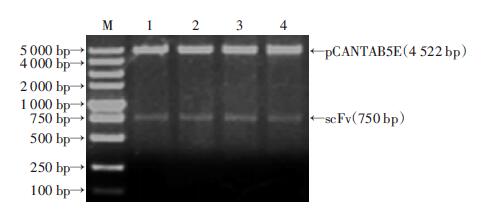 |
| M:DNA 标准;1~4:阳性质粒双酶切图 3 重组质粒双酶切鉴定 |
经过6轮筛选,抗体库效价逐轮提升,第6轮约为第1轮的110倍。ELISA检测到随机挑选的16个噬菌体抗体中有12个与ABCG2抗原呈阳性反应,阳性展示率达75%,且相对特异性与MDA-MB231(1.41)和CNE2细胞(1.28)相比,该scFv与A549细胞的结合(2.25)具有特异性(图 4)。ICC结果也表明与对照组细胞相比,A549细胞能与scFv特异性结合,DAB染色可见胞质棕色深染 (图 5)。
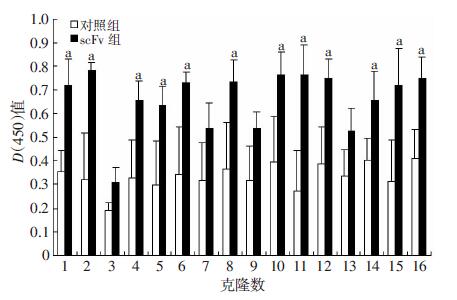 |
| a:P<0.05,与对照组相比图 4 ELISA检测单链抗体scFv的特异性 |
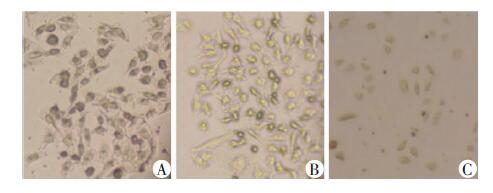 |
| A:A549细胞;B:MDA-MB231细胞;C:CNE2细胞图 5 ICC检测单链抗体scFv的特异性 (DAB染色×100) |
纯化的scFv经SDS-PAGE和Western blot鉴定,结果显示在34×103处有一条清晰的条带 (图 6)。A549细胞经scFv处理后,ABCG2蛋白表达降低(图 7),差异有统计学意义(P<0.05)。
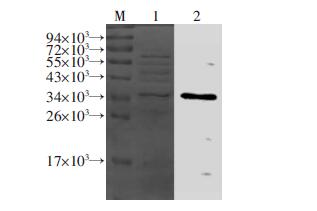 |
| M:蛋白标准;1:SDS-PAGE检测;2:Western blot检测图 6 ScFv可溶性表达鉴定 |
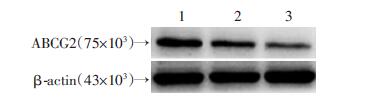 |
| 1:对照组;2:scFv 40 μg/mL处理组;3:scFv 80 μg/mL处理组图 7 单链抗体scFv对A549细胞ABCG2蛋白表达的影响 |
A549细胞经scFv处理后对顺铂的敏感性明显增加,IC50值与对照组相比显著降低(表 1),且其化疗增敏作用与剂量呈正比关系。
| scFv量(μg) | IC50值(μg/mL) | P值 |
| 0 | 5.009 ± 0.390 | 1 |
| 5 | 3.119 ± 0.565 | 0.051 1 |
| 10 | 1.779 ± 0.138 | 0.001 5 |
| 15 | 0.707 ± 0.175 | 0.000 5 |
| 20 | 0.158 ± 0.128 | 0.000 2 |
肿瘤细胞的耐药是一个多因素参与的复杂过程[6],重要机制之一是通过高表达三磷酸腺苷结合蛋白(ATP-binding cassette,ABC)药物转运体,将细胞内的药物转运到细胞外,保护肿瘤细胞免受药物的杀伤作用。Xie等[7]对结肠癌的研究发现ABCG2的过表达与化疗失败、肿瘤复发和侵袭有关。Dai等[8]研究表明通过抑制ABCG2蛋白的功能能够逆转其介导的多药耐药作用。在NSCLC患者中ABCG2高表达与铂类治疗耐药有关,并且以顺铂为基础的术后辅助化疗患者中,ABCG2阳性患者生存率明显低于阴性者[4, 9],由此推论肺癌细胞内ABCG2蛋白的表达水平是促发耐药的形成关键因素之一。此外,与ABC家族的其他成员P-gp、MRP1相比,ABCG2还在肿瘤起始细胞(TICs/CSCs)方面具有独特的功能和调节机制[3],是极具潜力的治疗靶点。
基因工程抗体已应用于临床肿瘤治疗并取得了较好的疗效[10]。而单链抗体scFv由于其分子量小、渗透快、靶部位结合力强、清除迅速、具有较好的药代动力学特征和全人源性已成为最有应用前景的重组抗体形式[11]。为保证较高的库容和后续实验的有效进行,我们课题组根据自身研究基础[12, 13],利用肺腺癌患者癌旁阳性淋巴结中存在产生IgG抗体的B淋巴细胞,以其作为构建抗体库的来源,从中扩增出单链抗体基因,构建了库容较大、特异性较好的噬菌体抗体库。
合理的筛选方法也是富集到特异性抗体、保证其高效性能发挥的关键。主要的抗体库筛选方法有全细胞筛选、固相抗原筛选、液相抗原筛选和组织筛选。不同的筛选方法的综合运用可有效提高筛选效率。本研究在对抗体库进行特异性筛选之前先采用负性筛选法,用正常人支气管上皮细胞与抗体库孵育以除去非特异性抗体,再用A549细胞进行3轮全细胞筛选,在保证抗原天然构象的同时明显提高抗体的亲和力,最后以ABCG2纯化抗原固相筛选3轮,由于靶点明确筛选效率大为提高,抗体库效价不断提升,第6轮约为第1轮的110倍。最终筛选出的单链抗体经检验能够可溶性表达,分子量约为34×103,且能够特异性识别肺癌A549细胞和ABCG2抗原,下调其表达并显著增加A549细胞对常规化疗药物顺铂的敏感性。
要实现人源化的单链抗体scFv的特异性靶向治疗作用,除了良好的抗原特异性,还需有功能性的抗原抑制作用。通过上述优化筛选策略,我们制备的单链抗体与目的靶标有特异结合能力并观测到A549细胞中ABCG2表达的降低。考虑其原因,一是抗原抗体结合产生的抗体依赖细胞介导的细胞毒作用,该功能是通过全细胞筛选策略,尽可能富集更多A549细胞表面复合抗原而得到。二是针对ABCG2的纯化抗原筛选,从而富集到针对ABCG2的特异抗体,通过抗体特异性结合封闭A549细胞表面ABCG2蛋白的表达位点,从而降低其表达。我们拟在后续研究中进一步论 证scFv与靶细胞结合后的效应,包括抗体的穿膜能力、抗体的体内分布、抗体在体内与靶肿瘤结合的能力等。
| [1] | NSCLC Meta-analysis Collaborative Group. Preoperative che-motherapy for non-small-cell lung cancer: a systematic review and meta-analysis of individual participant data[J]. Lancet, 2014, 383(9928): 1561-1571. |
| [2] | Burdett S, Pignon J P, Tierney J, et al. Adjuvant chemotherapy for resected early-stage non-small cell lung cancer[J]. Cochrane Database Syst Rev, 2015, 3: CD011430. |
| [3] | Nakanishi T, Ross D D. Breast cancer resistance protein (BCRP/ABCG2): its role in multidrug resistance and regulation of its gene expression[J]. Chin J Cancer, 2012, 31(2): 73-99. |
| [4] | Yoh K, Ishii G, Yokose T, et al. Breast cancer resistance protein impacts clinical outcome in platinum-based chemotherapy for advanced non-small cell lung cancer [J].Clin Cancer Res, 2004, 10(5): 1691-1697. |
| [5] | 王净, 王慧, 袁媛, 等. 全人源抗乳腺癌噬菌体单链抗体库的构建[J]. 现代肿瘤医学, 2011, 19(11): 2139-2142. |
| [6] | He H, Ni J, Huang J. Molecular mechanisms of chemoresistance in osteosarcoma (Review)[J]. Oncol Lett, 2014, 7(5): 1352-1362. |
| [7] | Xie Z Y, Lv K, Xiong Y, et al. ABCG2-meditated multidrug resistance and tumor-initiating capacity of side population cells from colon cancer[J]. Oncol Res Treat, 2014, 37(11): 666-668, 670-672. |
| [8] | Dai C L, Liang Y J, Wang Y S, et al. Sensitization of ABCG2-overexpressing cells to conventional chemotherapeutic agent by sunitinib was associated with inhibiting the function of ABCG2 [J].Cancer Lett, 2009, 279(1): 74-83. |
| [9] | Filipits M, Haddad V, Schmid K, et al. Multidrug resistance proteins do not predict benefit of adjuvant chemotherapy in patients with completely resected non-small cell lung cancer: International Adjuvant Lung Cancer Trial Biologic Program[J]. Clin Cancer Res, 2007, 13(13): 3892-3898. |
| [10] | Nelson A L, Dhimolea E, Reichert J M. Development trends for human monoclonal antibody therapeutics[J]. Nat Rev. Drug Discov, 2010, 9(10): 767-774. |
| [11] | Farajnia S, Ahmadzadeh V, Tanomand A, et al. Development trends for generation of single-chain antibody fragments[J]. Immunopharmacol Immunotoxicol, 2014, 36(5): 297-308. |
| [12] | 罗弋, 庞华, 李淑杰, 等. 人源抗Peroxiredoxin I 肺腺癌噬菌体抗体的制备及鉴定[J]. 南方医科大学学报, 2010, 30(1): 30-34. |
| [13] | Luo Y, Pang H, Li S,et al . Production and radioimmunoimaging of novel fully human phage display recombinant antibodies and growth inhibition of lung adenocarcinoma cell line overexpressing Prx I[J]. Cancer Biol Ther, 2009, 8(14): 1369-1377. |



