以5-FU为基础的化疗在结直肠癌(特别是复发和晚期结直肠癌)的治疗中仍起着重要作用[1]。但有超过1/2的患者存在耐药现象,其中绝大多数患者是在连续使用5-FU化疗后敏感性降低而对5-FU产生的获得性耐药[2]。通过研究5-FU耐药机理认为肿瘤微环境在介导肿瘤获得性耐药和抵抗细胞凋亡的生理性调节中发挥了重要作用[3, 4]。而巨噬细胞是浸润性肿瘤细胞微环境的重要组成成分,其与肿瘤的发生、发展、转移、侵袭密切相关[5, 6],但与耐药的关系尚无研究。本研究以结肠癌细胞为研究对象,旨在阐明巨噬细胞与5-FU获得性耐药的关系,并探讨揭示巨噬细胞引起结肠癌细胞5-FU耐药的分子机制。
1 材料与方法 1.1 实验动物50只BABL/C雌性小鼠由第三军医大学动物实验中心提供,年龄6~8周,体质量18~20 g。
1.2 主要材料和仪器结肠癌CT26细胞、巨噬细胞RAW264.7由本实验室保存。恒温CO2培养箱、超灵敏度化学发光系统(美国BIO-RAD公司)、全自动酶标仪(美国BIO-RAD公司)、5804R高速冷冻离心机(德国Eppendorf公司)由第三军医大学西南医院中心实验室提供,流式细胞仪(美国BIO-RAD公司)由第三军医大学西南医院病理研究所提供。DMEM培养基购自美国Gibco公司,胎牛血清购自以色列BI公司。胰蛋白酶购自美国Sigma公司。CCK-8试剂盒购自日本同仁公司,细胞凋亡检测试剂盒购自上海贝博生物公司。鼠抗人Cleaved Caspase-3、p-JNK单克隆抗体均购自美国Cell Signaling公司。兔抗人β-actin单克隆抗体及二抗(羊抗鼠和羊抗兔)均购于北京中杉金桥生物技术有限公司。JNK信号转导通路特异性阻断剂SP600125购于美国Serologllcais公司。5-FU由第三军医大学西南医院肿瘤科提供。DFMO购自英国Tocris公司。蛋白质抽提试剂试剂盒、BCA蛋白质定量试剂购自碧云天生物技术研究所。
1.3 细胞培养小鼠结肠癌细胞和巨噬细胞应用常规RPMI 1640培养基+10%胎牛血清+1%青链霉素,培养于37 ℃、5%CO2的温箱中。
1.4 预先经5-FU处理的巨噬细胞培养上清的收集将10 mmol/L 5-FU原液用2.5%胎牛DMEM稀释至10 μmol/L,混匀并加14 mL至已扩增贴壁的巨噬细胞中,37 ℃、5%CO2的温箱培养24 h后,再加6 mL培养24 h,收集培养上清即为CM(5-FU),-20 ℃保存。
1.5 CCK-8检测在96孔板中接种小鼠结肠癌细胞CT26(100 μL/孔)。将培养板放在培养箱中预培养(37 ℃,5% CO2)。待细胞贴壁后用正常培养基(NM组)、巨噬细胞培养上清(CM组)、预先用10 μmol/L 5-FU处理过的巨噬细胞培养上清[CM(5-FU)组]、正常培养基加10 μmol/L 5-FU(NM+5-FU组)、巨噬细胞培养上清加10 μmol/L 5-FU(CM+5-FU组)、预先用5-FU处理过的巨噬细胞培养上清加10 μmol/L 5-FU[CM(5-FU)+5-FU组]处理24 h,向每孔加入10 μL CCK溶液。将培养板在培养箱内孵育1~4 h后,用酶标仪测定波长450 nm处的光密度值[D(450)]。
1.6 细胞凋亡检测将CT26细胞接种于6孔板中,分组同1.5,离心收集6组悬浮细胞,弃培养基,用冷PBS洗涤细胞2次。用400 μL 1×Binding Buffer悬浮细胞,细胞数为1×106/mL。在细胞悬浮液中加入5 μL Annexin V-FITC,轻轻混匀后于2~8 ℃避光条件下孵育15 min;加入10 μL PI后轻轻混匀于2~8 ℃避光条件下孵育5 min;1 h内用流式细胞仪或荧光显微镜检测。
1.7 Western blot检测蛋白表达在6孔板中接种小鼠结肠癌细胞CT26。将培养板放在培养箱中预培养(37 ℃,5% CO2)。分组同1.5,收集6组细胞提取总蛋白,紫外分光光度法测定总蛋白浓度,行10%、15%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),蛋白上样量20 μL/孔;在垂直电泳槽中电泳后转膜至硝酸纤维素膜上,5% TBST封闭4 h,加入稀释Cleaved Caspase-3、p-JNK、c-JUN的一抗(工作浓度1 :300)4 ℃孵育过夜;TBST洗膜10 min×3次,加入稀释的二抗(工作浓度1 :2 000)孵育3 h,增强化学发光(ECL)荧光试剂显影。以β-actin为内参照,凝胶成像分析系统处理数据,以Cleaved Caspase-3、p-JNK与内参照的灰度比值作为两者蛋白的相对表达量。
1.8 动物饲养和模型的建立选6~8周的雌性BALB/c小鼠饲养于12 h阳光照、12 h黑暗的清洁级动物实验室,以5×106皮下接种结肠癌细胞CT26,待移植瘤最大直径长至0.5 cm左右时,用3种条件培养基[NM、CM、CM(5-FU)]行瘤周皮下注射(75 μL/只,2 d注射1次)及P-JNK抑制剂(SP600125配制成浓度10 μmol/L,行瘤周皮下注射,100 μL/只,2 d注射1次)进行干预处理分组(每组至少3只),然后用5-FU化疗(5-FU行腹腔内注射,50 mg·kg-1·d-1,1次/d),动态观察并记录移植瘤生长情况。待小鼠处死后,收集肿瘤标本进行免疫组化或WB证实TS和凋亡相关通路的变化。
1.9 统计学处理 数据以x±s表示,采用SPSS 18.0统计软件进行方差分析及t检验。 2 结果 2.1 5-FU可诱导结肠癌CT26细胞凋亡以发挥抗癌作用流式细胞仪检测结果表明,5-FU处理组CT26细胞凋亡数目较对照组显著增加,NM+5-FU组凋亡细胞百分比[(27.31±2.33)%]较NM组[(13.2±1.68)%]显著升高(P<0.05,图 1)。Western blot检测结果显示,NM+5-FU组细胞凋亡相关蛋白Cleaved Caspase-3表达较NM组也显著升高(图 2)。由此,提示5-FU可能是通过激活结肠癌CT26细胞Caspase-3凋亡信号来发挥抗癌作用。
 |
| A: NM组;B:NM+5-FU组图 1 PI/Annexin-V 流式细胞仪检测 CT26细胞的凋亡情况 |
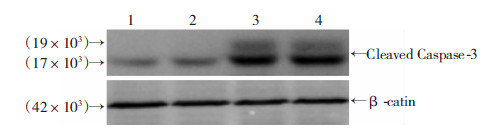 |
| 1,2: NM; 3,4: NM+5-FU 图 2 Western blot检测CT26细胞凋亡相关蛋白caspase-3 的表达 |
Western blot检测发现NM+5-FU组结肠癌CT26细胞P-JNK表达量较对NM组也显著增加(图 3)。由此我们假设:5-FU诱导结肠癌CT26细胞凋亡通路的激活是依赖于P-JNK的。用P-JNK特异性抑制剂(SP600125)及5-FU同时处理结肠癌CT26细胞24 h后,提取蛋白做Western blot检测结果显示,NM+JNK inhibitor+5-FU组较NM+5FU组凋亡相关蛋白Cleaved Caspase-3的表达显著降低(图 4),说明P-JNK抑制剂能显著抑制由5-FU诱导的结肠癌CT26细胞凋亡途径的激活,进一步验证了5-FU激活结肠癌细胞CT26凋亡信号是依赖于P-JNK的这一假说。
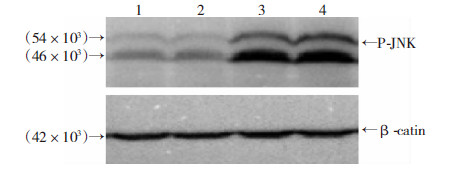 |
| 1,2: NM; 3,4: NM+5-FU 图 3 Western blot检测CT26细胞P-JNK的表达 |
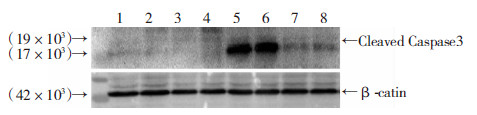 |
| 1,2: NM; 3,4: NM+JNK inhibitor; 5,6:NM+5-FU; 7,8: NM+ JNK inhibitor+5-FU 图 4 Western blot检测CT26细胞P-JNK的表达 |
建立小鼠结肠癌CT26细胞移植瘤模型,用P-JNK特异性抑制剂(SP600125)行瘤周皮下注射抑制P-JNK信号通路后,用5-FU行腹腔内注射观察疗效。结果显示,NM+JNK inhibitor组用或不用5-FU化疗肿瘤平均直径的变化量较NM组显著减少(P<0.05,图 5),NM+JNK inhibitor+5-FU组肿瘤明显较NM+5-FU组大(P<0.05,图 5),说明用P-JNK特异性抑制剂抑制P-JNK信号通路后再给予5-FU化疗,其化疗效果明显降低。提示5-FU诱导结肠癌细胞CT26凋亡是依赖于P-JNK信号通路的激活的。
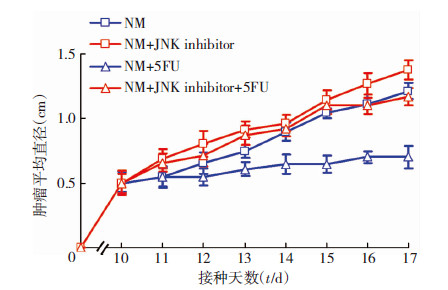 |
| 图 5 小鼠移植瘤模型肿瘤生长情况 |
NM、CM和CM(5-FU)处理结肠癌CT26细胞并给予10 μmol/L的5-FU处理24 h后,用CCK-8测定3种处理条件下5-FU的化疗敏感性。结果显示,CM(5-FU)组用5-FU处理前后细胞存活数的减少量较NM组明显降低(P<0.05,图 6),对5-FU的敏感性明显降低;而CM组用5-FU处理前后细胞存活数的减少量与NM组差异无统计学意义(P>0.05,图 6)。随后,将5-FU可诱导巨噬细胞引起结肠癌细胞对5-FU产生获得性耐药这一发现在小鼠体内实验中进行验证。将小鼠结肠癌CT26细胞分成6组,分别用NM、CM和CM(5-FU)瘤周注射处理后,给或不给予5-FU腹腔注射化疗,结果显示:CM(5-FU)组用或不用5-FU化疗肿瘤平均直径的变化量较NM组显著减少(P<0.05,图 7),化疗敏感性显著降低,而CM组用或不用5-FU化疗肿瘤平均直径的变化量较NM组则差异无统计学意义(P>0.05,图 7),且CM(5-FU)+5-FU组肿瘤明显较NM+5-FU组大(P<0.05,图 7),但CM+5-FU组与NM+5-FU组肿瘤大小差异无统计学意义(P>0.05,图 7)。提示5-FU可诱导巨噬细胞引起结肠癌细胞对5-FU产生获得性耐药。
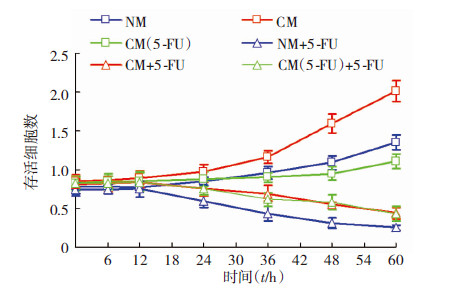 |
| 图 6 CCK8法检测CT26细胞增殖情况 |
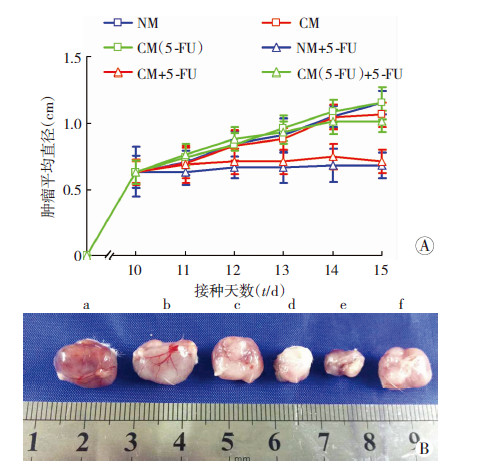 |
| A:小鼠移植瘤模型肿瘤生长情况 B:小鼠移植瘤模型化疗结束后移植瘤大体观 a:NM组;b:CM组;c:CM(5-FU)组;d:NM+5-FU组; e:CM+5-FU组;f:CM(5-FU)+5-FU组 图 7 小鼠移植瘤模型观察肿瘤生长情况 |
NM、CM和CM(5-FU)处理结肠癌CT26细胞,并给予10 μmol/L 5-FU处理24 h后,用流式细胞仪检测细胞凋亡情况,结果发现:CM(5-FU)组用或不用5-FU处理,凋亡细胞百分比的变化量较NM组显著降低(P<0.05,图 8),说明CM(5-FU)显著减少由5-FU诱导的结肠癌CT26细胞的细胞凋亡数目,而CM组与NM组差异无统计学意义(P>0.05,图 8)。Western blot检测发现CM(5-FU)+5-FU组凋亡相关蛋白Cleaved Caspase-3、P-JNK表达较NM+5-FU组明显降低(图 9),说明CM(5-FU)能显著抑制由5-FU有诱导的P-JNK依赖的Caspase-3凋亡通路的激活,而CM则无此作用。因此,初步证实了5-FU可诱导巨噬细胞引起结肠癌细胞对5-FU产生获得性耐药,其机制可能是通过抑制P-JNK/Caspase-3凋亡通路的激活的。
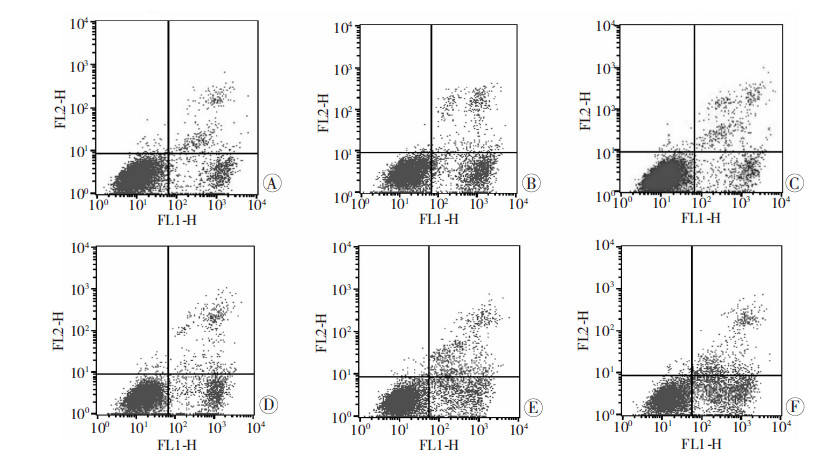 |
| A:NM组;B:NM+5-FU组; C:CM组; D:CM+5-FU组;E:CM(5-FU)组; F: CM(5-FU)+5-FU组 图 8 CT26细胞凋亡情况的PI/Annexin-V 流式细胞仪检测结果 |
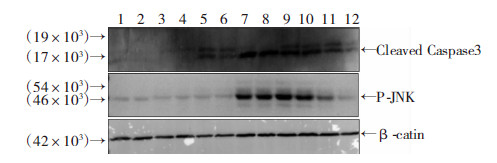 |
| 1、2:NM组;3、4:CM组;5、6:CM(5-FU)组;7、8:NM+5-FU组;9、10:CM+5-FU组;11、12:CM(5-FU)+5-FU组 图 9 Western blot检测CT26细胞Caspase-3及P-JNK 的表达 |
传统观念认为化疗药物是通过直接作用于核酸、微管蛋白及其他化疗作用靶点来发挥抗癌活性的。但随着分子肿瘤学的发展,越来越多的研究发现信号传导通路与肿瘤化疗耐药密切相关,且近年研究证实化疗药物也可通过诱导肿瘤细胞发生细胞凋亡来发挥作用,而很多化疗抵抗的发生也正是通过抑制了由化疗药物诱导的细胞凋亡信号通路的激活来实现的[7]。5-FU是尿嘧啶5位上的氢被氟取代的衍生物。它在细胞内转变为5-氟尿嘧啶脱氧核苷酸(5-FdUMP),能与胸苷酸合成酶(TS)结合成不解离的复合物,阻止脱氧尿苷酸(dUMP)甲基化转变为脱氧胸苷酸(dTMP),从而影响DNA的合成,诱导细胞凋亡来产生抗癌作用[2]。我们前期实验也证实5-FU可诱导结肠癌CT26细胞发生细胞凋亡以发挥其抗癌作用。
进一步研究发现5-FU诱导的细胞凋亡信号通路的激活是P-JNK依赖的。C-Jun氨基末端激酶(JNK)是丝裂原活化蛋白激酶(MAPK)家族的一个主要成员,参与调节细胞生长、发育、分裂、死亡以及细胞间的功能等一系列生命活动[8]。新近研究表明,JNK既有促进凋亡又有抑制凋亡的作用,这取决于细胞类型、刺激的性质和其他信号通路的活性等[9]。本课题组实验发现P-JNK在由5-FU诱导的细胞凋亡信号通路的激活中发挥了重要作用,而P-JNK特异性抑制剂(SP600125)能显著降低由5-FU诱导的细胞凋亡数。因此我们初步证实了5-FU对结肠癌CT26细胞发挥抗癌效应可能是通过激活其P-JNK依赖的Caspase-3的凋亡信号通路。
新近研究认为肿瘤微环境在介导肿瘤获得性耐药和抵抗细胞死亡的生理性调节中发挥了重要作用[3, 4]。在肿瘤微环境中富含多种细胞,包括肿瘤细胞和免疫细胞,如淋巴细胞、树突状细胞、自然杀伤细胞、巨噬细胞等,其中巨噬细胞是浸润性肿瘤细胞微环境的重要组成成分,它可通过复杂的自分泌与旁分泌途径在促进肿瘤的生长、转移、侵袭等方面扮演着重要的角色[10],但其在肿瘤化疗耐药中的作用尚无研究。本研究初步证实了5-FU可诱导巨噬细胞引起结肠癌细胞对5-FU产生获得性耐药,且机制可能是通过抑制了由5-FU激活的P-JNK/Caspase-3凋亡信号通路。
综上所述,本研究进一步验证了5-FU可能是通过激活结肠癌CT26细胞P-JNK依赖的Caspase-3的凋亡信号通路以发挥抗癌效应,且初步阐明了巨噬细胞在5-FU获得性耐药中的重要作用,其可能是通过抑制由5-FU诱导的P-JNK依赖的Caspase-3的凋亡信号通路的激活来拮抗其抗癌作用。
| [1] | Chintala L, Vaka S, Baranda J, et al. Capecitabine versus 5-fluorouracil in colorectal cancer: where are we now?[J]. Oncol Rev, 2011, 5(2): 129-140.DOI:10.1007/s12156-011-0074-3 |
| [2] | Yang S Y, Miah A, Sales K M, et al. Inhibition of the p38 MAPK pathway sensitises human colon cancer cells to 5-fluorouracil treatment[J]. Int J Oncol, 2011, 38(6): 1695-1702. |
| [3] | Wei Y, Au L S. Role of Tumour Microenvironment in Chemoresistance[J]. Cancer Growth & Progression, 2006, 15: 285-321. |
| [4] | Castells M, Thibault B, Delord J P, et al. Implication of tumor microenvironment in chemoresistance: tumor-associated stromal cells protect tumor cells from cell death[J]. Int J Mol Sci, 2012, 13(8): 9545-9571.DOI:10.3390/ijms13089545 |
| [5] | Noy R, Pollard J W. Tumor-associated macrophages: from mechanisms to therapy[J]. Immunity, 2014, 41(1): 49-61.DOI:10.1016/j.immuni.2014.06.010 |
| [6] | Qian B Z, Pollard J W. Macrophage diversity enhances tumor progression and metastasis[J]. Cell, 2010, 141(1): 39-51.DOI:10.1016/j.cell.2010.03.014 |
| [7] | Weng H, Huang H, Dong B, et al. Inhibition of miR-17 and miR-20a by oridonin triggers apoptosis and reverses chemoresistance by derepressing BIM-S[J]. Cancer Res, 2014, 74(16): 4409-4419.DOI:10.1158/0008-5472.CAN-13-1748 |
| [8] | 侯炳旭, 冯丽英. JNK信号通路介导的凋亡在疾病中的作用[J]. 世界华人消化杂志, 2011, 19(17): 1819-1825. |
| [9] | Sabapathy K. Role of the JNK pathway in human diseases[J]. Prog Mol Biol Transl Sci, 2012, 106: 145-169.DOI:10.1016/B978-0-12-396456-4.00013-4 |
| [10] | Biswas S K, Allavena P, Mantovani A. Tumor-associated macrophages: functional diversity, clinical significance, and open questions[J]. Semin Immunopathol, 2013, 35(5): 585-600.DOI:10.1007/s00281-013-0367-7 |



