丙泊酚是已经得到证实的具有心肌保护作用的围术期常用麻醉药物之一[1, 2, 3],目前实验研究对象多为成年健康动物,临床上发生急性心肌梗死的患者大多高龄并有高血压等合并症,心肌保护机制的研究也应该关注高血压等合并症可能对药物性保护机制的影响。桂波等[4]研究发现,给予丙泊酚预处理对合并高血压的离体心肌同样具有保护作用。缺血后处理通常与经典的缺血预处理有相似的心肌保护效果并更有临床应用价值。近期的研究认为线粒体通透性转换孔(mitochondrial permeability transition pore,mPTP)在心肌缺血再灌注损伤过程中的大量开放是导致心肌细胞坏死的重要原因[5],我们假设临床常用诱导剂量的丙泊酚后处理对肾性高血压大鼠(renal hypertensive rats,RHR)心肌缺血再灌注损伤(myocardial ischemic reperfusion injury,MIRI)有保护作用,使用特异性线粒体通透性转换孔开放剂苍术苷(Atractyloside,ATR),拟进一步探讨其可能的线粒体机制,为临床围术期高血压患者心肌保护提供参考依据。
1 材料与方法 1.1 药物及试剂丙泊酚(propofol,AstraZeneca公司),苍术苷(ATR,sigma公司),TUNEL试剂盒(Roche公司),其余试剂为国产分析纯试剂(国药集团上海化学试剂公司)。
1.2 动物模型制备及分组 1.2.1 肾性高血压模型制备健康成年雄性SD大鼠,体质量200~220 g(重庆医科大学实验动物中心)。参照经典的“两肾一夹”的方法制作肾性高血压大鼠(RHR)模型24只。SD大鼠腹腔注射10%水合氯醛麻醉(0.3 mL/100 g),经腹正中切口分离大鼠左肾动脉,在左肾动脉上方0.5 cm处以4号丝线结扎,逐层缝合腹部切口。喂饲常规饲料。术后第8周用尾动脉血压计测量,收缩压(SBP)大于160 mmHg视为高血压模型成功。
1.2.2 心肌缺血/再灌注损伤模型制备24只RHR大鼠麻醉后气管切开并插管,接小动物呼吸机机械通气(潮气量:20 mL/kg,呼吸频率:50~60 /min)。分离右侧颈总动脉并置管,经换能器连接BL-420F生物机能实验系统。连续监测心率(HR)、收缩压(SBP)、舒张压(DBP),肢导联心电图连续监测Ⅱ导联心电图。剪开胸腔后在动脉圆锥与左心耳之间冠状静脉处用5/0丝线结扎左冠状动脉前降支(LAD)。以左室前壁呈蓝紫色及同步心电图示ST段抬高为结扎成功标志,剪断丝线复灌时左室前壁缺血区紫色消失。
1.2.3 分组24只RHR大鼠按照随机数字表法分成3组(n=8):缺血再灌注组(I/R),缺血30 min,再灌注同时尾静脉注入生理盐水1.5 mL,再灌注60 min;丙泊酚组(P组),缺血30 min,再灌注同时 通过尾静脉缓慢注入丙泊酚(2 mg/kg),再灌注至60 min; 丙泊酚+ATR组(PA组),缺血30 min,再灌注同时尾静脉注入丙泊酚(2 mg/kg)+ATR(5 mg/kg ),再灌注至60 min。所有药物均以生理盐水稀释至1.5 mL。
1.3 监测指标 1.3.1 血流动力学指标记录LAD结扎前(T0)、结扎后15 min(T1)、30 min(T2)、再灌注15 min(T3)、再灌注30 min(T4)、再灌注60 min(T5)时SBP、DBP和HR。
1.3.2 电子显微镜下观察心肌细胞超微结构再灌注60 min时,留取1 mm×1 mm左心室前壁组织,2.5 %戊二醛磷酸盐缓冲液固定过夜。制作电镜标本,行超薄切片,黏附于铜网,醋酸铀与柠檬酸双重染色。H-600投射电子显微镜下观察心肌细胞超微结构变化情况。
1.3.3 TUNEL法检测细胞凋亡再灌注60 min时,取心室左前壁组织常规石蜡包埋连续切为4 μm厚组织片,参照TUNEL试剂盒操作步骤进行。TUNEL染色及苏木精复染后,凋亡细胞的细胞核被染为棕黄色,正常细胞核呈蓝色。随机选取10个高倍视野,计算凋亡指数(apoptosis index,AI)即凋亡细胞数占视野中总细胞数的比例。
1.4 统计学分析采用SPSS 13.0统计分析软件,计量资料以x±s表示,组内比较采用配对t检验,组间比较采用重复测量的方差分析,组间概率比较采用Fisher精确概率法,P<0.05为差异有统计学意义。
2 结果 2.1 血流动力学变化I/R、P和PA组SBP和DBP的比较显示,随着再灌注时间的延长,3组大鼠SBP和DBP均呈进行性下降,T5 时点SBP和DBP较T0时点低(P<0.05);P组T3和T4时点SBP和DBP较I/R组和PA组高(P<0.05);3组各时点HR变化差异无统计学意义(P>0.05,表 1)。
| (x±s, n=8) | |||
| 组别 | SBP(mmHg) | DBP(mmHg) | HR(次/min) |
| I/R组 | |||
| T0 | 168±6 | 96±4 | 378±46 |
| T1 | 168±8 | 97±8 | 379±34 |
| T2 | 159±7 | 96±10 | 367±39 |
| T3 | 132±10a | 82±13a | 350±34 |
| T4 | 124±12a | 79±7a | 340±35 |
| T5 | 123±12a | 76±8a | 331±57 |
| P组 | |||
| T0 | 167±4 | 103±11 | 369±35 |
| T1 | 169±7 | 10±27 | 369±33 |
| T2 | 164±6 | 97±6 | 350±42 |
| T3 | 155±9bc | 95±7abc | 343±41 |
| T4 | 140±10abc | 88±6abc | 326±33 |
| T5 | 132±17a | 74±8a | 316±50 |
| PA组 | |||
| T0 | 169±5 | 100±9 | 377±28 |
| T1 | 163±6 | 99±7 | 357±32 |
| T2 | 158±4 | 95±4 | 329±38 |
| T3 | 132±13a | 83±4a | 322±26 |
| T4 | 124±9a | 75±8a | 311±29 |
| T5 | 123±12a | 75±10a | 294±41 |
| a: P<0.05,与T0比较; b: P<0.05,与I/R比较;c: P<0.05,与PA比较 | |||
电镜下观察心肌细胞超微结构,I/R组和PA组线粒体明显肿胀,数量减少,线粒体嵴排列紊乱,稀疏;P组心肌纤维排列均匀,横纹明显,线粒体膜结构完整,仅轻度水肿,线粒体嵴清晰(图 1)。
 |
| A: I/R组 B:P组 C:PA组(箭头示细胞内线粒体) 图 1 电子显微镜下观察心肌细胞超微结构 |
光镜下观察,凋亡细胞核和/或细胞碎片呈深浅不一的棕黄色,正常细胞的细胞核为蓝色,见图 2。I/R组心肌细胞凋亡指数[(48±5)%]和PA组[(38±8)%]较P组[(16±4)%]高(P<0.05)。
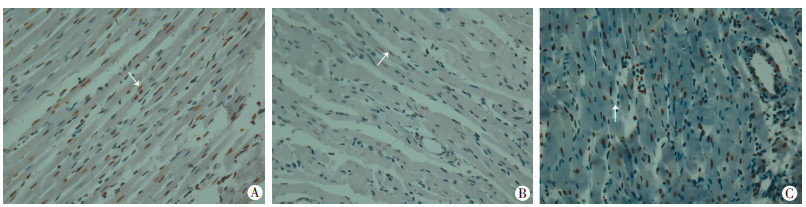 |
| A: I/R组; B:P组; C:PA组 正常细胞核为蓝色,凋亡细胞核呈棕黄色(箭头示) 图 2 TUNEL检测细胞凋亡( ×400) |
在研究丙泊酚后处理对成年健康大鼠心肌保护作用的基础上,本研究探讨丙泊酚后处理对肾性高血压大鼠(RHR)的心肌保护作用及其可能的线粒体机制,旨在为临床围术期高血压患者心肌保护提供参考。本研究结果显示P组T3和T4时点SBP和DBP较I/R组和PA组高(P<0.05),提示常用诱导剂量的丙泊酚后处理可改善肾性高血压大鼠缺血再灌注后的血压。表明丙泊酚后处理能够较好的维持再灌注后的心脏功能。本研究结果显示P组心肌细胞凋亡指数低于I/R组和PA组(P<0.05),提示丙泊酚后处理可有效抑制RHR大鼠缺血再灌注损伤后心肌细胞凋亡。此外,电镜观察其心肌细胞超微结构发现,P组线粒体结构基本完整,而ATR组和I/R组线粒体肿胀,数量减少,表明丙泊酚后处理能够较好维持RHR大鼠缺血再灌注损伤后心肌细胞线粒体的完整性,保存了细胞的能量工厂,从而为受损细胞的恢复提供保障。当PA组同时使用特异性线粒体通透性转换孔开放剂ATR和丙泊酚后,其结果显示丙泊酚的心肌保护效应消失。这点间接证实丙泊酚后处理对RHR大鼠再灌注后的心肌保护作用可能与在线粒体水平抑制mPTP开放,阻断凋亡信号传递有关。
多项临床研究已经证实丙泊酚对合并有基础心血管疾病的心肌具有保护作用,丙泊酚后处理可减轻冠脉搭桥手术患者的心肌损伤[6],体外循环心内直视手术过程中持续输注丙泊酚在维持麻醉同时可明显减轻心肌缺血再灌注损伤[7]。Sun等[8]研究认为丙泊酚可改善成年健康大鼠缺血再灌注损伤心脏梗死面积,并较快恢复心脏损伤后的心功能。Li等[9]研究认为丙泊酚后处理对原代培养的新生大鼠心肌细胞可减少细胞凋亡,提高细胞存活率。丙泊酚可能通过多种途径,激活细胞内源性抗凋亡通路或抑制凋亡蛋白活化通路 来抑制致命性的心肌损伤[10, 11]。而缺血再灌注损伤过程中mPTP大量开放已被认为是导致细胞凋亡的重要 原因之一[12]。mPTP开放抑制剂环胞菌(cyclosporin)[13] 能够减少梗死面积,改善急性心肌梗死后左心功能[14],逆转高胆固醇血症对缺血后处理心肌保护作用的抑制[15]。抑制mPTP开放也是多种药物处理的心肌保护机制之一及靶点所在[16, 17]。再灌注开始时使用mPTP开放剂ATR可能抵消了丙泊酚后处理对凋亡细胞数的抑制效应和循环改善作用。这些研究结果与本实验结果相吻合。但是,另有研究发现高血糖能够取消吸入麻醉药七氟烷后处理的心肌保护作用[18]。而丙泊酚对缺血再灌注损伤的2型糖尿病大鼠心脏保护作用不明显[19],可其后的研究发现丙泊酚能减轻2型糖尿病大鼠的心肌损伤[20]。虽然目前的一些研究结果尚有争论,但临床选用具有心肌保护效果的药物时,仍应该考虑患者并存疾病对其保护效应的影响,尽可能选择不受合并症影响其效果的药物可能会更有益于患者。
由于本实验仅观察了RHR心肌缺血再灌注至60 min 时段范围内的血流动力学及心肌细胞超微结构变化,得出的结论也仅限于此时段范围内。丙泊酚后处理对合并高血压的心肌缺血再灌注损伤的远期保护作用仍有待进一步研究。
综上所述,本研究结果显示,丙泊酚后处理对肾性高血压大鼠的心肌缺血再灌注损伤具有保护作用,其保护机制可能与抑制线粒体通透性转换,减轻心肌细胞凋亡有关。
| [1] | Xu J,Li H,Irwin M G,et al.Propofol ameliorates hyperglycemia-induced cardiac hypertrophy and dysfunction via heme oxygenase-1/signal transducer and activator of transcription 3 signaling pathway in rats[J].Crit Care Med,2014,42(8): e583-e594.DOI:10.1097/CCM.0000000000000415 |
| [2] | King N,Al-Shaama M,Suleiman M S.Propofol improves recovery of the isolated working hypertrophic heart from ischemia-reperfusion[J].Pflugers Arch,2012,464(5): 513-522.DOI:10.1007/s00424-012-1152-5 |
| [3] | Soro M,Gallego L,Silva V,et al.Cardioprotective effect of sevoflurane and propofol during anaesthesia and the postoperative period in coronary bypass graft surgery: a double-blind randomized study[J].Eur J Anaesthesiol,2012,29(12): 561-569.DOI:10.1097/EJA.0b013e3283560aea |
| [4] | 桂波,曹红,曾因明.ERK1/2参与丙泊酚预处理对肾性高血压大鼠离体心肌缺血再灌注损伤的作用[J].中国药理学通报,2006,22(1): 76-80. |
| [5] | Miura T,Tanno M.The mPTP and its regulatory proteins: final common targets of signaling pathways for protection against necrosis[J].Cardiovasc Res,2012,94(2): 181-189.DOI:10.1093/cvr/cvr302 |
| [6] | 王海云,王国林,于泳浩,等.丙泊酚后处理对体外循环冠脉旁路移植术患者心肌缺血再灌注损伤的影响[J].天津医药,2010,38(4): 266-269. |
| [7] | 夏文芳,周青山,邹捍东.丙泊酚对体外循环心脏手术患儿心肌酶谱和预后的影响[J].医药导报,2011,30(9): 1171-1173. |
| [8] | Sun H Y,Xue F S,Xu Y C,et al.Propofol improves cardiac fuctional recovery after ischemia-reperfusion by upregulating nitric oxide synthase activity in the isolated rat hearts[J].Clin Med J(Engl),2009,122(24): 3048-3054. |
| [9] | Li H,Tan J,Zou Z,et al.Propofol post-conditioning protect against cardiomyocyte apoptosis in hypoxia/reoxygenation injury by suppressing nuclear factor-kappa B translocation via extracellular signal-regulated kinase mitogen-activated protein kinase pathway[J].Eur J Anaesthesiol,2011,28(7): 525-534.DOI:10.1097/EJA.0b013e32834296d5 |
| [10] | 邓琳,隋海静,杨雪,等.丙泊酚对大鼠心肌缺血再灌注损伤时凋亡蛋白Bax、Bcl-2的影响[J].哈尔滨医科大学学报,2013,47(3): 237-239. |
| [11] | 刘柳,庞勇,何东伟,等.丙泊酚后处理对离体大鼠缺血再灌注心肌的保护作用及机制[J].第三军医大学学报,2012,34(17): 1779-1782. |
| [12] | Ong S B,Samangouei P,Kalkhoran S B,et al.The mitochondrial permeability transition pore and its role in myocardial ischemia reperfusion injury[J].J Mol Cell Cardiol,2015,78: 23-34.DOI:10.1016/j.yjmcc.2014.11.005 |
| [13] | Hausenloy D J,Boston-Griffiths E A,Yellon D M.Cyclosporin A and cardioprotection: from investigative tool to therapeutic agent[J].Br J Pharmacol,2012,165(5): 1235-1245. |
| [14] | Sheu J J,Chua S,Sun C K,et al.Intra-coronary administration of cyclosporine limits infarct size,attenuates remodeling and preserves left ventricular function in porcine acute anterior infarction[J].Int J Cardiol,2011,147(1): 79-87. |
| [15] | Wu N,Li W N,Shu W Q,et al.Blocking the mitochondrial permeability transition pore with cyclosporine-A can restore cardioprotection of ischemic postconditioning in hypercholesterolemic rat heart[J].Eur Rev Med Pharmacol Sci,2015,19(3): 446-454. |
| [16] | Nazari A,Sadr S S,Faghihi M,et al.Vasopressin attenuates ischemia-reperfusion injury via reduction of oxidative stress and inhibition of mitochondrial permeability transition pore opening in rat hearts[J].Eur J Pharmacol,2015,760: 96-102.DOI:10.1016/j.ejphar.2015.04.006 |
| [17] | Onishi A,Miyamae M,Kaneda K,et al.Direct evidence for inhibition of mitochondrial permeability transition pore opening by sevoflurane preconditioning in cardiomyocytes: comparison with cyclosporine A[J].Eur J Pharmacol,2012,675(1/3): 40-46. |
| [18] | Huhn R,Heinen A,Weber N C,et al.Hyperglycaemia blocks sevoflurane-induced postconditioning in the rat heart in vivo: cardioprotection can be restored by blocking the mitochondrial permeability transition pore[J].Br J Anaesth,2008,100(4): 465-471.DOI:10.1093/bja/aen022 |
| [19] | 隋海静,邓琳,杨雪,等.丙泊酚对2型糖尿病大鼠心肌缺血-再灌注损伤的影响[J].临床麻醉学杂志,2012,28(1): 74-76. |
| [20] | 杨雪,隋海静,李冬梅,等.丙泊酚对2型糖尿病大鼠心肌缺血-再灌注损伤时凋亡蛋白Bax和Bcl-2的影响[J].临床麻醉学杂志,2014,30(4): 385-388. |



