结肠癌是严重危害人类健康的恶性肿瘤之一,随着生活方式、饮食习惯、环境因素等的变化,其发病率和死亡率呈明显的逐年上升趋势[1]。目前结肠癌除手术治疗外,尚无疗效确切的治疗药物。因此,探索新型的高效低毒的靶向抗癌药物对结肠癌的药物治疗显得非常重要。研究表明,天然植物中存在具有治疗价值的抗癌有效成分,以其低毒、有效、无耐药性及整体调节等优势,在肿瘤治疗中起着越来越重要的作用[2]。近年来,葫芦科植物的有效成分葫芦素的药用价值已逐渐受到重视[3, 4]。葫芦素E(cucurbitacin E,CuE)是从葫芦科植物中提取的四环三萜类化合物,具有抗肿瘤、抗化学致癌、抗炎等多种生物活性[5],能有效抑制卵巢癌、肝癌、乳腺癌等细胞的增殖与迁移[6, 7],被认为是极具潜力的抗肿瘤药物。本课题组新近研究[8]表明,CuE对人结肠癌细胞株Caco-2增殖与迁移具有明显抑制作用。但CuE抑制结肠癌细胞增殖的同时,是否也影响其凋亡呢?本研究分析CuE对人结肠癌细胞株Caco-2细胞凋亡的影响,初步探讨其可能的分子机制。
1 材料与方法 1.1 材料CuE购自宝鸡市晨光生物科技有限公司,用DMSO 配置成储存液,-20 ℃保存。DMEM培养基及胎牛血清购自美国Gibco公司,胰蛋白酶购自BBI公司,细胞培养箱购自美国Thermo公司,Hoechst 33258荧光染料购自上海碧云天公司,TUNEL凋亡检测试剂盒购自Vazyme公司,荧光显微镜是德国Leica公司产品,Annexin V-FITC、PI、FACSCalibur型流式细胞仪均为美国BD公司产品,UP-201型组织细胞超声细胞破碎仪购自日本TOMY公司,Caspase-3、PARP、cleaved PARP、Bcl-2抗体购自Cell Signaling公司,β-actin抗体购自Sigma公司,超敏ECL化学发光试剂盒购自美国GE公司,PVDF膜为MILIPORE公司产品,电泳及转膜、封闭系统、Chemi DocTM XRS+型凝胶成像仪均购自BIO-RAD公司。
1.2 方法 1.2.1 细胞培养人结肠癌细胞株Caco-2购自中国生命科学院上海细胞研究所,参照一般细胞培养技术,用pH 7.4、含10%胎牛血清、100 U/mL青霉素、100 μg/mL链霉素、1 mmol/L非必需氨基酸的DMEM培养基,于37 ℃、饱和湿度、5% CO2的培养箱中培养,每2天换液1次,每4天传代1次,取对数生长期细胞进行实验。
1.2.2 Hoechst 33258染色取无菌盖玻片置于24孔 板内,加入鼠尾胶原晾干,将Caco-2细胞接种于盖玻片上,细胞培养至50%~80%融合时分别用终浓度为0.001、0.01、0.1、1、10 μmol/L CuE进行处理,对照组仅用DMEM培养液。分别于CuE处理后24、48、72 h用PBS洗细胞1次,4% PFA固定25 min,PBS洗2次,用0.1% Triton X-100打孔,PBS洗涤,滴加Hoechst 33258染色液,染色10 min,PBS洗涤。滴加抗荧光衰减液后封片,置于荧光显微镜下观察并拍照。
1.2.3 TUNEL染色Caco-2细胞的处理同1.2.2 Hoechst 33258染色,TUNEL染色方法按试剂盒说明书操作。固定并洗涤细胞后,加入20 μg/mL Proteinase K室温孵育5 min,PBS洗涤,每个样本加入1×Equilibration Buffer室温孵育20 min,平衡后吸除液体,滴加TdT孵育缓冲液,37 ℃避光湿润孵育1 h,PBS洗涤2次,BSA洗涤3次,去离子水洗涤1次。封片后置于荧光显微镜下观察并拍照。
1.2.4 Annexin V-FITC/PI流式细胞术参照文献[9]方法,将Caco-2细胞接种于6孔板上,不同浓度 CuE处理24、48、72 h后,加入胰酶收集细胞,以1 ∶1 ∶50 的比例配置Annexin V-FITC、PI、1×apoptosis binding buffer液,每个样本加100 μL Annexin V-FITC/PI标记,室温避光15 min,加入1倍体积的binding buffer稀释样本,用BD公司的FACSCalibur型流式细胞仪进行分析,每个样本计数1×106个细胞,用ModFit 3.2软件进行数据分析。
1.2.5 蛋白印迹法检测Caspase-3、cleaved Caspase-3、PARP、cleaved PARP及Bcl-2蛋白表达将Caco-2细胞接种于6孔板,待细胞完全融合后,加入不同浓度CuE处理24 h,用PBS洗涤,加入细胞裂解液提取细胞总蛋白,细胞破碎后离心10 min(12 000 r/min,8 ℃),沸水变性蛋白。行10% SDS-PAGE电泳,再电 转移至PVDF膜上,用5%脱脂奶室温封闭1 h后加一抗4 ℃孵育过夜,Caspase-3、PARP、cleaved PARP、Bcl-2及 内参β-actin的一抗稀释度分别为1 ∶1 000、1 ∶1 000、1 ∶500、1 ∶1 000与1 ∶5 000。洗膜后加二抗室温孵育1 h,TBST洗涤4次后化学发光显色并凝胶成像采集图像,用BIO-RAD Quantity one 4.4.0 软件进行目的蛋白相对定量分析。
1.3 统计学分析采用SPSS 17.0统计软件,计量资料以x±s表示,组间比较采用单因素方差分析,两样本均数比较采用t检验,P<0.05为差异有统计学意义。
2 结果 2.1 Hoechst 33258染色观察CuE对Caco-2细胞核形态的影响不同浓度CuE处理Caco-2细胞后,细胞核形态发生明显变化,总体呈现出染色质边集、核固缩、核片断化、凋亡小体形成等改变(图 1)。0.001、0.1 μmol/L CuE处理72 h后,与对照组比较差异无统计学意义(P>0.05),其余各浓度及各时相点与对照组比较,差异均有统计学差异(P<0.05,图 2)。随着CuE浓度的增加和作用时间的延长,发生细胞核改变的细胞数量逐渐增多,甚至出现大片细胞脱落形成细胞脱失区。提示CuE对Caco-2细胞核形态的影响具有浓度依赖性和时间依赖性。
 |
| 图 1 荧光显微镜观察不同浓度CuE对Caco-2细胞形态的影响 (Hoechst 33258染色) |
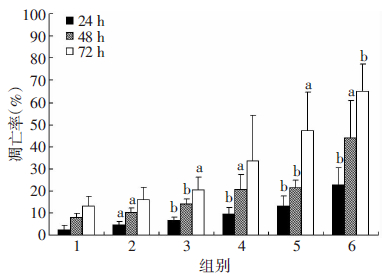 |
| 1:对照组;2~6:分别为0.001、0.01、0.1、1、10 μmol/L CuE组 a:P<0.05,b:P<0.01,与对照组比较图 2 定量分析不同浓度CuE对Caco-2细胞形态的影响 |
与对照组相比较,不同浓度的CuE处理Caco-2细胞后,TUNEL染色阳性细胞数量所占比例增加,表明凋亡的细胞明显增多。CuE引起Caco-2细胞凋亡呈现出浓度及时间依赖性,浓度越高及作用时间越长,CuE引起细胞凋亡越明显(图 3)。与对照组相比,1 μmol/L CuE作用72 h,10 μmol/L CuE作用24、48、72 h后阳性细胞所占比例明显增多(P<0.05),并随 着CuE浓度的增加和作用时间的延长,阳性细胞数量逐渐增多(图 4)。
 |
| 图 3 荧光显微镜观察不同浓度CuE对Caco-2细胞凋亡的影响 (TUNEL染色) |
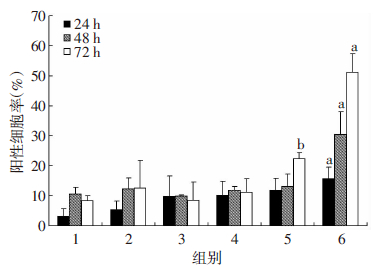 |
| 1:对照组;2~6:分别为0.001、0.01、0.1、1、10 μmol/L CuE组 a:P<0.05,b:P<0.01,与对照组比较图 4 |
与对照组相比,不同浓度CuE处理细胞24、48、72 h 后,随作用时间增加、药物浓度加大,细胞凋亡率逐渐升高(图 5)。
 |
| 图 5 流式细胞术检测不同浓度CuE对Caco-2细胞凋亡的影响 |
不同浓度CuE处理Caco-2细胞72 h后凋亡现象最显著。活细胞在总细胞中所占比例随浓度升高逐渐 减少,死细胞和细胞碎片所占比例增多; 与对照组相比,10 μmol/L CuE处理时显著增多(P<0.05)。细胞总凋亡率所占比例随浓度升高逐渐增加; 与对照组相比,1、10 μmol/L CuE处理时显著升高(P<0.05)。见图 6。
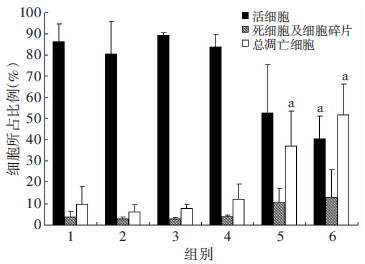 |
| 1:对照组;2~6:分别为0.001、0.01、0.1、1、10 μmol/L CuE组 a:P<0.05,与对照组比较图 6 不同浓度CuE处理Caco-2细胞72 h后活细胞、死细胞和凋亡细胞百分比 |
不同浓度CuE处理Caco-2细胞24 h后,0.001、 0.01 μmol/L CuE 对Caspase-3及cleaved Caspase-3蛋白表达均无明显影响,但0.1、1、10 μmol/L CuE能不同程度地引起Caspase-3蛋白表达降低,同时引起cleaved Caspase-3蛋白表达增加。与此一致,5种浓度的CuE均能不同程度地引起Caco-2细胞PARP蛋白表达降低,并引起cleaved PARP蛋白表达增加(图 7)。表明CuE能引起Caco-2细胞Caspase-3活化,导致PARP裂解。
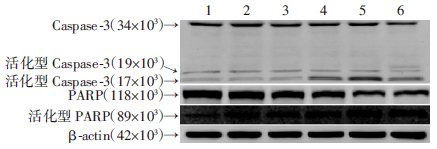 |
| 1:对照组;2~6:分别为0.001、0.01、0.1、1、10 μmol/L CuE组图 7 不同浓度CuE对Caco-2细胞Caspase-3、cleaved Caspase-3、PARP及cleaved PARP蛋白表达的影响 |
5种浓度CuE处理Caco-2细胞24 h后,Bcl-2蛋白表达较对照均有不同程度的降低。CuE浓度为0.001 μmol/L时Bcl-2蛋白表达仅有轻微降低,随着CuE浓度的增加,Bcl-2蛋白表达进一步降低(图 8)。表明CuE抑制Bcl-2蛋白表达具有浓度依赖性。
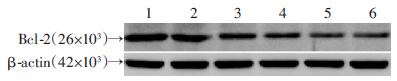 |
| 1:对照组;2~6:分别为0.001、0.01、0.1、1、10 μmol/L CuE组图 8 不同浓度CuE对Caco-2细胞Bcl-2蛋白表达的影响 |
细胞凋亡是在内源性凋亡相关基因控制下,由一系列细胞代谢变化引起的细胞程序性自主毁灭,通过合成特殊蛋白质而完成的细胞主动死亡过程,是细胞主要功能性活动的重要组成部分[10]。细胞凋亡涉及机体发育过程、组织损伤的修复、血细胞的生成、肿瘤发生、病毒致病等过程,对于多细胞动物正常生命活动有着重要的意义[11]。既往研究[12]表明,细胞凋亡的失控与肿瘤的发生发展密切相关,通过诱导肿瘤细胞凋亡的抗肿瘤措施可能比杀伤肿瘤细胞的抗肿瘤措施具有更明显的优越性。因此,寻找有效诱导肿瘤细胞凋亡的药物是抗肿瘤药物治疗研究的又一重要方面。
事实上,许多抗肿瘤药物均能通过抑制细胞增殖及诱导细胞凋亡这两个肿瘤发生发展的关键环节来发挥抗肿瘤效果。我们近期研究[8]发现,CuE呈剂量依赖性及时间依赖性地抑制培养的人结肠癌细胞Caco-2的增殖与迁移,其机制与CuE影响Caco-2细胞骨架肌动蛋白的聚合与解聚的动态平衡有关。但CuE是否对Caco-2的凋亡也有影响,目前尚不清楚。为进一步明确CuE抗结肠癌的分子机制,本研究分析了CuE在体外对结肠癌Caco-2细胞凋亡的影响。本研究细胞核染色、TUNEL染色及流式分析结果均表明,CuE能明显引起Caco-2细胞凋亡,且与浓度及作用时间有关。浓度越高、作用时间越长,CuE诱导细胞凋亡的效果越明显。与本研究结果相似,研究[13, 14, 15]表明,CuE能诱导膀胱癌T24细胞、口腔鳞状细胞癌SAS细胞以及乳腺癌MDA-MB-468与SW527细胞发生凋亡。
目前关于CuE诱导细胞凋亡的机制并不十分清楚。研究[13]认为,CuE诱导细胞凋亡可能与抑制细胞内STAT3磷酸化,升高P53和P21,并减少CDK1和cyclin B有关。另有研究[14]发现,CuE可通过线粒体途径和半胱天冬酶依赖途径诱导肿瘤细胞凋亡,Caspase-3在其中起着非常重要的作用。CuE诱导肿瘤细胞凋亡的机制也可能与其上调cyclin D1、survivin、Bcl-2和Mcl-1的表达有关[15]。
细胞凋亡受多个基因调控,其中最重要的是Bcl-2家族,主要是抑制细胞凋亡。同时,Caspase家族在细胞凋亡的过程中起着重要作用,其中Caspase-3是介导细胞凋亡的核心蛋白酶,被认为是细胞凋亡蛋白酶级联反应最关键的执行者,在各种因素启动的凋亡程序中起最后枢纽作用[16]。Caspase-3被上游信号Bcl-2等激活后可发生级联反应,通过切割其底物PARP,导致细胞凋亡发生[17]。为进一步明确CuE引起结肠癌细胞Caco-2发生凋亡的分子机制,本研究又检测了CuE对Caco-2细胞Bcl-2、Caspase-3及PARP蛋白表达的影响。结果表明,CuE能明显抑制Bcl-2蛋白表达,引起Caspase-3活化,以及Caspase-3的底物PARP被剪切。因此,推测CuE引起Caco-2细胞凋亡的机制 可能是通过抑制抗凋亡基因Bcl-2表达,激活Caspase-3,引起PARP裂解。至于CuE是如何抑制Bcl-2表达,目前尚不清楚,有待进一步研究。
综上所述,CuE能明显引起结肠癌细胞Caco-2发生凋亡,其分子机制可能与其抑制Bcl-2表达,激活Caspase-3,从而引起PARP裂解有关。
| [1] | 刘秀均, 李毅, 甄永苏. 博安霉素对小鼠结肠癌及其肝转移的抑制作用[J]. 药学学报, 2001, 36(1): 14-18. |
| [2] | 徐佳, 伍春莲, 彭聪, 等. 雷公藤红素对人肺癌细胞增殖与凋亡的影响[J].西华师范大学学报: 自然科学版, 2014, 35(1): 51-56. |
| [3] | Feng H, Zang L, Zhao Z X, et al. Cucurbitacin-E inhibits multiple cancer cells proliferation through attenuation of Wnt/beta-catenin signaling[J].Cancer Biother Radiopharm, 2014, 29(5): 210-214. DOI: 10.1089/cbr.2014.1614 |
| [4] | Ding T, Zhang Y, Chen A, et al. Effects of cucurbitacin e, a tetracyclic triterpene compound from Cucurbitaceae, on the pharmacokinetics and pharmacodynamics of warfarin in rats[J]. Basic Clin Pharmacol Toxicol, 2015, 116(5): 385- 389. DOI: 10.1111/bcpt.12329 |
| [5] | Chen J C, Chiu M H, Nie R L, et al. Cucurbitacins and cucurbitane glycosides: structures and biological acivities[J]. Nat Prod Rep, 2005, 22(3): 386-399. DOI: 10.1039/b418841c |
| [6] | Abe M, Matsuda K. Chemical factors influencing the feeding preference of three Aulacophora leaf beetle species (Coleoptera: Chrysomelidae) . Appl Entomol Zool, 2005, 40(1): 161-168. |
| [7] | Jayaprakasam B, Seeram N P, Nair M G. Anticancer and antiinflammatory activities of cucurbitacins from Cucurbita andreana[J]. Concer Lett, 2003, 189(1): 11-16. |
| [8] | 李丽, 随何欢, 黄家君. 葫芦素E对人结肠癌细胞Caco-2增殖与迁移的影响及其作用机制[J]. 第三军医大学学报, 2015, 37(13): 1342-1348. DOI: 10.16016/j.1000-5404.201411205 |
| [9] | Huang W W, Ko S W, Tsai H Y, et al. Cantharidin induces G2/M phase arrest and apoptosis in human colorectal cancer colo 205 cells through inhibition of CDK1 activity and caspase-dependent signaling pathways[J]. Int J Oncol, 2011, 38(4): 1067-1073. DOI: 10.3892/ijo.2011.922 |
| [10] | Hassan I H, Zhang M S, Powers L S, et al. Influenza A viral replication is blocked by inhibition of the inositol-requiring enzyme 1 (IRE1) stress pathway[J]. J Biol Chem, 2012, 287(7): 4679-4689. DOI: 10.1074/jbc.M111.284695 |
| [11] | 陈文强, 于淼, 李健. 内质网应激反应诱导细胞凋亡研究[J]. 哈尔滨商业大学学报: 自然科学版, 2014, 30(1): 21-24. DOI: 10.3969/j.issn.1672-0946.2014.01.005 |
| [12] | Kerr J F, Winterford C M, Harmon B V. Apoptosis. Its significance in cancer and cancer therapy[J]. Cancer, 1994, 73(8): 2013-2026. |
| [13] | Huang W W, Yang J S, Lin M W, et al. Cucurbitacin E induces G(2)/M phase arrest through STAT3/p53/p21 signaling and provokes apoptosis via Fas/CD95 and mitochondria-dependent pathways in human bladder cancer T24 cells[J]. Evid Based Complement Alternat Med, 2012, 2012: 952762. DOI: 10.1155/2012/952762 |
| [14] | Hung C M, Chang C C, Lin C W, et al. Cucurbitacin E as inducer of cell death and apoptosis in human oral squamous cell carcinoma cell line SAS[J]. Int J Mol Sci, 2013, 14(8): 17147-17156. DOI: 10.3390/ijms140817147 |
| [15] | Kong Y, Chen J, Zhou Z, et al. Cucurbitacin E induces cell cycle G2/M phase arrest and apoptosis in triple negative breast cancer. PLoS One, 2014, 9(7): e103760. DOI: 10.1371/journal.pone.0103760 |
| [16] | Pop C, Salvesen G S. Human caspases: activation, specificity, and regulation[J]. J Biol Chem, 2009, 284(33): 21777- 21781. DOI: 10.1074/jbc.R800084200 |
| [17] | Oliver F J, de-la-Rubia G, Rolli V, et al. Importance of poly(ADP-ribose) polymerase and its cleavage in apoptosis. Lesson from an uncleavable mutant[J]. J Biol Chem, 1998, 273(50): 33533-33539. |



