2. 266071 山东 青岛,解放军401医院干部病房三科
2. Third Department of Cadre’s Ward, No. 401 Hospital of PLA, Qingdao, Shandong Province, 266071, China
瑞舒伐他汀(可定)于2007年在国内上市,其临床应用日益广泛。大量试验表明,瑞舒伐他汀对调脂及逆转斑块具有作用,2006年3月公布的ASTEROID研究[1]是首个证实他汀类药物治疗能使冠状动脉粥样硬化逆转的临床研究。但国外开展的大型临床试验都采用了40 mg瑞舒伐他汀,而国内并未批准此剂量的适应证,临床应用的是10或20 mg(qd)剂量。因此,本研究主要综合国内有关瑞舒伐他汀治疗国人颈动脉粥样硬化的研究结果,进行Meta分析,比较不同剂量瑞舒伐他汀对低密度脂蛋白胆固醇(low density lipoprotein-cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein-cholesterol,HDL-C)和颈动脉内膜厚度(intima-media thickness,IMT)的影响及不良反应的发生,评估不同剂量瑞舒伐他汀对改善颈动脉粥样硬化的影响,以期为临床合理用药提供科学依据。
1 资料与方法 1.1 文献检索遵循Cochranehandbook 5.0.1版RCT检索策略,采用主题词与自由词相结合的方式。英文检索词:rosovastatin;carotid atherosclerosis;IMT。中文检索词:瑞舒伐他汀,颈动脉粥样硬化,动脉内膜中层厚度。计算机检索2007-2015年PubMed、Medline、EMBASE、中国知网(CNKI)、维普中文科技期刊、中国生物医学文献数据库关于瑞舒伐他汀治疗颈动脉粥样硬化的随机或半随机对照试验的文章,评价文章的方法学质量后纳入研究。
1.2 纳入与排除标准 1.2.1 文献纳入标准国内外公开发表的有关瑞舒伐他汀对国人颈动脉粥样硬化治疗的随机对照研究或半随机对照研究;研究方法及结果明确;文献提供足够信息可以计算出效应值;样本量达到统计分析标准。
1.2.2 文献排除标准不是瑞舒伐他汀10 mg与20 mg比较的临床试验,未能报道瑞舒伐他汀治疗后对颈动脉内膜厚度及血脂的测定,未明确描述不良反应者,数据资料不齐全者予以排除;重复发表的文献。
1.3 观察指标观察颈动脉内膜厚度IMT,血脂LDL-C、HDL-C及瑞舒伐他汀不良反应。
1.4 文献的方法学质量评价由两名独立的研究员参与文献的检索、筛选和评价,采用Jadad法[1]对各个独立研究进行质量评估,即是否采用随机化分组(2分),盲法(2分),以及陈述失访及理由(1分),总分范围为0~5分,总分0~2分为低质量文献,总分3~5分为高质量文献。
1.5 统计学分析参照医学统计学方法,使用系统评价软件Revman 5.0进行Meta分析。首先对纳入研究的数据行同质性检验,若I2>0.5或P<0.1,则各研究有差异性,可忽略差异采用随机效应模式合并分析,不能忽略者采用描述性分析。若I2<0.5或P>0.1,则各研究间一致性较好,可采用固定效应模型分析。效应量采用假设检验和区间估计(95%CI)。
2 结果 2.1 文献检索结果共检索出相关文献458篇,通过阅读文章题目和摘要,筛选出符合试验要求的32篇,进一步阅读全文,排除不符合纳入标准的文献,共纳入文献8项[2, 3, 4, 5, 6, 7, 8, 9],合计657例患者,均为瑞舒伐他汀20与10 mg的对照研究,除1项研究外,治疗时间为6个月。其中常规治疗组327例,强化治疗组330例(表 1)。
8项研究描述了10、20 mg瑞舒伐他汀抗颈动脉粥样硬化比较结果。首先进行齐性检验,I2为56.9%>0.5,P=0.02,各研究间异质性较差,采用随 机效应模型进一步Meta分析显示:IMT在20 mg组明显 低于10 mg组,MD=-0.13,95%CI(-0.17,-0.09),整体效果检验Z=6.34,P<0.000 01,表明20 mg瑞舒伐他汀较10 mg瑞舒伐他汀降低IMT差异有统计学意义(图 1)。
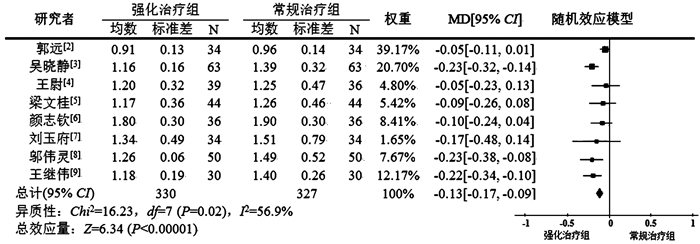 |
| 图 1 不同剂量瑞舒伐他汀对颈动脉粥样硬化IMT变化 |
8项研究首先进行齐性检验,I2为74.3%>0.5,P=0.000 3,研究间有异质性,采用随机效应模型进一步Meta分析显示:LDL-C在20 mg组明显低于10 mg组,MD=-0.50,95%CI(-0.61,-0.39),整体效果 检验Z=9.12,P<0.000 01,表明20 mg瑞舒伐他汀较10 mg瑞舒伐他汀降低IMT差异有统计学意义(图 2)。
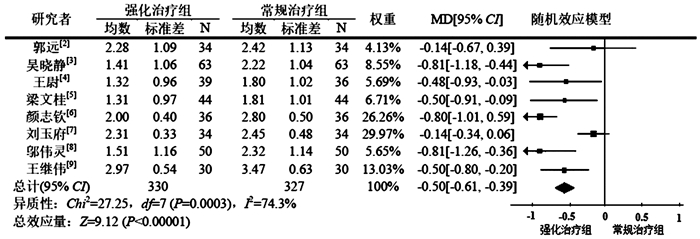 |
| 图 2 不同剂量瑞舒伐他汀对颈动脉粥样硬化LDL-C变化 |
对纳入的8项研究进行齐性检验,I2为18.3%<0.5,P=0.28>0.05,各研究间一致性较好,采用固定效应模型分析(Peto法)进一步Meta分析显示:HDL-C在20 mg组明显高于10 mg组,MD=0.13,95%CI(0.09,0.17),整体效果检验Z=6.23,P<0.000 01,表明20 mg瑞舒伐他汀较10 mg瑞舒伐他汀提高LDL-C差异有统计学意义(图 3)。
 |
| 图 3 不同剂量瑞舒伐他汀对颈动脉粥样硬化HDL-C变化 |
研究[2, 4, 7]瑞舒伐他汀20 mg组各出现1例患者发生转氨酶一过性升高,自行好转。研究[3]瑞舒伐他汀20 mg组2例出现转氨酶轻度升高,自行好转。各研究中瑞舒伐他汀10 mg组均未发现肝功能异常等副反应。
2.6 发表偏倚本研究采用漏斗图分析结果显示图形对称性较好(图 4),表明所选文献的偏倚性不大。
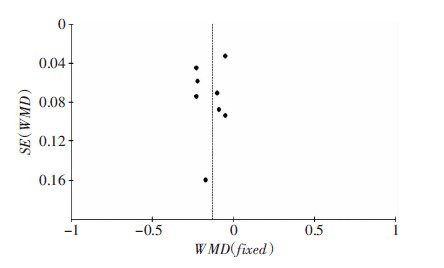 |
| 图 4 不同剂量瑞舒伐他汀对颈动脉粥样硬化Meta分析的漏斗图 |
动脉粥样硬化最先累及的血管是颈动脉[10],而且由于颈动脉是表浅的大血管,其动脉粥样硬化斑块可以通过彩色多普勒超声测量,远比通过血管内超声(IVUS)测量冠脉血管粥样斑块要方便,简单,而且无创。因此临床上多采用彩色多普勒超声测量颈动脉内膜中层厚度(IMT),作为评价颈动脉粥样硬化程度的有效标志。研究显示,颈动脉IMT和斑块体积是心脑血管病的独立危险因素[11]。高脂血症是导致动脉粥样硬化的最重要因素之一,本分析纳入的8项研究中,患者均存在脂代谢异常,调节血脂对预防治疗动脉粥样硬化尤其关键。
大剂量他汀类药物可以延缓或逆转动脉粥样硬化斑块的进展。REVERSAL研究[12]、ASTEROID研究[1] 和METEOR研究[13]等均证实,他汀强化降脂(80 mg阿托伐他汀或40 mg瑞舒伐他汀)18~24个月,经IVUS检测显示斑块进展延缓,甚至出现斑块逆转。其机制主要为胆固醇的转运和逆转运,上述临床试验显示,若要阻止冠脉斑块的进展,需要把LDL-C降低到70~80 mg/dL以下,同时把HDL-C升高至45~55 mg/dL以上,以减少胆固醇流入斑块,增加其流出斑块,从而实现斑块逆转。AS病变发生逆转和消退的主要成分是斑块中的脂质核心,而平滑肌、钙化及胶原成分则几乎不会发生消退。以上研究均针对西方人群,且瑞舒伐他汀40 mg/d在国内未经批准用于临床。对于东方人群,中小剂量他汀治疗也进行了一系列研究。2009年的TWINS研究[14]发布了以日本人群为研究对象,首次应用血管内镜和IVUS评估AS病变。结果显示,阿托伐他汀10~20 mg/d治疗28周后,斑块体积明显缩小9.4%,到80周时斑块体积缩小18.9%。近期,COSMOS研究[15]同样以日本人群为研究对象,其结果显示服用过他汀类药物的稳定型冠心病患者,使用平均少于20 mg/d瑞舒伐他汀,可观察到冠脉内AS斑块体积明显缩小。因此,在亚洲人群中即使是使用一般的剂量也可以看到逆转AS的作用,充分地证明了瑞舒伐他汀逆转斑块的作用。上述临床试验的结果证实,对于东方人群来讲,长期采用常规剂量的他汀类药物治疗仍可发挥逆转AS斑块的作用,而且随着治疗时间的延长,获益可以进一步增加,这无疑为我们在中国人群用药选择上提供了循证医学的依据。
瑞舒伐他汀对于血脂水平的控制有剂量依赖关系,在本文中可以看出,20 mg瑞舒伐他汀相比10 mg瑞舒伐他汀,使用6个月后可以更加有效地降低LDL-C水平,提高HDL-C水平,从而降低IMT。研究显示,经瑞舒伐他汀治疗后斑块数量无明显减少,但斑块面积明显缩小[16]。这一现象与使用的瑞舒伐他汀剂量有关,说明瑞舒伐他汀可通过减少脂质含量,缩减颈动脉斑块,并呈现一定的剂量依赖性关系。
肝功能异常是他汀类药物最常见的临床副反应,而且往往具有剂量相关性,既往研究证实,与阿托伐他汀及辛伐他汀相比,其转氨酶升高没有差异[17]。在瑞舒伐他汀降脂治疗的多个相关研究中,各剂量组中发生转氨酶升高超过上限3倍的发生率为0.2%[18],而本结果显示,瑞舒伐他汀20 mg组共发生5例转氨酶升高超过上限,发生率为1.5%,但未说明是否超过上限的3倍,10 mg组未观察到转氨酶升高,但上述升高均为一过性,可自行恢复,提示在使用中注意监测肝功能,而无需调整剂量。大剂量瑞舒伐他汀引起的蛋白尿及肾功能受损是另一个关心的问题,但本文纳入的各个研究对蛋白尿、肌酐等常见他汀类不良反应未进行观察。
| [1] | Nissen S E, Nicholls S J, Sipahi I, et al. Effect of very high-intensity statin therapy on regression of coronary atherosclerosis: the ASTEROID tria1[J]. JAMA, 2006, 295(13): 1556-1565. DOI: 10.1001/jama.295.13.jpc60002 |
| [2] | 郭远, 宝辉, 李卫, 等. 不同剂量瑞舒伐他汀对老年糖尿病患者颈动脉粥样硬化的影响[J].中国新药杂志, 2011, 20(21): 2123-2126, 2138. |
| [3] | 吴晓静, 孙学仁. 瑞舒伐他汀钙强化降脂治疗颈动脉粥样硬化的疗效与安全性[J].山东医药, 2011, 51(9): 83-84. DOI: 10.3969/j.issn.1002-266X.201 1.09.048 |
| [4] | 王尉. 王浩. 陈亭亭. 不同剂量瑞舒伐他汀对颈动脉粥样硬化合并高血脂患者疗效及安全性的对照分析[J]. 中国当代医药, 2012, 19(18): 69-70, 72. DOI: 10.3969/j.issn.1674-472 1.2012.18.034 |
| [5] | 梁文桂. 不同剂量瑞舒伐他汀治疗老年冠心病合并颈动脉粥样硬化斑块的疗效及安全性[J]. 大家健康: 学术版, 2013, 7(8): 78. |
| [6] | 颜志钦, 易兴阳, 虞君儒, 等. 瑞舒伐他汀强化降脂对缺血性脑卒中血脂及颈动脉粥样硬化斑块的影响[J]. 中国药物与临床, 2013, 13(11): 1408-1410. DOI: 10.11655/zgywylc2013.11.007 |
| [7] | 刘玉府, 刘春岭. 瑞舒伐他汀强化降脂治疗对缺血性脑卒中颈动脉粥样斑块的影响[J]. 中国实用神经疾病杂志, 2014, 17(17): 107-108. DOI: 10.3969/j.issn.1673-5110.2014.17.077 |
| [8] | 邬伟灵. 刍议应用瑞舒伐他汀钙强化降脂治疗颈动脉粥样硬化的临床疗效[J].中外医学研究, 2014, 12(24): 25-26. |
| [9] | 王继伟.瑞舒伐他汀钙强化降脂对颈动脉粥样硬化的影响[J].临床合理用药杂志, 2015, 3(3): 5-6. |
| [10] | Cohn J N, Duprez D A, Grandits G A. Arterial elasticity as part of comprehensive assessment of cardiovascular risk and drug treatment[J]. Hypertension, 2005, 46(1): 217-220. DOI: 10.1161/01.HYP.0000165686.50890.c3 |
| [11] | Polak J F, Pencina M T, Pencina K M, et al. Carotid-wall intima-media thickness and cardiovascular events[J]. N Engl J Med, 2011, 365(3): 213-221. |
| [12] | Nissen S E. Halting the progression of atherosclerosis with intensive lipid lowering: results from the Reversal of Atherosclerosis with Aggressive Lipid Lowering (REVERSAL) trial[J]. Am J Med, 2005, 118 Suppl 12A: 22-27. DOI: 10.1016/j.amjmed.2005.09.020 |
| [13] | Crouse J R 3rd, Raichlen J S, Riley W A, et al. Effect of rosuvastatin on progression of carotid intima-media thickness in low-risk individuals with subclinical atherosclerosis: the METEOR Trial[J]. JAMA, 2007, 297(12): 1344-1353. DOI: 10.1001/jama.297.12.1344 |
| [14] | Hiro T, Kimura T, Morimoto T, et al. Effect of intensive statin therapy on regression of coronary atherosclerosis in patients with acute coronary syndrome: a multicenter randomized trial evaluated by volumetric intravascular ultrasound using pitavastatin versus atorvastatin (JAPAN-ACS study)[J]. J Am Coll Cardiol, 2009, 54(4): 293-302. DOI: 10.1016/j.jacc.2009.04.033 |
| [15] | Takayama T, Hiro T, Yamagishi M, et al. Effect of rosuvastatin on coronary atheroma in stable coronary artery disease: multicenter coronary atherosclerosis study measuring effects of rosuvastatin using intravascular ultrasound in Japanese subjects (COSMOS)[J]. Circ J, 2009, 73(11): 2110-2117. |
| [16] | Rosenson R S, Otvos J D, Hsia J. Effect of rosuvastatin and atorvastatin on LDL and HDL particle concenltrations in patients with metabolic syndrome: a randomized, double-blind, controlled study[J]. Diabetes Care, 2009, 32(6): 1087-1091. DOI: 10.2337/dc08-1681 |
| [17] | Davidson M H. Rosuvastatin safety: lessons from the FDA review and post-approval surveillance[J]. Expert Opin Drug Saf, 2004, 3(6): 547-557. |
| [18] | Kargiotis K, Katsiki N, AthyrosV G, et al. Effect of rosuvastatin on non-alcoholic steatohepatitis in patients with metabolic syndrome and hypercholesterolaemia: a preliminary report[J]. Curr Vasc Pharmacol, 2014, 12(3): 505-511. |



