急性肺损伤(acute lung injury,ALI)是由多种因素导致的肺泡细胞及毛细血管内皮细胞损伤。富含蛋白质的肺泡水肿液因重吸收困难而过多地聚集在肺泡腔内,是导致ALI患者发展成严重低氧性呼吸功能不全的重要原因,也是治疗难点[1, 2]。肺泡上皮钠离子通道(alveolar epithelial sodium channel,ENaC)属于阿米洛利-敏感钠离子通道,它广泛分布于肺泡Ⅱ型上皮细胞中,由α、β、γ3种亚基构成。α亚基承担了最主要的生物学功能,如肺泡内水肿液重吸收和调节细胞内环境。本课题组前期研究表明,胰岛素对肺组织产生一定的保护作用,并进一步发现胰岛素是通过激活雷帕霉素蛋白复合体Ⅱ(mammalian target of rapamycin complex 2,mTORC2)上游的PI3K受体靶点而调控mTORC2/SGK1信号通路,同时使ENaC的表达上调,但具体作用机制待进一步阐释。本研究拟选用胰岛素、mTORC1选择性抑制剂雷帕霉素和mTORC1与mTORC2的双效抑制剂PP242对小鼠ALI模型和 A549细胞进行干预,探讨mTORC2/SGK1信号通路、磷酸泛素化连接酶(E3 ubiquitin protein ligase,Nedd4-2) 及ENaC-α之间的作用机制,并进一步阐明mTORC2/SGK1途径对肺水清除(alveolar fluid clearance,AFC)方面的影响。
1 材料与方法 1.1 材料6~8周龄雄性BALB/c小鼠50只,清洁级,体质量18~22 g,购自重庆医科大学实验动物中心。A549细胞购自中国科学院典型培养细胞库。TRIzol RNA提取试剂盒、逆转录试剂盒、PCR引物及DNA marker均由日本TaKaRa公司提供;Western blot配胶试剂盒购自西安碧云天生物技术公司。ELISA试剂盒购自欣博盛生物有限公司。RPMI1640培养基和小牛血清购自Gibco公司。rictor单克隆抗体、糖皮质激素调 节蛋白激酶1(serum and glucocorticoid-regulated protein kinase1,SGK1)及P-SGK单克隆抗体购自美国Immunoway公司;nedd4-2、ENaC-α单克隆抗体购自英国Abcam公司。β-actin多克隆抗体购自美国Proteintech公司。HRP标记山羊抗兔IgG二抗,HRP标记山羊抗兔(抗鼠)荧光二抗均购自Abbkine公司。
1.2 方法 1.2.1 动物分组及处理将50只雄性小鼠按随机数表法分成5组,10只/组。分为对照组(Blank组)、模型组(LPS组)、胰岛素组(LPS+Insulin组)、雷帕霉素组(LPS+Rapamycin组)、PP242抑制剂组(PP242组)。按4 μL/g的比例腹腔注射4%水合氯醛麻醉,滴鼻给予5 mg/kg LPS构建ALI小鼠模型。 造模2 h后,分别腹腔注射生理盐水、0.8 U/kg胰岛素、4 mg/kg 雷帕霉素、60 mg/kg PP242分别干预动物模型,并监测血糖。于8 h后处死小鼠,收取标本。
1.2.2 细胞分组及处理将A549细胞用含有10%小牛血清的RPMI1640的培养基培养,待细胞融合度达90%以上,将细胞平均接种于6孔板中。分别以培养基(对照组)、10 mmol/mL胰岛素(胰岛素组)、5 mmol/mL雷帕霉素(雷帕霉素组)、5 mmol/mL PP242(PP242组)处理A549细胞,24 h后收集细胞。
1.2.3 测定肺湿干质量比(W/D)和肺泡灌洗液(BALF)中IL-6、TNF-α水平处死小鼠,全肺灌洗3次,收集肺泡液,离心保存。取出右上肺组织,称湿质量。放于60 ℃烤箱烘干24 h后,称干质量。计算湿干质量比W/D。按ELISA试剂盒说明测定肺泡灌洗液中IL-6及TNF-α水平。
1.2.4 肺组织病理切片及肺损伤评分全肺灌洗后取左肺,用10%甲醛固定,石蜡包埋、切片,行HE染色。光镜下观察各组肺组织病理形态改变。肺损伤评分标准:①肺泡充血;②出血;③肺泡或血管腔内中性粒细胞浸润或聚集;④肺泡壁增厚和/或透明膜形成。依据病变轻重程度评0~4分(0分:无病变或非常轻微;1分:轻度病变;2分:中度病变;3分:重度病变;4分:极重度病变)。ALI总评分为各项评定分数相加总和。
1.2.5 Real-time PCR检测SGK1、Nedd4-2 及ENaC-α的mRNA表达提取各组A549细胞总RNA,逆转录合成cDNA,按照TaKaRa扩增试剂盒说明书建立 20 μL 反应体系,PCR 扩增目的和内参基因。引物序列见表 1。 经预变性、变性、退火、延伸及再循环等过程,用Bio-Rad 1.6软件系统分析SGK1、Nedd4-2、ENaC-α与β-actin相对比值表示mRNA转录水平。
基因 | 上游引物 | 下游引物 | 产物 大小(bp) | |
| SGK1 | 5′-CAACAGCACAACATCC-ACCTTC-3′ | 5′-TACAAGACAGCTCCCA-GGCAC-3′ | 114 | |
| Nedd4-2 | 5′-GAGAAACGAGGCTCGA-ACAC-3 | 5′-AAAAGTACAGAGTTGA-CAGCAAAA-3′ | 289 | |
| α-ENaC | 5′-CAATGACACCCAGTAT-AAGATGACC-3′ | 5′-CAATGAGGCACAGCAC-CGA-3′ | 271 | |
| β-Actin | 5′-AGCGAGCATCCCCCAA-AGTT-3′ | 5′-GGGCACGAAGGCTCAT-CATT-3′ | 285 |
提取总蛋白,经上样、电泳、转膜、封闭后,分别按比例稀释rictor、SGK1,SGK-ser422、Nedd4-2及α-ENaC的抗体于
抗体孵育盒,4 ℃孵育过夜;PBST(或TBST)洗膜 3次,每次10 min。加入HRP标记的二抗,37 ℃孵育1 h;PBST洗膜3次,每次15 min。ECL试剂盒显色,凝胶系统成像,并用Quantity One软件系统分别分析目的条带与β-actin的比值表示各指标的蛋白表达水平。
细胞计数法将8×104个细胞均匀接种于放有灭菌载玻片的24孔板内,设对照组、胰岛素组、雷帕霉素组及PP242组,细胞生长稳定后分别给予药物处理。24 h后,经PBS洗涤和多聚甲醛固定,取出载玻片将其放于湿盒上用山羊血清封闭30 min,4 ℃孵育一抗过夜。PBS洗涤3次后,37 ℃避光孵育二抗1 h并封片、成像。
1.3 统计学分析数据以x±s表示,采用SPSS 13.0统计软件,多样本间比较采用单因素方差分析。
2 结果 2.1 各组小鼠肺W/D比值与模型组比较,胰岛素组W/D比值明显降低(P<0.05),PP242组明显增高(P<0.05),雷帕霉素组稍微升高,但差异无统计学意义(P>0.05,表 2)。
| (n=10,x±s) | |||
| 组别 | W/D | IL-6(pg/mL) | TNF-α(pg/mL) |
| 对照组 | 5.07±0.38 | 3.21±0.74 | 10.03±3.09 |
| 模型组 | 6.19±0.38a | 77.48±6.04a | 116.20±13.5a |
| 胰岛素组 | 5.40±0.17ab | 49.17±8.49ab | 92.40±8.37ab |
| 雷帕霉素组 | 6.30±0.16 | 73.79±9.99 | 111.00±21.36 |
| PP242组 | 6.96±0.13ab | 100.60±14.69ab | 192.50±16.01ab |
| a:P<0.05,与对照组比较;b:P<0.05,与模型组比较 | |||
与模型组比较,胰岛素组中IL-6、TNF-α值显著降低(P<0.05);PP242组中IL-6、TNF-α值显著增高(P<0.05);雷帕霉素组中IL-6、TNF-α值略微降低,但差异无统计学意义(P>0.05,表 2)。
2.3 各组小鼠肺组织病理改变与模型组肺损伤评分[(3.4±0.3)分]比较,PP242组[(4.5±0.1)分]中肺组织炎症、充血水肿等情况明显增多(P<0.05);胰岛素组[(2.4±0.5)分]中肺组织炎症、充血水肿等情况有明显改善(P<0.05);而雷帕霉素组[(3.6±0.6)分]与模型组比较则改变不明显(P>0.05,图 1)。
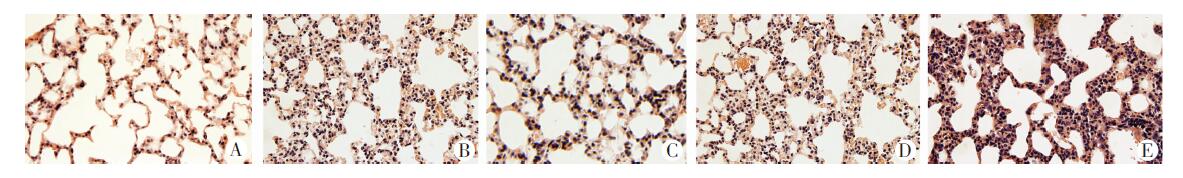 |
| A:对照组;B:模型组;C:胰岛素组;D:雷帕霉素组;E:PP242组图 1 光镜观察各组小鼠肺组织病理学改变 (HE ×200) |
与对照组比较,胰岛素组中SGK1 mRNA表达显著增高(P<0.05),PP242组中SGK1 mRNA表达显著降低(P<0.05)。而雷帕霉素组较对照组各指标无明显差异。而各组中下游Nedd4-2、ENaC-α mRNA的表达基本与上游SGK1变化趋势相同(P<0.05,图 2)。
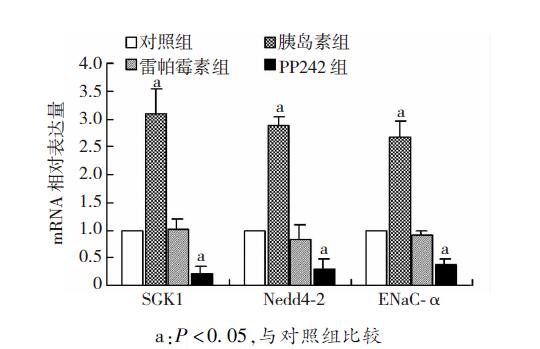 |
| a:P<0.05,与对照组比较图 2 Real-time PCR检测各组A549细胞中SGK1、Nedd4-2及ENaC-α的mRNA表达 |
与对照组比较,胰岛素组中rictor蛋白表达明显增高(P<0.05);PP242组中rictor蛋白表达明显减低(P<0.05),而雷帕霉素组中rictor表达较对照组则无明显改变。各组中SGK-ser422、 SGK1、Nedd4-2、ENaC-α蛋白表达变化趋势与上游rictor基 本一致(P值均<0.05,图 3、4)。
 |
| A: Western blot检测;B:半定量分析 a:P<0.05,与对照组比较图 3 Western blot检测各组A549细胞中rictor SGK-ser422、SGK1的蛋白表达 |
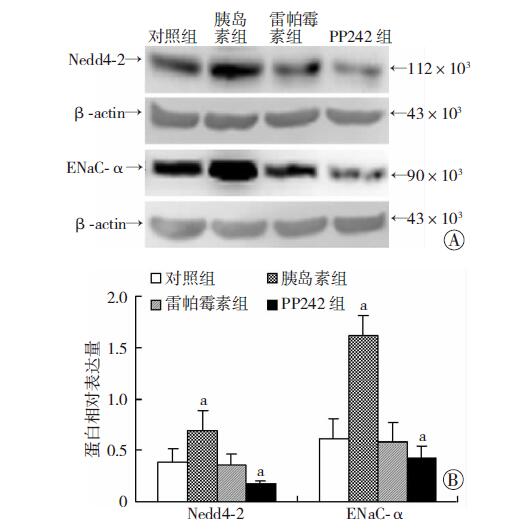 |
| A: Western blot检测;B:半定量分析 a:P<0.05,与对照组比较图 4 Western blot检测各组A549细胞中的Nedd4-2、ENaC-α的蛋白表达 |
细胞免疫荧光结果提示:与对照组相比较,胰岛素组中ENaC-α膜蛋白平均荧光强度增高,ENaC-α表达增强,PP242组中ENaC-α表达强度减弱,表达量减弱。而雷帕霉素组中ENaC-α表达与对照组比较无明显差异(图 5)。
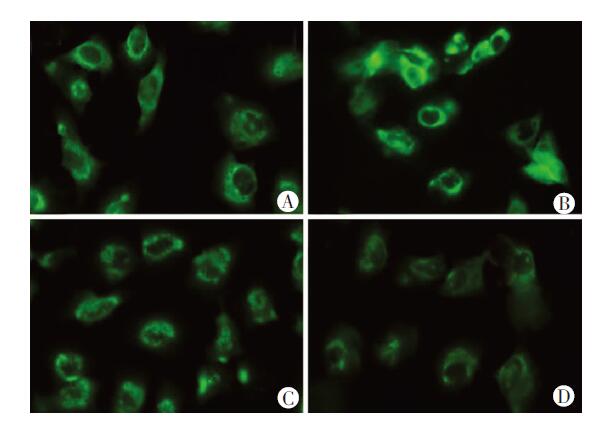 |
| A:对照组;B:胰岛素组;C:雷帕霉素组;D:PP242组图 5 免疫荧光观察各组A549细胞中膜蛋白ENaC-α荧光强度 (×200) |
目前,对于急性肺损伤/呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)的研究主要集中在肺泡间炎症介质和肺水清除两大方面[3]。而在肺水转运方面主要是通过ENaC,Na+-K+-ATPase,水通道蛋白(AQP)等方式实现[4]。因此,采用有效的途径增加肺泡上皮细胞中ENaC对肺泡液的清除能力是控制急性肺损伤的恶化和改善难治性低氧血症及发挥其对肺组织保护作用的新方向[5]。mTOR是一种丝氨酸/苏氨酸蛋白激酶组成的复合物,以mTORC1及mTORC2两种形式存在于生物体中[6, 7]。mTORC2复合体中rictor大分子与culin-1 链接组成E3泛素连接酶形成rictor/culin-1 E3复合体参与下游SGK1信号蛋白的调控[8, 9]。也有研究证明:mTORC2下游的重要节点SGK1属于AGC激酶家族,它选择性地与mTORC2的特异性大分子rictor和Sin1结合发挥生物学效应[10]。
本研究动物实验部分,我们采用胰岛素、雷帕霉素及PP242对ALI小鼠干预并检测各组肺W/D比值、BALF中炎症介质IL-6、TNF-α及病理形态学的变化,发现胰岛素对急性肺损伤具有一定的保护作用,抑制炎症产生的同时也提高了肺水清除能力。相反,PP242(mTORC1与mTORC2的双效抑制剂)干预小鼠ALI模型后加速急性肺损伤的形成和阻碍肺水清除能力。由于尚未发现mTORC2的特异性抑制剂,我们运用雷帕霉素(mTORC1特异性抑制剂)干预小鼠ALI模型,结果显示无明显改变。因此,我们推测ALI小鼠肺组织病理变化、炎症因子改变、肺水清除与mTORC2信号通路和ENaC有密切关系。据部分国外文献报道,ALI/ARDS时,炎症细胞产生IL-6、TNF-α炎症因子呈剂量依赖性下调ENaC-α的表达,影响ENaC的正常功能[11],这与本研究结果相一致。为了进一步探索调控ENaC-α的上游途径,我们在后期的体外实验中发现各组ENaC-α表达水平与SGK1、Nedd4-2成正相关。同时发现当mTORC2抑制时,rictor大分子表达下降,伴随下游SGK1-Ser422磷酸化位点效应的阻断,这与我们前期的部分实验结果一致[12, 13]。由此可推论mTORC2-rictor复合大分子对SGK1-Ser422的磷酸化作用是整个SGK1激活过程的限速步骤[14]。活化的SGK1可通过磷酸化泛素连接酶Nedd4-2,促使其下游的Nedd4-2与伴侣蛋白14-3-3结合,而失去结合和泛素化连接ENaC的能力,进而减少ENaC的进一步泛素化降解而使之保留在细胞膜上,使ENaC的生物效应增加[15, 16]。当肺泡内水肿液重吸收时,Na+从肺泡上皮细胞顶膜的ENaC进入到细胞内,在基底侧的Na+-K+-ATP酶的协同作用下泵出细胞外,细胞内外渗透压变化的过程驱动了肺泡内水肿液的重吸收。因此,找到有效途径清除肺泡腔内过多的水肿液,对维持良好的肺组织内环境稳态和气体交换功能具有十分重要的意义,一定程度上决定了ALI /ARDS的预后。
本研究结果表明:调控mTORC2/SGK1信号通路使其下游Nedd4-2泛素化,可直接影响ENaC-α的表达,从而调节肺上皮细胞钠水转运和肺水肿液清除,为治疗ALI/ARDS提供新的理论途径。
| [1] | Li H, Qiang Y, Wang L, et al. Repair of lipopolysaccharide-induced acute lung injury in mice by endothelial progenitor cells, alone and in combination with simvastatin . Chest, 2013, 144(3): 876-886. |
| [2] | Rafat N, Dacho C, Kowanetz G, et al. Bone marrow-derived progenitor cells attenuate inflammation in lipopolysaccharide-induced acute respiratory distress syndrome . BMC Res Notes, 2014, 7: 613. |
| [3] | Matthay M A, Zemans R L. The acute respiratory distress syndrome: pathogenesis and treatment . Ann Rev Pathol, 2011, 6: 147-163. |
| [4] | Wu Q, Wang F, Hou Y, et al. The effect of allogenetic bone marrow-derived mesenchymal stem cell transplantation on lung aquaporin-1 and -5 in a rat model of severe acute pancreatitis . Hepatogastroenterology, 2012, 59(116): 965-976. |
| [5] | Kellenberger S, Hoffmann-Pochon N, Gautschi I, et al. On the molecular basis of ion permeation in the epithelial Na+ channel. J Gen Physiol, 1999, 114(1): 13-30. |
| [6] | Li J, Ren J, Liu X, et al. Rictor/mTORC2 signaling mediates TGFbeta1-induced fibroblast activation and kidney fibrosis . Kidney Int, 2015, 88(3): 515-527. |
| [7] | Barquilla A, Crespo J L, Navarro M. Rapamycin inhibits trypanosome cell growth by preventing TOR complex 2 formation . Proc Natl Acad Sci U S A, 2008, 105(38): 14579-14584. |
| [8] | Moss S C, Lightell D J Jr, Marx S O, et al. Rapamycin regulates endothelial cell migration through regulation of the cyclin-dependent kinase inhibitor p27Kip1. J Biol Chem, 2010, 285(16): 11991-11997. |
| [9] | Liu L, Das S, Losert W, et al. mTORC2 regulates neutrophil chemotaxis in a cAMP- and RhoA-dependent fashion. Dev Cell, 2010, 19(6): 845-857. |
| [10] | Cardenas-Rodriguez M, Irigoin F, Osborn D P, et al. The Bardet-Biedl syndrome-related protein CCDC28B modulates mTORC2 function and interacts with SIN1 to control cilia length independently of the mTOR complex. Hum Mol Genet, 2013, 22(20): 4031-4042. |
| [11] | Drummond H A, Grifoni S C, Abu-Zaid A, et al. Renal inflammation and elevated blood pressure in a mouse model of reduced {beta}-ENaC . Am J Physiol Renal Physiol, 2011, 301(2): F443-F449. |
| [12] | Qi D, He J, Wang D, et al. 17ss-estradiol suppresses lipopolysaccharide-induced acute lung injury through PI3K/Akt/SGK1 mediated up-regulation of epithelial sodium channel (ENaC) in vivo and in vitro . Respir Res, 2014, 15: 159. |
| [13] | Zhu T, Wang D X, Zhang W, et al. Andrographolide protects against LPS-induced acute lung injury by inactivation of NF-kappaB . PLoS One, 2013, 8(2): e56407. |
| [14] | He J, Qi D, Wang D X, et al. Insulin upregulates the expression of epithelial sodium channel in vitro and in a mouse model of acute lung injury: role of mTORC2/SGK1 pathway . Exp Cell Res, 2015, 331(1): 164-175. |
| [15] | Lagnaz D, Arroyo J P, Chavez-Canales M, et al. WNK3 abrogates the NEDD4-2-mediated inhibition of the renal Na+-Cl- cotransporter . Am J Physiol Renal Physiol, 2014, 307(3): F275-F286. |
| [16] | Deng J, Wang D X, Deng W, et al. Regulation of alveolar fluid clearance and ENaC expression in lung by exogenous angiotensin ii . Respir Physiol Neurobiol, 2012, 181(1): 53-61. |



