脑脊液鼻漏是指脑脊液经破裂或者缺损的蛛网膜、硬脑膜和颅底骨板流入鼻腔或鼻窦,再经前鼻孔或鼻咽流出,为鼻-鼻颅底外科常见的疾病之一,按病因学分为外伤性和非外伤性。外伤性脑脊液鼻漏又分为意外伤害性和医源性,前者大约占80%,后者大约占16%。非外伤性或原发性(自发性)脑脊液鼻漏占的比例不足4%[1],临床较为罕见,国内未见大宗病例报道。因自发性脑脊液鼻漏病因不明确,漏口定位困难,往往给临床诊断与治疗带来不便。本研究回顾分析2000-2014年我院收治的7例自发性脑脊液鼻漏患者临床资料,现总结报告如下。
1 资料与方法 1.1 一般资料患者7例,包括男性2例,女性5例。年龄19~64岁,平均41岁。病程3~15个月,平均8个月。左侧鼻漏4例,右侧3例。患者体质量指数(body mass index,BMI)为23.6~56.1 kg/m2,平均33.1 kg/m2。2例患者有头痛症状,5例患者除单侧鼻腔渗液无其他症状。患者均无头部外伤及医源性损害病史。入院后收集鼻腔渗液行葡萄糖定量分析,葡萄糖均超过1.7 mmol/L确诊为脑脊液鼻漏。术前均行腰 椎穿刺测得脑脊液压力为905~2 360 Pa(92.4~241.0 mmH2O),平均1 553 Pa(158.6 mmH2O)。患者均接受头部、鼻窦CT及MRI检查,除外颅内肿瘤。
1.2 术前诊断与漏口定位7例患者术前均行鼻内镜检查,其中有4例提示中鼻道可见搏动性溢液,3例蝶筛隐窝处有清亮液体溢出(图 1),压迫同侧颈内静脉液体量流出增多。术前常规行鼻窦CT冠状位、轴位薄层扫描及三维重建检查,6例显示颅底骨质缺损(图 2、3),缺损直径在2~10 mm,1例患者无法显示骨质缺损。7例患者均行MRI检查,3例存在空蝶鞍。MRI水成像均成功显示漏口,表现为鼻窦或鼻腔内的液体信号与颅内蛛网膜下腔的脑脊液信号有线状相连。术前诊断漏口位于额窦后壁1例、筛顶2例、筛板1例、蝶窦3例。
 |
| 图 1 术前鼻内镜检查见蝶筛隐窝有清亮液体流出 |
 |
| 图 2 术前鼻窦CT示左侧蝶窦顶外侧壁骨质缺损(黑色箭头) |
 |
| 图 3 术前鼻窦CT三维重建示左侧蝶窦顶壁骨质缺损 |
患者就诊后均行2周保守治疗,包括绝对卧床休息,避免咳嗽、打喷嚏及撸鼻涕,适当予甘露醇降颅压等措施。7例患者经保守治疗后仍反复出现鼻漏症状,故均接受手术治疗。手术前1 d,常规置腰大池引流。手术方法:患者均采用经口插管全身麻醉,手术在鼻内镜下完成。生理盐水与1‰的肾上腺素按照10 ∶1配成溶液浸湿棉片收缩鼻腔黏膜,用3%碘伏反复冲洗鼻腔。对于鼻中隔偏曲,影响术中视野者,应行常规矫正。疑脑脊液漏来自蝶窦的3例患者采用Wigand手术方式,开放后组筛窦及扩大蝶窦自然口,由内向外充分去除蝶窦前壁,暴露蝶窦腔、蝶窦顶壁及外侧壁。鼻内镜下仔细寻找漏口,见清亮液体流出时用吸引器追踪,直至找到漏口。若无明显脑脊液漏出则可压迫同侧颈内静脉或者通过腰池引流管注入10 mL生理盐水增加颅内压,促使脑脊液流出,漏口处黏膜多苍白、水肿,甚至局部膨隆呈肉芽样改变。发现漏口后可清除漏口周围水肿黏膜及肉芽瘢痕组织形成新鲜创面,同时去除少许漏口周围骨质及骨膜,做出超过原漏口边界2~3 mm的移植床,注意勿伤及硬脑膜外血管。刮除蝶窦外侧壁黏膜时动作需要轻柔细致,否则可能损伤海绵窦、视神经及颈内动脉等重要结构。3例蝶窦漏口位于蝶窦顶壁及顶外侧壁,其中2例漏口直径约分别为3 mm及5 mm,采用“浴缸塞法”[2]修补漏口。“浴缸塞法”指取略大于瘘口适量耳垂脂肪,用可吸收线穿过脂肪长轴在一端打结。将脂肪栓子填塞入漏口,用探针配合拉紧缝线,形成对漏口的封堵,再将缝线穿过钩突黏膜片,拉紧缝线,将黏膜片涂生物胶粘覆于漏口骨壁,蝶窦腔内填塞可降解纳吸绵,鼻腔填塞碘仿纱条。另1例蝶窦顶壁瘘口骨质缺损呈细筛孔状,予骨蜡封闭骨质缺损区域,用生物蛋白胶将略大于上述区域面积的钩 突黏膜粘覆于骨面,同法填塞蝶窦腔及鼻腔。疑脑脊液漏来自筛顶的2例患者采用Messerkling方式由前向后开放筛窦,彻底清除筛窦气房及筛顶黏膜后找到瘘口。瘘口位于筛板的1例患者,去除鼻腔顶嗅裂区部分黏膜后显示瘘口。筛顶及筛板的瘘口同样采用“浴缸塞法”修补。疑脑脊液漏来自额窦后壁的1例患者,因其患侧的额窦发育欠佳,窦腔较小,手术操作较困难,故开放额隐窝后,尽量去除额窦内黏膜,然后予无菌腹直肌肌肉碎浆、自体脂肪紧密填塞窦腔,额窦口用涂有生物蛋白胶的钩突黏膜封闭,以碘仿纱条填塞鼻腔支持固定。
1.4 术后处理所有患者术后予腰大池引流1周,注意匀速,24 h总量不超过250 mL。头高位绝对卧床7 d,清淡低盐低脂饮食,限制饮水量,保持大便通畅,避免用力咳嗽、打喷嚏及擤鼻等颅内压增高因素。术后1周常规予能透过血脑屏障的头孢曲松钠2 g,静脉滴注1次/d预防感染。术后1周停止腰大池引流,予20%甘露醇125 mL静脉滴注2次/d降颅压治疗1周。术后2周抽出鼻腔碘仿纱条。术后1周至1个月口服乙酰唑胺250 mg,每天2次降颅压治疗。术后1、3个月腰椎穿刺测颅内压。
2 结果 2.1 术后随访本组7例自发性脑脊液鼻漏患者确诊后经保守治疗无效,均采用鼻内镜下修补手术。1例患者术后3个月复发,再次行修补手术。术后随访6个月至7年,脑脊液鼻漏均未再复发,未出现脑膜炎等并发症,一次手术修补成功率86%,二次手术修补成功率100%。脑脊液压力监测结果:术后1个月腰椎穿刺测颅内压,脑脊液压力为64.1~198.5 mmH2O,平均135.5 mmH2O。术后3个月腰椎穿刺测颅内压,脑脊液压力为105.7~ 203.0 mmH2O,平均189.8 mmH2O。
2.2 典型病例病例1:男性,42岁,因“左鼻腔间断流清涕8个月”入院。入院后确诊自发性脑脊液鼻漏,鼻窦CT提示蝶窦顶壁骨质缺损(图 4A)。术前颅脑MRI提示蝶窦顶壁黏膜下液体信号与颅内蛛网膜下腔脑脊液信号有线状相连(图 4B)。内镜下采用Wigand手术方式,开放后组筛窦及扩大蝶窦自然口,由内向外充分去除蝶窦前壁,暴露蝶窦腔、蝶窦顶壁及外侧壁。发现漏口直径约为5 mm,采用“浴缸塞法”修补漏口。术后1个月鼻内镜检查脂肪组织没有脱出,与周围黏膜融合生长,无脑脊液漏(图 5)。随访半年,未见复发。
 |
| A:术前鼻窦CT提示蝶窦顶壁骨质缺损(黑色箭头);B:术前颅脑MRI提示蝶窦顶壁黏膜下液体信号与颅内蛛网膜下腔相通(黑色箭头)图 4 自发性脑脊液鼻漏患者1术前超声检查 |
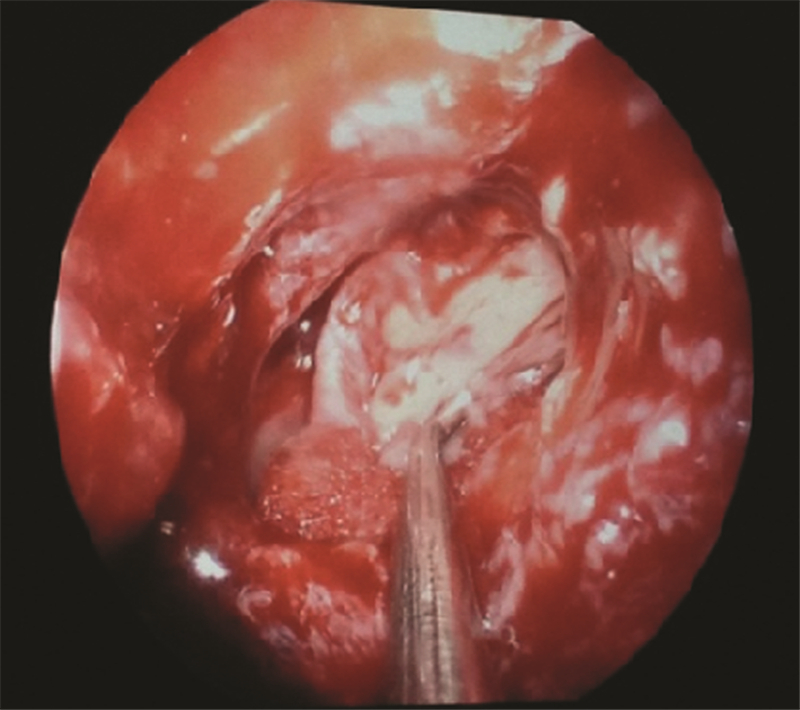 |
| 图 5 自发性脑脊液鼻漏患者1术后1个月鼻内镜复查 |
病例2(图 6):女性,60岁,因“发现左侧鼻腔反复流清水样涕半年”于2014年6月入院。入院后确诊自发性脑脊液鼻漏,鼻窦CT提示蝶窦顶外侧壁骨质缺损。鼻内镜下暴露蝶窦腔、蝶窦顶壁及外侧壁。发现漏口直径约为3 mm,采用“浴缸塞法”修补漏口。术后3个月鼻内镜检查见图 7,随访3年,未见复发。
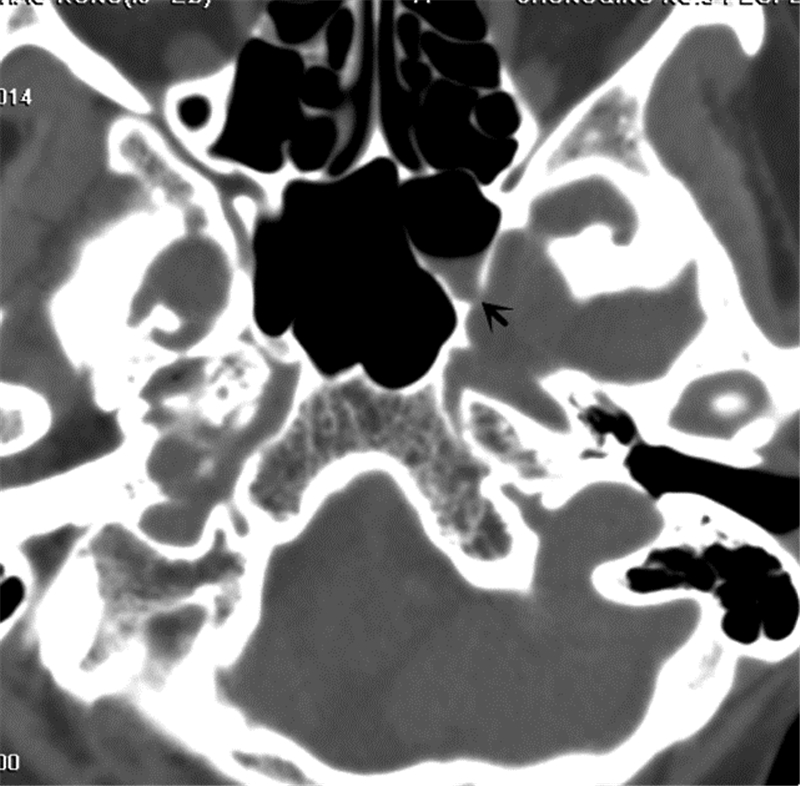 |
| 图 6 自发性脑脊液鼻漏患者2术前鼻窦CT提示蝶窦顶外侧壁骨质缺损(黑色箭头) |
 |
| 图 7 患者2术后3个月鼻内镜复查,脂肪组织已与周围黏膜融合,无脑脊液漏 |
脑脊液鼻漏的治疗已取得了比较满意的效果,文献报道鼻内镜下脑脊液鼻漏修补手术一次手术成功率已经超过90%,再次手术成功率已达97%[3]。但是,自发性脑脊液鼻漏的修复率相对较低,国外报道的修复成功率为25%~98%。随着自发性脑脊液鼻漏的病因、发病机制研究的进一步发展,自发性脑脊液鼻漏的修补成功率已经有了明显的提高[4]。
3.1 自发性脑脊液鼻漏的发病原因及机制目前自发性脑脊液鼻漏的病因及发病机制仍不十分清楚,因此常被命名为特发性或原因不明性脑脊液鼻漏。肥胖是一个非常重要的危险因素。肥胖会增加腹腔及胸腔内压力,可能影响颅内静脉的血液循环,导致颅内压增高。研究表明自发性脑脊液鼻漏容易发生在 肥胖的妇女[5]。本组7例患者中有6例BMI>25 kg/m2,其中5例为女性,与文献[5]报道一致。自发性脑脊液鼻漏也可继发于嗅神经萎缩,这使得嗅神经与其穿过筛板的通道间形成缝隙。由于脑脊液压力持续作用于颅底骨质,这些缝隙变得更加薄弱。如果颅内压突然增高,硬脑膜可能发生破裂,则出现脑脊液鼻漏。
良性颅内压增高(benign intracranial hypertension,BIH)目前被认为是自发性脑脊液鼻漏的重要病因[4, 5, 6, 7]。BIH是除外出血、感染、肿瘤等引起颅内压增高相关病因的颅高压综合征。增高的颅内压作用于颅底薄弱区(如筛板、蝶窦外侧隐窝等),从而导致这些区域骨质变薄和重塑,最终形成骨质缺损,在这基础上脑膜和(或)脑组织可从骨质缺损处疝出,一旦硬脑膜及蛛网膜的破裂则发生脑脊液鼻漏。自发性脑脊液鼻漏伴BIH的患者CT常有如下表现:①颅底骨可能出现较广泛的薄弱区域,甚至部分骨质裂开。②空蝶鞍。在本研究中患者术前腰椎穿刺测定脑脊液的压力为92.4~241.0 mmH2O,平均158.6 mmH2O。因为已经有脑脊液漏出,腰椎穿刺压力应该低于形成脑脊液鼻漏时的颅内压,说明患者在发生脑脊液鼻漏之前的颅内压是增高的。另外7例患者中有3例术前影像学检查报告存在空蝶鞍,与文献报道[8]相符。
鼻窦气化良好可能是发生自发性脑脊液鼻漏的另一个重要因素。若筛窦气化良好,筛板或筛顶变薄弱,特别是筛前动脉经过筛板或筛顶处的骨质更加菲薄,故这两个区域为自发性脑脊液鼻漏的常见漏区。另外,当蝶窦外侧隐窝气化明显时,蝶窦和颅中窝之间骨质菲薄,故蝶窦外侧隐窝容易发生脑脊液鼻漏。Shetty等[8]研究发现蝶窦外侧隐窝的气化在自发性脑脊液鼻漏患者发生率高达91%,而在正常人群中仅为23%~43%。
3.2 脑脊液鼻漏的诊断与漏孔定位若怀疑为自发性脑脊液鼻漏病例,均应常规行鼻漏出液的葡萄糖定量或β-2 转铁蛋白检测。当葡萄糖定量>1.7 mmol/L或β-2转铁蛋白检测阳性,是确诊脑脊液鼻漏的主要标准[9]。通常定性诊断脑脊液鼻漏并不困难,关键是漏口的定位诊断。这关系到如何选择手术进路及修补方法,这些重要因素可能决定手术成败。鼻内镜检查、薄层CT和MRI检查为目前临床最重要的定位方法。术前鼻内镜检查需从前到后检查嗅裂区、中鼻道、上鼻道、蝶筛隐窝及咽鼓管咽口等部位,观察上述部位有无清亮液体流出,但术前通常只能大致判断脑脊液流出部位,最终需术中开放鼻窦及清除鼻腔鼻窦黏膜方可显示漏口。薄层高分辨率CT目前已成为脑脊液鼻漏患者重要及首选检查,漏口处颅底骨质不连续为直接影像学表现,窦腔积液为间接表现。高分辨率CT冠状位扫描对骨质显示最佳,而冠状位MRI水成像显示脑脊液鼻漏漏口最佳。本组7例患者MRI水成像序列图像上成功显示漏口,表现为鼻窦或鼻腔内的液体信号与颅内蛛网膜下腔的脑脊液信号有线状相连。结合鼻内镜检查、薄层高分辨率CT及冠状位MRI水成像,术前均准确定位颅底瘘口,并在术中得到证实。
3.3 治疗方法自发性脑脊液鼻漏多不能自愈,保守治疗效果差,特别是病程较长者,故需要手术治疗。本组7例患者经2周保守治疗无效,均接受鼻内镜下修补手术。术前准确定位漏口、选择合适的手术方式、术中良好的视野及暴露,这些均是手术成功的关键。本组研究病例中,7例患者术中均成功找到漏口,通过助手按压颈内静脉或者经腰池引流管注入生理盐水等措施增加颅内压,可清晰地看到漏口有清亮的脑脊液流出。瘘口位于额窦后壁的1例患者额窦发育欠佳,窦腔较小,手术操作较困难。在开放额隐窝后,直接予脂肪及肌肉组织填塞额窦腔,最终成功修补漏口。修补材料包括自体材料与非自体材料,自体材料具有排异性小,取材方便、修补物易存活、总体花费少等优点,故在临床上广泛采用。修补材料种类包括:①自体带蒂组织:如鼻中隔黏膜瓣等;②自体游离组织:脂肪、肌浆、鼻黏膜、阔筋膜和骨片等;③非自体组织:人工硬脑膜、钛板、生物蛋白胶及骨蜡等。Hegazy等[10]认为不同的自体修补材料对手术成功率无影响。本组临床资料中,应用钩突黏膜、脂肪、肌肉浆、下鼻甲黏膜瓣、骨蜡等,疗效满意。鼻内镜下脑脊液鼻漏修复方法较多,可有硬脑膜内内置法、硬脑膜外内置法、外置法、三明治法及浴缸塞法等。通常根据漏口骨质缺损的大小选用不同的修补材料及修补方法。吴瑕等[11]总结对于漏口<5 mm的患者,多采用鼻中隔软骨膜或中、下鼻甲黏膜外置法修复漏口,若漏口骨质缺损>10 mm可采用颞肌加颞肌筋膜、大腿肌肉加阔筋膜或带蒂鼻中隔黏膜瓣进行修复。文献报道鼻内镜下采用脂肪组织“浴缸塞法”修补脑脊液鼻漏具有成功率高、操作简单、并发症低等优点[12]。脂肪组织具有以下优点:脂肪的油性,在脑脊液中的表面张力很强,可阻止脑脊液渗漏;脂肪组织柔软、易塑形,在颅底漏口硬脑膜内侧表面可以很好的填塞而不移位;根据“浴缸塞原理”,颅内压力在硬脑膜内侧将“脂肪栓子”压向颅底,可有效阻止脑脊液的渗漏,同时脂肪组织容易和硬脑膜创面融合生长。在本研究中,我们在鼻内镜下采用脂肪组织“浴缸塞法”修补脑脊液鼻漏取得满意疗效,未出现任何并发症,具有安全、简便、可靠等优点,值得推广应用。
3.4 围手术期及术后脑脊液压力管理文献[13]报道自发性脑脊液鼻漏患者术后复发率高达25%~87%,而颅内压持续增高是导致复发、手术失败的重要因素,因此围手术期及术后较长时间对颅内压的管理对于手术成败至关重要。我们的经验是围手术期安置腰池引流及术后1个月药物控制颅内压。本研究采取手术前1 d置腰池引流,术中开放引流脑脊液降低颅内压,脑脊液流出减少可保证手术的顺利进行。术后匀速引流脑脊液,并动态监测脑脊液压力,尽量控制脑脊液压力在正常范围。术后1个月是漏口修复的关键时期,而腰池引流时间超过1周会增加颅内感染风险,我们选择在术后1周停腰池引流改静滴甘露醇降颅内压,同时1周至1个月予口服乙酰唑胺降颅压治疗。术后1个月7例患者中6例行腰穿测得颅内压在正常范围,1例颅内压增高。术后 3个月7例患者腰穿测得颅内压均再次增高,提示瘘口修补术后自发性脑脊液鼻漏患者颅内压增高的因素并未得到解除,并且由于漏口封堵导致颅内压可能明显增高。本研究中,1例患者术后3个月复发,漏口为蝶窦顶外侧壁,再次手术修补成功。该患者术前腰穿测颅内压为198.5 mmH2O,术后3个月测颅内压高达203 mmH2O,考虑复发与术后颅内压再次明显增高密切相关。对于类似患者,需长期随访观察,必要时需行脑室腹腔分流手术从根本解决颅内压增高。由于本组病例数较少,自发性脑脊液鼻漏患者术前及术后的颅内压变化规律尚不完全明确,仍需进一步研究。
总之,自发性脑脊液鼻漏的病因及发病机制目前尚未完全明确,术后复发的风险仍较高。经鼻内镜修补脑脊液鼻漏是目前治疗自发性脑脊液鼻漏的首选方法,具有创伤小、术后恢复快、并发症少、成功率高及可重复操作等优点,其中准确的术前定位、选择合适的手术方式、围手术期及术后对颅内压的控制是手术成功的重要因素。
| [1] | Wise S K, Schlosser R J. Evaluation of spontaneous nasal cerebrospinal fluid leaks[J]. Curr Opin Otolaryngol Head Neck Surg, 2007, 15(1): 28-34. |
| [2] | Wormald P J, McDonogh M. The bath-plug closure of anterior skull base cerebrospinal fluid leaks[J]. Am J Rhinol, 2003, 17(5): 299-305. |
| [3] | 董俊华, 万保罗. 鼻内镜下脑脊液鼻漏修补术[J]. 临床耳鼻咽喉头颈外科杂志, 2013, 27(20): 1153-1155. |
| [4] | Schlosser R J, Wilensky E M, Grady M S, et al. Cerebrospinal fluid pressure monitoring after repair of cerebrospinal fluid leaks[J]. Otolaryngol Head Neck Surg, 2004, 130(4): 443-448. |
| [5] | 翟翔, 张金玲, 刘钢. 空蝶鞍合并脑脊液鼻漏的特点及临床治疗[J]. 临床耳鼻咽喉头颈外科杂志, 2012, 26(23): 1063-1066. |
| [6] | Soler Z M, Schlosser R J. Spontaneous cerebrospinal fluid leak and management of intracranial pressure[J]. Adv Otorhinolaryngol, 2013, 74: 92-103. |
| [7] | Vaphiades M S, Ranganath N K, Woodworth B A. Spontaneous cerebrospinal fluid otorrhea and rhinorrhea in idiopathic intracranial hypertension patients[J]. J Neuroophthalmol, 2013, 33(4): 416. |
| [8] | Shetty P G, Shroff M M, Fatterpekar G M, et al. A retrospective analysis of spontaneous sphenoid sinus fistula: MR and CT findings[J]. AJNR Am J Neuroradiol, 2000, 21(2): 337-342. |
| [9] | Bachmann-Harildstad G. Diagnostic values of beta-2 transferrin and beta-trace protein as markers for cerebrospinal fluid fistula[J]. Rhinology, 2008, 46(2): 82-85. |
| [10] | Hegazy H M, Carrau R L, Snyderman C H, et al. Transnasal endoscopic repair of cerebrospinal fluid rhinorrhea: a meta-analysis[J]. Laryngoscope, 2000, 110(7): 1166-1172. |
| [11] | 吴瑕, 王彦君, 乐建新, 等. 脑脊液鼻漏修补术成败的关键因素研究[J]. 临床耳鼻咽喉头颈外科杂志, 2014, 28(9): 618-620. |
| [12] | 葛文彤, 倪鑫, 李云川, 等. 鼻内镜下脂肪压塞技术修补前颅底脑脊液鼻漏和脑膜脑膨出[J]. 临床耳鼻咽喉头颈外科杂志, 2013, 27(15): 832-835. |
| [13] | Perez M A, Bialer O Y, Bruce B B, et al. Primary spontaneous cerebrospinal fluid leaks and idiopathic intracranial hypertension[J]. J Neuroophthalmol, 2013, 33(4): 330-337. |



